Enzymes
1/39
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
40 Terms
Quelles sont les deux spécificités de réaction des enzymes concernant les acides aminés ?
La décarboxylase (dégradation de l'alpha-COOH) et la désaminase (hydrolyse de l'alpha-NH3+).
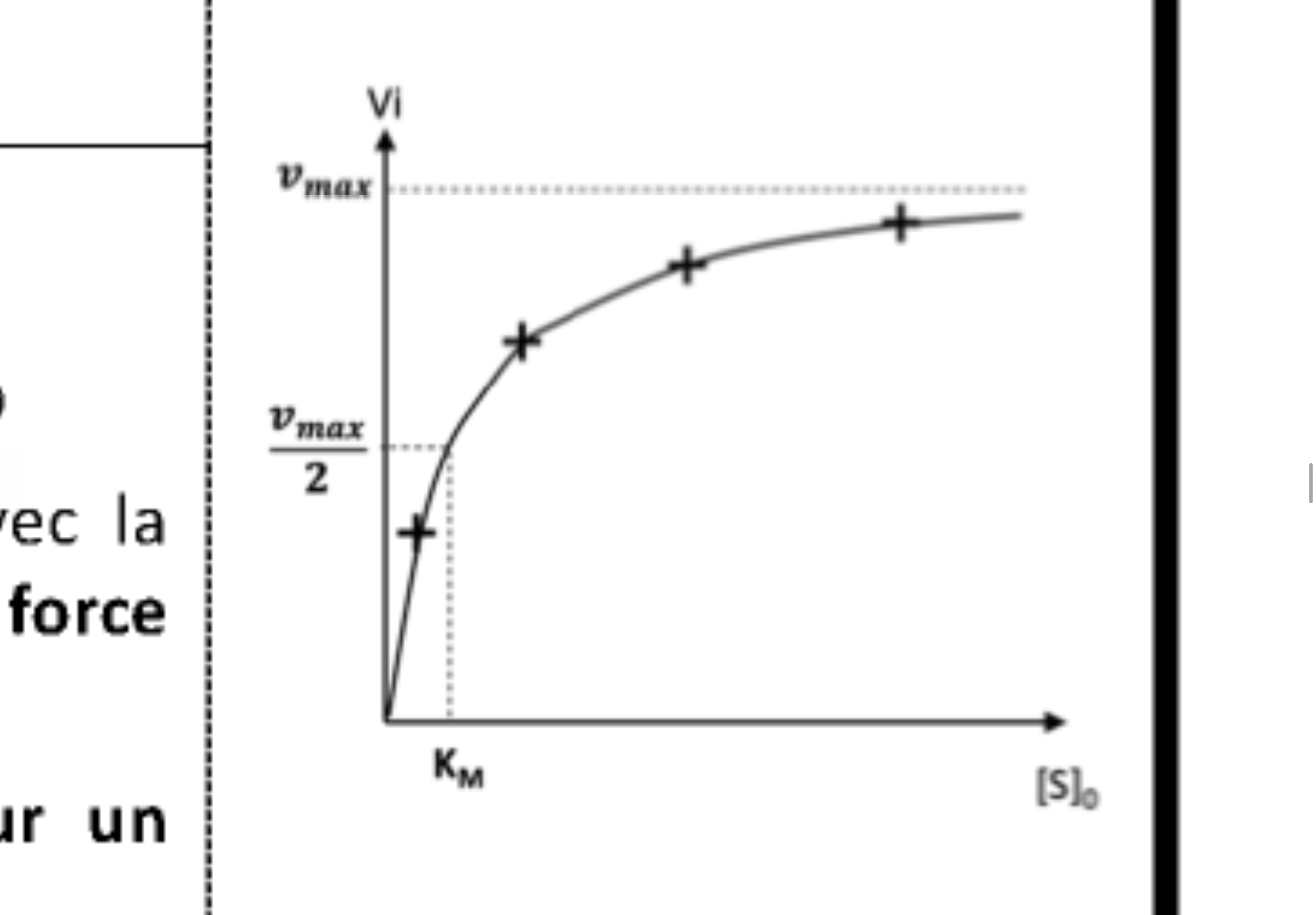
Équation et quelle courbe ?
MM
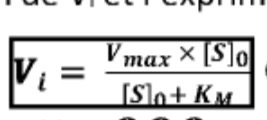
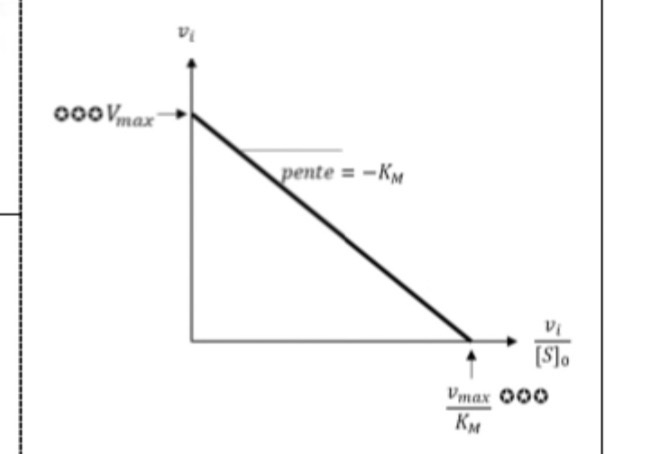
Équation et quelle courbe ? Il
Eadie H
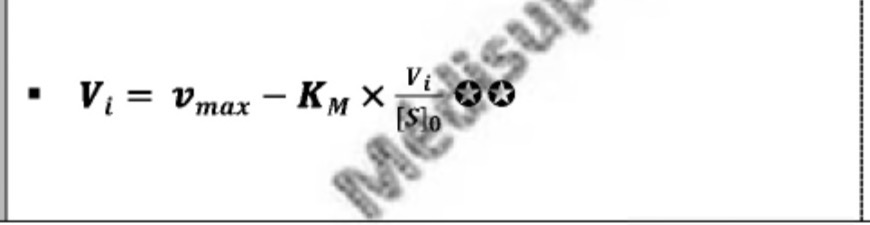
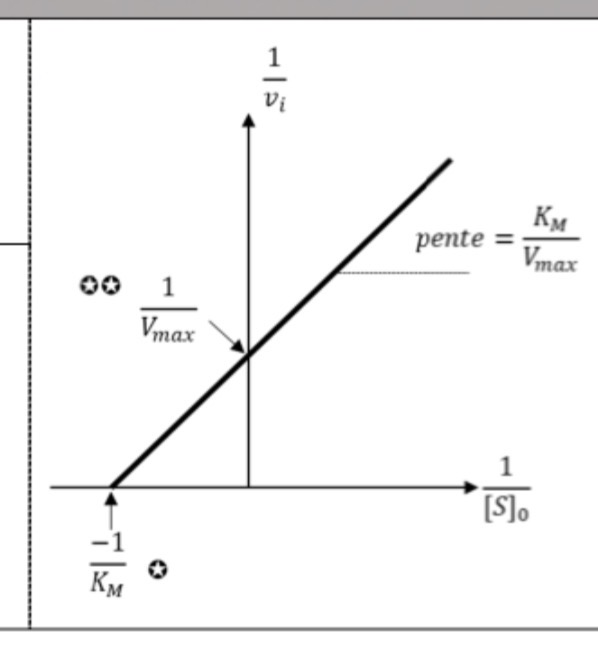
Équation et quelle courbe ?
LB
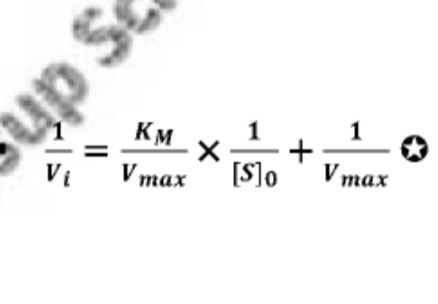
Dans quel milieu se déroulent les réactions enzymatiques et quel est le facteur d'augmentation de la vitesse ?
En solution aqueuse ; la vitesse augmente d'un facteur 10 puissance 7 à 10 puissance 11.
Toutes les enzymes sont-elles de nature protéique ?
Non, il existe des ARN catalytiques appelés ribozymes.
Quelle condition de structure est indispensable pour qu'il y ait catalyse ?
La conservation de la conformation native de l'enzyme.
Quelle est la différence de composition entre une holoprotéine et une hétéroprotéine enzymatique ?
L'holoprotéine est entièrement protéique, l'hétéroprotéine possède une apoenzyme et un cofacteur.
Quelles sont les caractéristiques de l'apoenzyme ?
C'est la partie protéique, thermolabile, qui donne la spécificité.
Quelles sont les caractéristiques du cofacteur ?
C'est la partie non protéique, thermostable, qui réalise la catalyse et n'est pas spécifique.
C'est quoi une oxydoréductase ?
Elle catalyse le transfert d'électrons lors de réactions d'oxydation ou de réduction.
C'est quoi une transférase ?
Elle catalyse le transfert de groupements chimiques.
C'est quoi une hydrolase ?
Elle catalyse la rupture d'une liaison covalente à l'aide d'une molécule d'eau.
C'est quoi une lyase ?
Elle catalyse la réaction d'une liaison covalente sans molécule d'eau.
C'est quoi une isomérase ?
Elle catalyse la réaction réversible de modification de l'arrangement des atomes.
C'est quoi une ligase ?
Elle catalyse la réaction irréversible de formation d'une liaison covalente entre deux molécules en présence d'ATP.
Quels sont les trois états de la catalyse et leurs niveaux d'énergie libre ?
Initial, Transition (NRJ supérieure à l'initial) et Final (NRJ inférieure à l'initial).
Quel est le rôle précis de l'enzyme sur la barrière énergétique ?
Elle provoque l'abaissement de l'énergie d'activation sans modifier l'équilibre.
Quel type de liaisons se forme entre l'enzyme et son substrat ?
Des liaisons faibles.
Quels paramètres sont suivis en cinétique enzymatique ?
La variation de la quantité de produits ou du substrat.
Quelles sont les deux étapes de la catalyse enzymatique ?
Formation du complexe ES (rapide et réversible) puis libération de E + P (limitante et irréversible).
Que se passe-t-il durant la phase 1 de la courbe de cinétique en hyperbole ?
La vitesse initiale est constante et les produits formés sont inférieurs à 10 % du substrat initial (S0).
Quelle est la formule de la vitesse initiale (Vi) en phase 1 ?
Vi = Pente x dP / dt.
Que se passe-t-il durant les phases 2 et 3 de la courbe de cinétique ?
Phase 2 : diminution de la vitesse. Phase 3 : vitesse nulle (l'équilibre est atteint).
Que signifie l'état stationnaire pour le complexe ES ?
La concentration du complexe ES est quasi constante.
Quelle condition de concentration est nécessaire pour la courbe de saturation ?
La concentration en substrat S0 doit être toujours très supérieure à celle de l'enzyme E0.
Quelle est la formule de la vitesse maximale (Vmax) ?
Vmax = k2 x E0.
Quelle est la formule de la constante de Michaelis (Km) ?
Km = (k-1 + k2) / k1.
De quels facteurs dépend la grandeur expérimentale Km ?
De la structure du substrat, du pH, de la température et de la force ionique.
Quelle est l'équation de Michaelis-Menten ?
Vi = (Vmax x S0) / (S0 + Km).
Que vaut Vi si S0 est très supérieur à 20 fois le Km ?
Vi = Vmax.
Que vaut Vi si S0 est égal au Km ?
Vi = Vmax / 2.
Qu'est-ce que la constante catalytique (kcat) ?
Elle correspond à la constante de vitesse d'ordre 1 : kcat = Vmax / E.
Quelle est l'unité de kcat et sa définition ?
Exprimée en seconde -1, c'est le nombre de molécules de S converties en P par une seule molécule d'enzyme en une seconde.
À quoi correspond l'efficacité catalytique ?
Au rapport kcat / Km.
Comment varie l'efficacité catalytique avec l'affinité ?
Plus l'affinité est grande (Km faible) et plus c'est rapide, plus l'efficacité est grande.
Qu'est-ce que le site actif ?
Une petite région qui se lie au substrat ou à un coenzyme.
Quelles sont les caractéristiques physiques du site actif ?
Résidus non polaires, absence d'eau et micro-environnement particulier.
Qu'est-ce qu'un résidu catalytique ?
Un acide aminé qui participe directement à la catalyse (peut être éloigné dans la structure primaire).
Qu'est-ce qu'une triade catalytique ?
L'association de trois résidus éloignés qui forment un ensemble pour une catalyse plus efficace.