AMINE, AMINO ACID, PEPTIDE, PROTEIN VÀ ENZYME
1/51
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
52 Terms
Khái niệm Amine là gì?
Amine là dẫn xuất của ammonia (NH₃), trong đó nguyên tử hydrogen trong NH₃ được thay thế bằng gốc hydrocarbon.
Làm thế nào để xác định bậc của amine?
Bậc của amine được tính bằng số gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
Phân biệt Alkylamine và Arylamine?
Alkylamine: nhóm amine liên kết với gốc alkyl. Arylamine: nhóm amine liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Tên thông thường của C₆H₅NH₂?
Aniline.
Các loại tên của amine?
Tên gốc chúc - Tên thay thế - Tên thường
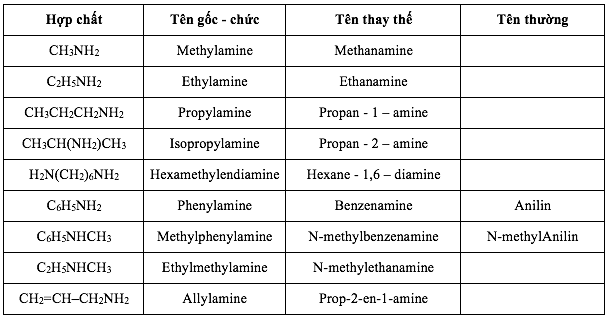
Trạng thái vật lí của amine có phân tử khối nhỏ?
Methylamine, ethylamine, dimethylamine, trimethylamine là chất khí ở điều kiện thường.
Vì sao amine có nhiệt độ sôi cao hơn hydrocarbon cùng phân tử khối?
Do amine bậc một và hai có khả năng tạo liên kết hydrogen liên phân tử.
So sánh tính base của Alkylamine và Arylamine?
Alkylamine có tính base mạnh hơn NH₃ và aniline. Aniline có tính base yếu hơn NH₃ do vòng benzene hút electron.
Hợp chất amine nào làm đổi màu quỳ tím sang xanh?
Các alkylamine làm quỳ tím hóa xanh. Aniline không làm đổi màu quỳ tím.
Phản ứng của amine với acid?
Amine + acid → muối. Ví dụ: CH₃NH₂ + HCl → CH₃NH₃Cl.
Phản ứng tạo kết tủa hydroxide của amine?
Amine phân tử nhỏ + dung dịch muối kim loại → kết tủa hydroxide. Ví dụ: với FeCl₃ tạo Fe(OH)₃.
Phản ứng đặc trưng để nhận biết Alkylamine?
Tạo phức màu xanh lam với Cu(OH)₂.
Sản phẩm của Alkylamine bậc một khi tác dụng với HNO₂?
Tạo alcohol và giải phóng khí N₂.
Sản phẩm của Aniline với HNO₂/HCl ở 0-5 °C?
Muối diazonium (phẩm nhuộm)
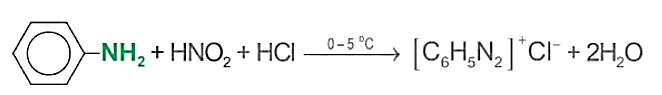
Phản ứng thế ở nhân thơm của aniline?
Aniline dễ tham gia phản ứng thế H ở vòng benzene hơn benzene.
Hiện tượng khi cho aniline tác dụng với Br₂ (nước brom)?
Tạo 2,4,6-tribromoaniline (kết tủa trắng).
Khái niệm Amino acid là gì?
Hợp chất hữu cơ tạp chức, chứa đồng thời nhóm amino (-NH₂) và nhóm carboxyl (-COOH).
Dạng tồn tại chủ yếu của amino acid?
Dạng ion lưỡng cực H₃N⁺-CH(R)-COO⁻ do tương tác nội phân tử.
α-Amino acid là gì?
Amino acid có nhóm -NH₂ gắn với carbon α (C số 2 tính từ -COOH). Đa số amino acid tự nhiên là α-amino acid.
5 a.a phải nhớ?
Gly 75
Ala 89
Val 117
Glu 147
Lys 146
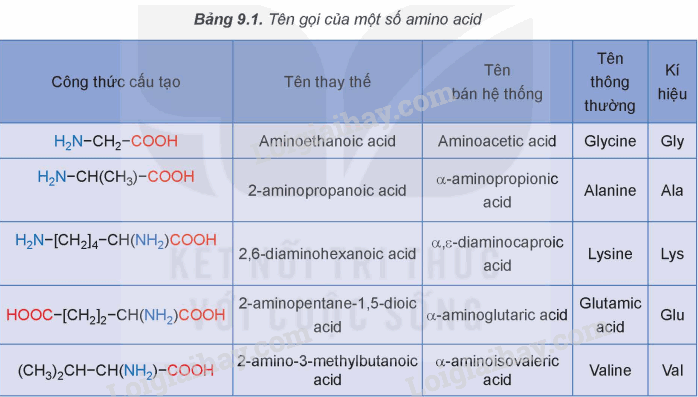
Đặc điểm vật lí nổi bật của amino acid?
Là chất rắn, có nhiệt độ nóng chảy cao, tan tốt trong nước.
Tính chất hóa học đặc trưng nhất của amino acid?
Tính lưỡng tính: vừa tác dụng với acid mạnh, vừa tác dụng với base mạnh.
Sản phẩm khi glycine tác dụng với HCl?
Muối ClH₃N-CH₂-COOH.
Sản phẩm khi glycine tác dụng với NaOH?
Muối H₂N-CH₂-COONa.
Điều kiện để amino acid tham gia phản ứng ester hóa?
Nhóm -COOH phản ứng với alcohol khi có xúc tác acid mạnh.
Loại amino acid tham gia phản ứng trùng ngưng?
Các ε-amino acid và ω-amino acid → polyamide.
Tính điện di (Electrophoresis) là gì?
Khả năng di chuyển khác nhau trong điện trường tùy pH môi trường.
Amino acid di chuyển về cực nào trong môi trường pH thấp?
Chủ yếu ở dạng cation → di chuyển về cực âm.
Amino acid di chuyển về cực nào trong môi trường pH cao?
Chủ yếu ở dạng anion → di chuyển về cực dương.
Amino acid thiết yếu là gì?
Amino acid cơ thể không tự tổng hợp được, phải lấy từ thức ăn.
Công thức và tên amino acid đơn giản nhất?
H₂N-CH₂-COOH (glycine).
Tên thông thường của 2-aminopropanoic acid?
Alanine (H₂N-CH(CH₃)-COOH).
Khái niệm Peptide là gì?
Hợp chất tạo từ α-amino acid liên kết qua liên kết peptide (-CO-NH-).
Liên kết peptide hình thành thế nào?
Giữa -COOH của amino acid này và -NH₂ của amino acid kia.
Thứ tự amino acid trong peptide?
Đầu N (-NH₂) viết bên trái, đầu C (-COOH) viết bên phải.
Peptide có tính đồng phân không?
Có. Thay đổi thứ tự amino acid → đồng phân cấu tạo (Gly-Ala khác Ala-Gly).
Sản phẩm thủy phân hoàn toàn peptide?
Các α-amino acid.
Phản ứng màu Biuret nhận biết loại peptide nào?
Peptide có ≥ 2 liên kết peptide (trừ dipeptide).
Hiện tượng phản ứng màu Biuret?
Tạo phức màu tím với Cu(OH)₂ trong kiềm.
Khái niệm Protein là gì?
Hợp chất cao phân tử tạo từ một hoặc nhiều chuỗi polypeptide.
Phân biệt Protein đơn giản và phức tạp?
Đơn giản: chỉ gồm amino acid. Phức tạp: có thêm thành phần phi protein (acid nucleic, lipid...).
Đặc điểm vật lí của Protein dạng sợi?
Ví dụ: α-keratin, fibroin. Không tan trong nước.
Đặc điểm vật lí của Protein dạng cầu?
Ví dụ: hemoglobin, albumin. Tan trong nước tạo dung dịch keo.
Phản ứng hóa học đặc trưng nhất của protein?
Thủy phân (tạo amino acid) và hiện tượng đông tụ.
Phản ứng màu protein với HNO₃ đặc?
Tạo hợp chất màu vàng (do nitro hóa vòng benzene trong amino acid thơm).
Hiện tượng đông tụ protein là gì?
Protein biến tính và tách khỏi dung dịch khi đun nóng hoặc thêm acid, base, muối kim loại nặng (Pb²⁺, Hg²⁺).
Vai trò cốt lõi của Protein với sự sống?
Xây dựng tế bào, vận chuyển (hemoglobin), điều hòa (insulin), xúc tác (enzyme).
Chất nào xúc tác thủy phân Protein trong hệ tiêu hóa?
Enzyme protease (peptidase).
Khái niệm Enzyme là gì?
Chất xúc tác sinh học, phần lớn là protein, xúc tác cho phản ứng hóa học và sinh hóa.
Tính chất quan trọng nhất của Enzyme?
Tính chọn lọc cao: mỗi enzyme xúc tác cho một (hoặc vài) phản ứng nhất định.
Enzyme nào thủy phân tinh bột trong nước bọt?
Amylase (phân giải tinh bột → dextrin, maltose).
Lĩnh vực ứng dụng chính của Enzyme?
Y học, dược phẩm (định lượng glucose, urea, cholesterol); công nghiệp thực phẩm (bia, bánh mì).