2. FENOLI
1/60
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
61 Terms
Struktura fenola
Posjeduju OH skupinu direktno vezanu na benzenski prsten
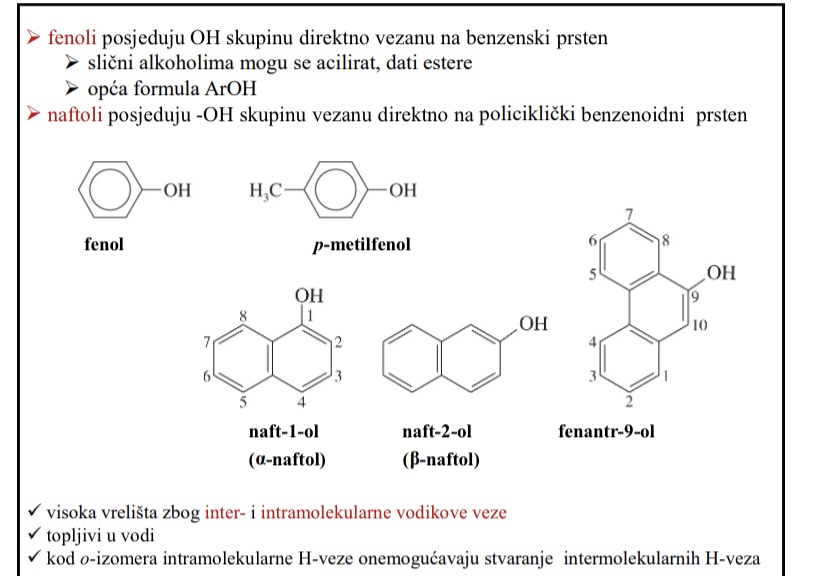
Kojim spojevima su fenoli slicni
Slicni alkoholima mogu se acilirati, dati estere
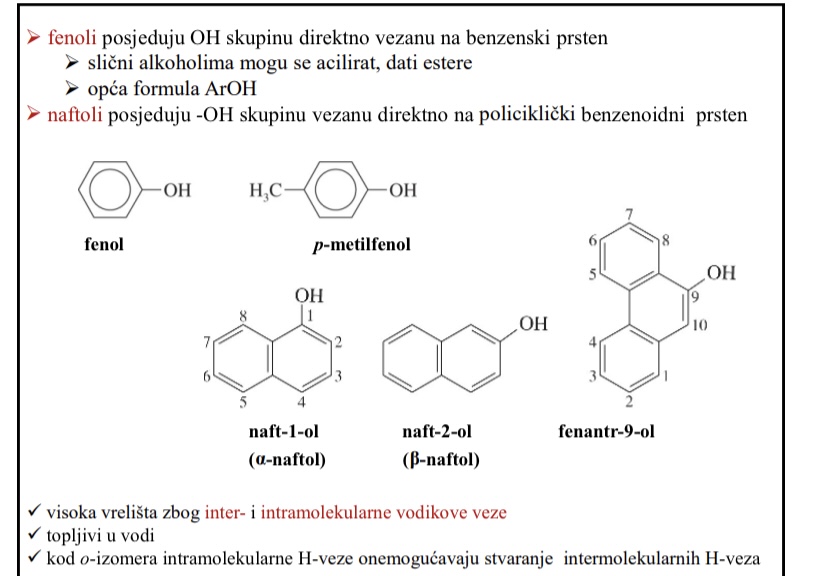
Opca formula fenola
ArOH
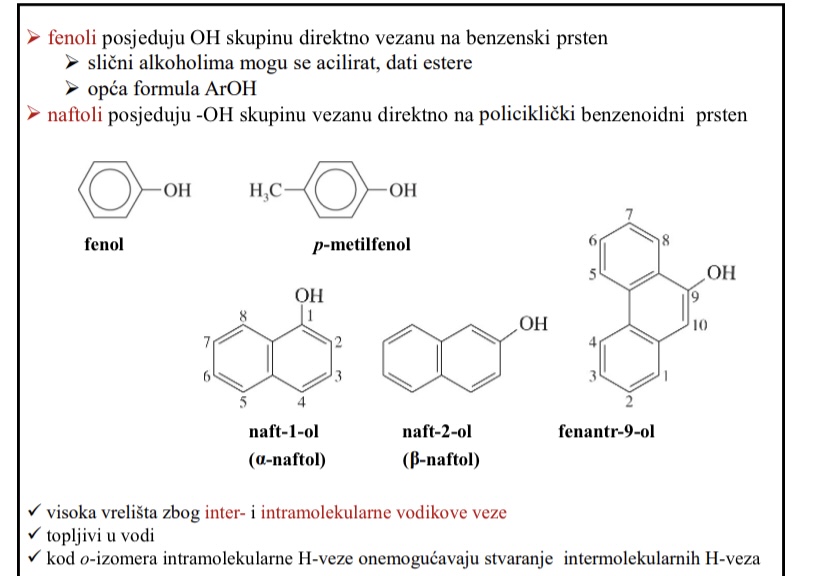
Struktura naftola
Posjeduju OH skupinu vezanu direktno na policiklicki benzenoidni prsten
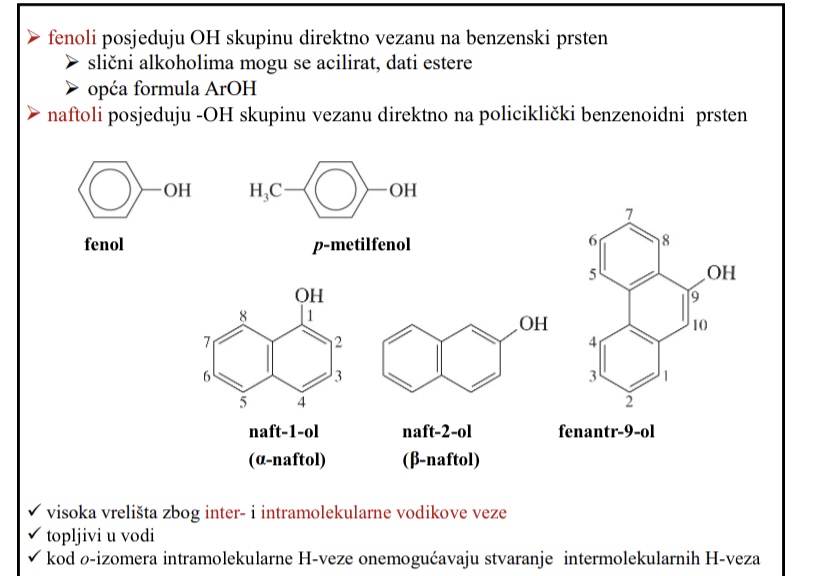
Svojstva fenola
Visoka vrelista zbog inter i intramolekularne vodikove veze
Topljivi u vodi
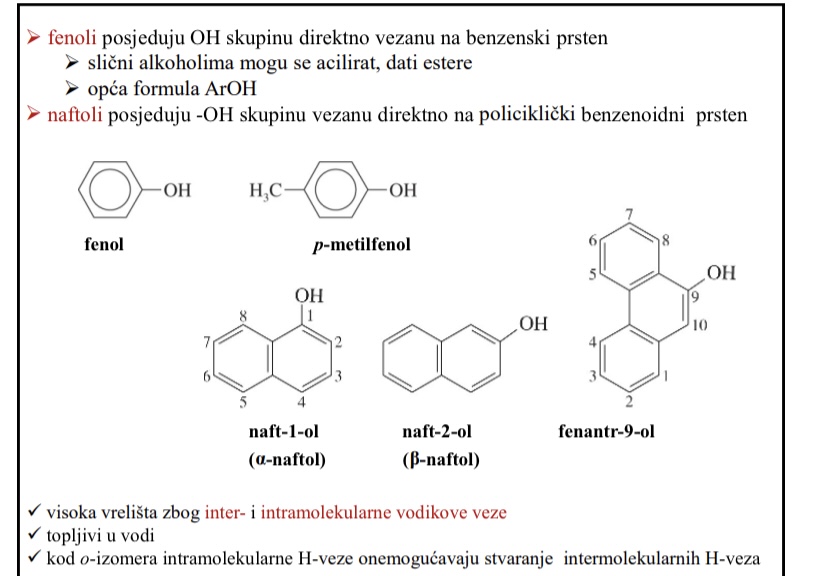
Specificno kod svojstava o-izomera fenola
Kod o-izomera intramolekularne H-veze onemogucavaju stvaranje intermolekularnih H-veza
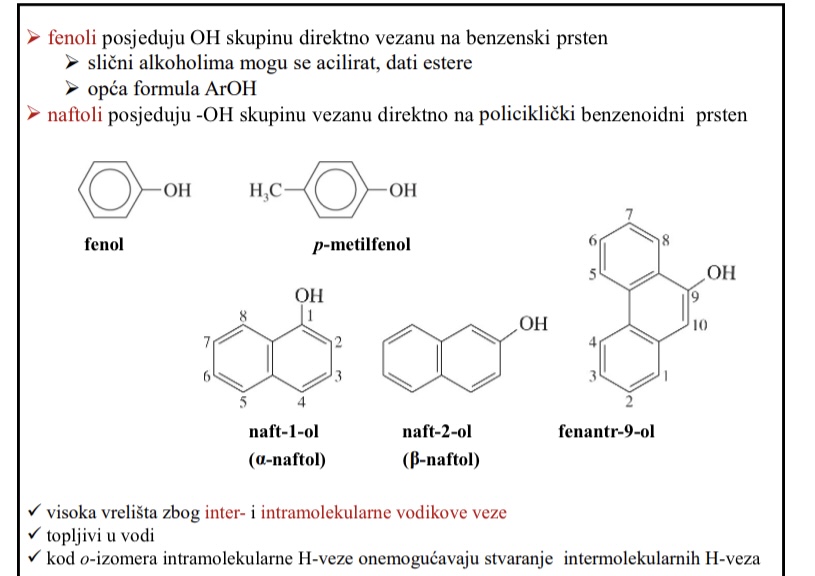
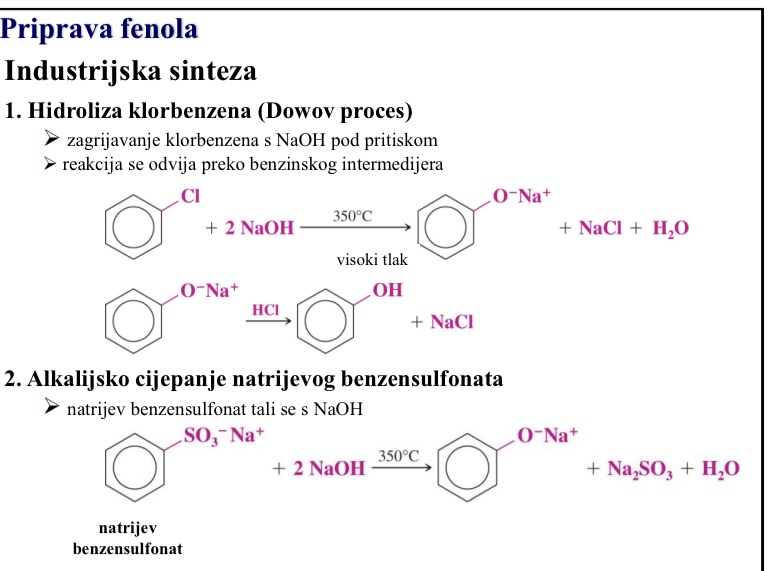
Priprava fenola - industrijska sinteza 3 postupka
Hidroliza klorbenzena (Dowov proces)
Alkalijeko cijepanje natrijevog benzensulfonata
Kumenski postupak
Priprava fenola - industrijska sinteza - hidroliza klorbenzena
Dowov proces
Zagrijavanje klorbenzena s NaOH pod pritiskom
Reakcija se odvija preko benzinskog intermedijera
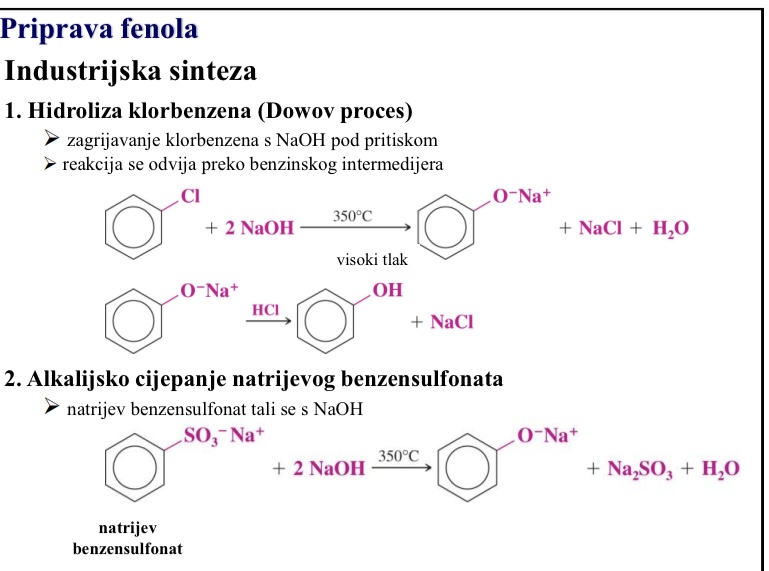
Priprava fenola - industrijska sinteza - alkalijsko cijepanje natrijevog benzensulfonata
Natrijev benzensulfonat tali se s NaOH
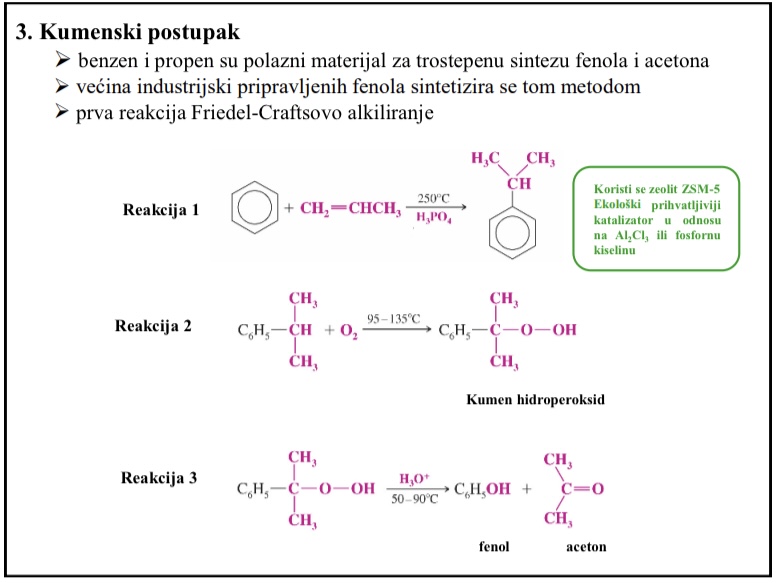
Priprava fenola - industrijska sinteza - Kumenski postupak
Benzen i propen su polazni materijali za trostepenu sintezu fenola i acetona
Vecina industrijski pripravljenih fenola sintetizira se tom metodom
Prva reakcija Friedel-Craftsovo alkiliranje
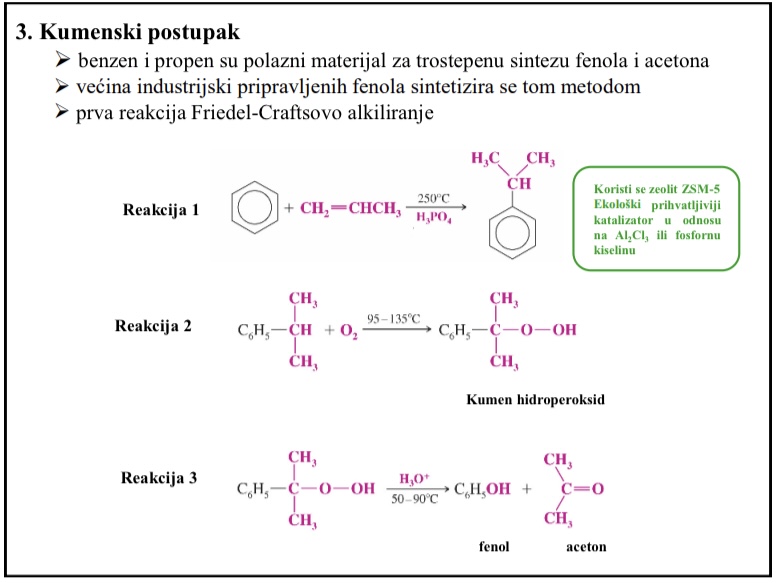
Kumenski postupak - koji se katalizator koristi
Zeolit ZSM-5 kao ekoloski prihvatljiviji katalizator u odnosu na Al2Cl3 ili fosfornu kiselinu
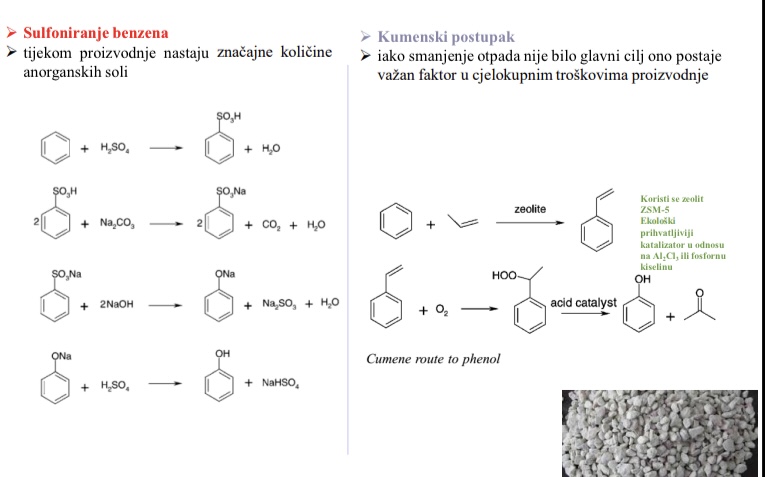
Koja je razlika sulfoniranja benzena i kumenskog postupka
Sulfoniranje benzena - tijekom proizvodnje nastaju znacajne kolicine anorganskih soli
Kumenski postupak - iako smanjenje otpada nije bio glavni cilj ono postaje vazan faktor u cjelokupnim troskovima proizvodnje
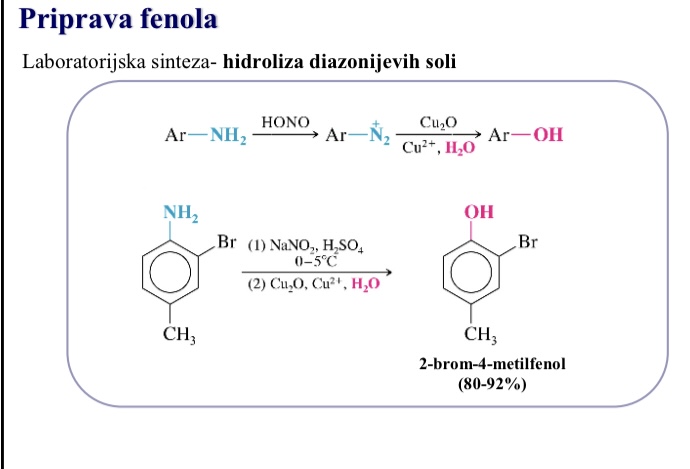
Priprava fenola - laboratorijska sinteza
Hidroliza diazonijevih soli
Koji je spoj kiseliji fenol ili cikloheksanol
Fenol je znatno kiseliji od cikloheksanola
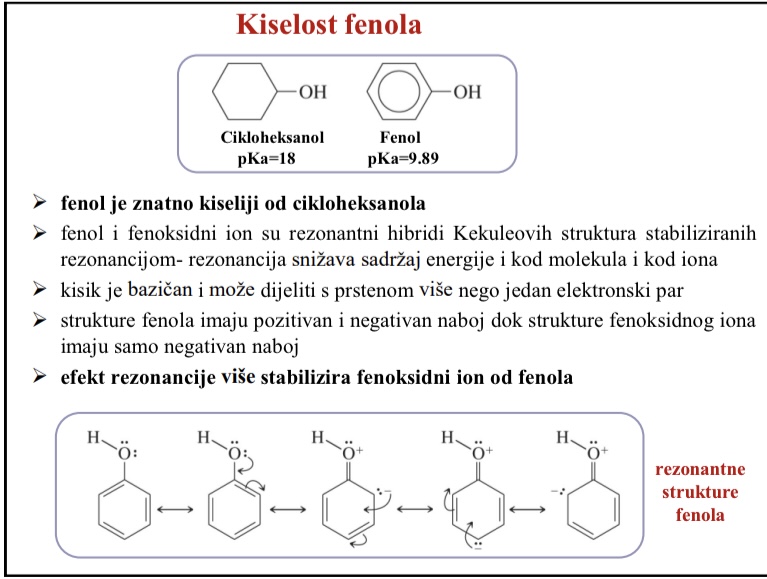
Kako su fenol i fenoksidni ion povezani s rezonancijom i kiselosti
Fenol i fenoksidni ion su rezonantni hibridi Kekuleovih struktura stabiliziranih rezonancijom
Rezonancija snizava sadrzaj energije i kod molekula i kod iona
Razlika struktura fenola i fenoksidnog iona povezano s kiselosti
Kisik je bazican i moze dijeliti s prstenok vise nego jedan elektronski par
Strukture fenola imaju pozitivan i negativan naboj dok strukture fenoksidnog iona imaju samo negativan naboj
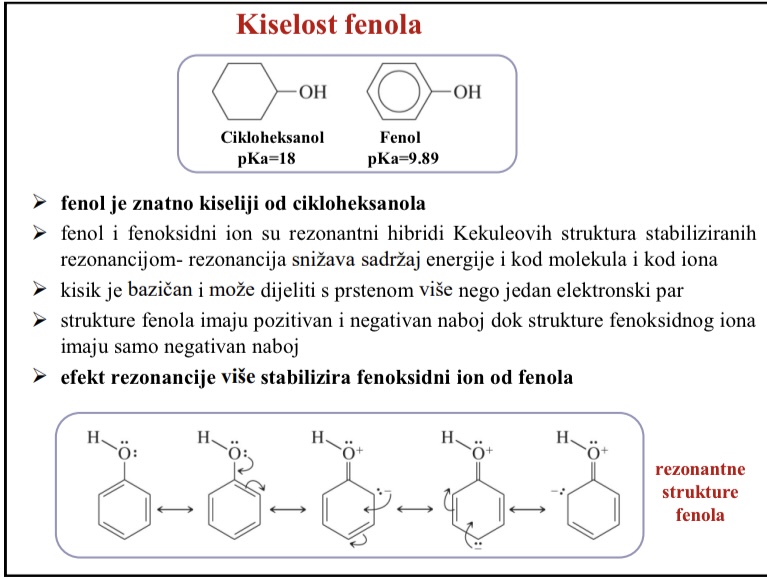
Koji je stabilniji fenol ili fenoksidni ion
Efekt rezonancije vise stabilizira fenoksidni ion od fenola
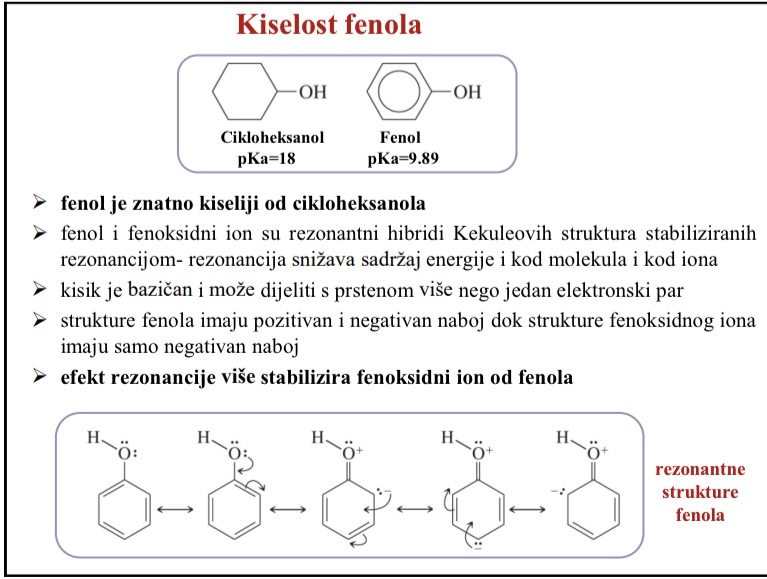
Koliko ima rezonantnih struktura fenoksidnog iona
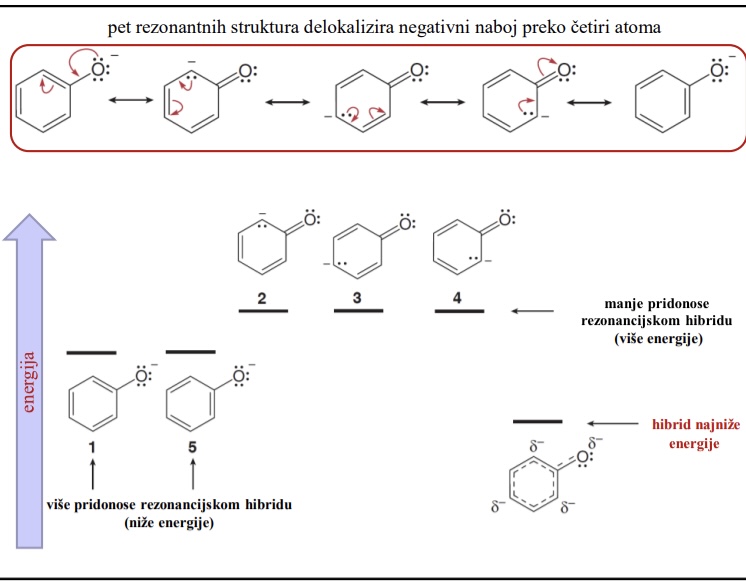
Pet rezonantnih struktura delokalizira negativni naboj preko cetiri atoma
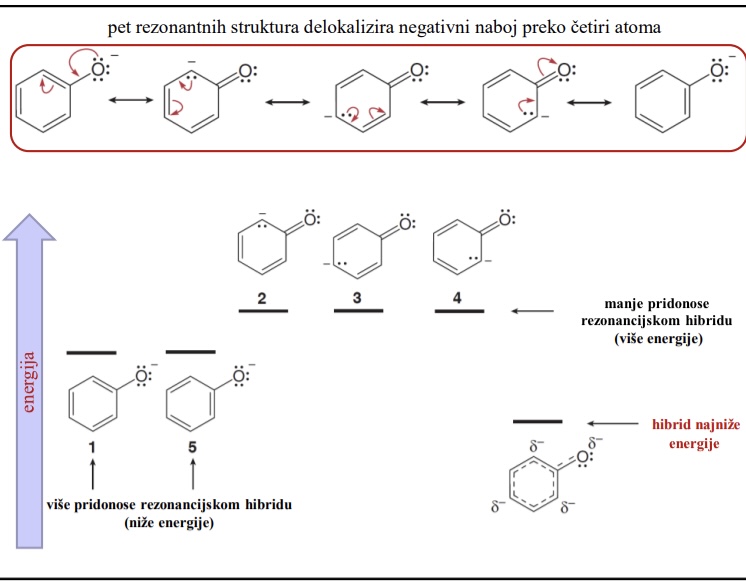
Koje rezonantne strukture fenoksidnog iona vise doprinose rezonancijskim hibridu
Nize energije koje imaju negativan naboj na elektronegativnijem atomu O
Razlika u kiselosti fenola, alkohola i karboksilnih kiselina - kako su topljivi u vodenoj otopini NaOH
Fenoli su topljivi u vodenoj otopini NaOH zbog njihove relativno visoke kiselosti
Vecina alkohola nije topljiva u vodenoj otopini NaOH

Razlika u kiselosti fenola, alkohola i karboksilnih kiselina - mogu li se alkoholi koji nisu topljivi u vodi odvojiti od fenola
Alkoholi koji nisu topljivi u vodi mogu se odvojiti od fenola ekstrakcijom fenola u vodenoj otopini NaOH

Razlika u kiselosti fenola, alkohola, karboksilnih kiselina - topjivost u vodenoj otopini NaHCO3
Fenoli nisu dovoljno kiseli da bi bili topljivi u vodenoj otopini natrijevoga hidrogenkarbonata NaHCO3
Karboksilne kiseline su topljive u NaHCO3

Razlika u kiselosti fenola, alkohola i karboksilnih kiselina - poredaj po kiselosti
RCOOH> ArOH > H2O

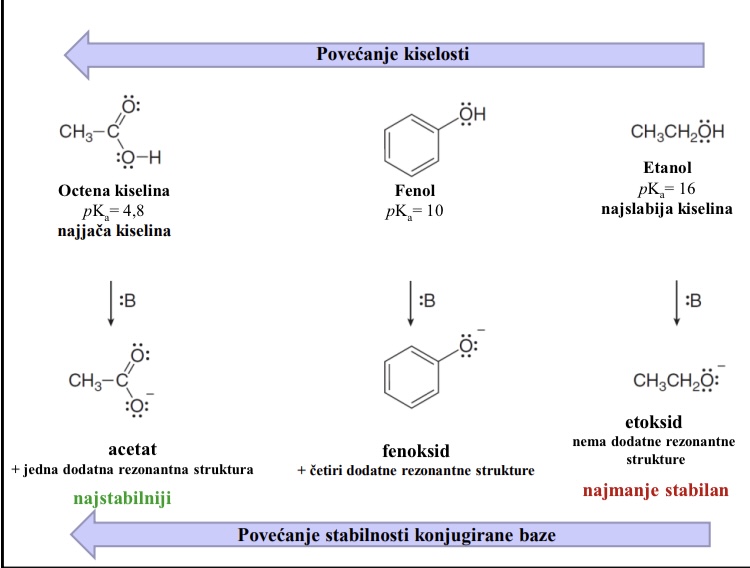
Dodatkom baze na octenu kiselinu, fenol i etanol koje konjugirane baze nastaju i kakve su njihove kisleosti i stabilnosti
Octena kiselina - najjaca kiselina - produkt acetat +jedna rezonantna struktura - najstabilniji
Fenol - srednja kiselost - produkt fenoksid + cetiri rezonantne strukture - srednje stabilna konjugirana baza
Etanol - najslabija kiselina - produkt etoksid nema dodatne rezonantne strukture - najmanje stabilna konjugirana baza
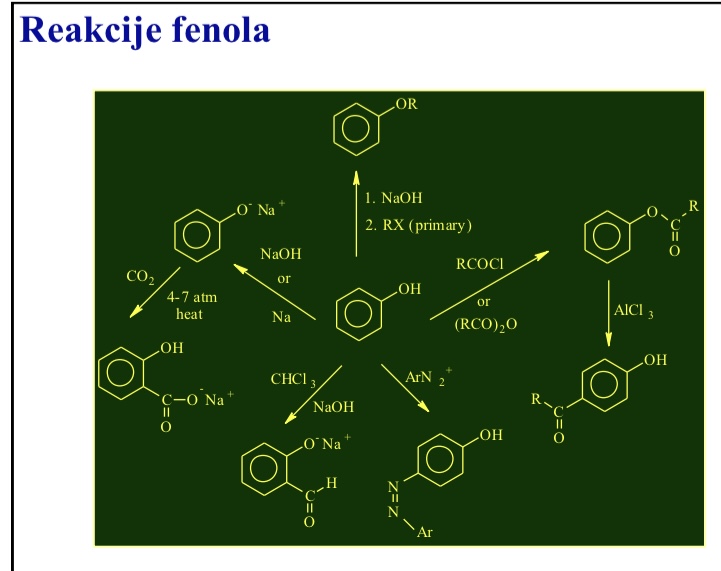
Reakcije fenola
Nastajanje soli
Williamsonova sinteza
Dobivanje estera
Supstitucija u prstenu
Kopulacija s diazonijevim solima
Oksidacija u kinone

Koje su reakcije fenola - supstitucija u prstenu (6)(EAS kod benzena)
Halogeniranje
Nitriranje
Nitroziranje
Sulfoniranje
Friedel-Craftsovo alkiliranje
Friedel-Craftsovo aciliranje: Friesova pregradnja
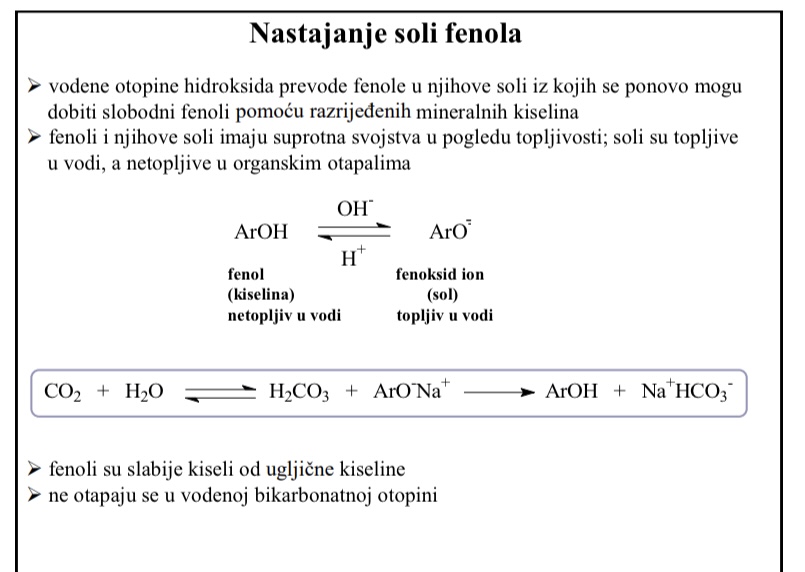
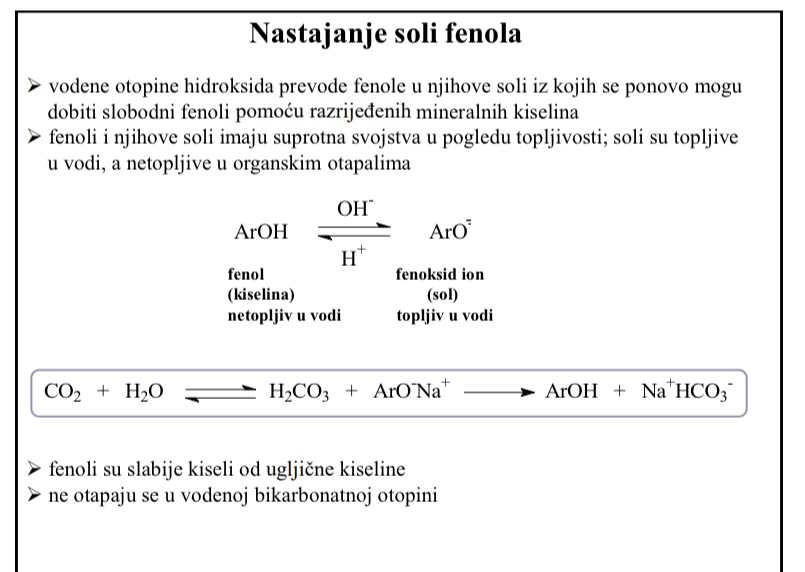
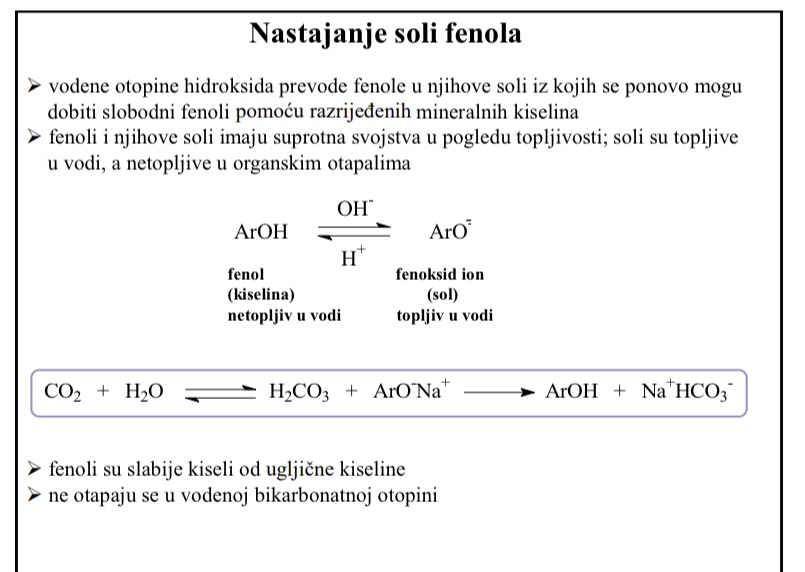
Nastajanje soli fenola
Vodene otopine hidroksida prevode fenole u njihove soli
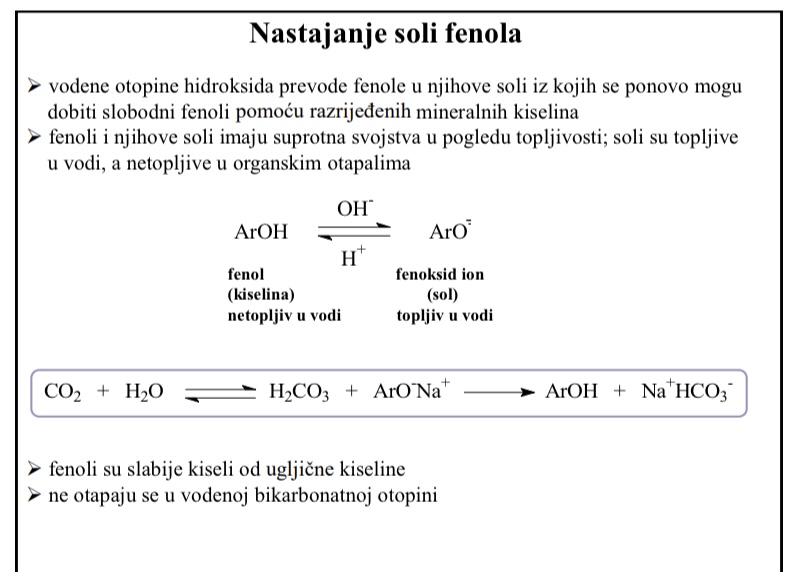
Kako se iz soli mogu opet dobiti fenoli
Iz soli se ponovno mogu dobiti slobodni fenoli pomocu razrijedenih mineralnih kiselina
Kakva su svojstva fenola imaju pozitivan njihovih soli s obzirom na topljivost
Fenoli i njihove soli imaju suprotna svojstva u pogledu topljivosti: soli su topljive u vodi, a netopljive u organskim otapalima
Kakva je kiselost fenola u usporedbi s ugljicnom kiselinom
Fenoli su slabije kiseli od ugljicne kiseline
Ne otapaju se u vodenoj bikarbonatnoj otopini
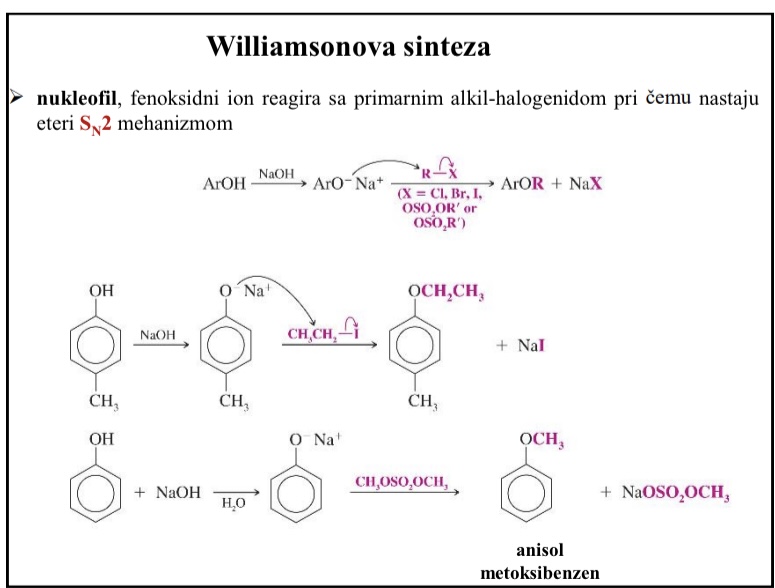
Williamsonova sinteza
Nukleofil, fenoksidni ion reagira sa primarnim alkil-halogenidom pri cemu nastaju eteri SN2 mehanizmom
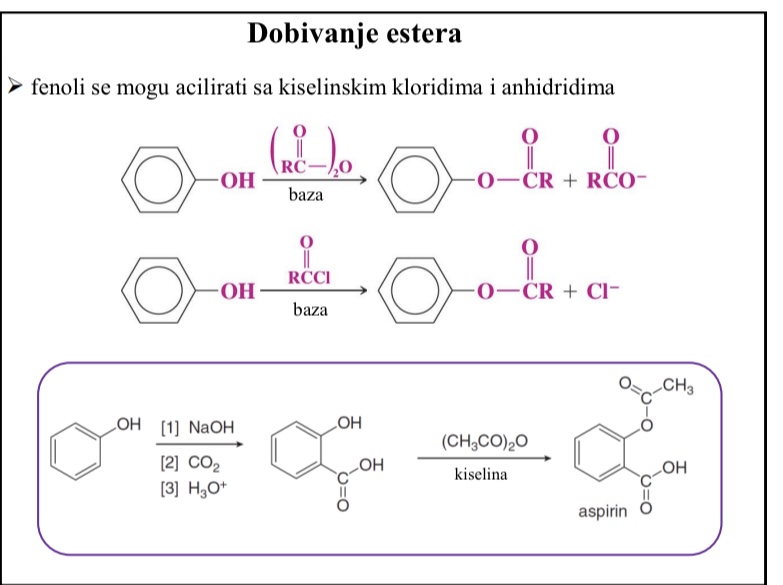
Dobivanje estera
Fenoli se mogu acilirati sa kiselinskim kloridima i anhidridima
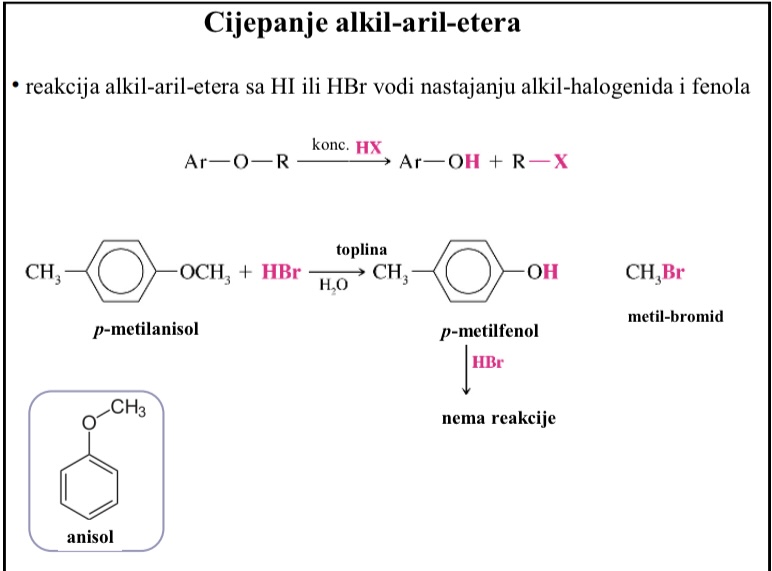
Cijepanje alkil-aril-etera
Reakcija alkil-aril-etera sa HI ili HBr vodi nastajanju alkil-halogenida i fenola
Nabroji reakcije elektrofilne aromatske supstitucije (6)
Nitriranje
Sulfoniranje
Halogeniranje
Alkiliranje
Aciliranje
Nitroziranje

Sto se dodaje s fenolom u nitriranju
razr. HNO3 u H2O ili CH3CO2H

Sto se dodaje s benzenom u nitriranju
HNO3 / H2SO4
Sto se dodaje s fenolom u sulfoniranju
konc. H2SO4
Sto se dodaje s benzenom u sulfoniranju
*H2SO4 ili SO3/ H2SO4
*dimeca sumporna kiselina ili oleum-kiselina
Dimeca sumporna kiselina
Oleum-kiselina koja sadrzi vise trioksida nego sto odgovara azeotropnoj smjesi, dimi se zbog njegovog viska
Sto se dodaje s fenolom u halogeniranju
X2
Sto se dodaje s benzenom u halogeniranju
X2 / Fe ili FeX3
Sto se dodaje s fenolom u alkiliranju
ROH / H+ ili RCl /AlCl3
Sto se dodaje s benzenom u alkiliranju
RCl / AlCl3
Sto se dodaje s fenolom u aciliranju
RCOCl / AlCl3
Sto se dodaje s benzenom u aciliranju
RCOCl / AlCl3
Sto se dodaje s fenolom u nitroziranju
vod. otop. NaNO2/H+
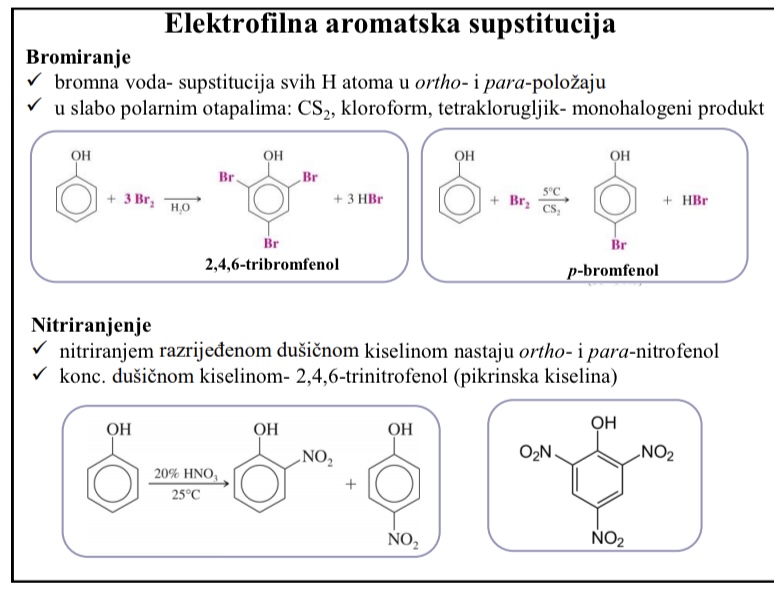
Elektrofilna aromatska supstitucija - bromiranje
Bromna voda - supstitucija svih H atoma u ortho i para polozaju
U slabo polarnim otapalima (CS2, kloroform, tetraklorugljik - monohalogeni produkt)
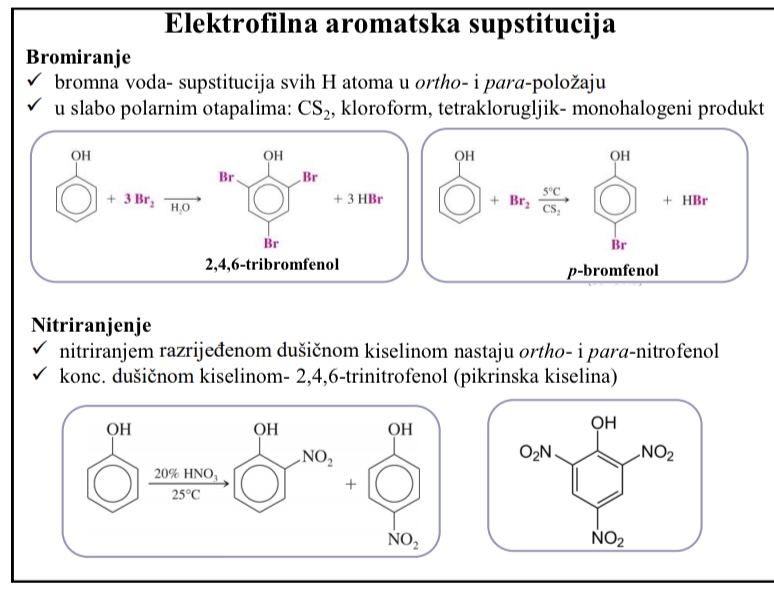
Elektrofilna aromatska supstitucija - nitriranje
Nitriranjem razrijedenom dusicnom kiselinom nastaju ortho i para-nitrofenol
Konc. Dusicnom kiselinom 2,4,6-trinitrofenol (pikrinska kiselina)
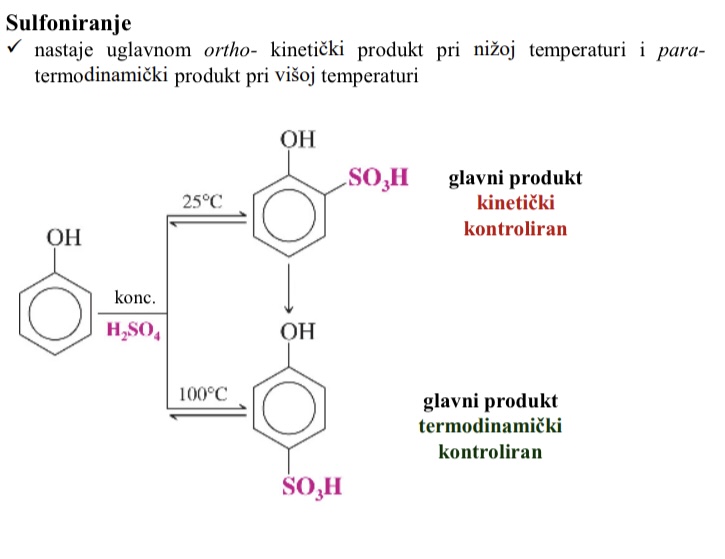
Sulfoniranje - sto nastaje
Nastaje uglavnom ortho kineticki produkt pri nizoj temperaturi
I para termodinamicki produkt pri visoj temperaturu
Nitroziranje - sinteza p-nitrozofenola - nitrozonijev ion
Nitrozonijev ion je slabo reaktivan, supstitucija se moze izvesti samo na aktiviranim supstratima (naftol, fenol, N,N-dimetilanilin)

Nitroziranje - sinteza p-nitrozofenola - nitrozo-spojevi
Nitrozo-spojevi se lako oksidiraju u nitro-spojeve i reduciraju u amine, meduprodukti su za dobivanje tih spojeva

Razlika C-aciliranje i O- aciliranje
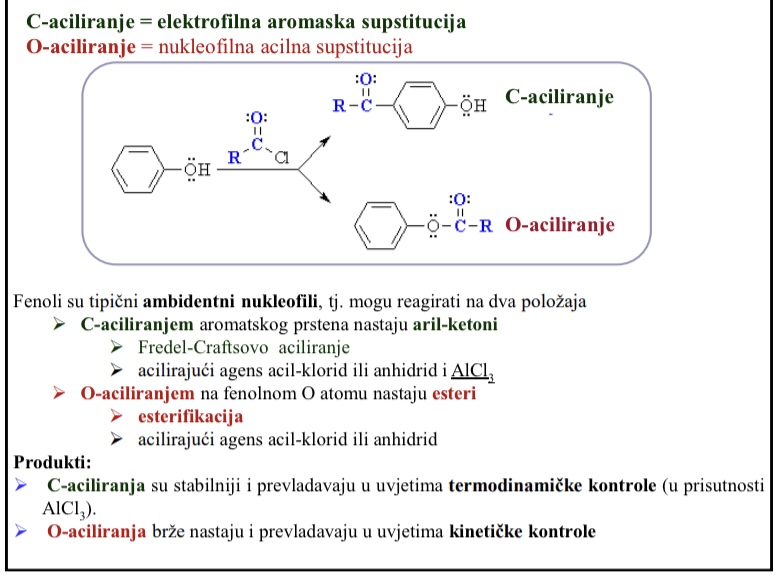
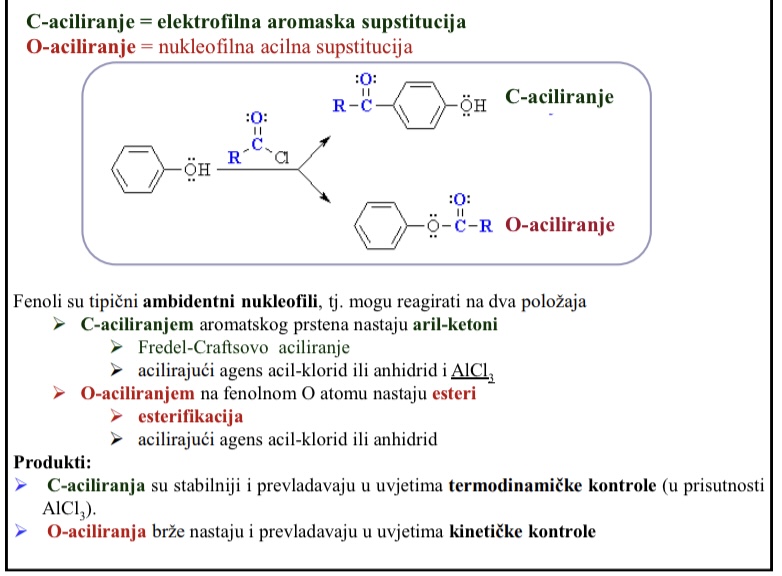
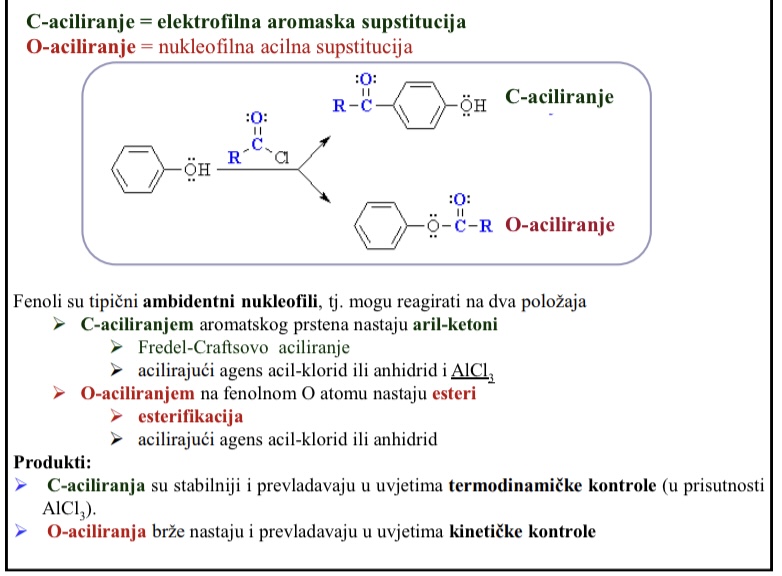
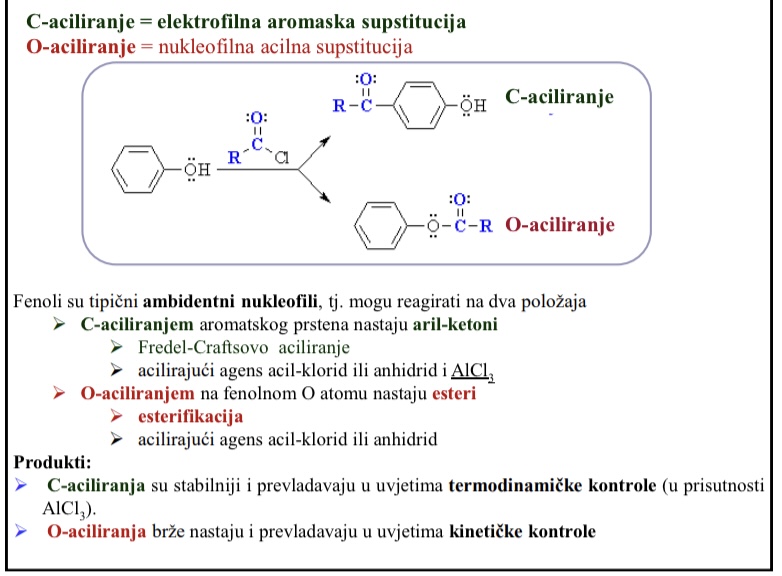
C- aciliranje = elektrofilna aromatska supstitucija
O-aciliranje = nukleofilna acilna supstitucija
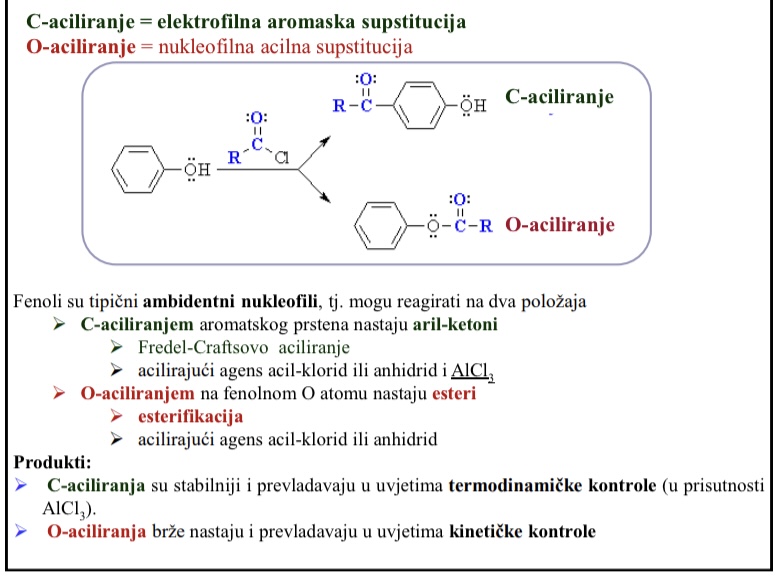
Ambidentni nukleofili
Fenoli su tipicni ambidentni nukleofili - mogu reagirati na dva polozaja;
C-aciliranje, O-aciliranje
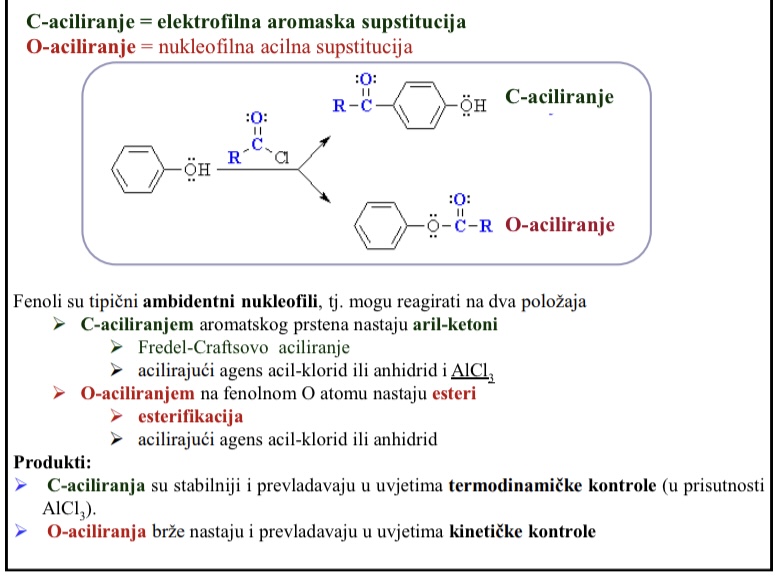
Sto je C-aciliranje
C- aciliranjem aromatskog prstena nastaju aril-ketoni
(Friedel-Craftsovo aciliranje)
Acilirajuci agens acil-klorid ili anhidrid i AlCl3
Sto je O-aciliranje
O-aciliranjem na fenolnom O atomu nastaju esteri
(Esterifikacija) acilirajuci agens acil-klorid ili anhidrid
Produkti C-aciliranja, kakvi su u kojim uvjetima prevladavaju
Produkti C-aciliranja su stabilniji i prevladavaju u uvjetima termodinamicke kontrole (u prisutnosti AlCl3)
Produkti O-aciliranja - kako nastaju u kojim uvjetima prevladavaju
Produkti O-aciliranja brze nastaju i prevladavaju u uvjetima kineticke kontrole
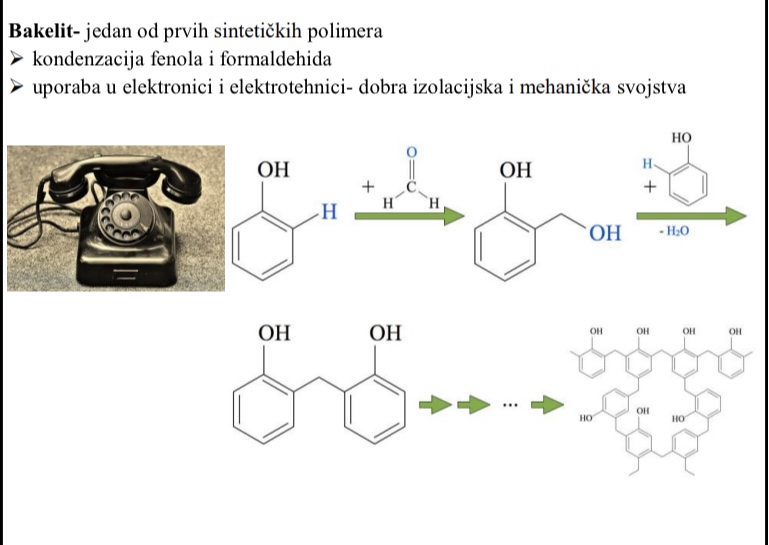
Bakelit - sto je kako nastaje i uporaba
Jedan od prvih sintetickih polimera
Nastaje kondenzacijom fenola i formaldehida
Upotrebljava se u elektronici i elektrotehnici - dobra izolacijska i mehanicka svojstva
Kolbeova reakcija
Klobeovom reakcijom iz natrijevog fenoksida nastaje salicilna kiselina (sintetski prekursor za acetilsalicilnu kiselinu / aspirin)
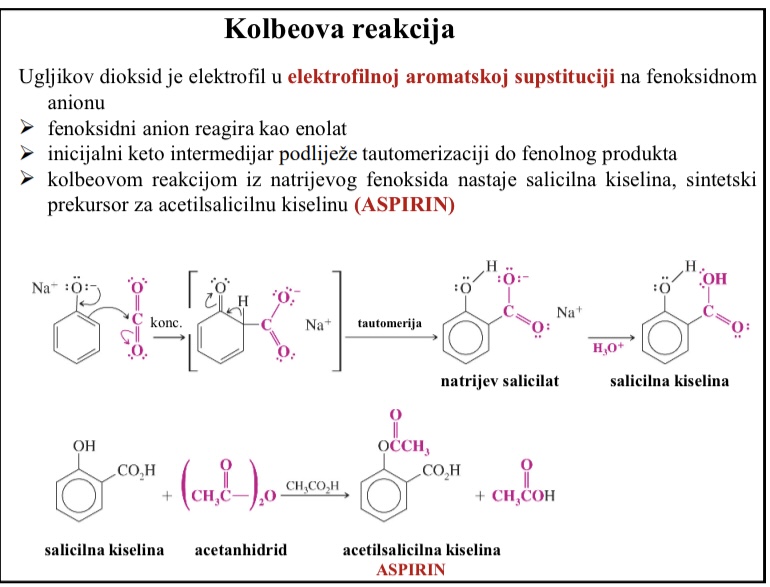
Kolbeova reakcija sto je u reakciji ugljikov dioksid
Ugljikov dioksid je elektrofil u elektrofilnoj aromatskoj suspstituciji na fenoksidnom anionu
Mehanizam Kolbeove reakcije
EAS
ugljikov dioksid elektrofil
Fenoksidni anion reagira kao enolat
Inicijalni keto intermedijer podlijeze tautomerizaciji do fenolnog produkta
Natrijev salicilat
Salicilna kiselina