Pré-requis
0.0(0)
Studied by 0 peopleCard Sorting
1/94
Earn XP
Description and Tags
Last updated 6:51 PM on 9/22/22
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
95 Terms
1
New cards
A. Noms et symboles des éléments
2
New cards
Comment sont ranger les éléments du tableau périodique/ Mendeleïev?
les élément y sont rangés par ordre croissant de nombre atomique (nombre de protons ou d'électrons)
3
New cards
régles d'écriture des symboles des éléments
abréviations constituées d'une majuscule, eventuellement suivie d'une minsucule & qui rappele certaines lettres du nom français, latin ou allemand de l'élément
4
New cards
S=
soufre
5
New cards
Sodium=
Na
6
New cards
Na=
natrium
7
New cards
comment est conseiller d'étudier les noms et les symboles des éléments?
En les groupant par familles ( colonnes du tableau périodiques)
8
New cards
GROUPES PRINCIPAUX
9
New cards
1(IA)
l'Hydrogène H & les alcalins: Li (lithium), Na (sodium), K (potassium), Rb (rubidium), Cs (césium), Fr (francium = radioactif)
10
New cards
2(IIA)
les alcalino-terreux: Be (béryllium), Mg (magnésium), Ca (calcium), Sr (strontium), Ba (baryum), Ra (radium = radioactif)
11
New cards
13 (IIIA)
Les terreux: B (bore), Al (aluminium), Ga (gallium), In (indium), Tl (thallium)
12
New cards
14 (IVA)
Les carbonides: C (carbone), Si (silicium), Ge (germanium), Sn ( étain), Pb (plomp)
13
New cards
15 (VA)
les azotides: N (azote), P (phosphore), As (arsenic), Sb (antimoine), Bi (bismuth)
14
New cards
16 (VIA)
les sulfurides / chalcogènes: O (oxygène) , S (soufre) , Se (sélénium) , Te (tellure), Po (polonium = radioactif)
15
New cards
17 (VIIA)
les halogènes: F(fluor) , Cl(chlore) , Br (brome) , I(iode) , At (astate = radioactif)
16
New cards
18 (VIIIA)
les gaz nobles/rares: He (hélium), Ne (néon), Ar(argon), Kr(krypton), Xe(xénon), Rn (radon =radioactif)
17
New cards
les éléments radioactifs
Fr (francium) , Ra(radium) , Po(polonium) , At(astate) , Rn(radon)
18
New cards
GROUPES TRANSITOIRES
19
New cards
les métaux de transition les plus courants
Cr(chrome) , Mn(manganèse) , Fe(fer) , Co(cobalt) , Ni(nickel) , Cu(cuivre) , Zn(zinc)
20
New cards
les métaux de transition lourds
Pd(palladium) , Pt(platine) , Ag(argent) , Au(or) , Cd(cadmium) , Hg(mercure)
21
New cards
GROUPES SUBTRANSITOIRES
22
New cards
Les lanthanides/terres rares
Ce (cérium) + les 13 éléménts aprés
23
New cards
Les actinides
Th(thorium) , U(uranium) , Pu(plutonium) + les éléments aprés = Sont tous radioactif
24
New cards
B. Noms et formules des corps simples
25
New cards
Quelles sont les 4 catégories de corps simples
Gaz nobles, non-métaux, semi-métaux, métaux
26
New cards
Gaz nobles
He , Ne , Ar , Kr , Xe , Rn
27
New cards
Non-métaux
F , Cl , Br , I , O , S , N , P , C , H
28
New cards
Semi-métaux
B , Si , Ge , As , Sb , Se , Te
29
New cards
Métaux
tous les autres éléments
30
New cards
Combiens d'éléments contient un corps simple
que 1
31
New cards
Comment se présente un corps simple a son état naturel , dans les conditions habituelles d'observations (25°C, 1atm)
sous forme d'atomes ou de molécules constituées de plusieurs atomes de cet élément
32
New cards
Comment se présentes les Gaz Nobles
Leur formule est le symbole de l'éléments, puisque il sons chimiquement inertes ou très peu réactifs ils sont tous monoatomiques
33
New cards
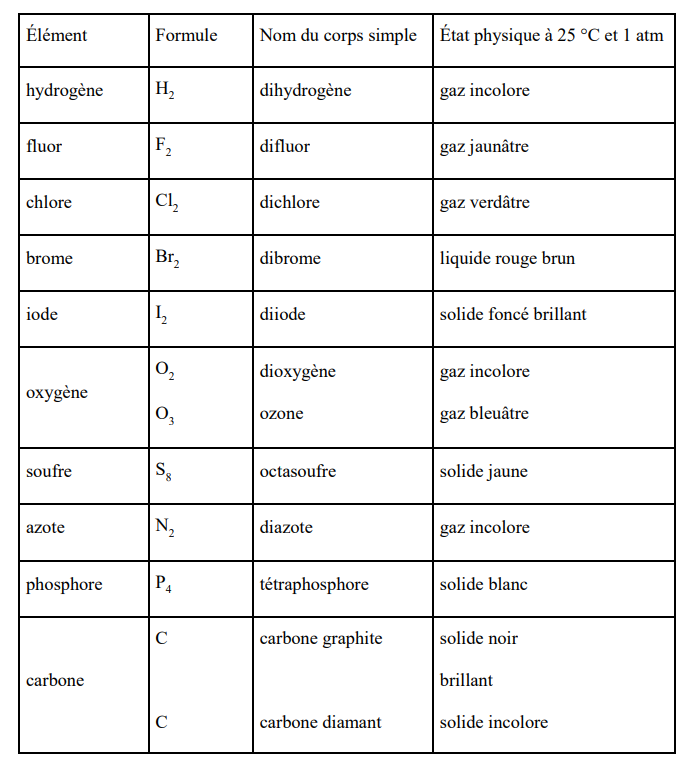
Constitution des Non-metaux
corps simples constitués soit d'un, soit de plusieurs atomes
34
New cards
Constitution Metaux & Semi-metaux
constitués par des nombreux atomes qui mettent en commun les électrons de leur coque valencielle , ils sont représentés par une formule composée simplement du symbole de l'élément correspondant
35
New cards
C. NOMS ET FORMULES DES OXYDES
36
New cards
Quels éléments forment des composés avec l'oxygène?
presque tous
37
New cards
Si un élément peut formes plusiers composés avec l'oxygène....
les proportions des constituants peuvent être indiquées à l'aide de préfixes numériques grecs (mono= généralements omis, di, tri, tétra, penta) précédant les noms des éléments auxquels ils se rapportent
38
New cards
Ce systeme de nomenclature=
généralement utilis pour les composés binaires des non métaux

39
New cards
Le proportios des constituant peuvent être aussi données indirectement....
le nombre d'oxydation ou la valence de l'élément est indiquée par un chiffre romain placé entre parenthèses immédiatement après le nom de l'élément
40
New cards
ce sytsème de l'élément=
généralment utilisé pour les composés des métaux

41
New cards
D. NOMS ET FORMULES DES COMPOSES
42
New cards
les corps composés ->
sont formés de plusiers éléments (ex: NH3, H3PO4,...)
43
New cards
A quoi correspondent ces formules?
souvent à des molecules, par exemple lorsque ces composés sont en phase gazeuse ou en phase liquide
44
New cards
what happens to beacoup de molecules mises en solution aquese?
ils se dissocient partiellement ou totalement en cations chargés positivement et anions chargés négativement
45
New cards
Les cations monoatomiques
ex: Fe2+ (cation fer II)
46
New cards
les cations polyatomiques
NH4+ (cation ammonium)
47
New cards
les anions monoatomiques
ex: Cl- = anion chlorure
48
New cards
les anions polyatomiques
PO3^3-
49
New cards
-ite=.... & -ate=....
le moins oxygéné & le plus oxygéné
50
New cards
s'il existe plus de deux composés...
préfixes hypo- et per-
51
New cards
si l'anion est hydrogéné....
préfixe hydrogéno- ou dihydrogéno-
52
New cards
les acides sont des composés du....
cation H+
53
New cards
RAPPEL DE QUELQUES PROPRIETES
54
New cards
L'HYDROGENE
55
New cards
que'est-ce que rend l'hydrogene different?
c'est le seul élément qui ne peut pas être classe dans aucune famille & il est le plus abondant dans l'univers (le soleil & bcp d'étoiles jeunes sons constitués presque uniquement d'ydrogène
56
New cards
constitution hydrogène naturel
mélange de 3 isotopes: l'hydrogène, le deutérium, tritium (radioactif)
57
New cards
dihydrogène...
= un gaz incolore, environ 15x plus léger que l'air -> échappe à l'attraction terrestre
58
New cards
NON - METAUX
59
New cards
GROUPE 17(VIIA) : LES HALLOGENES
sont si actifs sous formes de corps simples qu'ils n'existent dans la nature que sous formes de composés + caractere oxydant
60
New cards
Dichlore
élément le plus réactif
61
New cards
F2
gaz jaunâtre corrosif qui réagit avec presque tous les éléments à temp ordinaire
62
New cards
dichlore, Cl2
gaz jaune verdâtre
63
New cards
dibrome, Br2
liquide brun rouge très volatil
64
New cards
diiode, I2
solide foncé brillant, forte tension de vapeur
65
New cards
Cl2, Br2
relativement soluble dans l'eau; les solutions de ces halogenes sont appelees eau de chlore et eau de brome
66
New cards
GROUPE 16(VIA) : LES CHALOGENES OU SULFURIDES
67
New cards
whats special about DIOXYGENE
c'est l'élément le plus abondant sur la terre: present en quantites importantes dans latmosphere, dans les océans et dans la plupart des roches
68
New cards
quels corps simples correspondent à cet élément?
Deux -> le dioxugène O2, gaz incolore (21% de l'air, et le trioxygène (ozone) O3, gaz bleuté
69
New cards
oxydes =
des composés de l'oxygène avec tous les éléments (sauf les gaz nobles)
70
New cards
combustions=
les réactions exothermiques avec O2
71
New cards
la function des combustions
c'est l'énergie libérée par la combustion lente des aliments dans les organismes vivants qui leur permet de se développer, d'être animés de mouvement, de maintenir leur temp
72
New cards
Le TRIOXYGENE (OZONE) est
une molécule instable formée lors du passage d'une décharge électrique à
travers O2 (odeur caractéristique) ou par l'action des rayons solaires sur les couches atmosphériques
supérieures. C'est aussi un sous-produit des combustions à haute température dans les moteurs à explosion.
Son caractère très oxydant explique son action corrosive.
travers O2 (odeur caractéristique) ou par l'action des rayons solaires sur les couches atmosphériques
supérieures. C'est aussi un sous-produit des combustions à haute température dans les moteurs à explosion.
Son caractère très oxydant explique son action corrosive.
73
New cards
Le SOUFRE
peut se trouver dans la nature à l'état élémentaire : c'est un solide jaune qui peut exister sous plusieurs formes cristallines
74
New cards
Le soufre se combine avec de très nombreux éléments :
- il oxyde les métaux avec lesquels il forme de nombreux sulfures.
- il réduit les oxydants puissants
- il réduit les oxydants puissants
75
New cards
Le rôle du soufre
essentiel en biochimie + contribuent à la structure des
protéines.
protéines.
76
New cards
GROUPE 15(VA) : LES AZOTIDES
77
New cards
L'AZOTE est
un élément qui a un rôle essentiel aussi bien en chimie minérale qu'en chimie organique.
78
New cards
corps simple correspondant à azote
diazote N2, un gaz incolore, qui constitue 78 % de l'air et est chimiquement inerte vers 25 °C (sauf réactions avec certaines bactéries).
79
New cards
Le PHOSPHORE est
un réducteur qui réagit avec la plupart des non-métaux. Dans la nature, on le trouve toujours à l'état combiné (phosphates).
80
New cards
GROUPE 14(IVA) : LES CARBONIDES
Le carbone forme avec O deux composés gazeux : CO (toxique) et CO2.
La matière vivante a pour base les composés du carbone : l'élément C présente la propriété très remarquable de former un nombre quasi illimité de composés dans lesquels les atomes de carbone sont unis les uns aux autres. Ces composés sont en si grand nombre qu'ils constituent une chimie particulière très vaste : la chimie organique.
La matière vivante a pour base les composés du carbone : l'élément C présente la propriété très remarquable de former un nombre quasi illimité de composés dans lesquels les atomes de carbone sont unis les uns aux autres. Ces composés sont en si grand nombre qu'ils constituent une chimie particulière très vaste : la chimie organique.
81
New cards
METAUX
La réactivité des métaux dépend du nombre d'électrons valenciels : les alcalins et les alcalino-terreux sont extrêmement réducteurs et ne se trouvent jamais à l'état métallique dans la nature,
tandis que certains métaux transitoires "nobles" [Cu, Ag, Au et le groupe du Pt (Ru, Rh, Pd, Re, Os, Ir, Pt)] difficilement oxydables, existent à l'état libre dans la nature.
tandis que certains métaux transitoires "nobles" [Cu, Ag, Au et le groupe du Pt (Ru, Rh, Pd, Re, Os, Ir, Pt)] difficilement oxydables, existent à l'état libre dans la nature.
82
New cards
GROUPE 1(IA) : LES ALCALINS
Les ALCALINS ont un caractère réducteur très important : ils réagissent avec presque tous les non-métaux et leur réaction avec l'eau est tellement vive qu'ils doivent être conservés dans un solvant non polaire (par ex: l’huile, le benzène) à l'abri de la vapeur d'eau contenue dans l'air.
83
New cards
GROUPE 2(IIA) : LES ALCALINO-TERREUX
très réducteurs, ils réagissent avec de nombreux non-métaux et décomposent
l'eau :
l'eau :
84
New cards
GROUPES 3 À 12 (groupes B) : LES MÉTAUX DE TRANSITION
Les métaux de transition sont d'assez bons réducteurs, sauf Cu.
85
New cards
LES OXYDES
86
New cards
le comportement acido-basique des oxydes en solution aqueuse.
La plupart des tableaux périodiques en couleurs indiquent:
bleu = basique
rouge = acide
bleu/rouge = amphotère
blanc = inactif
bleu = basique
rouge = acide
bleu/rouge = amphotère
blanc = inactif
87
New cards
Oxydes acides :
souvent oxydes de non-métaux et de semi-métaux
88
New cards
Une particule qui réagit avec l'eau pour libérer un ion H3O+
est un acide.
89
New cards
Oxydes basiques :
souvent oxydes de métaux
90
New cards
Une particule qui réagit avec l'eau pour libérer un ion OH–
est une base.
91
New cards
Oxydes amphotères :
souvent oxydes de métaux ou de semi-métaux
92
New cards
Une particule qui peut réagir avec des ions H3O+ ou des ions OH–
est amphotère.
93
New cards
Oxydes neutres ou inertes :
souvent oxydes de non-métaux + Il arrive que certains oxydes ne réagissent absolument pas avec l'eau.
94
New cards
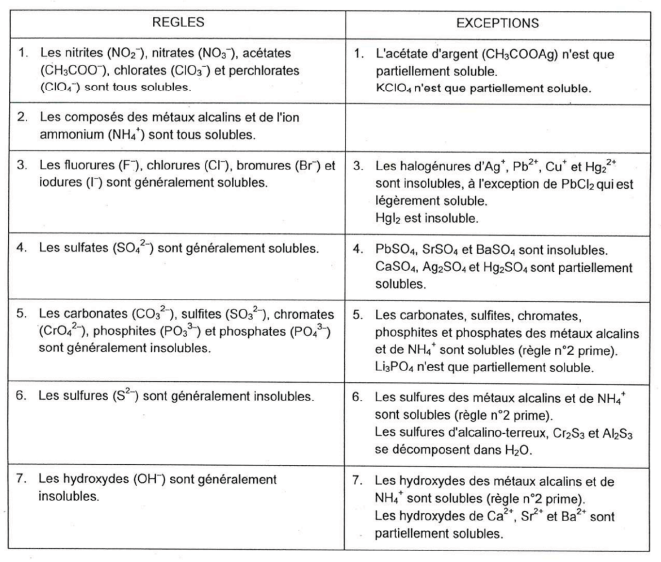
principales règles de solubilité des électrolytes en solution aqueuse à 25°C
95
New cards
Valences:
Le facteurs le plus imp. des reactions, la capacité d'un atome de donner, accepter et échanger electrons pour arriver au stade d'octate : le nombre max de liasons covalentes ou ioniques qu'il peut former on fonctions de sa config. éléctronique. How much can an atom bond with another atom?