Chem parcial 3 (Disoluciones acuosas)
1/55
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
56 Terms
Disoluciones
Mezclas homogeneas de 2 o mas sustancias puras
Soluto
Las demas sustancias
Disolvente
Se encuentra en mayor abundancia
Disolucion acuosa
Es una disolución en la que el disolvente es agua.
Solvatacion
La hidratacion es el proceso por el cual un ion es rodeado por moleculas de agua orientadas en una manera especifica
Disociacion
Pasa cuando una sustancia Ionica se disuelve en agua, el disolvente extrae los iones individuales del cristal y los solvata
Electrolito fuerte
se disocia por completo cuando se disuelve en agua, produce una solucion la cual conduce electricidad
Electrolito debil
se disocia parcialmente en solución acuosa, no posee conductividad eléctrica.
Electrolito fuerte (Ionico & Molecular)
Ionico: Todos
Molecular: Acidos fuertes
Electrolito debil (Ionico & Molecular)
Ionico: Ninguno
Molecular: Acios debiles & bases debiles
No electrolitos (Ionico & Molecular)
Ionico: Ninguno
Molecular: Todos los demas compuestos
Clasificaccion de solutos en solucion acuosa (electrolito fuerte)
HCl, HNO3, HClO4, H2SO4, NaOH, Ba(OH)2, compuestos ionicos
Clasificaccion de solutos en solucion acuosa (electrolito debil)
CH3COOH, HF, HNO2, NH3, H2O
Clasificaccion de solutos en solucion acuosa (no electrolito)
(NH2)2CO (urea), CH3OH (metanol), C2H5OH (etanol), C6H12O6 (glucosa), C12H22O11 (Sacarosa)
Clasificaccion de reacciones quimicas
1) reacciones acido base (Reacciones de neutralizacion)
2) Reacciones de percipitacion
3) Reacciones redox (reacciones de reduccion-oxidacion)
Reacciones de percipitacion
Los iones en los compuestos reactivos se intercambian o trasponen
AgNO3 (ac) + KCl (ac) ⎯→ AgCl (s) + KNO3 (ac)
Solubilidad
Maxima cantidad de solutoa que puede disolverse en 100mL ded agua a una temperatura especifica.
Ecuacion Molecular
Indica los reactivos y productos en su forma molecular
Ecuacion Ionica completa
Todos los elctrolitos fuertes (acidos fuertes, bases fuertes y sales ionicas solubles) se disocian en sus iones
Los unicos iones a la izquierda en la ecuaccion son los que cambian/ reaccionan en el curso de la reaccion.
ejemplo:
Ag+ (ac) + NO3 - (ac) + K+ (ac) + Cl- (ac) ⎯→ AgCl (s) + K+ (ac) + NO3 - (ac)
Iones espectadores
Iones que no cambian (borrados de la ecuaccion Ionica neta)
NO3 - (ac) + K+ (ac) ⎯→ K+ (ac) + NO3 - (ac)
Ecuacion Ionica Neta
Se descarta todo lo que no cambie del lado izquierdo hacia el derecho de la ecuaccion
Ecuaccion Ionica general
Ag+ (ac) + NO3 - (ac) + K+ (ac) + Cl- (ac) ⎯→ AgCl (s) + K+ (ac) + NO3 - (ac)
Ecuaccion Ionica Neta:
Ag+ (ac) + Cl- (ac) ⎯→ AgCl (s)
Percipitado
solido insoluble que se separa de la solucion
7 Acidos
Clorhidrico (HCl)
Bromhidrico (HBr)
Yodhidrico (HI)
Nitrico (HNO3)
Sulfurico (H2SO4)
Clorico (HClO3)
Perclorico (HClO4)
Arrhenius
Definio a las bases como sustancias que aumentan la concentracion de OH- cuando se disuelve en agua
Segun el, un acido es una sustancia que produce iones H+ (H3O+) en solucion acuosa (disociacion o ionizacion directa)
Una base, segun arrhenius, es una sustancia que produce OH- en solucion acuosa (por disociacion o ionizacion directa)
Bronsted y Lowry
Definio bases como aceptadoras de protones
Un acido de bronstead es un donador de protones (debe contener al menos un proton ionizable)
Una base de bronstead es un receptor de protones
Bases Fuertes
Sales metalivas solubles del ion hidroxido
-Metales alacalinos
-Bario
Reacciones acido-base
En una reaccion acido-base, el acido dona un proton (H+) a la base
Acidos monoprotonicos
HCl → H+ + Cl- (electroito fuerte acido fuerte)
HNO3 → H+ + NO3- (Electrolito fuerte, acido fuerte )
CH3COOH→← H+ + CH3COO- (Electrolito debil, acido debil)
Acidos diprotonicos
H2SO4 →H+HSO4- (Electrolito fuerte, acido fuerte)
HSO4→← Electrolito debil, acido debil (Electrolito debil, acido debil)
Acidos triprotonicos
H3PO4→← H+ + H2PO4- (Electrolito debil, acido debil)
H2PO4- →←H+ + H2PO4- (Electrolio debil, acido debil)
H2PO4-2 →←H+PO4-3 (Electrolio debil, acido debil)
reaccion de neutralizacion
acido + base → sal + agua
ejemplo:
HCl (ac) + NaOH (ac)→ NaCl (ac) + H2O
H+ + OH- →H2O
Reacciones con formacion de gases
Alguna reacciones acido-base no dan el producto esperado
𝐶𝑎𝐶𝑂3 (𝑆) + 𝐻𝐶𝑙(𝑎𝑐) → 𝐶𝑎𝐶𝑂2(𝑎𝑐) + 𝐶𝑂2(𝑔) + 𝐻2O(l)
en esta reaccion el producto esperado (H2CO3) se descompone para formar un producto gaseoso (CO2)
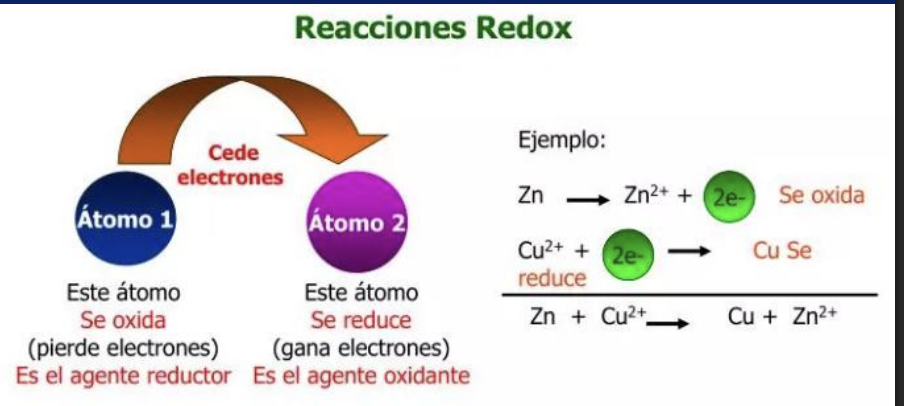
Reacciones redox
Oxido reduccion (redox)
Oxidacion ocurre cuando un atmo o ion pierde elctrones
Una reduccion sucede cuando un atomo o ion gana electrones
una accion no puede ocurrir sin la otra
Numero de oxidacion
La carga que el atomo tendria en una molcula (compuesto ionico) si los electrones de valencia fuesen transferido completamente
Que numero de oxidacion tienen los elementos libres (en estado puro)?
cero
Na, Be, K, Pb, H2 , O2 , P4 = 0
Que numero de oxidacion tienen los iones monoatomicos?
Es igual a la carga del ion
Li+ , Li = +1; Fe3+, Fe = +3; O2- , O = -2
Numero de oxidacion es generalmente de?
-2 en H2O y -1 en O2-2
Numero de oxidacion de hidrogeno
+1
excepcion en hidruros (hidrogeno metal) para ellos es -1
Numero de oxidacion para llos grupo IA y fluor?
IA: +1
Fluor: -1
K + Mg 2+ F –
Cual es la carga en la molcula o ion?
Es la suma de los numeros de oxidacion de todos los atomos en una molecula o ion
Los numeros de oxidacion siempre tienen que ser enteros?
No.
ejemplo:
Numero de oxidacion del oxigeno en el ion peroxido es -1/2
serie de actividad de los metales
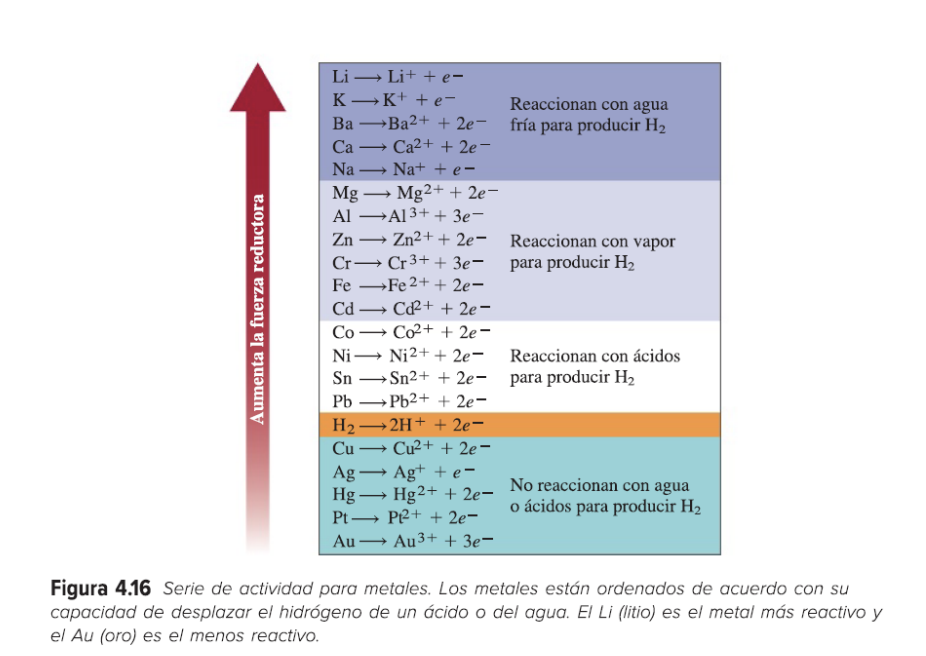
Reacciones de desplazamiento
En este reaccion los iones de plata oxidan el metal cobre
No ocurre la reaccion inversa
Reacciones de oxidacion-reduccion
Reacciones con transferencia de electrones)
Semireaccion de oxidacion
Da electron
ejemplo
Zn(s) + CuSO4(ac)→ ZnSO4(ac) + Cu(s)
Zn →Zn2+ + 2é
Zn se oxida
Zn es el agente reductor
Semireaccion de reduccion
acepta é
Ejemplo:
Zn(s) + CuSO4(ac)→ ZnSO4(ac) + Cu(s)
Cu2+ + 2e- → Cu
Cu2 se reduce
CuSO4 es el agente oxidante
Tipos de reacciones de oxidacion-reduccion
-Combinacion
-Descomposicion
-Combustion
-Desplazamiento
De hidrogeno
de metal
de halogeno
-Desproporcion
Reacciones de combinacion
A+B→C
ejemplo:
0 0 +3 -1
2Al + 3Br2 → 2AlBr3
Reaccion de descomposicion
C→ A+B
Ejemplo:
+1+5-2 +1 -1 0
2KClO3 →2KCl + 3O2
Reaccion de combustion
A+O2→ B
Ejemplo:
0 0 +4 -2
S + O2 → SO2
Reaccion de desplazamiento simple
A+BC→ AC + B
Desplazamiento de hidrogeno
Ejemplo:
0. +1 +2 0
Sr + 2H2O→ Sr(OH)2 + H2
Desplazamiento de metal
Ejemplo:
+4 0 0. +2
TiCl4 + 2Mg→ Ti + 2MgCl2
Desplazamiento de halogeo
Ejemplo:
0. -1. -1. 0
Cl2 + 2KBr → 2KCl + Br2
Reaccion de desproporcion
Elemnto se oxida y se reduce simultaneamento