Parcial 3 Quimica GASES
1/18
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
19 Terms
Elementos que existen como gases a 25°C y 1 atm de presion
H, He, Ne, Ar, Kr, Xe, Rn, Og, F, Cl, O, N
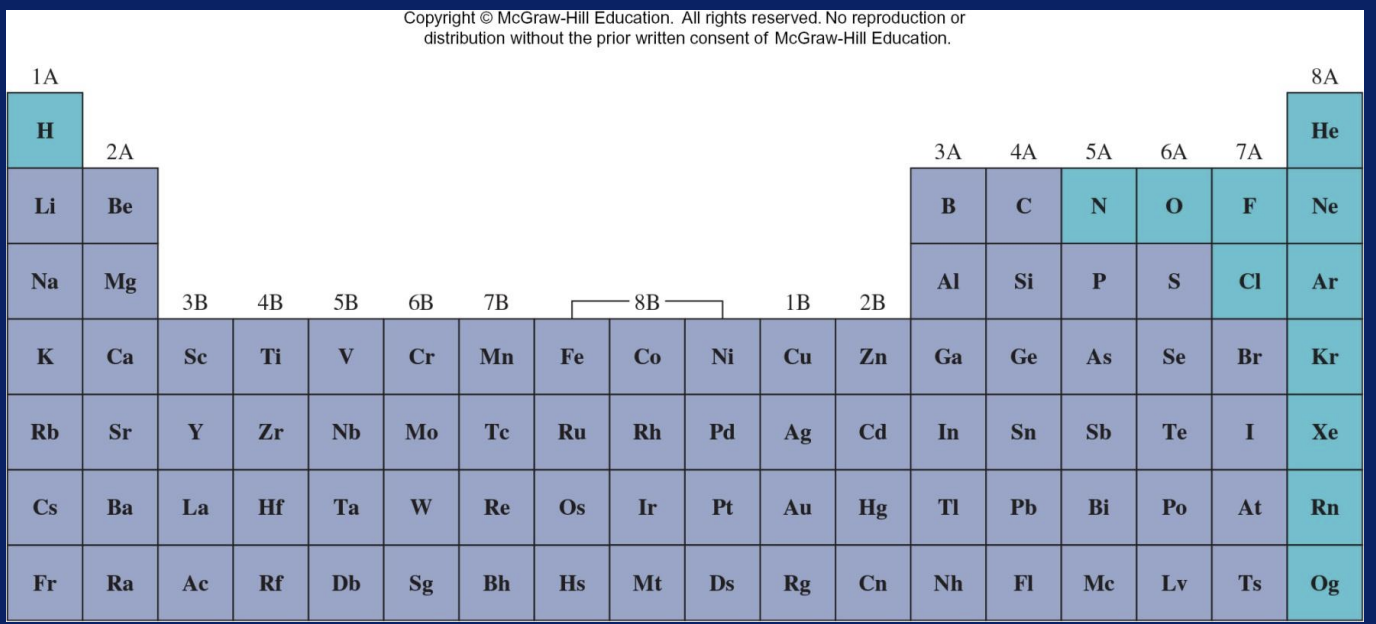
Gases comunes
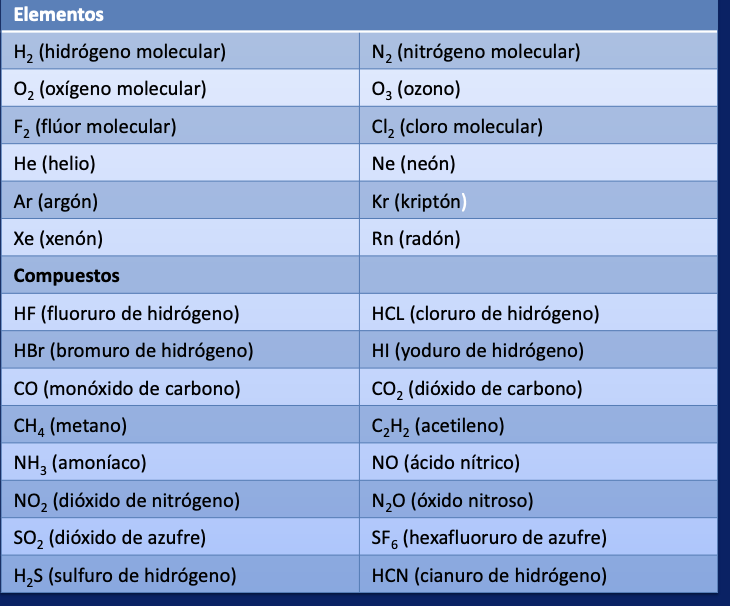
Caracteristicas
-Toman el volumen y forma de sus envases
-son el estado de la materia mas comprimible
-Se mezclan de manera uniforme y completa cuando estan confinados en el mismo envase
- Poseen densidades mucho mas bajas que liquidos y solidos
Presion atmosferica
Presion que ejerce la atmosfera de la tierra sobre la superfice terreste y se mide con barometro
Depende de:
Localizacion (altitud)
Temperatura
Condiciones climaticas
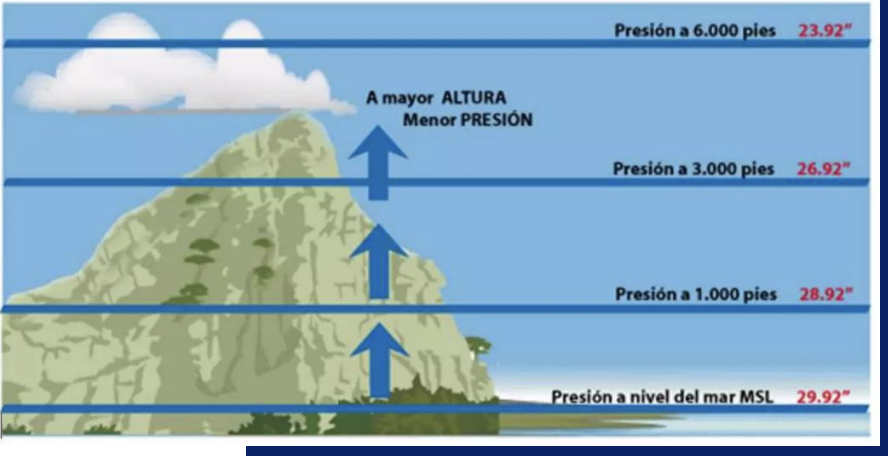
Presion
Presion= fuerza/ area
Fuerza
mase x aceleracion
Leyes de gases ideales: Ley de Boyle
Relaciona la presion y el volumen
La presion de una cantidad fija de gas a temperatura constante es inversamente proporcional al volmuen del gas
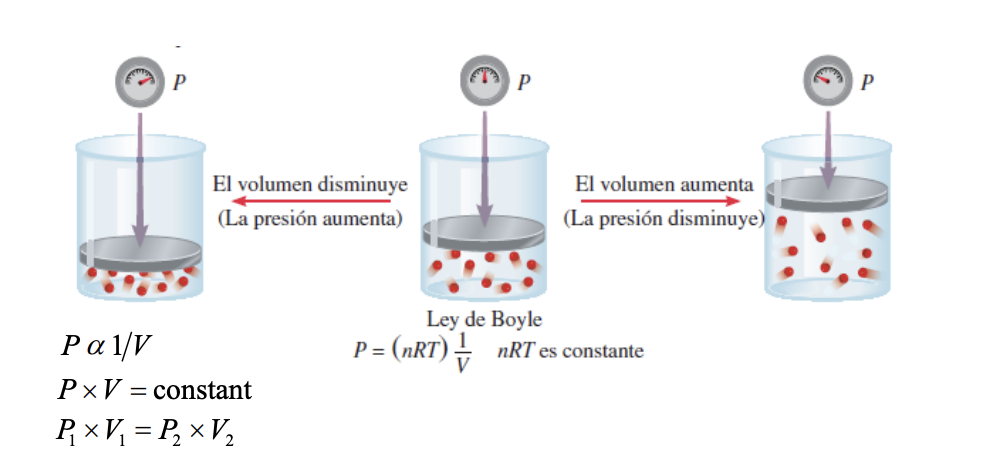
Leyes de gases ideales: Ley de charles
Relaciona la temperatura y el volumen
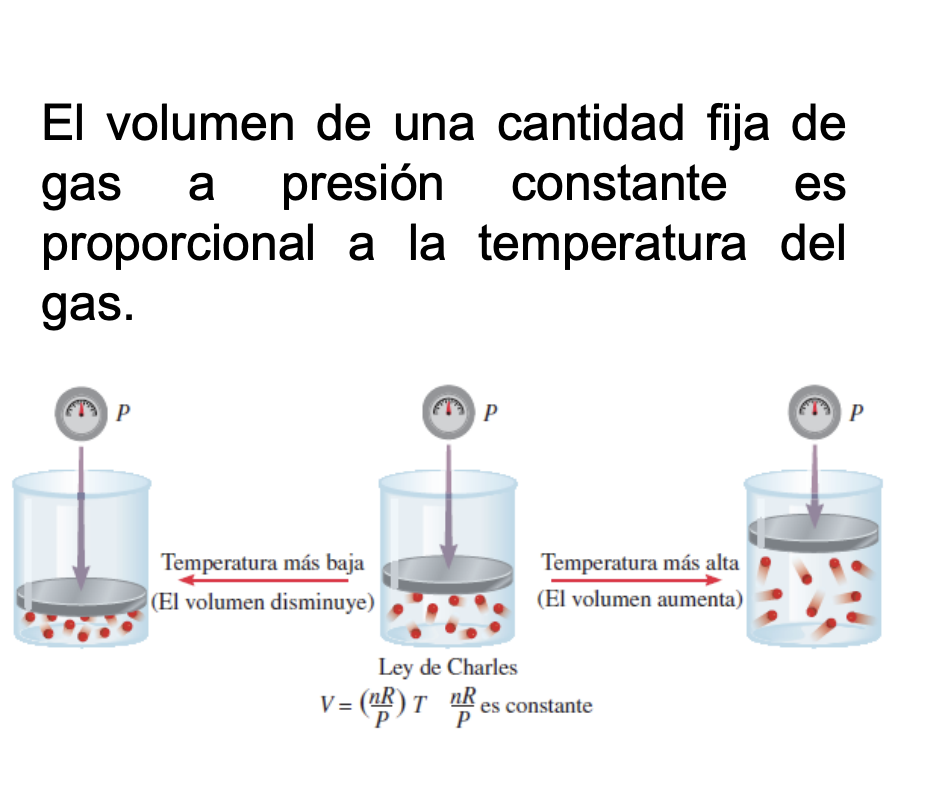
El volumen de una cantidad fija de gas a presion constante es proporcional a la temperatura del gas
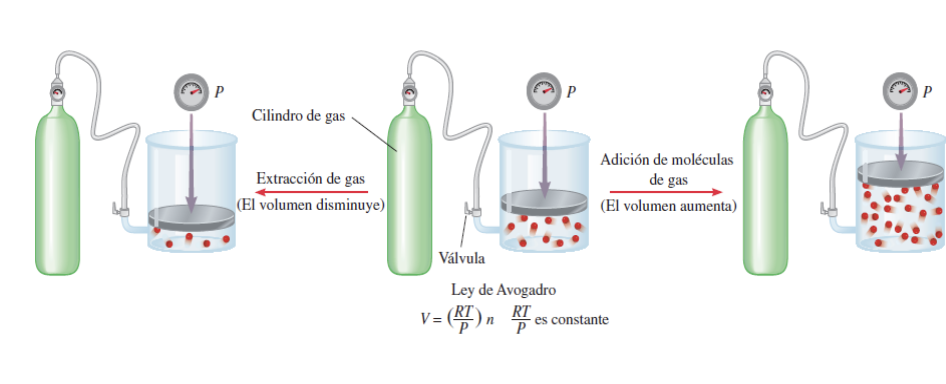
Leyes de gases ideales: Ley de avogadro
Relaciona el volumen y la cantidad de gas
V α moles del gas (n)
A presion y temp. constantes, el volumen de un gas es directamnete proporcional a la cantidad de moles de gas presente
Ecuacion de gases ideales que es?
Explica la relacion entre las 4 variables P,V,T y n
Un gas ideal es un gas hipotetico cuyo comportamiento de presion, volumen y temp, se pueden describir completamente con esta ecuacion
Ecuacion de gases ideales (leyes y constantes)

Ecuacion de gases ideales (terminos)
P: presión en atmósferas (atm)
V: Volumen en litros (L)
n: moles del gas
R: Constante de gases ideales = 0,082 atm L / K mol
T: Temperatura en kelvin (K)
Factos de la ecuacion de gases ideales
-La presion y el volumen de un gas es proporcional directamnete a la cantidad de moles presentes de gas y a la temp. en que se encuentra.
-Si se aumenta los moles del gas y la temp. aumenta la presion y volumen del gas
Temp y presion estandar (TPE)
Las condiones es 0°C y 1atm (TPE)
a TPE 1mol de gas ideal ocupa 22,414L

Temperatura y presion normal (TPN)
Cuando un gas este a temp. 25°C y presion de 1atm se encuentra en condiciones temp y presion normal
Ley de dalton (teoria)
Todos los casos que implican mezcla de gases, la presion total de gases se relaciona con presiones parciales (presiones de componentes gaseosos individuales)
Establece que la presion total de una mezlca de gases es igual a la suma de presiones que cada gas ejercieria si estuviera solo
Ley de dalton (applicacion)
La presion parcial de un gas A y de un gas B Se calcula como:
PA = XA PT
PB = XB PT
Que son XA, XB y PT
Son fracciones moleculares de A y B
PT es la presion total del sitema
PT= PA + PB
Ley de dalton presiones parciales
Para el calculo se deben considerarar fracciones molares (X) de los gases involucrados
XA= nA/ nT
XB= nB/nT
(XA y XB son las fracciones molares de A y B, respectivamente nT represnte los moles totales involucrados)
n=nA + nB