Aminokwasy, peptydy, białka
0.0(0)
Studied by 1 personCard Sorting
1/172
Earn XP
Description and Tags
Last updated 10:04 AM on 11/8/22
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
173 Terms
1
New cards
Aminokwasy z łańcuchami niepolarnymi
AWLIFTMPG
- alanina
- walina
- leucyna
- izoleucyna
- fenyloalanina
- tryptofan
- metionina
- prolina
- glicyna - wyjątek, nie ma łańcucha bocznego
- alanina
- walina
- leucyna
- izoleucyna
- fenyloalanina
- tryptofan
- metionina
- prolina
- glicyna - wyjątek, nie ma łańcucha bocznego
2
New cards
Aminokwasy z łańcuchami niepolarnymi definicja
- zawierają łańcuchy boczne bez grup funkcyjnych (wyj. glicyna)
- hydrofobowe
- hydrofobowe
3
New cards
Aminokwasy z łańcuchami polarnymi bez ładunku
STTCASG
- seryna
- treonina
- tyrozyna
- cysteina
- asparagina
- glutamina
- seryna
- treonina
- tyrozyna
- cysteina
- asparagina
- glutamina
4
New cards
Aminokwasy z łańcuchami polarnymi bez ładunku definicja
grupy -OH, -SH oraz -NH2 cechują się niesymetrycznym (polarnym) rozmieszczeniem ładunków elektrycznych, jednak w fizjologicznym pH nie dysocjują i wykazują zerowy ładunek elektryczny
5
New cards
grupa NH2 w glutaminie i asparaginie
- nie wiąże protonu
- w przedziale fizjologicznym nie jest nośnikiem ładunku elektrycznego
- w przedziale fizjologicznym nie jest nośnikiem ładunku elektrycznego
6
New cards
grupy -OH reszt seryny, treoniny i tyrozyczny
mogą być miejscem wiązania fosforanu, a także uczestniczyć w tworzeniu wiązań wodorowych
7
New cards
grupy -SH cysteiny
zawarte w łańcuchach bocznych, są ważnym elementem składowym miejsc aktywnych wielu enzymów
8
New cards
Miejsce wiązania składników cukrowych na aminokwasach z łańcuchami polarnymi bez ładunku
- grupa amidowa asparaginy
- grupy hydroksylowe seryny i treoniny
- grupy hydroksylowe seryny i treoniny
9
New cards
Aminokwasy z łańcuchami kwasowymi
- kwas asparaginowy
- kwas glutaminowy
- kwas glutaminowy
10
New cards
Aminokwasy z łańcuchami kwasowymi definicja
Łańcuchy boczne tych aminokwasów zawierają grupy karboksylowe. W obojętnym pH ulegają pełnej dysocjacji i stają sięnośnikami ładunku ujemnego.
11
New cards
Aminokwasy z łańcuchami zasadowymi
LAH
- lizyna
- arginina
- histydyna
- lizyna
- arginina
- histydyna
12
New cards
Aminokwasy z łańcuchami zasadowymi definicja
Ich łańcuchy boczne zawierają grupy wiążące protony
- grupa E-aminowa lizyny
- grupa guanidynowa argininy
- pierścień imidazolowy histydyny
- grupa E-aminowa lizyny
- grupa guanidynowa argininy
- pierścień imidazolowy histydyny
13
New cards
Aminokwasy egzogenne
aminokwasy, które nie są syntezowane w organizmie ludzkim a ich obecność i odpowiednie stężenie w białkach spożywczych decyduje o wartości spożywczej
- Wal
- Leu
- Ile
- Liz
- Met
- Thr
- Phe
- Trp
- Wal
- Leu
- Ile
- Liz
- Met
- Thr
- Phe
- Trp
14
New cards
Aminokwasy endogenne
aminokwasy syntetyzowane w organizmie ludzkim
- Gly
- Ala
- Tyr
- Asp
- Glu
- Gln
- Pro
- Cys
- Arg
- His
- Gly
- Ala
- Tyr
- Asp
- Glu
- Gln
- Pro
- Cys
- Arg
- His
15
New cards
Aminokwasy proteogenne
Aminokwasy dla których w kodzie genetycznym są zawarte kodony
16
New cards
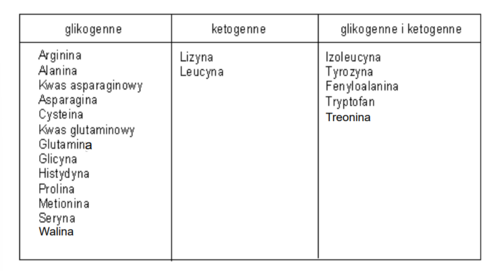
Aminokwasy glikogenne
ich metabolizm prowadzi do wytwarzania glukozy
17
New cards
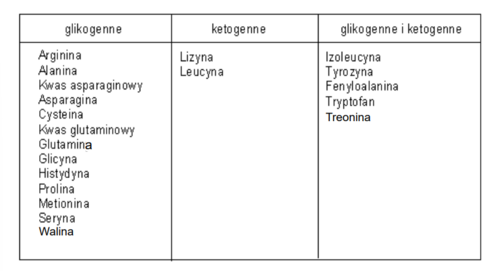
Aminokwasy ketogenne
Ich metabolizm prowadzi do wytwarzania związków ketonowych
18
New cards
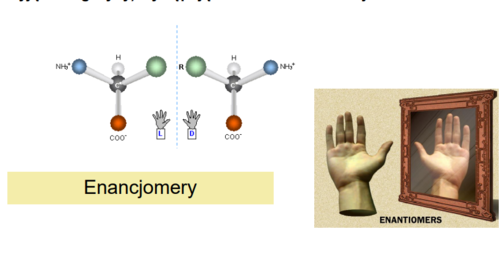
Właściwości optyczne aminokwasów
Enancjomery
- aminokwasy to związki optycznie czynne
- ich roztwory skręcają płaszczyznę światła spolaryzowanego
- aminokwasy to związki optycznie czynne
- ich roztwory skręcają płaszczyznę światła spolaryzowanego
19
New cards
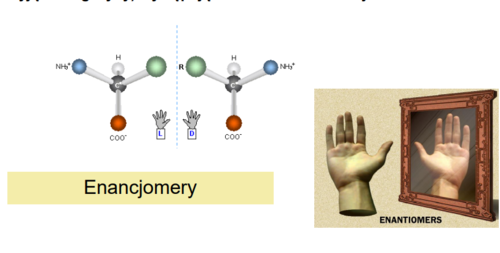
Węgiel alfa każdego aminokwasu (podaj też wyjątek)
Węgiel alfa każdego aminokwasu jest węglem asymetrycznym - wiąże cztery różne podstawniki
wyjątek: GLICYNA - nie zawiera węgla asymetrycznego -> optycznie nieczynna
wyjątek: GLICYNA - nie zawiera węgla asymetrycznego -> optycznie nieczynna
20
New cards
W jakiej formie występują niemal wszystkie naturalne aminokwasy?
w formie L (inna to D)
21
New cards
Jaki charakter nadaje aminokwasowi grupa aminowa
zasadowy - wiąże proton przechodząc w kation
22
New cards
Jaki charakter nadaje aminokwasowi grupa karboksylowa
kwasowy - dysocjuje uwalniając proton i przechodząc w anion
23
New cards
Pochodne aminokwasów białkowych powstające przez modyfikację po procesie translacji
- kwas gamma-karboksyglutaminowy (białko osocza krzepnięcie)
- Hydroksylizyna (kolagen)
- hydroksyprolina (kolagen, elastyna)
- pirydynolina, deoksypirydynolina (kolagen)
- 1-metylhistydyna, 3-metylhistydyna (białka mięśni)
- Hydroksylizyna (kolagen)
- hydroksyprolina (kolagen, elastyna)
- pirydynolina, deoksypirydynolina (kolagen)
- 1-metylhistydyna, 3-metylhistydyna (białka mięśni)
24
New cards
Aminokwasy wolne
Nie występujące w białach
- ornityna i cytrulina
- homoseryna i homocysteina
- Beta-alanina
- kwas gamma-aminomasłowy
- tyroksyna i trójjodotyrodonina
- tauryna
- ornityna i cytrulina
- homoseryna i homocysteina
- Beta-alanina
- kwas gamma-aminomasłowy
- tyroksyna i trójjodotyrodonina
- tauryna
25
New cards
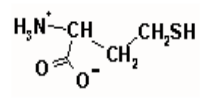
homocysteina
- aminokwas wolny
- bierze udział w metabolizmie aminokwasów i witamin
- bierze udział w metabolizmie aminokwasów i witamin
26
New cards
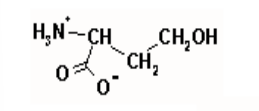
Homoseryna
wolny aminokwas
- bierze udział w metabolizmie aminokwasów
- bierze udział w metabolizmie aminokwasów
27
New cards
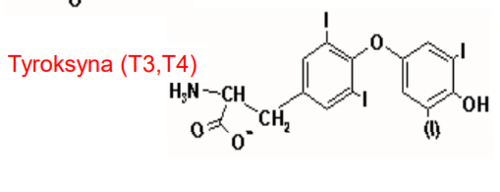
Tyroksyna (T3, T4)
wolny aminokwas, hormon tarczycy
28
New cards
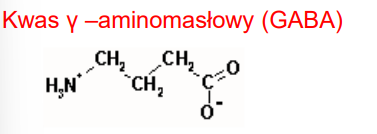
Kwas gamma-aminomasłowy
- inaczej GABA
- Wolny aminokwas
- mózg i inne tkanki
- neurotransmiter
- Wolny aminokwas
- mózg i inne tkanki
- neurotransmiter
29
New cards
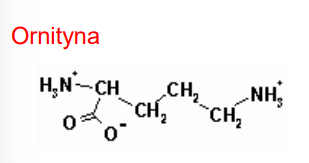
Ornityna
- wolny aminokwas
- bierze udział w syntezie argininy
- bierze udział w syntezie argininy
30
New cards
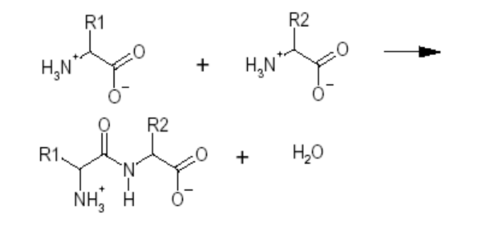
Wiązanie peptydowe
Węgiel grupy alfa-karboksylowej wiąże się z azotem grupy alfa-aminowej pojedynczym wiązaniem
31
New cards
Peptydy biologicznie czynne

32
New cards
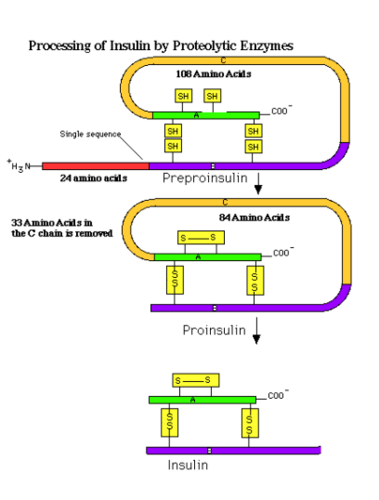
Insulina
- hormon polipeptydowy
- powstaje w komórkach beta wyspek langerhansa w trzustce
- bodziec - podwyższony poziom glukozy we krwi
- rola: obniża poziom cukru we krwi, zwiększa przepuszczalność BK dla glukozy, lipidów i K+
- wpływa na aktywację syntazy glikogenowej
- stymuluje syntezę glikogenu
- hamuje lipolizę i niektóre enzymy biorące udział w glukoneogenezie
- powstaje w komórkach beta wyspek langerhansa w trzustce
- bodziec - podwyższony poziom glukozy we krwi
- rola: obniża poziom cukru we krwi, zwiększa przepuszczalność BK dla glukozy, lipidów i K+
- wpływa na aktywację syntazy glikogenowej
- stymuluje syntezę glikogenu
- hamuje lipolizę i niektóre enzymy biorące udział w glukoneogenezie
33
New cards
Glukagon
- jednołańcuchowy polipeptyd
- 29 aminokwasów
- powstaje w komórkach alfa wysepek Langerhansa
- antagonista insuliny
- stymuluje glikogenolizę i glukoneogenezę - podwyższa poziom cukru we krwi
- właściwości lipolityczne
- bodziec przekazywany poprzez cyklazę adenylanową
- 29 aminokwasów
- powstaje w komórkach alfa wysepek Langerhansa
- antagonista insuliny
- stymuluje glikogenolizę i glukoneogenezę - podwyższa poziom cukru we krwi
- właściwości lipolityczne
- bodziec przekazywany poprzez cyklazę adenylanową
34
New cards
Glutation biosynteza i funkcje
katalizowana przez synterazę glumatylocysteinową i glutationową
- chroni lipidy przed samoiutlenieniem
- aktywator określonych enzymów
- występuje w formie utlenionej i zredukowanej
- chroni lipidy przed samoiutlenieniem
- aktywator określonych enzymów
- występuje w formie utlenionej i zredukowanej
35
New cards
Kalikreina i bradykinina
Peptydy, które:
- rozszerzają naczynia krwionośne
- kurczą mięśnie gładkie przewodu pokarmowego
- rozszerzają naczynia krwionośne
- kurczą mięśnie gładkie przewodu pokarmowego
36
New cards
Angiotensynogen
Peptyd, który zamienia się w Angiotensynę I a ta w Angiotensynę II
- kurczy m. gładkie naczyń krwionośnych
- podnosi ciśnienie krwi
- zwiększa siłę skurcuz m. sercowego
- nasila aktywność AUN (współczulnego)
- reguluje wydzielanie hormonów
- kurczy m. gładkie naczyń krwionośnych
- podnosi ciśnienie krwi
- zwiększa siłę skurcuz m. sercowego
- nasila aktywność AUN (współczulnego)
- reguluje wydzielanie hormonów
37
New cards
Enkefaliny i endorfiny
Pentapeptydy występujące w mózgu wykazujące silne działanie przeciwbólowe
38
New cards
Oksytocyna i wazopresyna
Nanopeptydy wytwarzane przez tylny płat przysadki
- oksytocyna - pobudza czynność skurczową macicy podczas porodu
- wazopresyna - pobudza resorpcję wody w kanalikach nerkowych, kurczy naczynia krwionośne, podnosi ciśnienie krwi
- oksytocyna - pobudza czynność skurczową macicy podczas porodu
- wazopresyna - pobudza resorpcję wody w kanalikach nerkowych, kurczy naczynia krwionośne, podnosi ciśnienie krwi
39
New cards
izomeryczne postacie wiązania peptydowego
dwie rezonujące struktury pozostające we wzajemnej równowadze - wiązanie C-N przechodzi w C=N tak jak C=O przechodzi w C-O
- wiązanie peptydowe jest sztywne i ma cechy wiązania podwójnego o konfiguracji trans
- wiązanie peptydowe jest sztywne i ma cechy wiązania podwójnego o konfiguracji trans
40
New cards
Peptydy jako struktury nierozgałezione
Posiadają dwa charakterystyczne końce:
- koniec N - aminokwas z wolną grupą alfa-aminową
- koniec C - aminokwas z wolną grupą alfa-karboksylową
- koniec N - aminokwas z wolną grupą alfa-aminową
- koniec C - aminokwas z wolną grupą alfa-karboksylową
41
New cards
Peptyd cykliczny
Kiedy grupa końcowa aminokwasu C-końcowego wchodzi w reakcję z grupą aminową aminokwasu N-Końcowego
42
New cards
nazewnictwo peptydów
1) nazwa reszty aminokwasu N-końcowego
2) nazwy kolejnych reszt aminokwasowych
3) Nazwa aminokwasu C-końcowego w jej oryginalnym brzmieniu
2) nazwy kolejnych reszt aminokwasowych
3) Nazwa aminokwasu C-końcowego w jej oryginalnym brzmieniu
43
New cards
Nazwij tetrapeptyd o sekwencji aminokwasowej Arg-Lys-Val-Leu
Arginylolizylowaliloleucyna
44
New cards
Glutation
Tripeptyd składający się z trzech reszt aminokwasowych
- glutaminian - aminokwas N-końcowy
- cysteina
- glicyna
- glutaminian - aminokwas N-końcowy
- cysteina
- glicyna
45
New cards
Wiązanie pomiędzy glutaminianem a cysteiną w glutationie
nietypowe - nie uczestniczy w nim grupa alfa-karboksylowa glutaminianu, lecz jego grupa y-karboksylowa.
46
New cards
Glutation zredukowany
Posiada wolną grupę sulfhydrylową (-SH)
47
New cards
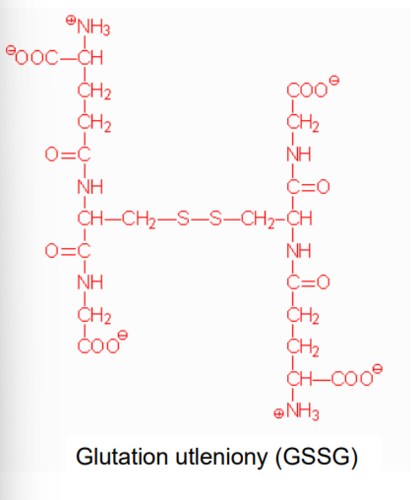
Glutation utleniony
Powstaje przez odłączenia pary atomów od grup -SH dwóch cząsteczek glutationu zredukowanego (powstanie mostka disulfidowego/disiarczkowego)
48
New cards
Białko
Produkt zawierający ponad 100 reszt aminokwasowych i wykazujący masę cząsteczkową powyżej 10 kDa
49
New cards
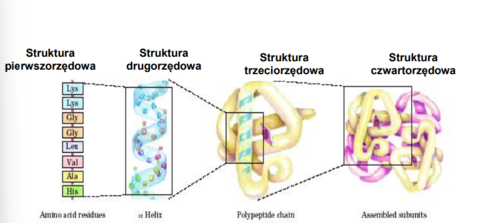
Struktura pierwszorzędowa białka
sekwencja, czyli kolejność aminokwasów w łańcuchu białkowym
- zakodowana w DNA
- określa strukturę trzeciorzędową
- zakodowana w DNA
- określa strukturę trzeciorzędową
50
New cards
Liczba możliwych kombinacji aminokwasów w białkach
- w większości białek występuje 20 aminokwasów w różnych kombinacjach
- przy długości łańcucha odpowiadającej 100 resztom aminokwasowym liczba możliwych kombinacji wynosi 20^100
- przy długości łańcucha odpowiadającej 100 resztom aminokwasowym liczba możliwych kombinacji wynosi 20^100
51
New cards
Co determinuje sekwencje aminokwasową w białku
genetyka
52
New cards
Białka homologiczne
białka wykazujące duże podobieństwo sekwencji aminokwasowej, które zwykle pełnią podobne funkcje
np. trypsyna i chymotrypsyna - enzymy proteolityczne
łańcuchy alfa i łańcuchy beta hemoglobiny i mioglobiny - wiążą tlen cząsteczkowy
np. trypsyna i chymotrypsyna - enzymy proteolityczne
łańcuchy alfa i łańcuchy beta hemoglobiny i mioglobiny - wiążą tlen cząsteczkowy
53
New cards
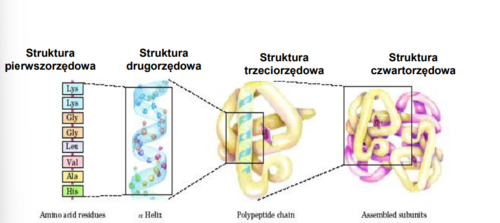
Struktura drugorzędowa białek
sposób przestrzennego rozmieszczenia łańcucha polipeptydowego
- helisa alfa
- harmonijka beta
- helisa alfa
- harmonijka beta
54
New cards
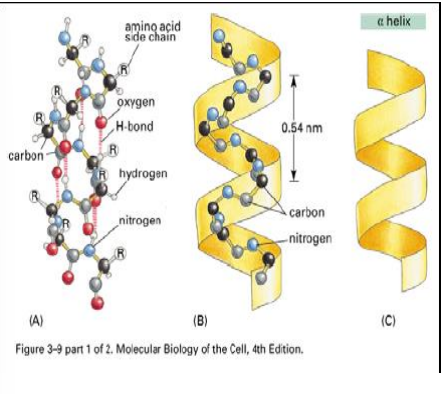
helisa alfa
- najczęściej spotykana
- na jeden skręt helisy alfa przypada 3,6 reszt aminokwasowych
- na zewnątrz sterczą łańcuchy boczne (R)
- wiązanie wodorowe powstaje pomięzy atomem wodoru w grupie N-H a tlenem grupy C=O należącej do czwartego z kolei aminokwasu
- na jeden skręt helisy alfa przypada 3,6 reszt aminokwasowych
- na zewnątrz sterczą łańcuchy boczne (R)
- wiązanie wodorowe powstaje pomięzy atomem wodoru w grupie N-H a tlenem grupy C=O należącej do czwartego z kolei aminokwasu
55
New cards
Helisa w białkach zbudowanych z L-aminokwasów jest....
prawoskrętna
56
New cards
Jakie aminokwasy nie mogą wytwarzać helisy alfa
- aminokwasy o łańcuchach polarnym obdarzonych ładunkiem elektrycznym
- aminokwasy o łańcuchach rozgałęzionych
- iminokwasy: proliny i hydroksyproliny
- aminokwasy o łańcuchach rozgałęzionych
- iminokwasy: proliny i hydroksyproliny
57
New cards
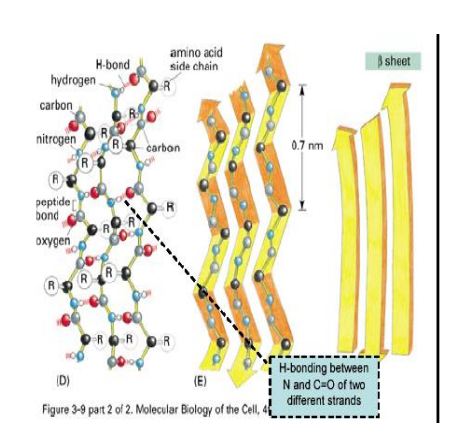
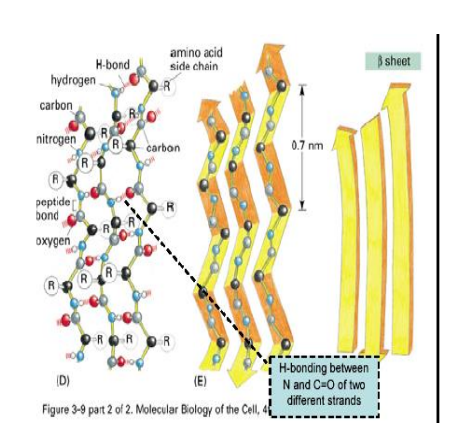
Harmonijka Beta
- struktura pofałdowanej kartki
- wiązanie peptydowe jest tak skonstruowane, że atomy grup C=O i N-H oraz dwa sąsiednie atomy węgla tworzą jedną płaszczyznę
- wiązania wodorowe powstają pomiędzy grupami C=O i N-H sąsiednich łańcuchów i są usytuowane poprzecznie do ich długiej osi
- wiązanie peptydowe jest tak skonstruowane, że atomy grup C=O i N-H oraz dwa sąsiednie atomy węgla tworzą jedną płaszczyznę
- wiązania wodorowe powstają pomiędzy grupami C=O i N-H sąsiednich łańcuchów i są usytuowane poprzecznie do ich długiej osi
58
New cards
Jakie aminokwasy występują w miejscach zagięcia B-harmonijki
Pro, Gly i aa złańcuchami bocznymi obdarzonymi ładunkiem
59
New cards
Jaka struktura białka tworzy się gdy opuszcza ono rybosom
drugorzędowa
60
New cards
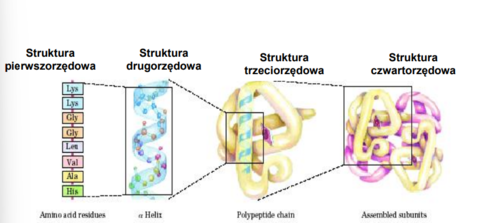
Struktura trzeciorzędowa białek
określa sposób wtórnego, trójwymiarowego pofałdowania cząsteczki białka z zachowaniem elementów struktury drugorzędowej.
61
New cards
Co determinuje sposób przestrzennego upakowania cząsteczki białka w strukturze trzeciorzędowej
Struktura pierwszorzędowa
62
New cards
Co jest odpowiedzialne za szybkie przybieranie przez peptydy struktury trzeciorzędowej?
Białkowa izomeraza disulfidowa
chaperony (biała opiekuńcze)
chaperony (biała opiekuńcze)
63
New cards
Domena białkowa
wydzielony, zwarty fragment struktury trzeciorzędowej, pełniący w białku określoną funkcję
64
New cards
Polipeptydy zawierające ponad 200 reszt aminokwasowych na ogół tworzą ile domen
conajmniej 2
65
New cards
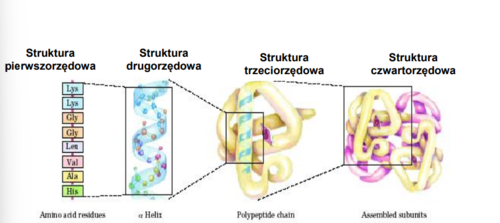
Struktura czwartorzędowa biała
Określa oddziaływanie pomiędzy poszczególnymi łańcuchami polipeptydowymi w wielołańcuchowym białku
- skład podjednostkowy i wzajemny układ przestrzenny podjednostek w obrębie jednej cząsteczki białkowej
- tylko w niektórych białakch
- skład podjednostkowy i wzajemny układ przestrzenny podjednostek w obrębie jednej cząsteczki białkowej
- tylko w niektórych białakch
66
New cards
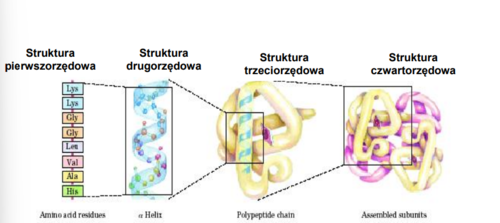
Białka oligomeryczne
białka o wysokiej masie cząsteczkowej, które składająsięz dwóch lub większej liczby łańcuchów polipeptydowych (monomerów), zwanych podjednostkami.
67
New cards
Cechy charakterystyczne struktury trzeciorzędowej
- giętkość łańcucha w punktach niestabilności
- tworzenie wiązań niekowalencyjnych - mostki solne, oddziaływanie hydrofobowe
- tworzenie mostków disulfidowych pomiędzy resztami Cys
- Domeny białkowe
- tworzenie wiązań niekowalencyjnych - mostki solne, oddziaływanie hydrofobowe
- tworzenie mostków disulfidowych pomiędzy resztami Cys
- Domeny białkowe
68
New cards
Heterooligomery
Białka z różnych podjednostek np. hemoglobina
69
New cards
Homooligomery
Białka z identycznych podjednostek np. enzym jabłczanowy
70
New cards
Jaką strukturę stabilizują wiązania peptydowe
Pierwszorzędową
71
New cards
Jaką strukturę stabilizują wiązania wodorowe
drugorzędową
72
New cards
Jaką strukturę stabilizują wiązania hydrofobowe
Pomiędzy niepolarnymi grupami łańcuchów bocznych aminokwasów - struktura trzecio- i czwartorzędowa białek
73
New cards
Jaką strukturę stabilizują wiązania dwusiarczkowe
trzeciorzędową (kowalencyjne)
74
New cards
Inhibitory biosyntezy białka w komórkach eukariotycznych ważne!!!
- toksyna błonicza
- rycyna
- cykloheksimid
- puromycyna
- rycyna
- cykloheksimid
- puromycyna
75
New cards
Rycyna
Toksyczne białko (enzym) produkowane przez rącznika
Wykazuje aktywność N-glikozydazy katalizującej hydrolizę adeniny 28S rRNA
Wykazuje aktywność N-glikozydazy katalizującej hydrolizę adeniny 28S rRNA
76
New cards
Toksyna błonicza
enzym produkowany przez patogen powodujący błonnicę, wykazuje aktywnośćADP-rybozylotransferazy, katalizującej ADP-trybolyzację eEF2 - w konsekwencji hamuje proces translacji, a konkretnie blokuje ona czynnik elongacji (eEF2 przesuwa nić o jeden kodon)
- podobnie działa exotoxyna
- podobnie działa exotoxyna
77
New cards
Cykloheksimid
Związek produkowany przez streptomyces griceus, który hamuje elongacje
78
New cards
Puromycyna
aminonukleozyd produkowany przez streptomyces alboniger
przypomina 3'-koniec aminoacylo-tRNA - wchodzi w miejsce A i powoduje zahamowanie translacji
przypomina 3'-koniec aminoacylo-tRNA - wchodzi w miejsce A i powoduje zahamowanie translacji
79
New cards
Mechanizm działania toksyny błoniczej
- wykazuje aktywność ADP-rybozylotransferazy - katalizuje ona ADP-rybozylację - hamuje proces translacji
80
New cards
Ile % i jakie biała ulegają transportowi przez blony
50% białka sekrecyjne
- hormony polipeptydowe np. insulina
- albumina
- kolagen
- immunoglobuliny
- hormony polipeptydowe np. insulina
- albumina
- kolagen
- immunoglobuliny
81
New cards
Ile % i jakie białka są białkami błonowymi
- receptory hormonów polipeptydowych
- białka transportowe
- kanały jonowe
- biała budujące cytoszkielet
- białka transportowe
- kanały jonowe
- biała budujące cytoszkielet
82
New cards
Ile % białek jest rozpuszczonych
20%
83
New cards
Peptydylotransferaza
rybozym, który wykazuje aktywność katalityczną 28S RNA, znajdujący sięw dużej 60S podjednostce rybosomu
- katalizuje translacje
- katalizuje translacje
84
New cards
SRP
SIGNAL RECOGNITION PARTICLE
- cząstka rozpoznająca sygnał
- cząstka rozpoznająca sygnał
85
New cards
Sekwencja sygnałowa
kilka białek związanych 7SL RNA
- wszystkie białka przeznaczone do jakiegoś konkretnego miejsca mają taką samą sekwencję sygnałową
- wszystkie białka przeznaczone do jakiegoś konkretnego miejsca mają taką samą sekwencję sygnałową
86
New cards
SRP-R
białko dokujące znajdujące się na błonie ER
87
New cards
Zarówno SRP jak i SRP-R wiążą i wykazują aktywność....
- GTP
- GTPazy
- GTPazy
88
New cards
Co dzieje się z sekwencja sygnałową po wejściu do ER
zostaje odcięta przez peptydazę sygnałową
89
New cards
Hsc-70
białko opiekuńcze potrzebne do nadania białku kształtu oraz przyłączania odpowiednich elementów
90
New cards
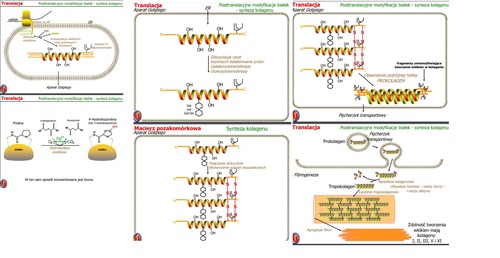
Synteza kolagenu
1. Wejście białka do ER
2. Odcięcie sekwencji sygnałowej przez peptydazę sygnałową.
3. Hydroksylacja niektórych reszt prolinowych i lizynowych z udziałem Fe2+ i askorbinianu
4. Tworzenie mostków disiarczkowych pomiędzy cysteinami
5. Przyłączanie reszt cukrowych (glikozylacja) przez galaktyozylotransferazę i glukozyotransferazę - ułatwiają one utrzymanie cząstek prokolagenu w formie rozpuszczalnej
6. Łączenie sięze sobą peptydów w jeden Prokolagen z potrójną helisą (przez tworzenie się mostków disiarczkowych)
7. Cząstki prokolagenu wydostają się na zewnątrz przez pęcherzyki transportowe
8. Peptydaza kolagenowa odcina końcowe oligosacharydy
9. Oksydaza lizylowa - niektóre reszty lizyny zmieniają się w reszty allizyny w określonych punktach ->> łączenie tropokolagenów (mostki poprzeczne pomiędzy lizyną a allizyną)
10. Powstają włókna kolagenowe
2. Odcięcie sekwencji sygnałowej przez peptydazę sygnałową.
3. Hydroksylacja niektórych reszt prolinowych i lizynowych z udziałem Fe2+ i askorbinianu
4. Tworzenie mostków disiarczkowych pomiędzy cysteinami
5. Przyłączanie reszt cukrowych (glikozylacja) przez galaktyozylotransferazę i glukozyotransferazę - ułatwiają one utrzymanie cząstek prokolagenu w formie rozpuszczalnej
6. Łączenie sięze sobą peptydów w jeden Prokolagen z potrójną helisą (przez tworzenie się mostków disiarczkowych)
7. Cząstki prokolagenu wydostają się na zewnątrz przez pęcherzyki transportowe
8. Peptydaza kolagenowa odcina końcowe oligosacharydy
9. Oksydaza lizylowa - niektóre reszty lizyny zmieniają się w reszty allizyny w określonych punktach ->> łączenie tropokolagenów (mostki poprzeczne pomiędzy lizyną a allizyną)
10. Powstają włókna kolagenowe
91
New cards
Latryzm
Zaburzenia kości, stawów i naczyń - nasiona lathyrus odoratus seeds zawierają beta-aminopoprionitryl - inhibitor oksydazy lizylowej - brak mostków poprzecznych
92
New cards
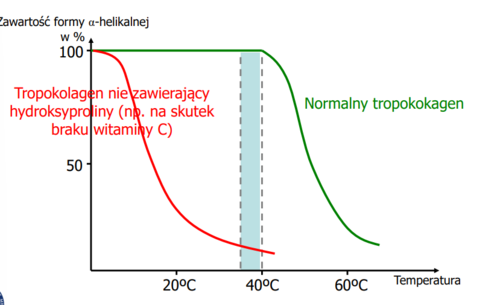
Rola Hydroksyproliny
wzmacnia odporność termiczną tropokolagenu
93
New cards
jakie wiązania powstają pomiędzy modyfikowanymi resztami lizyny, allizyny i 5-hydroksylizyny
kowalencyjne wiązania krzyżowe (mostki poprzeczne?) - stabilizują włókienka kolagenu
94
New cards
Jakie metaloproteinazy degradują kolagen
- żelatynazy
- kolagenazy
- stromielizyny
- błonowe MMP
- kolagenazy
- stromielizyny
- błonowe MMP
95
New cards
Regulacja aktywnośći MMP
Inhibitory MMP
- inhibitory niespecyficzne (alfa-2-makroglobulina)
- inhibitory specyficzne (TIMP)
- inhibitory niespecyficzne (alfa-2-makroglobulina)
- inhibitory specyficzne (TIMP)
96
New cards
Gdzie jest produkowana większość białek mitochondrialnych?
w cytoplazmie
97
New cards
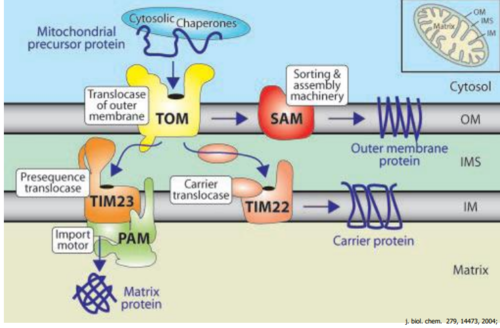
Transport białek do mitochondriów
Poprzez system translokaz
- TOM - translocase of outer membrane
- TIM - translocase of inner membrane
- TOM - translocase of outer membrane
- TIM - translocase of inner membrane
98
New cards
NLS
Sekwencja kierująca do jądra; w gotowym białku
99
New cards
Importyny
kompleks białek w porze jądrowym, ich ruch przepycha towar przez por
100
New cards
Prebiałka
peptydy zawierające sekwencję sygnałową