Chapitre 1 : Méthode de production
1/131
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
132 Terms
Pourquoi les virus sont-ils si abondants et importants dans le corps humain ?
Les virus sont les microorganismes les plus abondants dans le corps humain.
Une personne saine contient environ 3x10¹³ virus.
Les virus présents sont majoritairement des bactériophages.
Les bactériophages affectent les bactéries du tube digestif.
Les virus se transmettent principalement par aérosol.
Chaque fois que l’on éternue, on peut projeter plus de 100 millions de virus.
Quelle est la différence entre la biomasse des virus et celle des bactéries ?
En termes de biomasse, les virus ne sont pas les plus lourds.
Ce sont les bactéries qui ont une biomasse plus importante que celle des virus.
Qu'est-ce que l'infection par le virus de l'herpès entraîne ?
Une fois infecté par le virus de l'herpès, l’individu est infecté à vie.
Le virus reste latent dans le corps et peut se réactiver plus tard.
Combien de notre génome provient des rétrovirus ?
Environ 8% de notre génome provient de rétrovirus (1,5% du génome code pour des protéines)
Ces rétrovirus ont été insérés mais d’autres virus aussi
→ S’ils sont insérées au niveau de notre lignée germinale, ils peuvent être transmis à la descendance.
Les rétrovirus incluent des gènes comme les syncytines.
Les syncytines sont responsables du développement du placenta chez les mammifères. Les syncitines dérivent des gènes de l’enveloppe des rétrovirus endogènes.
Quel exemple d'infection virale grave ?
Le virus Ebola est un exemple d’infection virale grave.
Le virus Ebola a causé environ 28 000 cas et 11 000 décès.
La mortalité était supérieure à 20%
Pourquoi la peur des virus est-elle parfois irrationnelle ?
Certains virus sont très mortels, mais leur contagiosité peut être faible.
Le virus Ebola a une mortalité très élevée mais se transmet uniquement par contact direct (pas par aérosol).
Le virus de la rage a une mortalité de 100%, mais est très peu contagieux.
Le virus HIV avait une mortalité très élevée, mais avec les traitements modernes, la mortalité a diminué.
Quel est l'impact de la vaccination contre la rougeole ?
La vaccination contre la rougeole a permis de réduire de 75% la mortalité due à ce virus (virus peu mortel mais très contagieux donc mortalité quantitativement importante dans le monde).
L'introduction du vaccin a eu lieu en Belgique en 1985.
Des cas de rougeole ont augmenté entre 2013 et 2017 en raison de la décision de certaines personnes de ne pas se faire vacciner.
Qu'est-ce que le virus Zika et comment se transmet-il ?
Le virus Zika a été découvert pour la première fois en 1947 en Ouganda.
Il est transmis par les moustiques.
Ce virus est asymptomatique pour 3 personnes sur 4.
Une personne sur 4 présente des symptômes comme :
Fièvre
Conjonctivite
Éruptions cutanées
Maux de tête
Le virus est dangereux pour les femmes enceintes car il se transmet au foetus et peut créer des pathologies comme il n’a pas encore développé son système immunitaire.
Quel est l'impact du réchauffement climatique sur la propagation du virus Zika ?
Le réchauffement climatique pourrait permettre aux moustiques porteurs du virus Zika de se déplacer vers de nouvelles régions car de base, il ne résiste pas au froid.
Cela augmenterait le risque d'infection dans des zones actuellement non touchées, comme la Belgique.
Les virus pathogènes pour l’homme sont-ils nombreux ?
Dans la majorité des cas, l’infection virale est contrôlée par notre système immunitaire.
Comment notre système immunitaire lutte-t-il contre les infections virales ?
La majorité des infections virales sont contrôlées par notre système immunitaire.
L’immunité cellulaire
Les anticorps neutralisants
Le facteur IF (interféron)
Les vaccins éduquent le système immunitaire contre les virus et renforcent la réponse immunitaire.
Quels sont les points positifs des virus ?
Certains virus induisent un changement de couleurs chez les tulipes.
Certains plantes résistent à des températures élevées lorsqu’elles sont infectées par un champignon et un virus en même temps
En quoi les bactériophages sont-ils positifs ?
Certains virus comme les bactériophages peuvent infectés des bactéries et les lyser. Les bactériophages sont utilisés sur des plaies ouvertes pour détruire les bactéries. Ils peuvent servir comme agents thérapeutiques contre les infections bactériennes (peuvent empêcher les septicémies).
Intérêt accru depuis la montée des résistances aux antibiotiques
Ils ont aussi un rôle régulateur sur la qualité de la flore intestinale (microbiote) bien que ce ne soit que démontré chez la souris
=> Les bactériophages ne sont pas toujours bénéfiques :
Exemple : dans la toxine diphtérique, c’est l’infection de la bactérie par un bactériophage qui permet la production de la toxine.
Certains bactéries ne sont pathogénies que si elles sont infectées par un virus
Comment certains virus sont-ils utilisés pour corriger des maladies génétiques ?
Ils peuvent servir de vecteurs pour amener un gène corrigé dans les cellules.
Exemples :
Enfants bulles (déficit immunitaire) : des virus ont été utilisés pour insérer un gène correct et permettre le développement du système immunitaire. Problème : intégration incontrôlée du virus → certains enfants ont développé une leucémie.
Atrophie musculaire spinale (paralysie) : grâce à un virus, un gène corrigé a pu être réintroduit.
Maladie génétique de la peau : perte de lambeaux de peau → cellules souches prélevées, correction génétique par virus, peau redevenue normale.
Comment les virus pourraient-ils être utilisés contre le cancer ?
Les virus ciblent les cellules à forte prolifération
Ils pourraient tuer sélectivement les cellules cancéreuses
Ils pourraient également activer le système immunitaire de manière plus efficace.
Quel autre potentiel intéressant pourrait offrir l'utilisation des virus ?
Ils pourraient offrir un nouveau moyen de produire de l’énergie.
Quels progrès scientifiques ont été permis grâce à l’étude des virus ?
Découverte des oncogènes
Découverte des interférons
Compréhension de la réplication de l’ADN
Découverte de l’épisage alternatif
Quel est le premier virus découvert ?
Le virus de la mosaïque du tabac
Comment a-t-on découvert le virus de la mosaïque du tabac ?
Une feuille malade a été filtrée à travers un filtre de 0,2 um (filtrant les bactéries)
Le filtrat, sans bactéries, a pu contaminer les feuilles saines
Conclusion : l’agent pathogène a une taille inférieure à 0,2 um → Il a été nommé virus = fluide contagieux vivant
Quand les virus infectant l’homme ont-ils été découverts ?
Début du 20ème siècle (virus de la fièvre jaune)
Premier virus humain visible au microscope : virus de la variole (1948)
Quelles sont les dates importantes dans la découverte de virus pathogènes pour l’homme ?
1901 : Virus de la fièvre jaune
1903 : Virus de la rage
1906 : Virus de la variole (Microscopie en 1948)
1908 : Poliovirus
1933 : Virus Influenza A
1983 : HIV
1989 : Virus de l’hépatite C (transmis par le sang)
2003 : SARS-COV
2012 : MERS-COV (transmis par chauve-souris ou dromadaire à l’homme)
Pourquoi les virus sont-ils considérés à part parmi les micro-organismes ?
Ils sont souvent vus comme non-vivants
La particule virale seule (vision) n’est pas dangereuse tant qu’elle ne rencontre pas la cellule
Elle doit infecter une cellule pour répliquer son génome et produire ses protéines virales
Quelles sont les différentes susceptibilités cellulaires face à un virus ?
Cellule résistante
Ne possède pas de récepteurs pour l’entrée du virus
Ou ne permet pas la réplication → Pas d’infection, le virus reste inerte
Cellule susceptible
Possède un/ des récepteurs pour l’entrée
Mais pas forcément la machinerie pour répliquer le virus
Cellule permissible
Permet la réplication du génome virale
Mais ne possède pas forcément les récepteurs pour l’entrée du virus
Infection virale complète (cycle viral) :
La cellule doit être à la fois susceptible et permissive
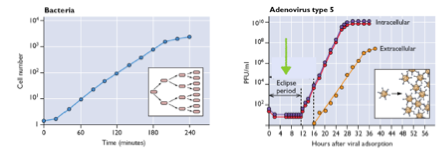
Qu’est-ce que la phase d’éclipse d’un virus ?
Période après l’entrée du virus où le virus réplique son génome
Aucun nouveau virus n’est produit
Ensuite, de nombreux virus sont produits en même temps
Après infection de toutes les cellules, un plateau est atteint
La durée de la phase d’éclipse varie selon les virus
Quels sont les trois caractères fondamentaux qui font des virus des entités originales ?
Ils sont des parasites intracellulaires obligatoires, sans exception
Ils ne peuvent pas se reproduire seuls
Ils utilisent obligatoirement la machinerie cellulaire
→ Différence majeure avec d’autres microbes comme les bactéries
Ils ne contiennent qu’un seul type d’acides nucléiques (ARN ou ADN).
Ce type unique constitue le génome viral
Il est protégé par une capside faite de protéines
→ une seule exception existe
Ils se reproduisent uniquement à partir de leur matériel génétique
Reproduction toujours par réplication (et non par division comme les cellules)
Pourquoi les virus sont-ils considérés comme des micro-organismes « non-vivants » ?
En dehors d’un environnement propice, le virus est inerte.
Il ne pourra jamais être infectieux sans rencontrer une cellule
Il doit impérativement infecter une cellule pour :
Se développer
Être infectieux
Se répliquer
Que désigne-t-on par « virion » ?
Particule virale infectieuse complètement mature
Inerte dans l’environnement tant qu’elle ne rencontre pas une cellule cible
Si elle rencontre une cellule cible, elle pourra se reproduire
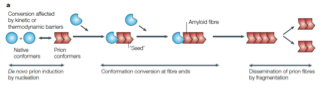
Qu’est-ce qu’un prion ?
Ce n’est pas un virus
C’est un agent infectieux constitué uniquement d’une protéine
Il ne contient pas d’acides nucléique
Il change de conformation pour devenir une forme plus stable
Il peut induire ce changement de conformation chez une protéine normale
Le prion résiste à la chaleur
Il est responsable de la maladie de Creutzfel-Jakob (maladie de la vache folle)
Maladie dégénérative du système nerveux central, causée par une accumulation de prions
Qu’est-ce qu’un viroïde ?
Petite molécule d’ARN sans capside
Infecte les plantes
Possède une structure particulière qui le rend résistant aux RNases
Une cellule peut-elle toujours être infectée par un virus ?
Toute cellule peut potentiellement être infectée par un virus
Un virus sera toujours de plus petite taille qu’une cellule
Quelle est la taille des virus ?
Les plus gros virus sont à la limite de la microscopie optique
Mimivirus, mégavirus, pandoravirus → Env. 750 nm
Ce sont des virus géants
Ils peuvent eux-mêmes être infectés par des virus de plus petites tailles
Ces virus géants peuvent-ils intervenir dans les pathologies humaines ?
Ils pourraient être impliqués dans des pathologies humaines.
Exemple :
Mimivirus → code pour des protéines ressemblant aux nôtres (ex : collagène).
Une personne atteinte d’arthrite pourrait potentiellement contenir ces mimivirus.
Le chlorovirus (autre virus géant) pourrait être responsable de troubles de la mémoire chez certaines personnes.
Existe-t-il de très petits virus ?
Oui :
Sputnik virus
Virophage
Ces petits virus peuvent infecter d’autres virus qui eux-mêmes infectent des cellules humaines.
Existe-t-il une diversité de formes et de tailles chez les virus ?
Oui, il existe une grande diversité :
De tailles
Et de formes
Comment produisait-on les virus avant l’invention de la culture cellulaire ?
On produisait les virus à partir d’animaux vivants.
Cette méthode est toujours utilisée aujourd’hui dans certains cas.
Quand un virus humain peut infecter un animal, quels modèles sont utilisés ?
Influenza (FLUAV) → furets
Ebola → souris
Varicelle (HHV-3) → cochon d’Inde sans poils (permet de mieux observer les signes cliniques)
Quand le virus humain ne peut pas infecter directement l’animal, quel modèle est utilisé ?
Virus HIV → on étudie son équivalent SIV (Simian Immunodeficiency Virus), qui infecte les singes rhésus.
Pourquoi les souris sont-elles les plus utilisées pour les études virales ?
Elles peuvent être modifiées génétiquement
Il existe des souris transgéniques exprimant les gènes early de virus humain
Exemple : Papillomavirus humain (HPV), virus qui n’infecte que l’humain
Souris modifiées pour exprimer les gènes oncogènes du virus sous le promoteur kératine 14
→ Expression dans toutes les cellules épithéliales, ce qui reproduit l’infection, puisque ce virus cible uniquement ces cellules
Comment rendre les souris immunologiquement proches de l’homme ?
On utilise les souris NSG (NOD scid gamma) :
Déficit immunitaire primaire.
Pas de production de lymphocytes B et T.
Mutation du gène du récepteur à l’interleukine 2 → pas d’activation des cellules NK.
On injecte à ces souris des cellules souches hématopoïétiques humaines.
Ces cellules vont coloniser la souris.
Résultat : on obtient un système immunitaire humain partiel.
Présence de macrophages humains, mais aussi murins.
Ces souris humanisées permettent de faire des études sur le HIV.
→ Le HIV infecte les lymphocytes et les macrophages humains.
→ Permet de tester des traitements antiviraux.
À quoi sert l’œuf embryonné de poule ?
C’est une méthode fréquente de production virale.
Exemple : production du vaccin contre la grippe saisonnière.
→ Chaque œuf permet la production d’1 à 2 doses de vaccin
Quels sont les risques liés à l’utilisation d’œufs ?
Il peut y avoir des contaminants d’œuf dans le vaccin.
Risques d’effets secondaires si la personne est allergique aux œufs.
Réaction immunitaire contre les protéines de l’œuf.
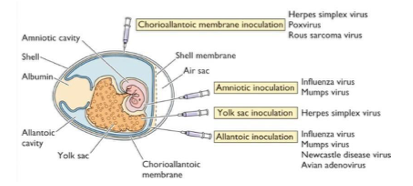
Comment fonctionne la production dans l’œuf ?
Selon le site d’injection, on obtient des virus différents
Le virus utilise la machinerie cellulaire de l’oeuf pour se développer
→ On ne peut pas produire tous les virus dans l’oeuf
Quelle est la première lignée cellulaire utilisée pour produire des virus ?
La lignée HeLa (du nom de Henrietta Lacks).
Patiente atteinte d’un cancer du col de l’utérus.
Infectée par le HPV-18.
Son médecin a prélevé des cellules tumorales épithéliales → placées en culture.
La culture a réussi → propagation possible → toujours utilisée aujourd’hui dans le monde entier.
Que permet la culture cellulaire actuelle ?
Permet de produire de nombreux types de virus
Certains cellules sont dites primaires
Elles ne sont pas immortelles
Nécessite un prélèvement régulier chez les animaux
Exemple du virus de la vaccine
Ce virus est lytique
Il est produit en culture
Les virus sont récupérés dans le surnageant après la lyse cellulaire
Un virus cytopathogène en culture l’est-il aussi chez l’homme ?
Pas forcément
Exemple avec le virus de la vaccine
Il provoque une forte lyse en culture
Mais chez l’homme, l’infection est bien contrôlée par le système immunitaire
Ce n’est pas parce qu’un virus est lytique en laboratoire qu’il est pathogène in vivo
Pourquoi faut-il une culture 3D pour produire certains virus ?
Ex. Papillomavirus (HPV), responsable du cancer du col de l’utérus
Il n’infecte que les cellules basales de l’épithélium
Il produit ses protéines tardives (late) dans les couches supérieures de l’épithélium
Il a besoin de la différentiation des kératinocytes pour produire ses capsides virales
Il est libéré par desquamation et non par lyse
Donc impossible à produire en culture en monocouche
Il faut recréer une culture 3D avec différentiation cellulaire
→ Quantité de virus produite très faible
Comment détecte-t-on une infection virale en culture cellulaire ?
En observant les cellules infectées
En repérant les effets cytopathogènes spécifiques
→ Ex. Coronavirus, paramyxovirus, herpésvirus → Formation de syncutiums entre les cellules
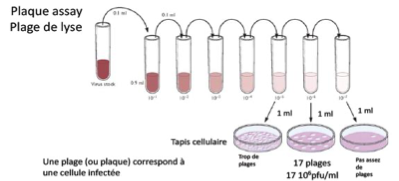
En quoi consiste le test des plages de lyse ?
Il consiste à réaliser des dilutions limite (de 10 en 10) que l’on place sur des tapis de cellules humaines (cellules permissives et susceptibles), animales ou bactéries.
Que faut-il prendre en compte pour choisir la dilution dans le test de plages de lyse ?
Il faut trouver une dilution avec suffisamment de cellules pour que ce soit reproductible mais pas trop non plus afin d’éviter que les plages fusionnent et ne soient plus comptabilisantes.
Que fait-on une fois la solution virale placée sur le tapis cellulaire ?
On recouvre d’agar afin que la diffusion se fasse de cellules en cellules
Que fait-on après quelques jours de culture sous agar ?
On enlève l’agar et on colore les cellules vivantes : ainsi les plages de lyse seront apparaitront blanches
Pourquoi peut-on affirmer qu’on meurt bien de cellules infectées dans ce test ?
Parce qu’on connait la lignée de cellules utilisées, ce sont donc bien les cellules infectées qui disparaissent
À quels types de virus le test des plages de lyse est-il applicable ?
Il est uniquement applicable aux virus lytiques (exemples de virus non lytiques : VIH, HV)
Quelles sont les deux choses que permet de faire le test de plage de lyse ?
Calculer le titre de particules virales
Quantifier les anticorps (West Nile Virus)
Comment peut-on utiliser ce test pour évaluer la neutralisation virale par des anticorps ?
On teste plusieurs concentrations de sérums contenant des anticorps et on regarde si à 2,5 ug/ml, le résultat est similaire au contrôle positif (sans anticorps). Cela permet d’évaluer si l’anticorps est neutralisant ou non, ou seulement partiellement neutralisant.
Que se passe-t-il lorsqu’on infecte toutes les cellules après une première inoculation ?
On obtient une courbe avec une période d’éclipse, une phase exponentielle de libération de virus, puis un plateau lorsque toutes les cellules ont été infectées et que les virus ont été libérés
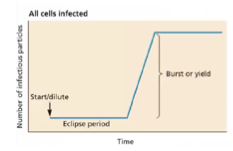
Que se passe-t-il si le titre viral est beaucoup plus faible au départ ?
Seules quelques cellules seront infectées, il y aura une première sortie virale exponentielle, qui infectera d’autres cellules, nécessitant une nouvelle période d’éclipse avant une seconde libération virale.
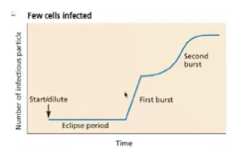
Pourquoi ne peut-on pas toujours inoculer le même nombre de particules virales ?
Parce qu’il existe une notion du nombre de particules virales pour qu’une infection ait lieu.
Que signifie « pfu » ?
Plaque Forming Unit : nombre de particules virales dans un échantillon rapporté au nombre de particules infectieuses.
Théoriquement, combien de particules virales sont nécessaires pour initier un cycle ?
Une seule particule virale suffit si elle infecte une cellule susceptible et permissive.
Mais en pratique, c’est rarement le cas, sauf pour les bactériophages
Pourquoi faut-il souvent plus d'une particule virale pour initier une infection dans les cellules humaines ?
Car :
Les particules virales peuvent être mal formées
Il peut y avoir des mutations
Le cycle infectieux peut être complexe (ex : HPV nécessite d’atteindre la couche basale + différentiation des kératinocytes)
Donne un exemple de virus peu infectieux.
Le virus de la grippe (influenza) nécessite 20 à 50 particules virales pour initier une infection.
Donne un exemple de virus très infectieux.
Rotavirus : 10 particules virales suffisent pour initier un cycle.
Que signifie « MOI » ?
Multiplicity of Infection = nombre de particules infectieuses ajoutées / cellule
Si on a 10⁷ virions pour 10⁶ cellules, quelle est la MOI ?
Le moi est de 10
Est-ce que chaque cellule reçoit exactement le nombre de virus correspondant à la MOI ?
Non, la relation virus-cellule est aléatoire car les virus ne possèdent aucun système de déplacement
Quelle loi statistique modélise la distribution des virus sur les cellules ?
La loi de Poisson = la probabilité qu’une cellule soit infectée par 1,2,3,4 … virions

Que permet de choisir une MOI forte ?
Infecter la majorité des cellules pour produire beaucoup de virus (exemple : fabrication de vaccins)
→ Premier graphique
Pourquoi choisir une MOI faible ?
Pour étudier le début du cycle viral ou suivre les premières étapes de l’infection.
→ Deuxième graphique
Pourquoi dit-on que le test de plages permet un stock « clonal » de virus ?
On récupère une plage de lyse d’une cellule infectée initialement. Cela permet d’isoler un type unique de virus
Pourquoi faut-il répéter trois fois le cycle de plages pour obtenir un clone pur ?
Parce que ce n’est pas nécessairement un seul type de virus qui a initié la plage, il faut donc répéter pour isoler un seul type de virus et obtenir une population homogène.
Quelle est la particularité des virus à ARN dans ce contexte ?
Ils mutent énormément, donc même les clones peuvent évoluer rapidement.
Pourquoi le test de plages de lyse n’est pas utilisable pour tous les virus ?
Parce que tous les virus ne sont pas lytiques
Sur quoi se base l’Endpoint dilution assay ?
Sur les effets cytopathogènes des virus
Donne un exemple de virus dont on détecte les effets cytopathogènes.
Le virus respiratoire syncitial provoque la formation de syncitium
Quelle est la méthode utilisée dans cet assay ?
On réalise des dilutions limite
On observe les puits dans lesquels des effets cytopathogènes sont observés
On calcule le TCID50 (Tissus Culture Infectious Dose 50%
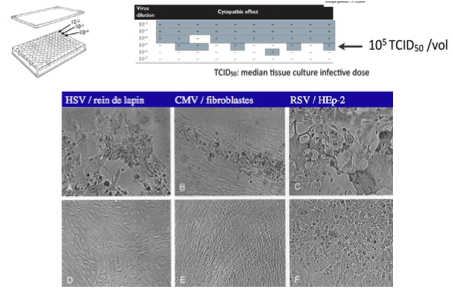
Que représente le TCID₅₀ ?
Quantité de virus nécessaire pour provoquer des effets cytopathogènes dans 50% des cultures infectées
Quel paramètre est important à noter dans cette technique ?
Le volume de virus placé dans les puits (TCID50/vol)
Qu’est-ce que les tests rapides de détection « physique » du virus ?
Ce sont des tests rapides permettant de détecter la présence de particules virales, mais pas leur pouvoir infectieux. On change ici de système de détection.
Quelle propriété virale est utilisée dans ces tests rapides ?
La présence d’hémagglutinine (HA) à la surface de certains virus comme celui de la grippe (Influenza)
Quel est le rôle de l’hémagglutinine ?
C’est une glycoprotéine qui reconnait les récepteurs cellulaires (acide salique) et permet l’agglutination des globules rouges. Elle aide le virus à entrer dans la cellule
Quel est le principe du test basé sur l’agglutination des globules rouges ?
En présence du virus, les globules rouges forment un tapis au fond du puits. En absence de virus, les globules rouges sédimentent en un seul point au fond du puits.
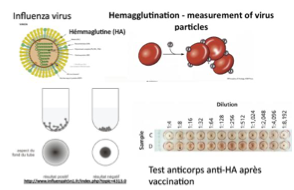
Pourquoi, à forte concentration de virus, n’observe-t-on pas un tapis mais un culot de globules rouges ?
À forte concentration, la neuramidase (une autre glycoprotéine viral) clive le lien entre l’hémaglutinine et les globules rouges, désagglutinant les GR. Elle aide le virus à sortir de la cellule.
Quel est l’effet de la neuraminidase dans ce test ?
Elle empêche l’agglutination en clivant le lien entre l’hémaglutinine et les globules rouges.
Pourquoi une faible concentration de virus est-elle plus efficace dans ce test ?
Parce que l’action de l’hémaglutinine prédomine celle de neuraminidase, permettant l'agglutination visible.
Peut-on détecter des anticorps anti-HA avec cette technique ?
Oui, elle permet de tester la présence d’anticorps anti-hémaglutinine par exemple après une vaccination contre la grippe.
Comment les anticorps anti-HA agissent-ils dans ce test ?
Ils bloquent l’hémaglutinine, empêchant l’entrée du virus dans la cellule cible et donc l’infection virale.
Quel est le génome du virus Influenza et où se réplique-t-il ?
C’est un virus à ARN qui se réplique dans le noyau de la cellule cible (exceptionnel pour un virus à ARN)
Comment détecte-t-on les virus par marquage fluorescent ?
Soit en fusionnant des protéines virales avec GFP (GREEN FLUORESCENT PROTEIN, isolée à partir de méduse et émettant une fluorescence verte quand le virus entre dans la cellule)
Soit en utilisant des anticorps couplés à de la fluorescence
Que permet la fluorescence dans ces techniques ?
Elle rend les particules virales visibles en microscopie optique et électronique et permet d’observer leurs interactions avec des récepteurs cellulaires.
Que détecte-t-on exactement avec ces techniques de marquage fluorescent ?
Des composantes du virus comme les protéines virales et non les particules infectieuses entières
Quelle méthode permet de détecter le génome du virus ?
La PCR (virus à ADN) et la RT-PCR (virus à ARN)
Que permet une PCR classique ?
Elle permet uniquement de confirmer la présence ou l’absence d’un virus
Comment peut-on quantifier le génome viral ?
Par qPCR en utilisant un agent intercalant comme le Sybergreen ou des sondes spécifiques (Taqman ou FRET) couplés à de la fluorescence.
Comment fonctionne le SybrGreen dans une qPCR ?
C’est un agent intercalant qui émet un signal fluorescent à chaque formation de double brin d’ADN.
Comment fonctionnent les sondes spécifiques comme Taqman ou FRET ?
Elles sont spécifiques à un virus donné, elles se fixent à l’ADN nouvellement synthétisé et émettent un signal fluorescent détectable.
Que permet la qPCR ?
D’obtenir le nombre de copie du génome viral par ml de sang (charge virale)
Quel est le lien entre le nombre de copies de génome et les particules infectieuses dans le cas du VIH ?
Il y a deux copies du génome par particules infectieuses, le nombre de particules infectieuses est environ la moitié du nombre de copies par ml
Quelle est la limite de détection actuelle de la qRT-PCR ?
4 copies/ml (anciennement 20 copies/ml) mais cela dépend du virus