H3 reacties || 2B - Organische chemie: reactiviteit - H3 Alkenen - reacties
1/5
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
6 Terms
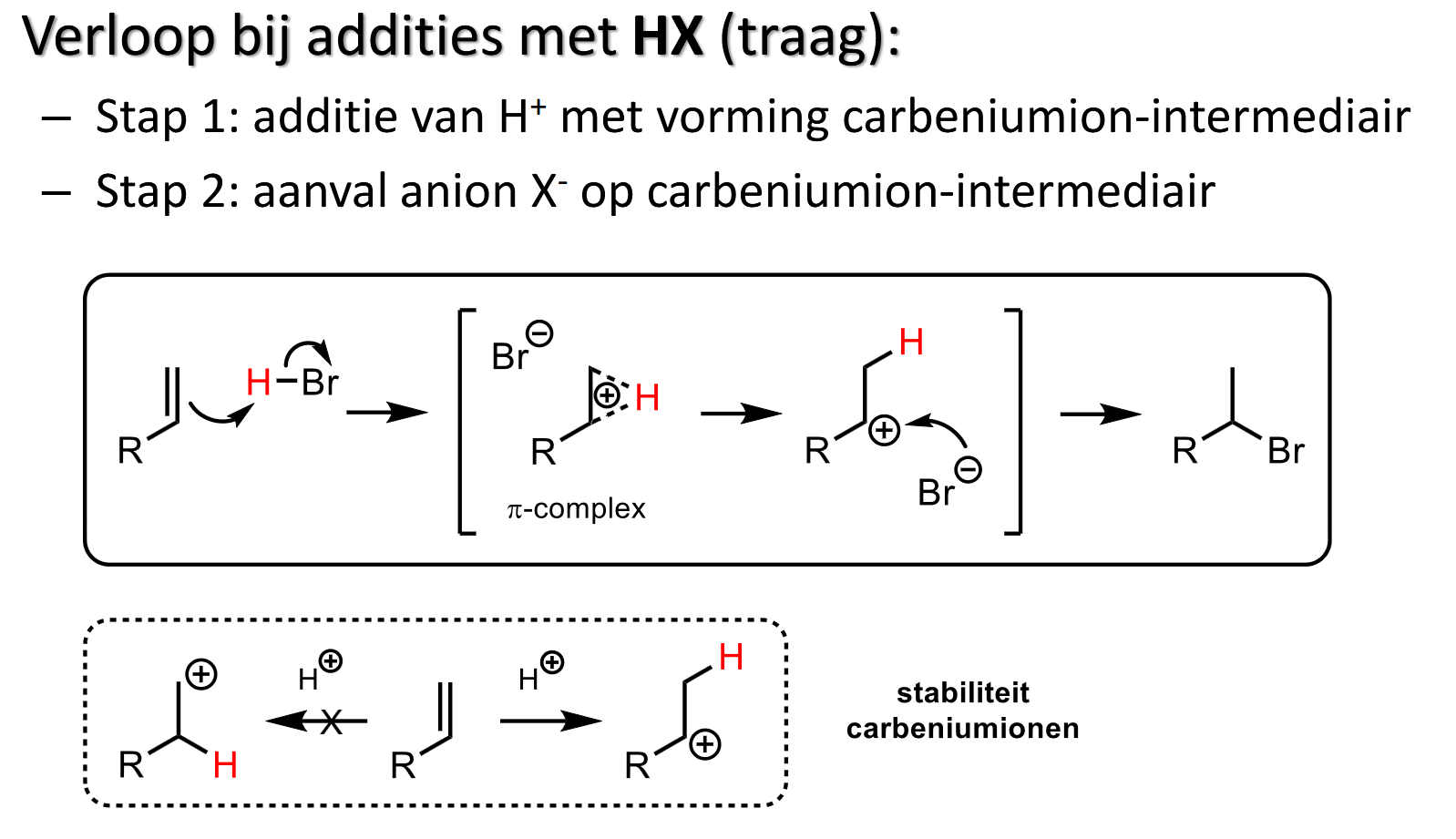
additie HX aan alkeen → halogeenalkaan
p17
Elektrofiele additie, ionaire reactie, traag
met HBr of HCl
H-Br is sterk zuur
vorming secundair carbeniumion → is veel stabieler dan primair carbeniumion (zie onderste kader) → uitgesproken voorkeur voor sec. ion
aflopende reactie wegens zwakke C=C pi-binding in substraat
syn-additie! → H en Cl beide aan zelfde kant vh vlak
(stabiliteit carbeniumion bepaalt hoogte vd energieberg van reactie)
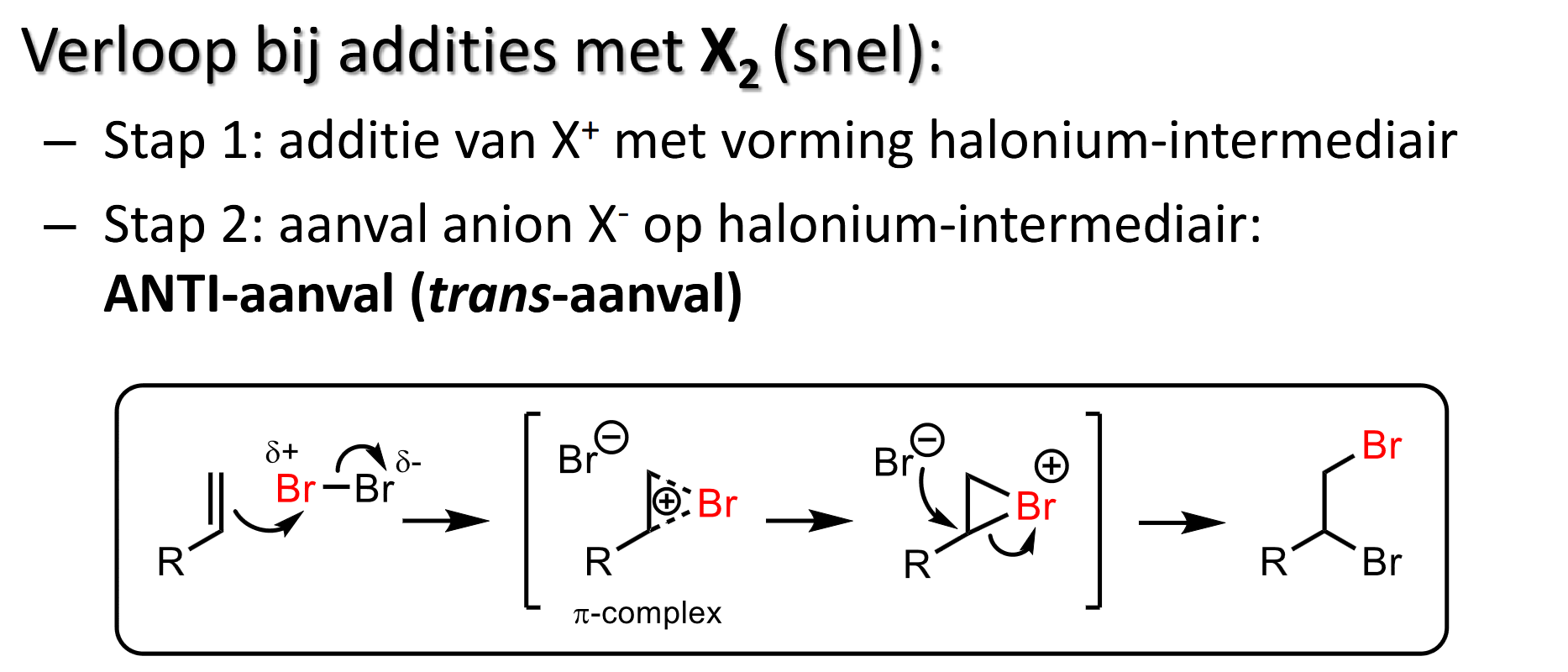
additie X2 aan alkeen → halogeenalkaan
p 17.5
Elektrofiele additie, ionaire reactie, snel
met Br2 of Cl2 (meestal met Br2 want Cl2 is gas)
Br2 in omgeving van // → afstoting elektronen → tijdelijk een kleine polarisatie → dus delta (+) en (-) → delta (+) wordt aangetrokken door pi-wolk van //
3-ring intermediair = verschil met HX-additie
oorspronkelijk delta (+) deeltje staat terminaal
trans-/anti-aanval
(naam halonium-intermediair ~)
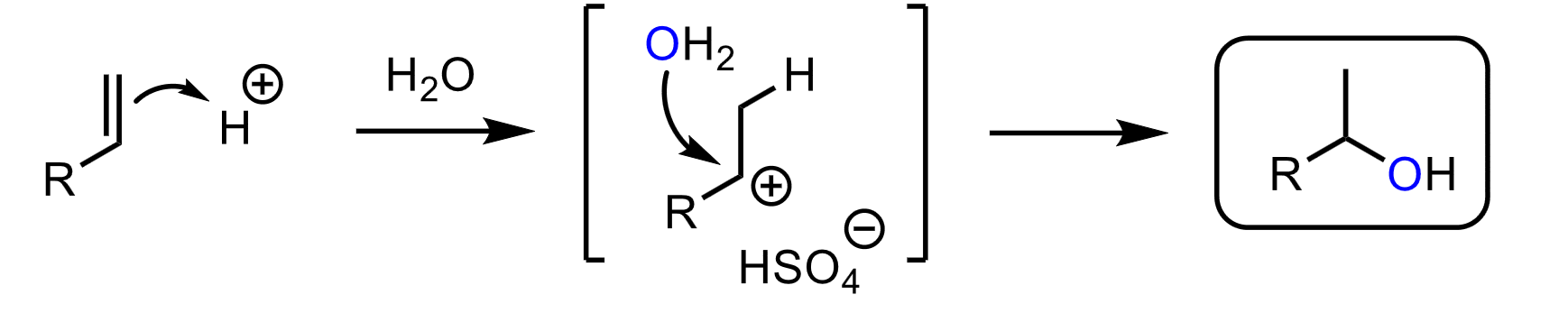
alkeen in zuur, waterig milieu → alcohol
p 17.5
voorbeeld van een HX-additie, in zuur waterig milieu
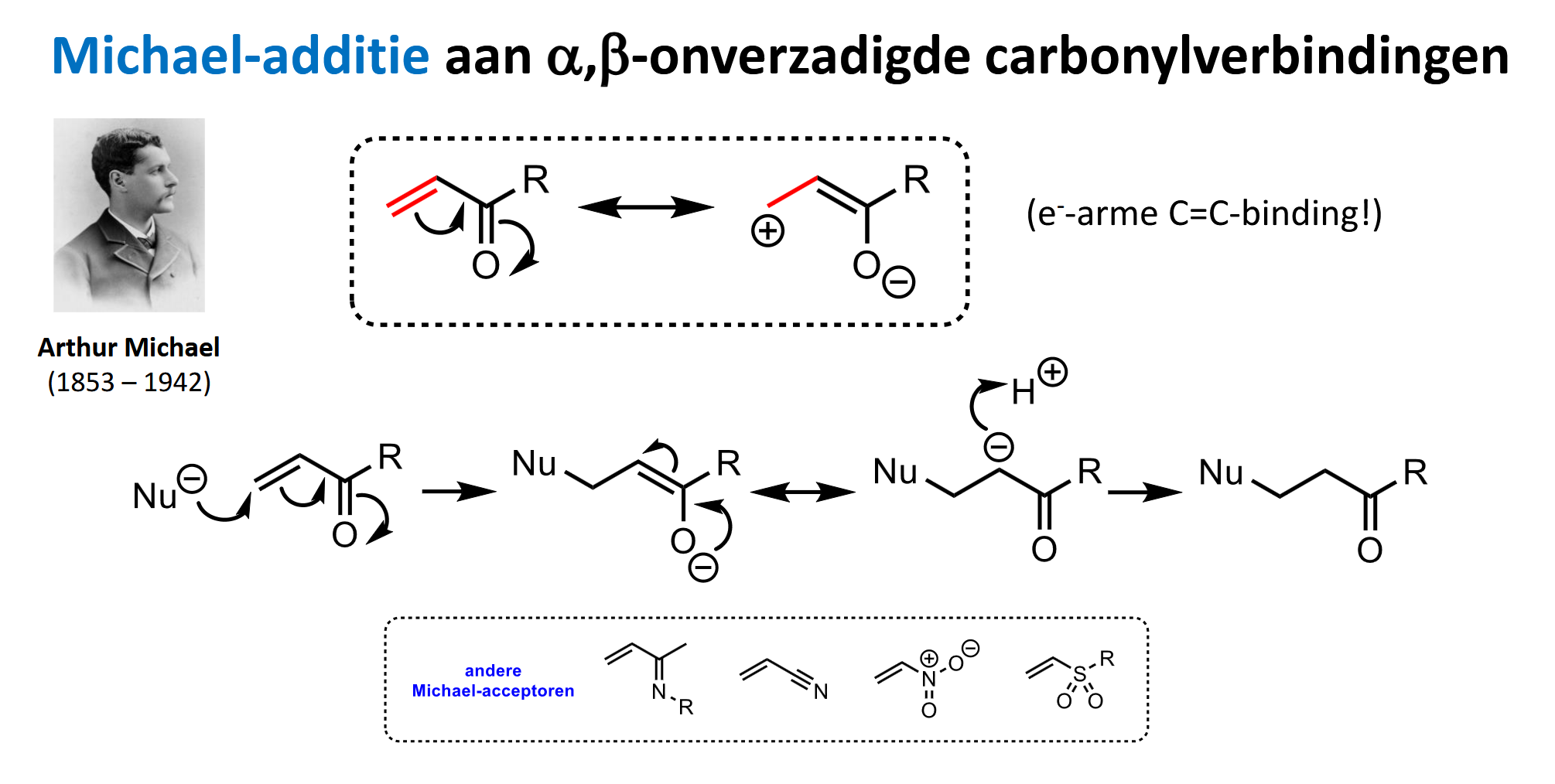
Michael-additie aan alfa, beta-onverzadigde carbonylverbindingen
nucleofiele additie aan Michael-acceptor
p18.5
nucleofiele additie
Michael-acceptor: dubbele binding in conjugatie met elektronenzuiger (aan andere //)
teken eerst mesomerie op (zoals in bovenste kader), daarna Nu- toevoegen
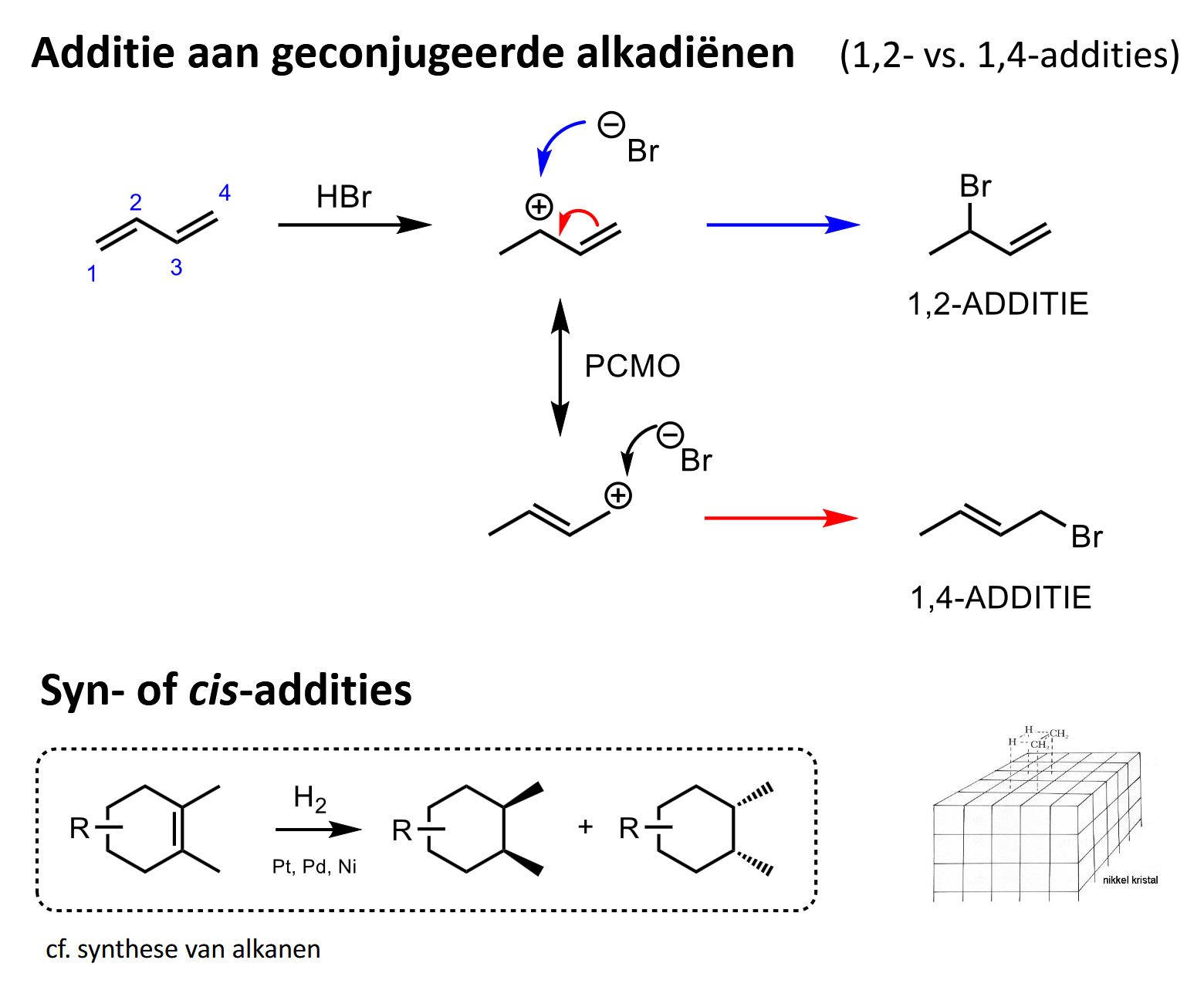
additie HX aan geconjugeerde alkadiënen
(HBr, HCl)
p19
H op (1) binden (stap extra uitschrijven !)
(+) op allylische positie (dus naast //) → via PCMO 2 uiterste mesomere vormen → Br- kan met ene of andere reageren → 1,2- of 1,4-additie
syn-/cis-additie?
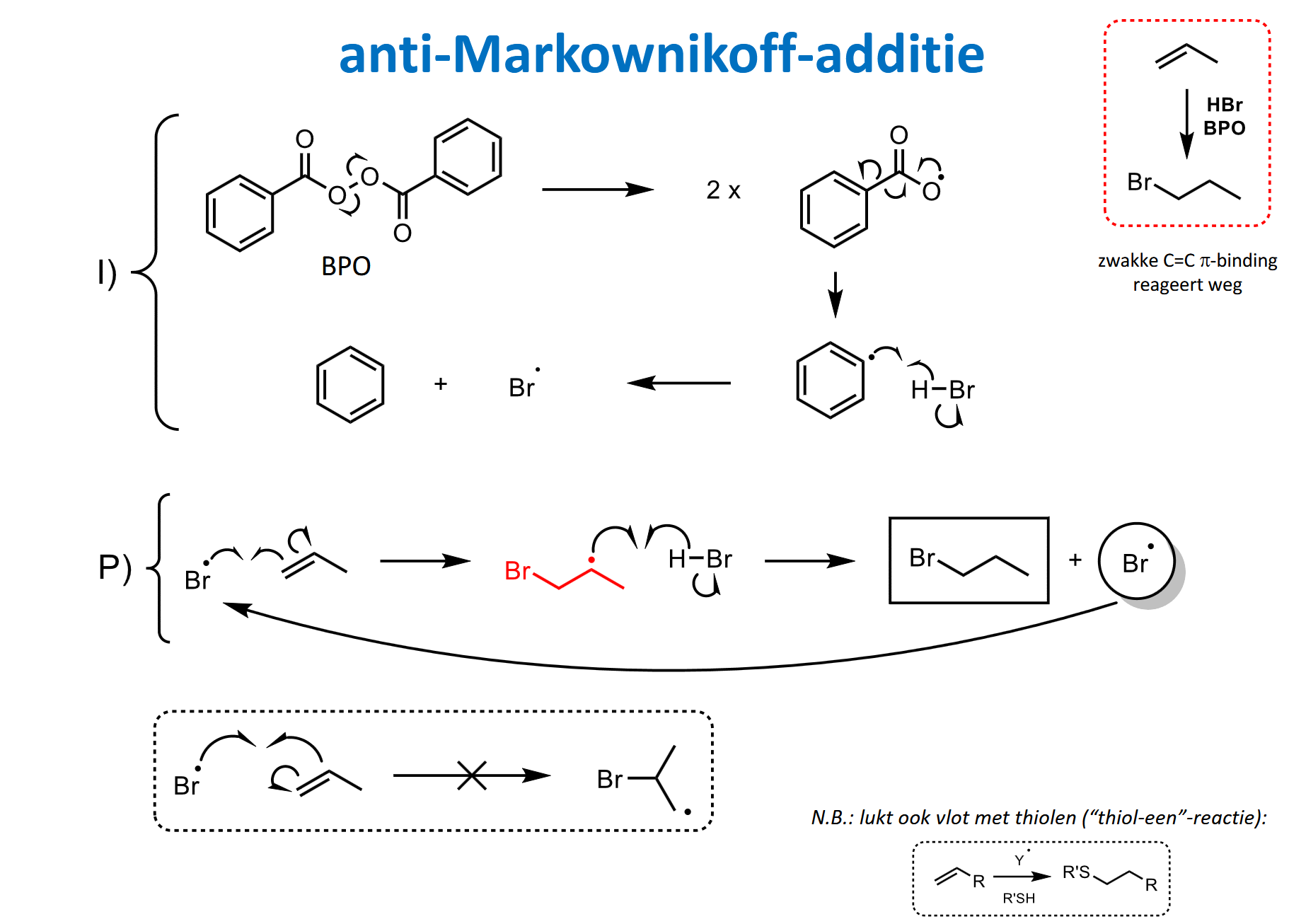
additie HX en BPO aan alkeen
anti-Markownikoff-additie
p19.5
HCl, HBr (in praktijk enkel met HBr)
zelfde reagentia als elektrofiele additie met HX, alleen nu ook met radicaalinitiator
vishaakpijlen!! (radicalaire reactie)
Initiatie:
via BPO
vorming Br radicaal
Propagatie:
Br radicaal valt zwakke pi-binding aan
secundair radicaal (want stabieler dan prim radicaal)
Terminatie:
doordat radicalen elkaar tegenkomen en wegreageren