Chimie PB- module 2
1/132
Earn XP
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
133 Terms
Liaisons chimiques
Force qui attire les atomes les uns vers les autres
dans un composé.
Les composés ioniques et covalents ont des propriétés differents ou semblabes? Pourqoui?
différent en raison
des types de liaisons chimiques qu’ils forment.
Liaison covalente
un partage d’électrons
entre des non-métaux (la plupart du temps)
Formation Liaison ionique
un transfert d’électrons
entre un métal et un non-métal.
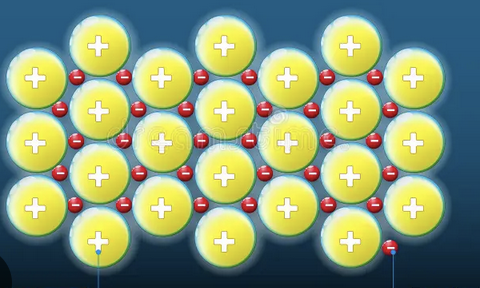
Liaison métallique
cations (métal) entourés
d’électrons délocalisés
La différence ΔEN indique quoi?
Indique le caractère ionique ou covalent.
Éléments à EN semblables forment?
Liason covalente
Éléments à EN très différentes forment?
Liason ionique
Pourquoi ΔEN faible = Covalente ?
Force égale → Partage d'électrons.
Pourquoi ΔEN forte = Ionique ?
Un atome est bcp plus fort → Transfert (vol) d'électron
Facteurs pour définir une liaison ?
1. ΔÉN et moyenne d’ÉN
2. propriétés du composé (plus ionique ou covalent?)
3. nature des composantes (métal vs non-métal)
4. Enthalapie réticulaire
L’élément avec le
charactère métallique le plus fort
Cs (pas Fr a cause que on a jamais vu un morceau)
Le composé le plus
ionique?
CsF
Cation = metaux ou non métaux?
Métaux
Anion = metaux ou non métaux?
Non-métaux
Liaison covalente non-polaire
un partage égal d’une paire d’électrons
entre 2 atomes.
Liaison covalente polaire
un partage inégal d’une paire d’électrons entre 2
atomes.
Liaison covalente polaire on la préscence des charges
Partielles
Quels électrons retire-t-on en premier pour un métal de transition ?
On retire les électrons de la couche 4s avant ceux de la 3d.
Pourquoi : La 4s est la couche d'énergie supérieure (la plus loin du noyau physiquement).
Prédit la charge de l’ion à partir des configurations
électroniques:
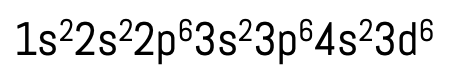
2+
Qaund t’écris la formule chimique EN CHIFFRE, c’est quoi l’ordre?
Métaux en premier, non-métaux en 2e. Ex : NaCl
Dans la nomenclature comment tu nom des cations
Meme nom que l’élement
Dans la nomenclature comment tu nom des métaux de transition
on indique la charge en chiffres romains avec le nom: Fe2+ : ion fer (II)
Dans la nomenclature comment tu nom des anions
nom de l’élément + terminaison ‘ure’
Élements de transition que on doivent pas utiliser des chiffres romains pour?
Sc,Y,Ag,Zn ou Cd
Nombre d'oxydation de Sc et Y ?
3+ (Sc3+,Y3+)
Nombre d'oxydation de Zn et Cd ?
2+ (Zn2+,Cd2+).
Nombre d'oxydation de Ag ?
1+ (Ag+).
ions polyatomiques
ions formés de deux ou plusieurs atomes.
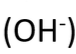
hydroxyde
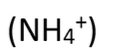
ammonium
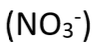
Nitrate
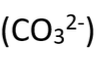
carbonate
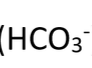
Hydrogénocarbonate
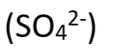
Sulfate
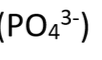
Phosphate
Structure des composés ioniques
structures réticulaires
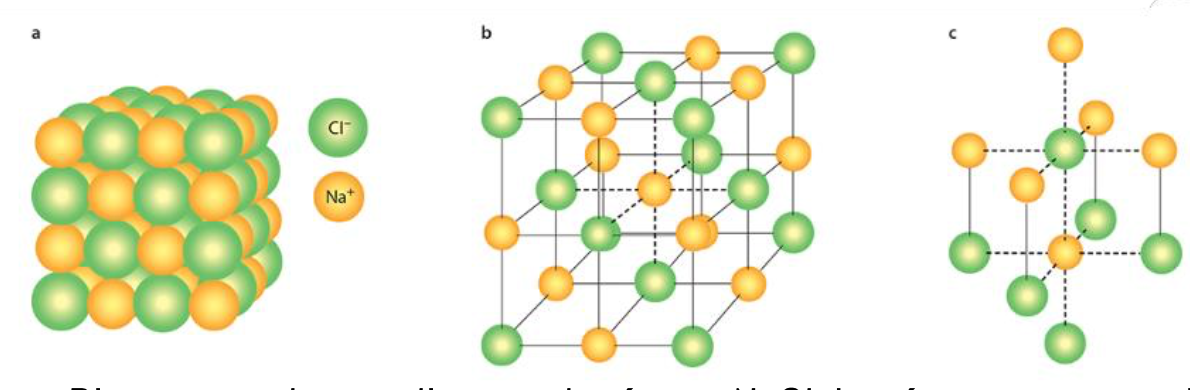
Est que il ya des molécules individuelles de NaCl?
Non
Structure réticulaires sont des tendances de majoritairement les..
Composés ioniques
Points de fusion/ébullition des composés ioniques ?
Tres élevé
Pourqoui le points de fusion/ébullition des composés ioniques est tres élevé?
Très grande force
électrostatique entre les ions
Volatilité des ions ?
Basse ( ne deveint pas gaz facilement)
Conductivité
électronique état solide et pourquoi
Ne conduit pas parce que les ions sont liés fortement dans
un réseau donc ils ne bougent pas.
Conductivité
électronique état liquide
Conduit bien
Conductivité
électronique en solution
aqueuse et pourqoui
Conduit bien parce que les ions sont libres en solution et bougent partout
Pourquoi l'eau (solvant polaire) dissout-elle le sel ?
L’eau est un molécule polaire. ses cotés - tirent sur les cotes des ions positifs et ses + tirent sur les ions négatifs.L'attraction de l'eau est assez forte pour "arracher" les ions du cristal et les disperser. On appelle ça l'attraction dipôle-ion
Pourquoi l'huile (solvant non-polaire) ne dissout pas le sel ?
Ils flottent autour du cristal sans rien faire. Ils n'ont aucune force d'attraction et poles + ou - pour tirer sur les ions.La force qui tient les ions ensemble est beaucoup plus forte que le solvant. Le cristal reste entier et tombe au fond.
Enthalpie réticulaire
Énergie nécessaire pour transformer 1 mole de solide ionique en ses ions gazeux séparés.
Plus haute qu’est l’énergie réticulaire, plus _____ qu’est le
composé
Ionique
Plus grande enthalpie réticulaire = point de fusion ± élevé?
Plus élevé
Plus grande qu’est la charge des ions= attraction est ± grande?
plus grande est l’attraction entre les ions
plus grande est l’attraction entre les ions = ± enthalpie réticulaire?
plus grande sera l’enthalpie réticulaire
réticulaire définition=
structure qui se répete
liason ionique
force d’attraction entre 2 charges opposés
Composition des sel binaires
Métal + non métal
Nommer des sels binaires?
(non- métal)ure de métal
Sel ternaire composition
Métal + ion polyatomique
Nommer sel ternaire
Base (hydroxyde) composition
Métal +hydroxyde
Nommer des bases
Hydroxyde de métal
Oxyde ionique composition
Métal + oxygène
Comment nommer un oxyde ionique?
Oxyde de [Nom du Métal]
Na2O→ Oxyde de sodium
MgO→ Oxyde de magnésium
Al2O3→ Oxyde d'aluminium
sel d’ammonium composition
Ammonium + anion
Nommer sel d’ammonium
ate/ure d’ammonium
1
mono
2
di ou bi
3
tri
4
tétra
5
penta
6
hexa
C’est qoui cette Composés covalents binaires : P205
pentoxyde de diphosphore
Déduis la formule du trioxyde de soufre.

Est que la terminaison de “hydrique” dans un acide veut dire un seul atome ou ion polyatomique?
Un seul atome
1. HCl(aq)
Acide chlorhydrique
2. H2SO4 (aq)
Acide sulfurique
Liaison double
Quand deux atomes partagent deux doublets
d’électrons
Liaison triple
Quand deux atomes partagent trois doublets
d’électrons
molécules diatomiques
à TPN (température et pression normale ce sont constituées de
Ce sont des molécules
constituées uniquement de deux atomes.
Nom tous molécules diatomiques
à TPN( témperature et pression normale) 7!!
H2, N2, O2, F2, Cl2, Br2, I2
doublet liant
2 électrons dans une liaison covalente
doublet non-liant
une paire d’électrons sur 1 atome, qui ne sont pas dans une
liaison)
La longueur de liaison est la distance entre quelle parties de l’atome
la distance entre les
noyaux de 2 atomes liés par une liaison chimique
Relation entre doublets liants et longueur ?
↑ Doublets liants → ↓ Longueur de liaison.
Relation entre longueur et force de liaison ?
↓ Longueur → ↑ Force/Énergie de liaison.
Quelle a une plus grande force de liason: liason simple ou triple?
Triple
En descendant un groupe du tableau périodique, qu'arrive-t-il à la liaison simple ? il ya 5 facteurs a considerer:
Rayon atomique/ionique
Distance paires d'électrons/noyau
Attraction électrostatique :
Force de la liaison :
Longueur de la liaison :
Rayon atomique/ionique : ↑ (augmente)
Distance paires d'électrons/noyau : ↑ (augmente)
Attraction électrostatique : ↓ (diminue)
Force de la liaison : ↓ (diminue)
Longueur de la liaison : ↑ (augmente)
L'Énergie de Liaison
Énergie requise pour briser 1 mole de liaisons chimiques
Liaison de coordination
Liaison covalente dans laquelle un des atomes fournis
les 2 électrons partagés.
Est que une liason de coordination se comporte de la même facon que toutes les autres liasons covalentes simples?
Oui
Synonme de liason covalente polaire
Dîpole
Molécule non-polaire 2 caracteristiques que définie
aucuns DNL + charges s’annulent
Forces intramoléculaires :
Forces entre les atomes à l’intérieur
d’une molécule
Forces intermoléculaires
Forces entre les molécules.
Étapes pour déterminer la polarité d’une molécule
1. Électronégativité
2. Structure Lewis
3. Forme( est que les charges s’annulent?)
Dipôle-dipôle se fait entre
2 molécules polaires
Qu'est-ce qu'une liaison hydrogène ? C’est enntre quelle de mol.?
Force dipôle-dipôle (polaire)
comment identifier une liason d’hydrogène?
contient un DNL
sur F O ou N
et H-O, H-N, ou
H-F
Liason d’hydrogène visuellement
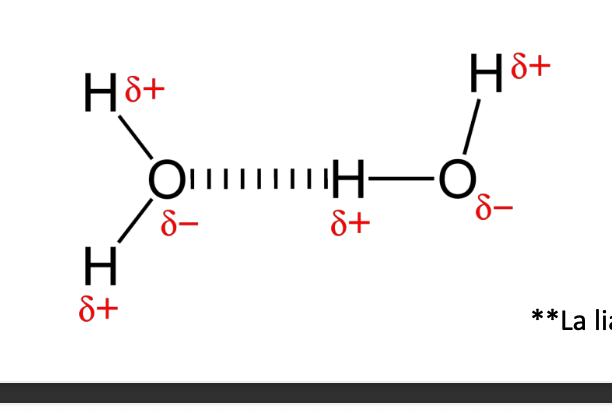
Dipôle-dipôle induit
Lorsqu’une molécule polaire polarise une molécule non-polaire
Les forces de dispersion de London
Quand une molécule non polaire est
capable d’induire un dipôle chez une
molécule voisine
(les électrons ne sont jamais à la même
place et bougent toujours)