BATTERIOLOGIA GENERALE PAG 1-32
1/45
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
46 Terms
La cellula batterica - dimensioni, forma e raggruppamento
La cellula batterica è una cellula procariotica di piccole dimensioni
Diametro → da frazioni di micrometro a pochi micrometri
Forma:
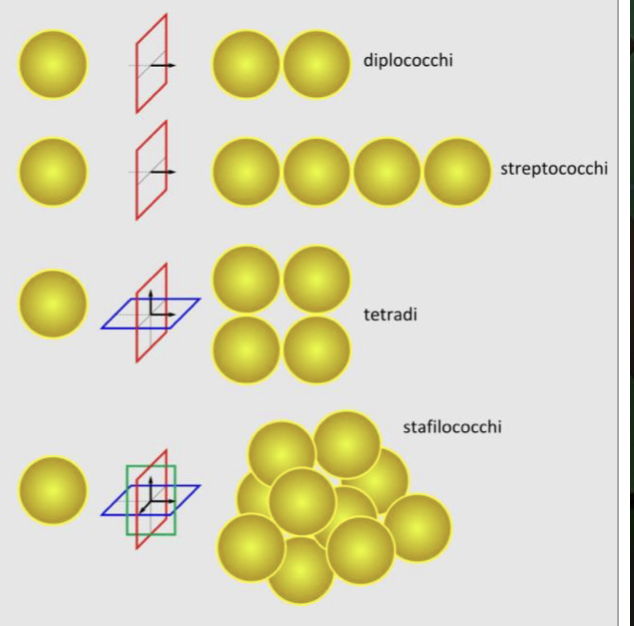
Sfera (cocchi)
se sono riuniti a due a due vengono chiamati diplococchi
se sono riuniti a grappolo vengono chiamati stafilococchi
se sono riuniti a catenelle vengono chiamati streptococchi
Cilindro (bacilli)
se sono particolarmente corti vengono chiamati coccobacilli
se presentano estremità assottigliate vengono detti bacilli fusiformi
se presentano curvature lungo l’asse maggiore, vengono definiti vibrioni o spirilli
come raggruppamenti principali abbiamo i diplobacilli e streptobacilli
La cellula batterica - composizione chimica
La componente più abbondante è l’acqua (fino all’80%):
E’ il solvente in cui sono disciolti i vari componenti organici e inorganici della cellula
Componenti inorganici più importanti:
Potassio, sodio
Calcio, magnesio
Ferro, zinco
Fosforo, zolfo
Sostanze organiche a basso peso molecolare:
Macromolecole o polimeri (componenti più complessi di una cellula batterica)
Colorazione di Gram
Distinguiamo:
Colorazioni Semplici:
Si eseguono mettendo a contatto, in un solo tempo, un unico colorante con il preparato contente i batteri da osservare
Hanno lo scopo di evidenziare la morfologia della cellula batterica
I coloranti più usati sono il Cristalvioletto, Fucsina Basica, Blu Di Metilene
Colorazioni Differenziali:
Prevedono l’utilizzo di più coloranti applicati in tempi successivi
Permettono di evidenziare differenze di colorazione tra specie batteriche diverse
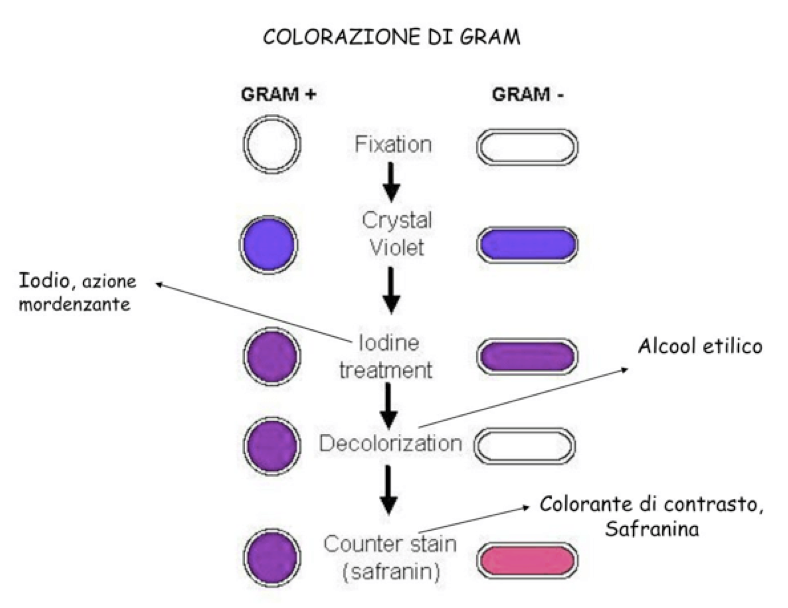
Colorazione di Gram:
E’ il metodo di colorazione differenziale più importante
Prevede 4 passaggi:
1. Il preparato contenente batteri viene trattato con una soluzione di cristalvioletto per 2-3 minuti
2. Si mordenza (fissa) la colorazione tramite soluzione di iodio e ioduro di potassio in acqua, detto liquido di Lugol (per un minuto)
i mordenti sono sostanze che formano composti insolubili con un colorante, rendendo più stabile la sua adesione al substrato
3. Si applica un decolorante sul preparato per 1-2 minuti (alcol etilico o acetone)
4. Si applica un secondo colorante per 1-2 minuti (fucsina o safranina, di colore rosso, facilmente distinguibile dal violetto del primo colorante)
Risultato:
Al termine della colorazione, i batteri che appaiono violetti sono detti Gram-Positivi
Quelli che appaiono rossi sono detti Gram-Negativi
Queste differenza di colorazione dipende dalla permeabilità degli involucri cellulari:
Nei Gram-Positivi il complesso cristalvioletto-iodio che si forma all’interno della cellula dopo il trattamento con Lugol non riesce ad attraversare la parete cellulare neanche dopo aver applicato alcol etilico o acetone
Nei Gram-Negativi invece i decoloranti riescono ad esportare il complesso cristalvioletto-iodio, permettendo così al secondo colorante di colorare la cellula
Questo significa che i batteri Gram-Positivi hanno maggiore spessore della parete cellulare che dà come risultato una minore permeabilità degli involucri nucleari
Architettura della Cellula Procariotica
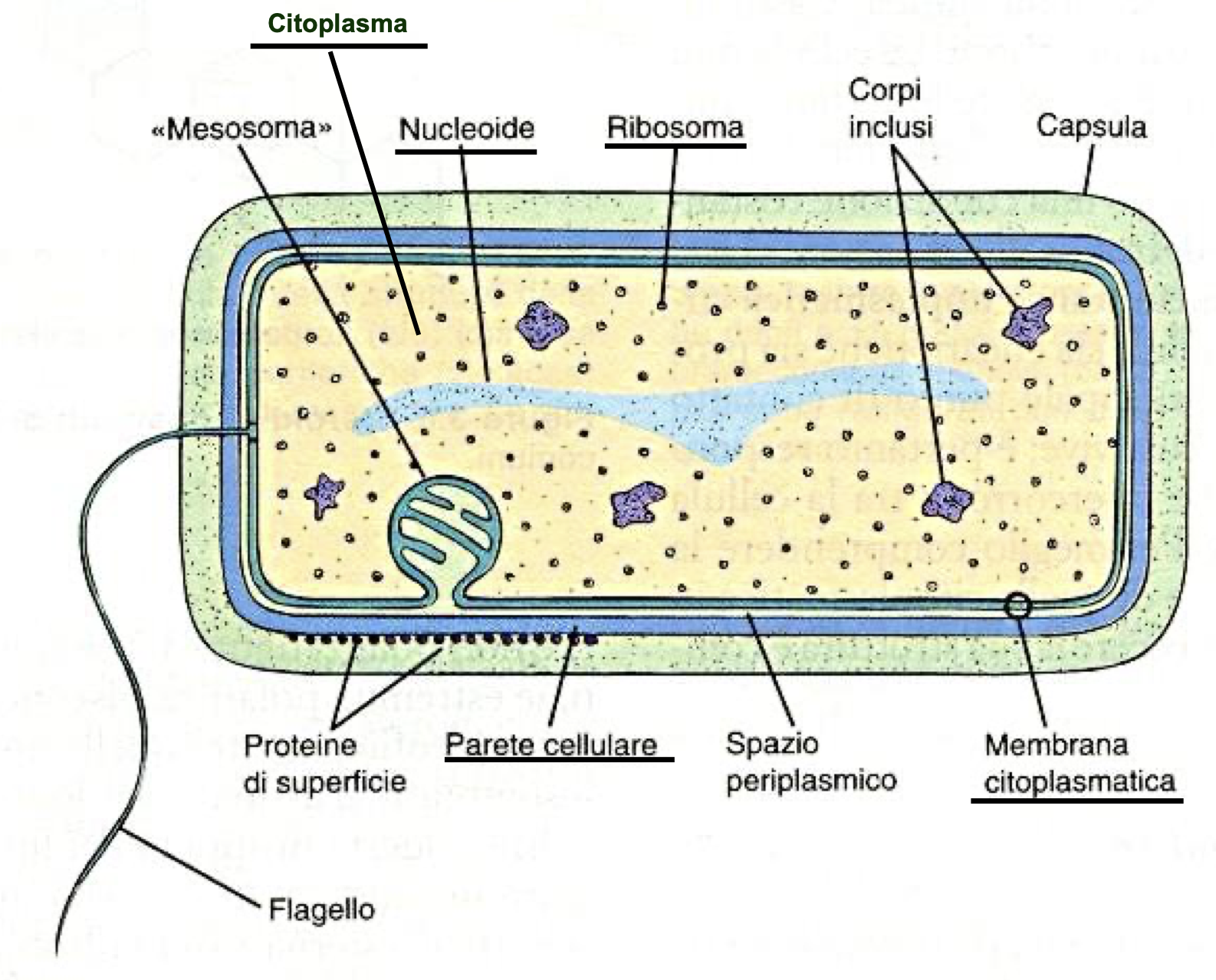
Architettura essenziale:
Dimensioni ridotte e assenza di compartimenti intracellulari separati da membrane
Struttura cromosomica semplice immersa direttamente nel citoplasma, senza membrana nucleare
Citoplasma delimitato dalla membrana citoplasmatica dalla quale si diramano verso l’interno delle invaginazioni che formano il sistema dei mesosomi
I mesosomi sono coinvolti nei processi di divisione cellulare, secrezione di esoenzimi e nei processi di fosforilazione ossidativa
I mesosomi sono più frequenti nei Gram-positivi
Tutta la struttura è racchiusa dalla parete cellulare (o sacculo), che sulla superficie presenta una capsula di natura polisaccaridica
In alcune specie abbiamo appendici libere:
Flagelli, importanti per la locomozione
Pili, importanti per la coniugazione
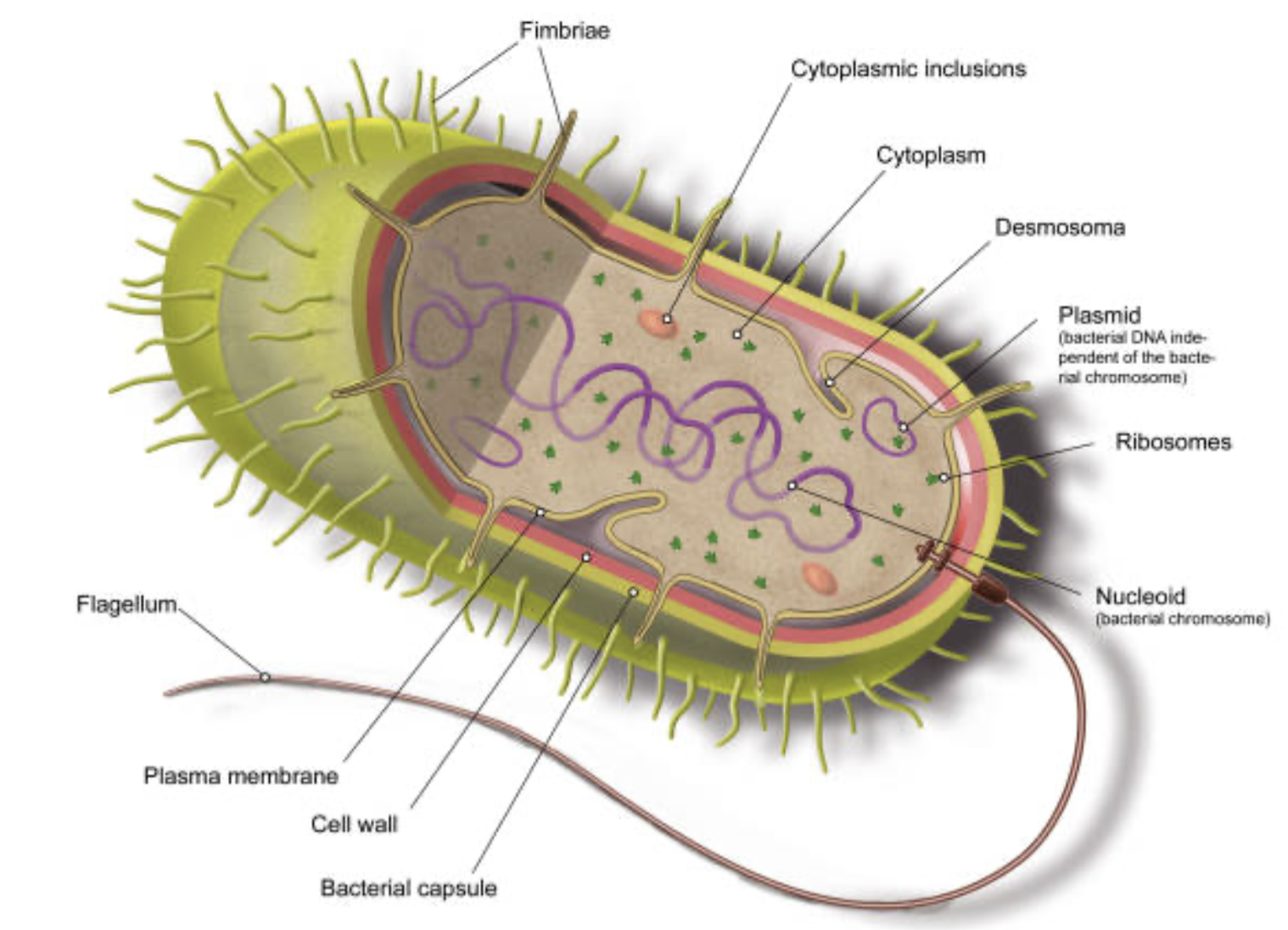
Il cromosoma batterico (nucleoide)
Nella cellula batterica materiale cromosomico è immerso direttamente nel citoplasma, senza membrana nucleare, questo lo chiamiamo Nucleoide:
Il nucleoide può essere considerato l’equivalente di un cromosoma, detto infatti cromosoma batterico o cromonema
Spesso un batterio può presentare più di una copia del cromosoma, ciò è dovuto alla mancanza di simultaneità tra la replicazione del materiale cromosomico e la divisione cellulare (nei batteri replicazione e divisione cellulare non sono sincrone, se la cellula inizia una nuova replicazione prima di dividersi, possono esserci più copie del cromosoma nella stessa cellula, questo è tipico in batteri a crescita rapida come l'Escherichia Coli)
Il DNA batterico appare come unico lungo filamento senza estremi liberi, quindi è circolare (ad eccetto di alcune Spirochete che hanno genoma lineare)
A differenza del DNA eucariotico, quello batterico non è legato agli istoni, ma complessato a proteine acidiche dalle quali può dissociarsi facilmente
Il cromosoma batterico è collegato alla membrana plasmatica in punti specifici
Oltre al cromosoma abbiamo molecole di DNA circolare più piccole chiamate Plasmidi, che hanno autonomia replicativa e possono condizionare gli aspetti fenotipici del batterio
Nel citoplasma batterico e i ribosomi batterici
Nel citoplasma batterico possono esserci accumuli di sostanze con funzione di riserva, costituiti da:
Glicogeno
Polimeri dell’acido beta-idrossibutirrico
Polisaccaridi
Polifosfati
Questi si colorano in rosso con il blu di toluidina (metacromasia) e vengono indicati come granuli metacromatici
Poi sono presenti anche i ribosomi:
Fondamentali per la sintesi proteica
I ribosomi procariotici presenta delle differenze fisiche rispetto quelli eucariotici che sono alla base della selettività di alcuni farmaci antibatterici che hanno come bersaglio proprio i ribosomi
differenze misurate con il coefficiente di sedimentazione di Svedberg (S) che indica la velocità di sedimentazione di una particella durante la centrifugazione
I ribosomi batterici sono costituiti da:
RNA (60%) e Proteine (40%)
70S composto da due sub-unità
Una minore 30S (21 proteine + una molecola di RNA 16S)
Una maggiore 50S (34 proteine + due tipi di RNA, 5S+23S)
I ribosomi eucariotici:
80S composto da due sub-unità
una maggiore 60S e una minore 40S
nelle cellule eucariotiche i ribosomi sono associati alla membrana del RE, in quelle procariotiche no perché il RE manca
La membrana citoplasmatica batterica
Come la eucariotica è formata da lipidi, proteine e piccole quantità di carboidrati, ma differisce per:
Composizione lipidica semplice:
Acidi grassi polinsaturi sono più rari
Acidi grassi ramificati e derivati dal ciclopropano sono più frequenti
Gli steroli sono completamente assenti, ad eccezione dei MIcoplasmi (che sono privi di parete cellulare)
Proteine di membrana:
Nelle eucariotiche sono per la maggior parte glicosilate, in quelle procariotiche no (ad eccetto di alcune Spirochete)
La quota di carboidrati presente nella membrana batterica sono legati alla componente lipidica a formare glicolipidi e glicosfingolipidi
Funzioni membrana citoplasmatica batterica:
Controllare gli scambi metabolici tra citoplasma e ambiente esterno, attraverso la diffusione passiva e trasporto attivo
E’ sede di processi biosintetici come la sintesi del peptidoglicano
Nei batteri che producono ATP con la respirazione, è sede di enzimi e vettori della catena respiratoria e del processo di fosforilazione ossidativa (cosa che negli eucarioti avviene nei mitocondri)
Sacculo o Parete Cellulare
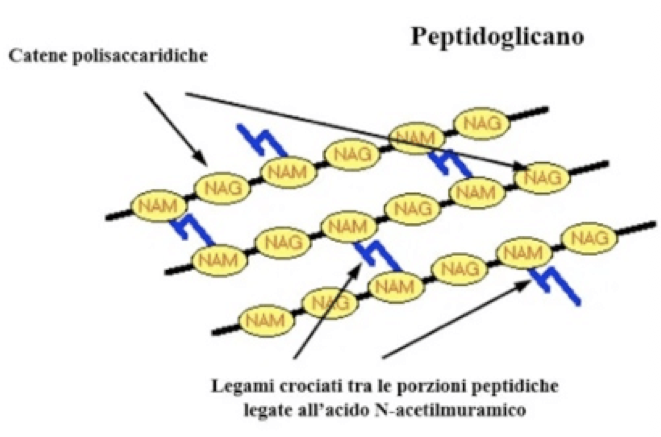
Struttura del peptidoglicano
La cellula batterica è racchiusa da una struttura rigida chiamata sacculo o parete cellulare:
Nei Gram positivi la superficie cellulare è costituita da:
membrana citoplasmatica
spesso strato peptidoglicano (spessore 200-800 angstrom)
Nei Gram negativi la superficie cellulare è costituita da:
membrana citoplasmatica
sottile strato di peptigoglicano (spessore 20-30 angstrom)
membrana esterna
Il peptigoglicano è il principale componente della parete cellulare:
E’ un grande polimero formato dalla ripetizione del disaccaride formato da:
N-acetilglucosamina
Acido N-acetilmuramico
Legate tra loro mediante legami beta-1,4 glicosidici a formare catene lineari
Poi questi polimeri lineari sono collegati trasversalmente attraverso un tetrapeptide che si lega al NAM e comprende:
D-alanina
Acido D-glutammico
Acido Diaminopilemico (nei gram-) o L-Lisina (nei gram +)
L-alanina
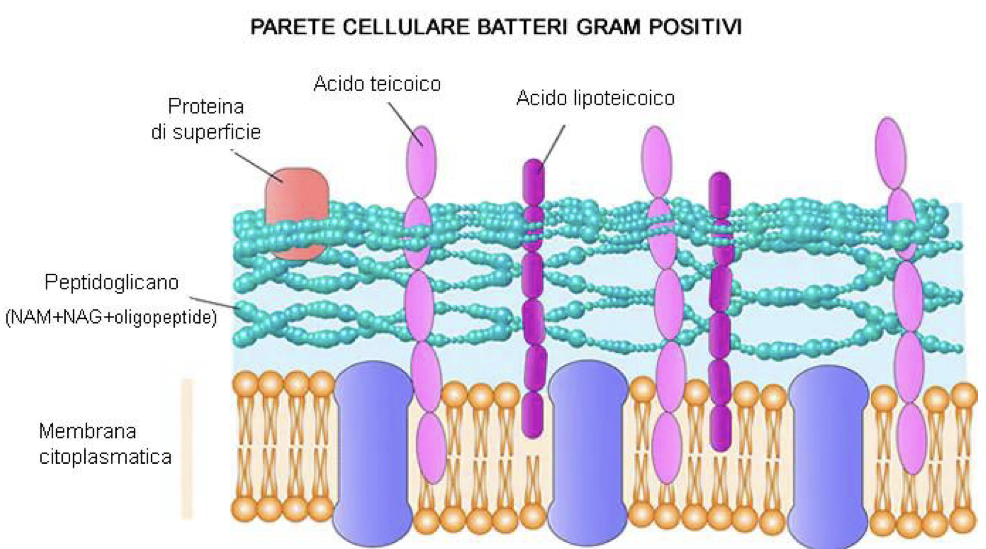
Parete cellulare dei batteri Gram Positivi
Abbiamo una membrana citoplasmatica con parete cellulare sovrastante formata da spesso strato di peptigoglicano e altri polimeri:
Tra gli altri polimeri, principalmente abbiamo gli Acidi Teicoici (non presente nei gram-):
che presentano una notevole variabilità di composizione, contribuendo alla specificità antigenica dei batteri
alcuni si legano alla porzione lipidica (acidi lipoteicoici) e sembrano essere importanti per ancorare la parete cellulare alla membrana citoplasmatica sottostante
La parete cellulare dei Gram Positivi è altamente polare, quindi si oppone al passaggio di molecole idrofobiche, mentre è permeabile alle molecole idrofile
a causa di questa polarità, lega grandi quantità di cationi che creano un ambiente ionico adatto al funzionamento degli enzimi presenti nella membrana citoplasmatica (in particolare quelli coinvolti nella sintesi del peptigoglicano, che richiedono ioni magnesio)
questa capacità di legare grandi quantità di cationi è dovuta alla tolleranza dei gram positivi a concentrazioni saline elevate, caratteristica sfruttata per preparare terreni di coltura selettivi per gram positivi.
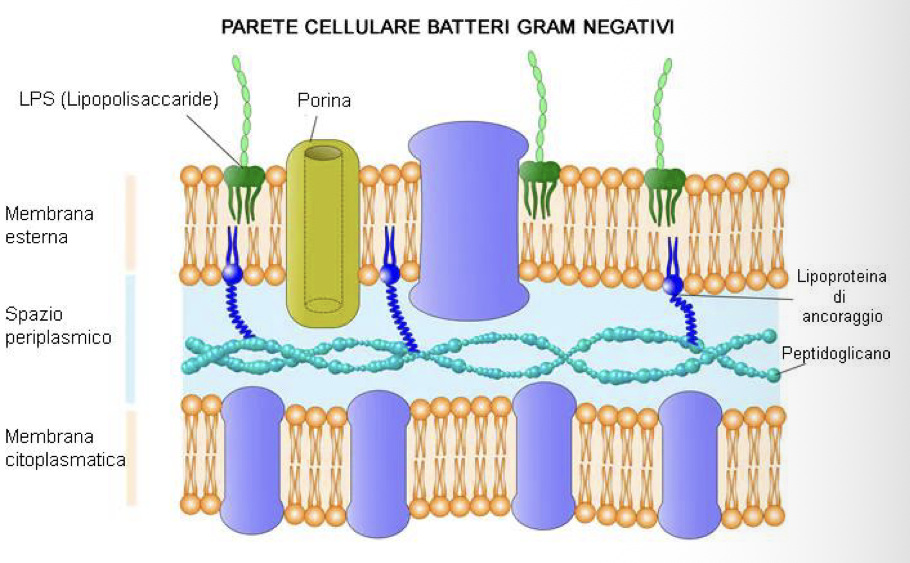
Parete cellulare dei Gram Negativi
Nei gram negativi la parete cellulare è formata esclusivamente da un sottile strato di peptigoglicano:
La parete cellulare non è in grado di contrastare il passaggio di molecole idrofobiche, che potrebbero danneggiare la membrana citoplasmatica
Per questo motivo, abbiamo una seconda membrana cellulare, la membrana esterna, situata al di sopra dello strato di peptigoglicano
La membrana esterna ha struttura bilaminare con organizzazione asimmetrica:
Foglietto interno formato da fosfolipidi
Foglietto esterno contenente il lipopolisaccaride batterico (LPS) coinvolto nell’azione patogena dei gram negativi
Il liposaccaride batterico è costituito da:
porzione lipidica, chiamata lipide A, che rappresenta l’endotossina vera a propria
formato da due residui di glucosammina fosforilata e lunghe catene di acidi grassi saturi
porzione polisaccaridica, formata a sua volta da:
una prima parte che costituisce il core della molecola → struttura costante, corta catena di zuccheri
la seconda parte è una lunga catena polisaccaridica con proprietà antigeniche (antigene O)
Le diverse catene polisaccaridiche sono in grado di legare cationi bivalenti come il magnesio, e fungono da ponte tra le varie catena conferendo compattezza
A causa della sua natura lipidica, la membrana esterna ostacola il passaggio oltre che alle molecole idrofobiche, anche a quelle idrofile:
Per questo motivo, abbiamo le porine (proteine) che nello spessore della membrana esterna formano canali e permettono la diffusione passiva di molecole idrofile come zuccheri, amminoacidi e alcuni ioni (con peso molecolare inferiore a circa 600-700 Dalton)
La membrana esterna è collegata alla parete cellulare sottostante tramite:
Lipoproteine con legami covalenti con lo strato di peptigoglicano
Porine con legami non covalenti con lo strato di peptigoglicano
Periplasma e Capsula
Periplasma:
Indica lo spazio tra membrana esterna e membrana citoplasmatica di un batterio gram negativo
Nei Gram+ esiste uno spazio analogo ma meno definito (tra membrana e spesso peptidoglicano)
Questo spazio contiene lo strato di peptigoglicano e proteine
Tra queste proteine abbiamo:
Proteine capaci di legare molecole idrofile
Enzimi con funzione digestiva (proteasi, nucleari, fosfatasi)
Enzimi detossificanti (in grado di inattivare farmaci antibatterici)
Capsula:
Involucro mucoso, viscoso per la presenza di polisaccaridi che rimangono aderenti alla superficie della cellula
eccezione fatta dal batterio bacillus anthracis, cui materiale è un peptide omopolimerico formato da polimeri di D-glutammato
Funzioni della capsula:
Conferisce al batterio proprietà di adesione (ad esempio lo Streptococcus mutans per aderire alla superficie dei denti)
Presenta proprietà antifagocitarie (come i meningiococchi, con uno spesso strato capillare che raggiungere gli organi bersaglio), cioè rende invisibile il batterio al sistema immunitario
E’ componente essenziale per formare il biofilm, che favorisce la persistenza per processo infettivo
I flagelli, il movimento della cellula batterica
I batteri osservati al microscopio in un liquido isotonico presentano un movimento oscillatorio:
Non dovuto alla sua motilità attiva, né alla sua vitalità
Si tratta di un movimento browniano
è un movimento casuale dovuto all'urto costante con le molecole del fluido
Invece i batteri che presentano i flagelli (generalmente i bacilli, vibrioni e spirilli, quindi forma cilindrica):
Sono strutture elicoidali che determinano movimento attivo attraverso la loro rotazione a livello del corpo basale
A differenza di quelli eucariotici, sono rigidi e presentano movimenti ondulatori
Distinguiamo:
Flagelli polari → quando presenti a uno o entrambi i poli della cellula (monotrichi se è presente solo un flagello, lofotrichi se è presente un ciuffo di flagelli)
Flagelli peritrichi → quando distribuiti sulla superficie cellulare
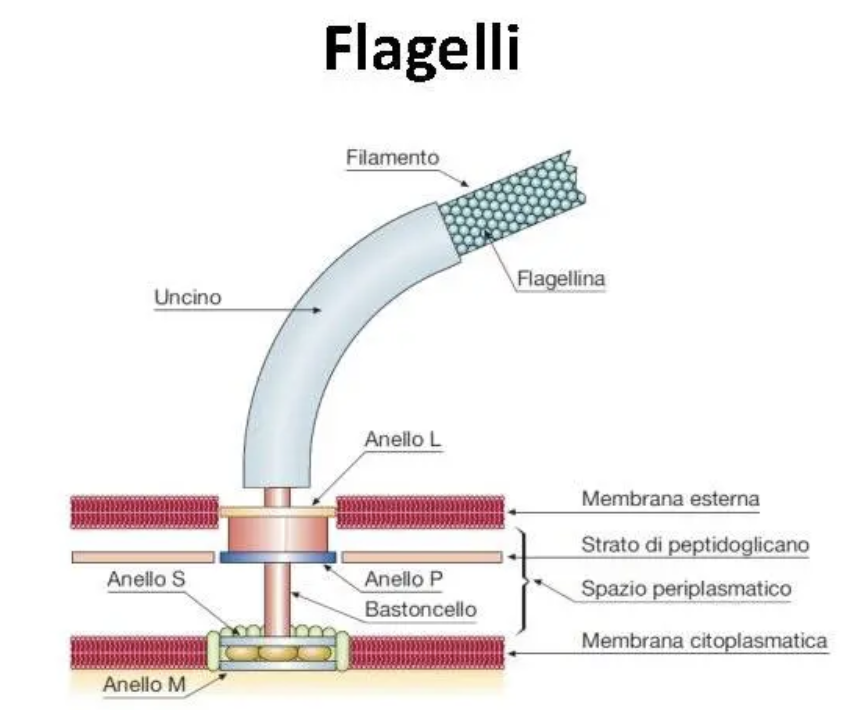
Un singolo flagello presenta tre parti principali:
Lungo filamento elicoidale che sporge dalla superficie cellulare per circa 5-10 micrometri:
E’ costituito da sub-unità proteiche di flagellina con proprietà antigeniche (antigene H) che si assemblano formando una struttura elicoidale
Gancio → struttura tubolare che collega il filamento al corpo basale
Corpo basale → struttura che ancora il flagello agli involucri cellulari e rappresenta il motore del movimento rotatorio del flagello
Il corpo basale è formato da alcune subunità proteiche:
Nei gram negativi le subunità formano 4 anelli:
Anello L → in corrispondenza del lipopolissacaride della membrana esterna
Anello P → in corrispondenza del peptigoglicano della parete cellulare
Anello S → sopra la membrana citoplasmatica
Anello M → in corrispondenza della membrana citoplasmatica
Nei gram positivi abbiamo solo:
Anello P e M
I flagelli sono strutture elicoidali avvolte in senso sinistroso:
La rotazione antioraria produce una propulsione monodirezionale della cellula (swimming)
La rotazione oraria produce un movimento disordinato avanti e indietro (tumbling)
La rotazione dei flagelli dipende da chemiorecettori di superficie che rispondono a stimoli attraenti o repellenti, e in base a ciò generano swimming o tumbling
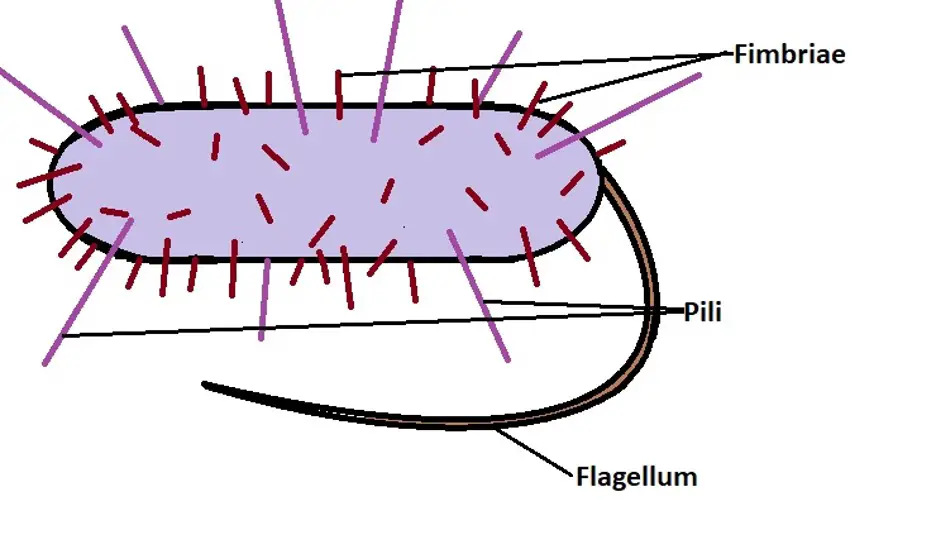
Fimbrie e Pili
Fimbrie:
Originano dalla membrana citoplasmatica e protrudono dalla superficie cellulare per 0,2-2 micrometri
Sono formate da subunità proteiche costituite da (una o due) Piline (specifiche per specie batteriche) che si organizzano a formare una struttura elicoidale, cilindrica e rigida
All’estremità libera presentano Adesine che conferisce proprietà adesiva verso substrati
in particolare verso carboidrati di glicoproteine di membrana di varie cellule animali
ma anche verso carboidrati presenti nelle proteine di membrana di globuli rossi (capacità emoagglutinante)
Classificabili in base ai carboidrati recettoriali che inibiscono la loro capacità adesiva:
Fimbrie di tipo 1 → adesione inibita dal mannosio
Tipo 2 → inibita dalla N-acetil-galattosammina
Tipo P → inibita da un dimero del galattosio
In alcuni enterobatteri (come escherichia coli e salmonella), abbiamo varianti delle fimbrie chiamate Curli:
più sottili e costituite da Curlina (proteina amiloide)
permettono al batterio di aderire a proteine come plasminogeno, fibronectina e proteine dell’MHC I
questa proteina è tossica e contribuisce alla sintomatologia morbosa
Un’altra classe di fimbrie è rappresentata dai Pili F (che sta per fertilità) o pili sessuali:
sono più lunghi e coinvolti nei processo di coniugazione batterica
Metabolismo Batterico - aerobiosi e anaerobiosi
Autotrofi ed eterotrofi
I batteri svolgono processi catabolici per produrre ATP che viene usata nelle reazioni biosintetiche (anaboliche) responsabili della crescita batterica.
In base ad esigenze metaboliche:
Aerobi Obbligati → vivono solo in presenza di ossigeno, quindi respirazione aerobia dove l’ossigeno è l’accettore finale degli ioni idrogeno che viene ridotto ad acqua
Aerobi o Anaerobi Facoltativi → vivono sia in presenza che in assenza di ossigeno. Quando in assenza, l’accettiore finale di ioni idrogeno è il nitrato, che viene ridotto a nitrito
Anaerobi Obbligati → vivono solo in assenza di ossigeno, quindi respirazione anaerobia o fermentativa (i batteri quindi muoiono in presenza di ossigeno)
Microaerofili → sono batteri crescono molto lentamente (o non crescono) in presenza di ossigeno, mentre crescono molto bene in assenza di ossigeno (o in aria con il 10% di anidride carbonica)
Autotrofi ed eterotrofi:
Autotrofi → sintetizzano costituenti usando sostanze inorganiche semplici
sono fotosintetici se usano luce solare
sono chemiosintetisi se usano composti inorganici (anche in assenza di luce)
Eterotrofi → possono metabolizzare composti già sintetizzati da altri organismi
sono saprofiti se ottengono cibo dalla materia vegetale e animale in via di decomposizione
sono parassiti se usano il metabolismo di altri animali per procurarsi cibo senza per forza recare danno
Azione battericida degli antibiotici
L’effetto battericida non dipende dal fatto che gli antibiotici bloccano la sintesi del peptidoglicano, ma dall’attivazione di enzimi autolitici (autolisine):
Questi enzimi formano una breccia nella parete cellulare, e siccome la sintesi del peptidoglicano è bloccata, si forma una breccia nella parete cellulare che porta alla lisi osmotica del batterio
Alcuni batteri come lo Streptococcus pneumoniae, può mutare e rendere inefficace l’attivazione di autolisine
Si osserva così tolleranza agli antibiotici che bloccano la sintesi del peptidoglicano
In questo caso non abbiamo azione battericida, ma il blocco della sintesi del peptidoglicano determina l’arresto della crescita e divisione cellulare batterica
Riproduzione Batterica
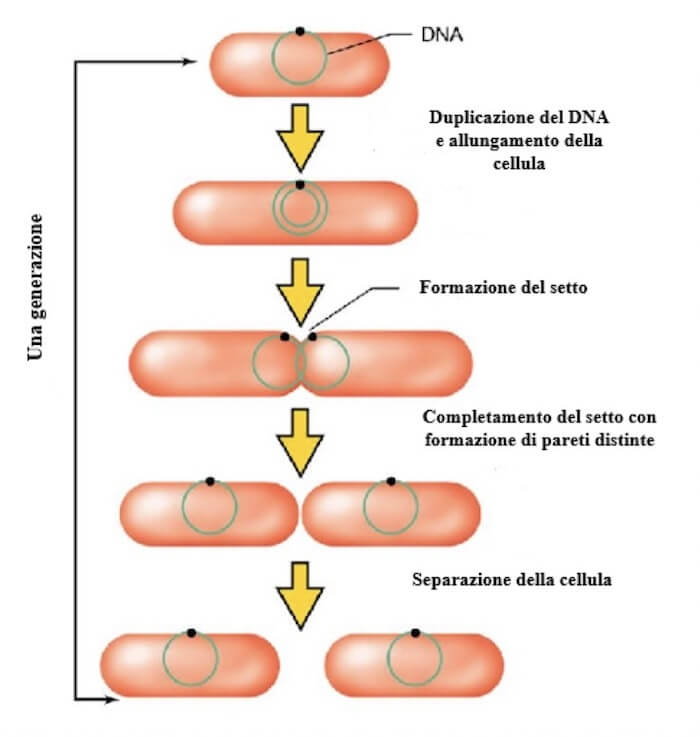
I batteri si riproducono per scissione binaria, prrocesso dove una cellula batterica si divide in due cellule figlie identiche alla madre, le fasi sono:
Dopo la duplicazione del cromonema (cromosoma batterico), le due molecole di DNA circolare risultanti si fissano in due punti differenti della membrana citoplasmatica
Successivamente accresce la regione di membrana interposta tra le due strutture cromosomiche che quindi si allontano tra loro
La membrana citoplasmatica si introflette al centro della cellula batterica allungata e si forma un setto
A setto completamente formato, avremo due pareti cellulari distinte → separazione della cellula batterica nelle due cellule figlie
Le Spore
Ultrastruttura della Spora
E’ una caratteristica di alcuni bacilli dei generi Bacillus e Clostridium:
Nei preparati colorati la spora appare come un piccolo corpo incolore all’interno del batterio, poiché è difficilmente penetrabile dai coloranti
Si osserva al microscopio ottico
Nei batteri di genere Bacillus il diametro della spora non supera quello della cellula batterica (o sporangio), nei batteri di genere Clostridium invece si e quindi appara ingrossato in corrispondenza della spora
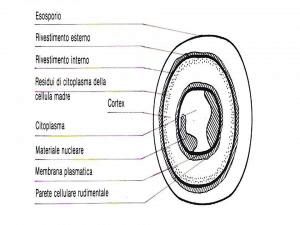
Ultrastruttura della Spora (dall’interno verso l’esterno):
All’interno della spora abbiamo il citoplasma circondato dalla membrana plasmatica, cui faccia interna è aderente al materiale nucleare, mentre la faccia esterna è aderente ad una parete cellulare rudimentale costituita da peptidoglicano
Esternamente alla parete cellulare poi abbiamo la Corteccia, formata principalmente da peptidoglicano e residui citoplasmatici dello sporangio
Poi abbiamo un rivestimento interno ed esterno proteico (coats), ricco di ponti disolfuro e piccole quantità di lipidi e peptidoglicano
Infine abbiamo l’Esosporio, sottile membrana fosfolipoproteica che contiene anche acidi teicoici, acido diaminopimelico e glucosamina
Componente caratteristico della spora è l’acido dipicolinico, un acido carbossilico localizzato insieme a grandi quantità di calcio nella corteccia
Funzione della Spora
Caratteristiche che la distinguono dalla cellula vegetativa (forma attiva del batterio):
Attività enzimatica e consumo di ossigeno molto ridotto
Assenza di sintesi macromolecolari
Estremamente resistente alla penetrazione di sostanze estranee (come i coloranti) a causa dei suoi spessi involucri esterni
Più resistente all’essiccamento, radiazioni UV e gamma
Notevole termoresistenza grazie ai due coats e la corteccia
Presenta antigeni esclusivi della spora.
Come fa ad essere così resistente?
Grazie al calcio, proteine acido-solubili, rivestimento sporale
La Sporificazione
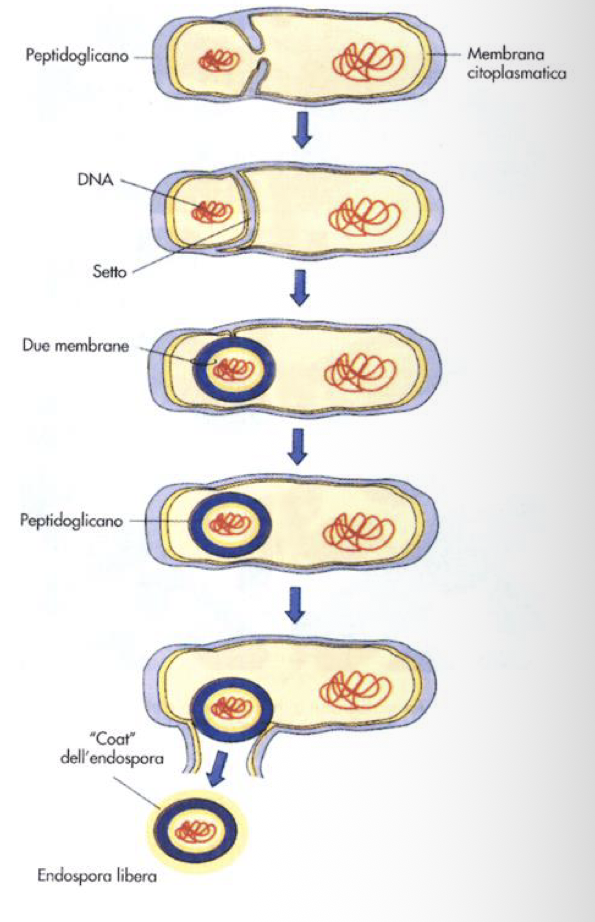
La Sporificazione:
Divisione del materiale nucleare
Uno dei nuclei risultati migra verso un polo della cellula e viene separato dal resto della cellula da un setto di membrana citoplasmatica → questa prima struttura la chiamiamo Prespora
A partire dalla prespora inizia la deposizione delle diverse membrana che formano la spora vera e propria, che completa dei suoi involucri, verrà liberata nell’ambiente esterno tramite degradazione dello sporangio
Tutto il processo dura dalle 6 alle 10 ore
Durante la formazione della spora si ha l’espulsione di oltre il 98% di acqua
Nei batteri sporigeni non è obbligatorio che si formi la spora, il batterio può essere mantenuto in fase vegetativa o essere indotto a formare la spora generalmente quando:
Si ha un progressivo esaurimento delle sostanze nutritive
Accumulo di cataboliti che rallentano la moltiplicazione batterica
Durante la fase di crescita, la produzione di spore non avviene
Con la sporificazione, si ha la modificazione del fattore sigma dell’RNA polimerasi → questo rende l’enzima incapace di trascrivere geni necessari alla vita vegetativa, e capace di trascrivere solo quelli coinvolti nella sporificazione
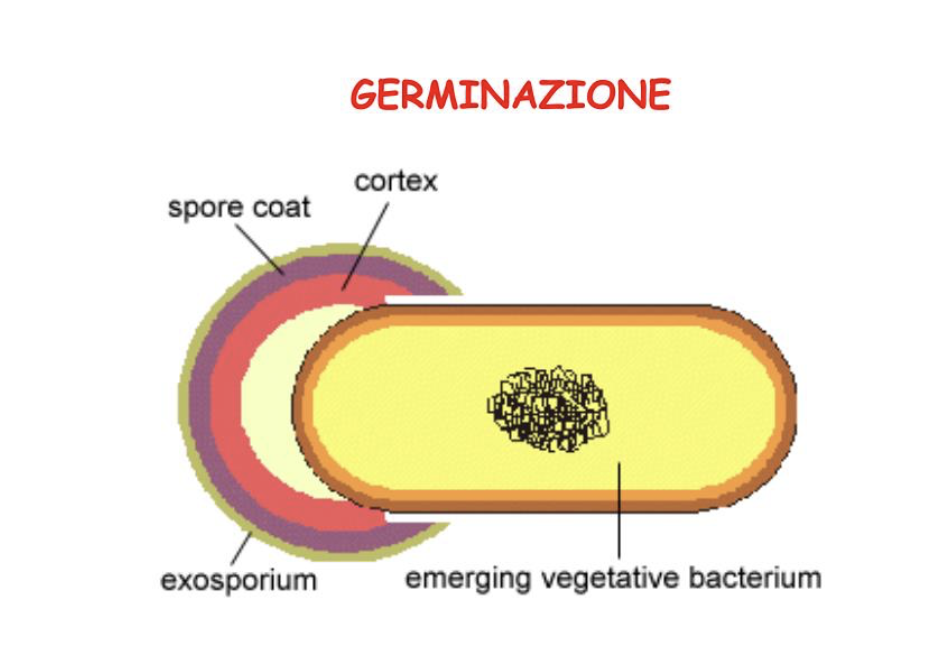
La Germinazione della spora
E’ il processo inverso, cioè da una spora si forma una nuova cellula vegetativa:
Avviene solo in condizioni favorevoli, in particolare quando sono disponibili sostanze nutritive
Spesso necessaria una fase di attivazione:
in laboratorio esponendo la spora a 65-80°C per alcuni minuti
in natura con l’invecchiamento della spora
Questa attivazione consiste in un danno che aumenta la permeabilità degli involucri della spora, che permette l’avvio degli scambi metabolici con l’ambiente
Tutto il processo dura circa 1-2 ore
Fasi:
Formazione di una parete cellulare completa, seguita dalla fuoriuscita della cellula vegetativa dagli involucri alterati
Si avrà l’eliminazione dell’acido dipicolinico e rilascio di grandi quantità di calcio
Ricompare la termosensibilità e sintesi macromolecolare
La cellula vegetativa neoformata può riprendere il ciclo di sporificazione o entrare in fase logaritmica di crescita
Come avviene l’eliminazione di una spora?
Non esistono farmaci per le spore.
Con il processo di Tindalizzazione o Sterilizzazione frazionata:
Riscaldare il materiale a 100°C per 30 minuti
Incubare a temperatura ambiente per 24 ore
Riscaldare nuovamente a 100°C per 30 minuti
Incubare altre 24 ore
Riscaldare per l’ultima volta
L’incubazione serve per far germinare le spore, poi le cellule vegetative vengono distrutte con il riscaldamento.
Importanza della metilazione
(dalle sbobine)
La metilazione è una modifica chimica che consiste nell’aggiunta di un gruppo metile a una base del DNA o RNA
Questa modifica regola l’espressione di geni, cioè decide se un gene deve essere più o meno attivo
Negli eucarioti la metilazione interessa la citosina, mentre nei procarioti interessa l’adenina in posizione 6
Negli eucarioti:
La metilazione favorisce una maggior compattazione della cromatina, in associazione con gli istoni nel nucleosoma
Quando il DNA è più compatto, i geni sono meno espressi
Dal punto di vista medico:
La metilazione può influenzare patologia, incluse le infezioni virali
La metilazione è un meccanismo di controllo dell’espressione che i virus sfruttano per:
replicarsi meglio
nascondersi
persistere nel tempo
L’Operone:
Un altro sistema di regolazione genetica nei batteri è dato dall’operone
E’ un sistema dove più geni consecutivi sono controllati da un unico promotore
In questo modo una cellula può attivare o silenziare più geni
Secrezione nei Procarioti - Pathways di secrezione proteica
I pathways di secrezione sec-dipendente (o pathway generale di secrezione):
Si tratta di un sistema tipico dei batteri, in grado di mediare la traslazione delle proteine attraverso la membrana plasmatica o per l’integrazione in essa.
Le proteine secrete vengono sintetizzate nel citosol come pre-proteine, che presentano un peptide segnale sull’N-terminale
Subito dopo la sintesi, una chaperonina (Sec-B) si lega al peptide segnale per non far ripiegare la proteina
A questo punto le proteine Sec-Y, Sec-E e Sec-G formano un canale transmembrana per far passare la pre-proteina
In particolare Sec-A guida il passaggio della pre-proteina attraverso la membrana sfruttando l’idrolisi di ATP.
Una volta attraversata la membrana, una peptidasi taglia il peptide segnale, così la proteina assume la sua conformazione finale
Un altro tipo è il Sistema Tat:
Tat sta per twin arginine traslocation, cioè indica la presenza di due arginine consecutive nella sequenza segnale
A differenza del sistema sec, le proteine trasportate sono completamente foldate
Pathway di secrezione di tipo II:
E’ proprio dei batteri gram negativi, costituito da 12-16 proteine, la maggior parte delle quali sono proteine di membrana
Trasporta dal periplasma alla membrana esterna le proteine traslocate dal sistema sec o tat (funziona come seconda porta)
Pathway di secrezione di tipo V:
Anch’esso tipico dei gram negativi
Detto anche sistema di autotrasporto perché una volta che le proteine vengono trasportate nel periplasma attraverso il sistema sec, formano un canale nella membrana esterna (con il loro dominio C-terminale) attraverso cui passano
La proteina così passa, poi proteasi lasciano la C-terminale all’interno della membrana esterna
Pathway di secrezione di tipo I o ABC:
Trasporta le proteine sia attraverso la membrana plasmatica che membrana esterna (forma un tunnel continuo)
E’ presente sia nei gram positivi che negativi
Si compone di un Trasportatore ABC inserito nella membrana plasmatica, che lega ATP e lo idrolizza per garantire il trasporto della proteina
Poi abbiamo una proteina adattatrice detta MFP (membrana fusion proteine) che lega il trasportatore alla proteina TolC presente sulla membrana esterna
Le molecole di questo sistema hanno grandezze variabili, generalmente è per tossine RTX e lipasi
Pathway di secrezione di tipo III:
Tipico dei gram negativi
Ha struttura a siringa che attraversa le due membrane e si inserisce sulla membrana della cellula ospite per rilasciare fattori di virulenza
Pathway di secrezione di tipo IV:
Sia in gram positivi che negativi
Responsabile della secrezione di proteine e DNA durante il processo di coniugazione batterica
N.B.:
Blebbing → fenomeno dei gram negativi che rilasciano vescicole di membrana contenenti fattori di virulenza
I micobatteri presentano uno specifico pathway detto ESX-1 e consente alle proteine di attraversare gli spessi strati di arebinogalactani e di acidi micolici che caratterizzano l’involucro esterno dei micobatteri
Genetica Batterica - I Plasmidi
Il batterio non ha solo il cromosoma principale, ma anche i plasmidi che sono elementi genetici extra-cromosomici di DNA circolare, bicatenario:
Molto più piccoli del cromonema: 1-200mila basi vs 1-5milioni di basi
I plasmidi non sono essenziali per vivere, ma danno vantaggi, generalmente codificano per:
Tossine
Pili/adesine
Fattori R (danno resistenza a farmaci)
Batteriocine (uccidono altri batteri)
Siderofori (catturano ferro fondamentale per la crescita)
Alcuni plasmidi sono detti coniugativi:
Permettono il contatto tra batteri, formando un ponte dove possono passare altri plasmidi o addirittura mobilizzare il cromonema
Altri plasmidi sono detti episomi che possono replicarsi in modo autonomo o integrarsi nel cromosoma batterico e replicarsi con esso.
Trasformazione
La trasformazione è un modo con cui i batteri prendono DNA libero dall’ambiente e lo incorporano nel proprio genoma per acquisire nuove caratteristiche genetiche
L’esperimento di Griffith (1920):
In una cavia viene inoculato:
batteri non capsulati vivi non virulenti
batteri capsulati uccisi, ma virulenti
L’esito dell’esperimento porta alla morte della cavia per setticemia e i batteri isolati corrispondevano a batteri capsulati virulenti vivi
Quello che è successo è che i batteri vivi hanno preso qualcosa da quelli morti e sono diventati virulenti → questa sostanza trasformante è il DNA
Il processo di trasformazione:
Il batterio accettrice deve trovarsi in uno stato di competenza:
questo si lega con il DNA nell’ambiente derivante dalla morte di un batterio donatore
un filamento viene distrutto dalle nucleasi e un’altro entra nella cellula
Differenza gram positivi e negativi:
Gram positivi producono il fattore di competenza che attiva proteine come autolisine che aprono la parete cellulare per esporre un tratto di membrana dove si posizionano proteine che legano il DNA bicatenario
Gram negativi invece non producono il fattore di competenza, quindi la trasformazione avviene solo in condizioni particolari (quindi più difficile)
Dalle sbobine → La trasformazione viene favorita attraverso:
Elettroporazione → shock elettrico rende le membrane permeabili al DNA
Calcio cloruro/heat shock → il calcio cloruro rende le cellule più fragili e permeabili, il calcio neutralizza le cariche negative del dna, poi lo shock termico facilita l’ingresso del dna
Trasduzione
La trasduzione è un trasferimento di DNA tra batteri mediato da un batteriofago:
Un fago è un virus che infetta i batteri, presenta tipica forma a spillo con:
una testa contenente l’acido nucleico
una coda che inietta il DNA
fibre che riconoscono il batterio
Il fago si lega al batterio, inietta il DNA e poi possiamo avere due possibilità:
Ciclo Litico → il fago si replica subito, produce tante copie che si liberano con la conseguente lisi della cellula ospite. Parliamo di fagi virulenti
Ciclo Lisogeno → il DNA del fago si integra nel batterio e si forma un profago. Poi resta silente e si replica insieme al batterio. Poi può riattivarsi e indurre un ciclo litico. Parliamo di fagi temperati
Durante questi processi, il fago può trasferire DNA batterico da un batterio all’altro, distinguiamo due tipi di trasduzione:
Trasduzione Generalizzata → avviene nel ciclo litico. Durante la replicazione il fago sbaglia e prende DNA batterico invece che suo. Così infettando un altro batterio trasferisce quel DNA.
Trasduzione Specializzata → avviene nel ciclo lisogeno. il DNA virale a un certo punto si stacca da quello batterico, però erroneamente può portarsi via anche un pezzo di DNA batterico.
La differenza tra i due tipi è che il primo prende DNA batterico casuale, quindi può trasferire qualsiasi gene, mentre il secondo prende un pezzo specifico, quindi trasferisce geni specifici
Conversione lisogenica
Nei batteri lisogeni abbiamo detto che il DNA del profago rimane generalmente silente, ma in alcuni casi una parte del genoma del profago viene espressa.
Quando questo succede si ha la codifica per prodotti che modificano il fenotipo del batterio.
Questi prodotti non sono coinvolti nei processi replicativi del virus, non servono all’economia generale del fago e sono meno sensibili al controllo repressivo.
Questi prodotti possono rendere il batterio più virulento, resistente e capace di produrre tossine.
Coniugazione Batterica
Consiste nel diretto trasferimento di materiale genetico da un batterio a un altro, attraverso un contatto fisico tra le due cellule:
Questo processo avviene per mezzo di Plasmidi Coniugativi, tra cui il plasmide F
Plasmide F (presente in E.coli e altri enterobatteri):
E’ una molecola di DNA circolare bicatenario, che si replica autonomamente
geni “tra” codificano per un pilo F e proteine per la replicazione del DNA (pathway tipo IV)
Quando una cellula contente il plasmide F (cellula F+, donatrice) incontra una che non lo ha (cellula F-, accettrice):
Si formano coppie coniugali
Il pilo F della cellula F+ si lega alla cellula F- e si stabilisce un ponte coniugativo
Poi il plasmide F viene tagliato al punto “oriT” (origine di trasferimento) e parte il trasferimento
Trasferimento:
Un singolo filamento di DNA passa al ricevente
Contemporaneamente:
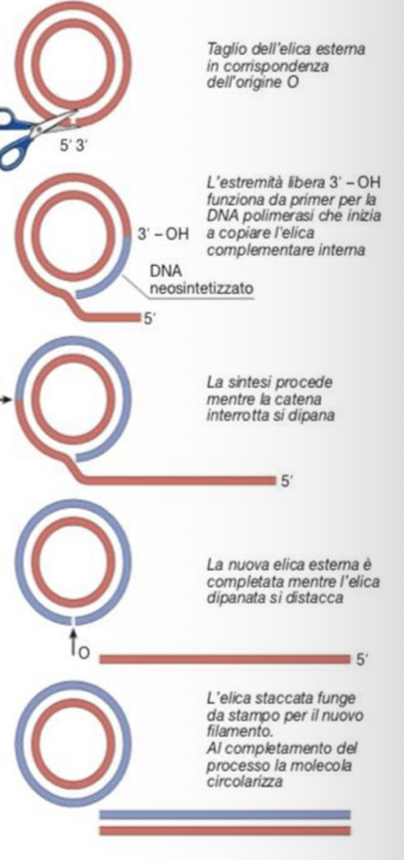
nel donatore avviene la replicazione (Rolling Circle)
nel ricevente avviene la sintesi del filamento complementare
Risultato → il ricevente diventa F+
Come avviene il trasferimento del materiale cromosomico?
A volte il plasmide F si integra nel cromosoma batterico grazie a sequenze di inserzione (IS) → queste cellule si chiamano Hfr (high frequency of recombination)
Quindi quando una cellula Hfr incontra una cellula F-, oltre il plasmide F viene trasferito anche DNA cromosomico
ma il trasferimento è lungo, lento e il ponte è fragile, quindi il cromosoma non viene trasferito mai completamente
quindi il ricevente resta F-
Meccanismo alternativo dei Gram positivi:
Non usano i pili F (come enterococcus faecalis), ma usano ferormoni
Rilasciati da cellule accettrici, si legano a recettori presenti sulle cellule donatrici (F+)
Questa interazione induce il rilascio di sostanza aggregante da cellule donatrici, che forma accumuli che stabiliscono un contatto tra cellule.
Così il plasmide coniugativo passa da cellula a cellula attraverso contatto diretto
La coltivazione dei batteri - terreni di coltura
Il terreno di coltura rappresenta un mezzo artificiale attraverso cui i batteri possono crescere, svilupparsi ed essere studiati, le principali caratteristiche che deve avere sono:
Nutrienti adeguati per la crescita batterica
Giusta umidità
pH adatto
Sterilità
Componenti principali del terreno:
Peptoni → derivano da proteine (caseina, soia) per idrolisi (acida o enzimatica)
NaCl → aggiunta per necessità osmotiche richieste ad alcuni microrganismi
Zuccheri
Estratti di lievito, carne e d’organo → ricchi di fattori di crescita e sali
Arricchimenti → sangue, emoglobina, vitamine per batteri più esigenti
Supplementi selettivi → come antibiotici o sali biliari per bloccare alcuni batteri e favorirne altri
Indicatori → sostanze coloranti (come il fenolo) che cambiano colore in base al pH, così da seguire il processo fermentativo del batterio in studio.
Classificazione dei terreni di coltura in base allo stato fisico
In base allo stato fisico distinguiamo terreni liquidi e solidi:
Liquidi:
Sono brodi (senza solidificante)
Con lo sviluppo dei batteri il terreno diventa torbido → questo intorpidimento può essere uniforme, a granuli o solo in zone specifiche
Solidi:
Differiscono per la presenza di un solidificante (agar)
L’Agar è un polisaccaride acido estratto da alcune alghe, il quale, disciolto a temperature maggiori a 80°C in un liquido, ne provoca la gelificazione durante il successivo raffreddamento
L’agar non è tossico per i batteri e solo pochissimi batteri sono in grado di depolimerizzarlo liquefacendo il terreno
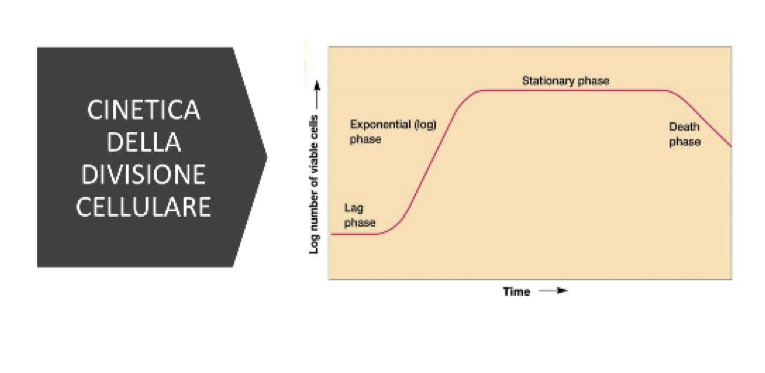
Curva di crescita batterica
E’ il grafico che descrive come cresce una popolazione batterica nel tempo:
Fase di latenza → qui non si osserva nessun aumento di batteri, perché prima devono sintetizzare gli enzimi necessari alla metabolizzazione dei substrati del terreno
Fase di accelerazione di crescita → inizia la crescita e moltiplicazione
Fase esponenziale o logaritmica → fase di crescita e divisione rapida
Fase di decelerazione di crescita → i nutrienti piano piano si esauriscono e le scorie tossiche che aumentano andranno a ridurre la crescita
Fase stazionaria → il numero di batteri che nascono e quelli che muoiono si bilanciano, quindi il loro numero rimane costante
Fase di morte o declino → i batteri muoiono di più di quanto nascono
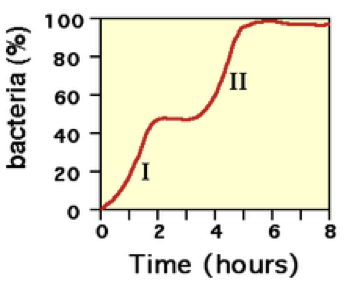
Curva di crescita diauxica (studiato da Monod):
Particolare tipo di crescita, dove osservò che alcuni batteri coltivati in presenza di due zuccheri, uno semplice e uno più complesso, i batteri usavano prima lo zucchero semplice e poi quello complesso
Si osservano così due fasi esponenziali separate da una pausa che serve al batterio per sintetizzare gli enzimi atti a metabolizzare il secondo substrato
Nel grafico della foto la curva parte da zero → il prof fa notare che è un errore
Dalle sbobine → possibile domanda di esame: disegnare curva di crescita batterica (non farla partire dall’origine degli assi)
Dalle sbobine → fattori che influenzano la fase di latenza:
condizioni chimico-fisiche: temperatura, pH, osmolarità, nutrienti
caratteristiche dell’inoculo: numero di batteri, stato dei batteri (vivi o morti, fase di provenienza)
Composizione chimica dei terreni di coltura
I terreni di base per batteri non esigenti sono:
Brodo normale (liquido) → costituito da peptoni, estratto di carne, nacl e tampone fosfato (che mantiene ph intorno a 7)
Agar normale (solido) → brodo normale + agar 1,5%
A questi terreni standard si possono aggiungere sostanze per coltivare batteri più esigenti, come:
Sangue → arricchisce il terreno e permette di rilevare tossine emolitiche
Siero → non solo arricchisce il terreno, ma elimina sostanze tossiche grazie all’albumina (che le lega)
Liquido Ascitico
Estratto di Lievito
Classificazione funzionale dei terreni di coltura
Classificazione in base alla funzione:
Terreni di arricchimento (o elettivi) → favorisce la crescita del batterio di interesse
Terreni selettivi → presenta sostanze batteriostatiche (come cirstalvioletti, sali biliari, tellurico di potassio) che inibiscono lo sviluppo di molte specie, isolando così solo quelli resistenti
Terreni differenziali → contengono indicatori (di solito di pH) che permettono di distinguere i batteri in base al loro metabolismo
Preparazione di un terreno di coltura
Pesatura dei componenti
Aggiunta di acqua distillata
Solubilizzazione: agitazione fino a completa dissoluzione
Controllo del pH
Chiusura della beuta → non chiudere ermeticamente perché durante la sterilizzazione, la temperatura e pressione sale, quindi si ha rischio esplosione (in fase di raffreddamento). Per questo vengono usati tappi in cotone che permettono il passaggio d’aria per bilanciare la pressione
Sterilizzazione → con autoclave
Raffreddamento → terreni liquidi raffreddati fino a 25°C, quelli solidi versati nelle piastre di Petri prima che solidifichino
Solidificazione (per agar)
Semina → si inocula il batterio nel terreno solidificato
Teniche di semina
La semina consiste nel depositare i batteri su un terreno di coltura. Le tecniche sono:
Semina per isolamento (striscio)
La più usata
Con un ansa sterile si striscia sulla superficie dell’agar in varie zone per disperdere le varie cellule
Semina per inclusione
Usata per la conta di colonie batteriche
Si mescola la sospensione batterica con un agar liquido che successivamente solidificherà
Spesso si fanno diluizioni (con NaCl 0,9%) per diminuire il numero di cellule seminate ed avere un numero contabile di colonie
Semina per infissione
Avviene in provetta mediante un ago da inoculo che si infilza nel terreno agar molle
Permette di studiare la crescita in alto (aerobica), in basso (anaerobica) o diffusa (anaerobio facoltativo)
Permette di studiare anche la motilità del batterio, se la crescita è diffusa allora il batterio è mobile (flagelli)
Se uso Nutrient Gelatine testo l’attività proteolitica del batterio, se il batterio degrada la gelatina sarà proteolitico
Disinfezione e Sterilizzazione
Differenza principale:
La disinfezione elimina i microrganismi patogeni
La sterilizzazione elimina TUTTI i microrganismi (comprese le spore)
Disinfezione:
Avviene attraverso sostanze chimiche (disinfettanti)
Meccanismi d’azione:
Denaturazione delle proteine → alcoli, fenoli e metalli pesanti si combinano a proteine provocandone le loro in’attivazione e precipitazione
Ossidazione dei gruppi sulfidrilici liberi o altri gruppi funzionali di enzimi → si usano perossidi (come il perossido di idrogeno, altre sostanze sono lo iodio, cloro, permanganati) che danneggiano gli enzimi
Alterazione delle membrane per solubilizzazione dei lipidi → calcoli, fenoli, ammonio quaternario, clorexidina
Sterilizzazione:
Metodi Chimici:
Formaldeide (vapori)
Ossido di etilene (gas)
Per materiali sensibili al calore
Metodi Fisici:
Calore secco (stufa) → 2 ore a 180 o 3 ore a 140°C
Calore umido (autoclavi) → calore del vapore acqueo sotto pressione che consentono una sterilizzazione sicura a temperature e tempistiche minori (110-120°C per 15-20 minuti)
Filtrazione → per sostanze particolarmente termolabili, presentano pori e il materiale può essere cellulosa, vetro e porcellana
N.B:
La bollitura non garantisce una sterilizzazione assoluta perché alcune spore possono resistere alla temperatura di ebollizione dell’acqua (100°C) → motivo per cui usiamo l’autoclave che ci permette di raggiungere temperature più elevate
Anche le radiazioni ionizzanti possono essere usate per la sterilizzazione → queste possono agire sul DNA e strutture cellulari attraverso la formazione di perossidi instabili
Dalle Sbobine → Come identifichiamo un batterio?
Identificazione biochimica:
Usato in passato
Si identificava il suo metabolismo e ricercati i suoi geni fondamentali
Spettrometria di massa:
E’ il metodo usato oggi
Dalle Sbobine → Dove, nel genoma dei procarioti anche singole mutazioni puntiformi sono incompatibili con la vita?
Nei geni ribosomiali 16s, perché qui la probabilità che quella piccola mutazione dia un vantaggio è infinitesimale
Dalle Sbobine → Glicocalice Batterico
Struttura accessoria del batterio - Glicocalice:
Rivestimento esterno della cellula batterica presente sia nei gram + che -
Composto principalmente da polisaccaridi
Serve soprattutto per protezione e adattamento dell’ambiente
Può presentarsi in due forme:
Capsula → ben organizzata, compatta e rigida, ben aderente alla cellula, con funzione principale di protezione
Slime (strato mucoso) → meno organizzato, più lasso e meno compatto, poco aderente, con funzione principale di adesione e formazione di biofilm → concetto importante nei pazienti con fibrosi cistica
Nella fibrosi cistica:
Si accumula muco denso nelle vie respiratorie che rappresenta un terreno favorevole per la colonizzazione batterica e un ostacolo per la funzione di difesa dell’apparato respiratorio
In questo contesto, il batterio Pseudomonas Aeruginosa, che è un batterio opportunista, può causare infezioni polmonari croniche
questi batteri, grazie allo strato mucoso, si aggregano e formano il biofilm che risulta fino a 1000 volte più resistente al sistema immunitario e antibiotici
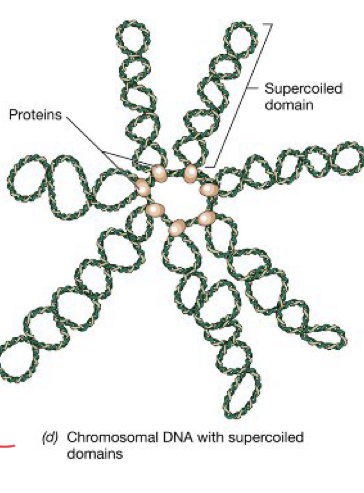
Dalle Sbobine - Come fa il cromosoma batterico ad essere compattato?
Il DNA batterico è circolare e molto lungo, quindi deve essere compattato:
Non è un’unica superelica, ma diviso in domini superavvolti (loop)
Ogni loop è stabilizzato da proteine del nucleoide
Viene fuori una forma a margherita
Dalle sbobine - il citoscheletro procariotico
Per molto tempo si è pensato che i procarioti fossero privi di citoscheletro, ma oggi sappiamo che ci sono proteine omologhe ai princiapali elementi del citoscheletro eucariotico:
Queste hanno un ruolo chiave nella divisione cellulare, nella localizzazione delle proteine e nella determinazione della forma batterica
ParM è simile all’actina ed è coinvolta nella segregazione attiva di alcuni plasmidi, cioè sono fondamentali durante la replicazione dei plasmidi e loro successiva distribuzione alle cellule figlie
La distribuzione dei plasmidi si basa su due modalità:
Probabilistica → maggiore è il numero di plasmidi, maggiore è la possibilità che si distribuiscono ad entrambe le cellule nascenti
Molecolare → tipica dei plasmidi a basso numero di copie. Una volta replicati i plasmidi, i filamenti di ParM ne determinano l’allontanamento fisico, spingendoli ai poli opposti così che ogni cellula figlia ne riceva una copia.
Dalle sbobine - Corpi di inclusione
Il citoplasma dei procarioti è costituito principalmente da acqua in cui sono sospesi il nucleoide, ribosomi e corpi di inclusione.
I corpi di inclusione organica sono fondamentali per il metabolismo batterico e sono:
Glicogeno → riserva di glucosio e energia
Poli-beta-idrossibutirrato (PHB) → riserva di carbonio
Granuli di cianoficina → riserva di azoto
Carbossisomi → contengono l’enzima RuBisCo importante nella fissazione del carbonio
Vacuoli gassosi → ruolo cruciale nel galleggiamento dei cianobatteri
Magnetosomi → strutture contenenti cristalli magnetici che permettono al batterio di orientarsi rispetto al campo magnetico terrestre
Dalle sbobine - Il Biofilm
Il biofilm è una comunità microbica immersa in una matrice extracellulare autoprodotta costituita da una miscela di carboidrati, acqua, proteine e altre sostanze, aderente a una superficie inerte o vivente, all’interno della quale è dispersa la comunità batterica.
E’ una struttura che può apparire lassa, ma risulta estremamente compatta e resistente.
Funzioni:
Protezione → da enzimi degradativi e variazioni di pH
Adesione → permette al batterio di colonizzare superfici e resistere a sollecitazioni meccaniche (ad esempio, il flusso di urina non riesce a eliminare un biofilm)
Virulenza → protegge il batterio dal sistema immunitario e antibiotici
Rilevanze clinica:
Esempi tipici di biofilm si formano su cateteri vescicali, accessi venosi, protesi
Identificare il batterio e iniziare l’antibiotico può non essere sufficiente per la guarigione, proprio perché la resistenza data dalla matrice, può ostacolare il raggiungimento del target da parte del farmaco.
Per superare questo ostacolo bisogna valutare una terapia poli-farmacologica, cioè si selezionano gli antibiotici con migliore capacità di penetrare nel biofilm
(la formazione del biofilm avviene in pochi giorni)
Biofilm come comunità:
Nell’ambiente del biofilm, i batteri si attivano a vicenda → il batterio di “destra” produce molecole necessarie per il batterio di “sinistra” e viceversa → è favorita così la crescita cellulare
Quando la popolazione batterica raggiunge il “quorum sensing”, il batterio beneficia dell’appartenenza alla comunità e comincia a crescere e manifestare i propri fattori di virulenza
Principali produttori di biofilm:
P. aeruginosa (polmoni)
E. Coli, Enterococcus (prostatite)
Streptococcus mutans (carie)
Streptococchi viridanti (valvole mitraliche)
Dalle Sbobine - Il Blebbing
Il blebbing è il processo con cui le cellule, compresi i batteri, rilasciano vescicole extracellulari usate per la comunicazione → questo fenomeno è importante soprattutto nell’asse intestino-cervello, dove molecole di origine batterica possono influenzare anche funzioni del sistema nervoso.
Nei batteri gram negativi queste vescicole sono chiamate OMV e derivano dalla membrana esterna:
Possono contenere LPS e altre molecole, quindi hanno un ruolo importante nell’infiammazione e interazione con l’ospite
Oggi è molto studiato il loro possibile coinvolgimento nel superamento di barriere biologiche come quella intestinale o emato-encefalica
(anche i gram positivi possono produrre vescicole, ma in un processo più complesso per la presenza della spessa parete di peptidoglicano)
In generale, queste vescicole possono modulare la risposta infiammatoria.
Abbiamo visti che un batterio può acquisire il DNA in tre modi:
Trasformazione, Trasduzione, Coniugazione
La quarta modalità è il trasferimento genico orizzontale e verticale mediato dalle OUTER MEMBRANE VESCICLES
Dalle Sbobine - La PCR e la Taq Polimerasi
La PCR (polimerasi chain reaction) è una tecnica che permette di amplificare un frammento di DNA:
Il processo avviene attraverso cicli ripetuti di riscaldamento e raffreddamento → prima ili DNA si separa, poi si legano i primer e infine la polimerasi sintetizza nuovi filamenti
L’enzima fondamentale è la Taq Polimerasi:
Isolata da microrganismi termofili
La sua importanza sta nel fatto che resiste alle alte temperature (circa 95°C) necessarie durante la PCR
Prima della sua scoperta bisognava aggiungere nuova DNA polimerasi dopo ogni ciclo, perché il calore la inattivava, invece con la Taq, la PCR è diventata un processo automatico.
Dalle Sbobine - Come contiamo le cellule procariotiche?
Metodi diretti:
Conteggio in camera contaglobuli
la camera contaglobuli è un vetrino con griglia incisa
si osserva al microscopio una quantità nota di sospensione e si contano le cellule presenti nei quadranti, così si calcola quante cellule ci sono in un ml
Conta reale su piastra
Si prende la coltura batterica, si fanno diluizioni e poi si semina il campione, dopo l’incubazione si contano le colonie cresciute e, conoscendo la diluizione, si risale al numero di batteri vitali presenti nella soluzione iniziale
Filtrazione su membrana
La soluzione passa attraverso una membrana con pori che trattengono i batteri, e poi questa viene posta su una piastra per contare le colonie
Metodi indiretti:
Spettrofotometro
misura quanta luce attraversa una soluzione contenente batteri
se in soluzione ci sono molte cellule, passa meno luce e la coltura appare più torbida, se invece passa più luce significa che la crescita è minore
ma questo metodo non distingue le cellule vive e morte
Peso secco
si centrifuga la coltura, si elimina la parte liquida e si pesa il pelle batterico per stimare la quantità di microrganismi presenti