Cellesignalering: ECM
1/91
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
92 Terms
Hvad er den extracellulære matrix, ECM?
Et netværk af makromolekyler uden for cellerne, som giver væv mekanisk støtte, struktur og signaler til cellerne.
ECM er en aktiv og organiseret struktur, som påvirker cellers form, adfærd og vævets egenskaber.
Celler ligger indlejret i et fibrøst og gel-lignende netværk, som de både påvirker og påvirkes af.
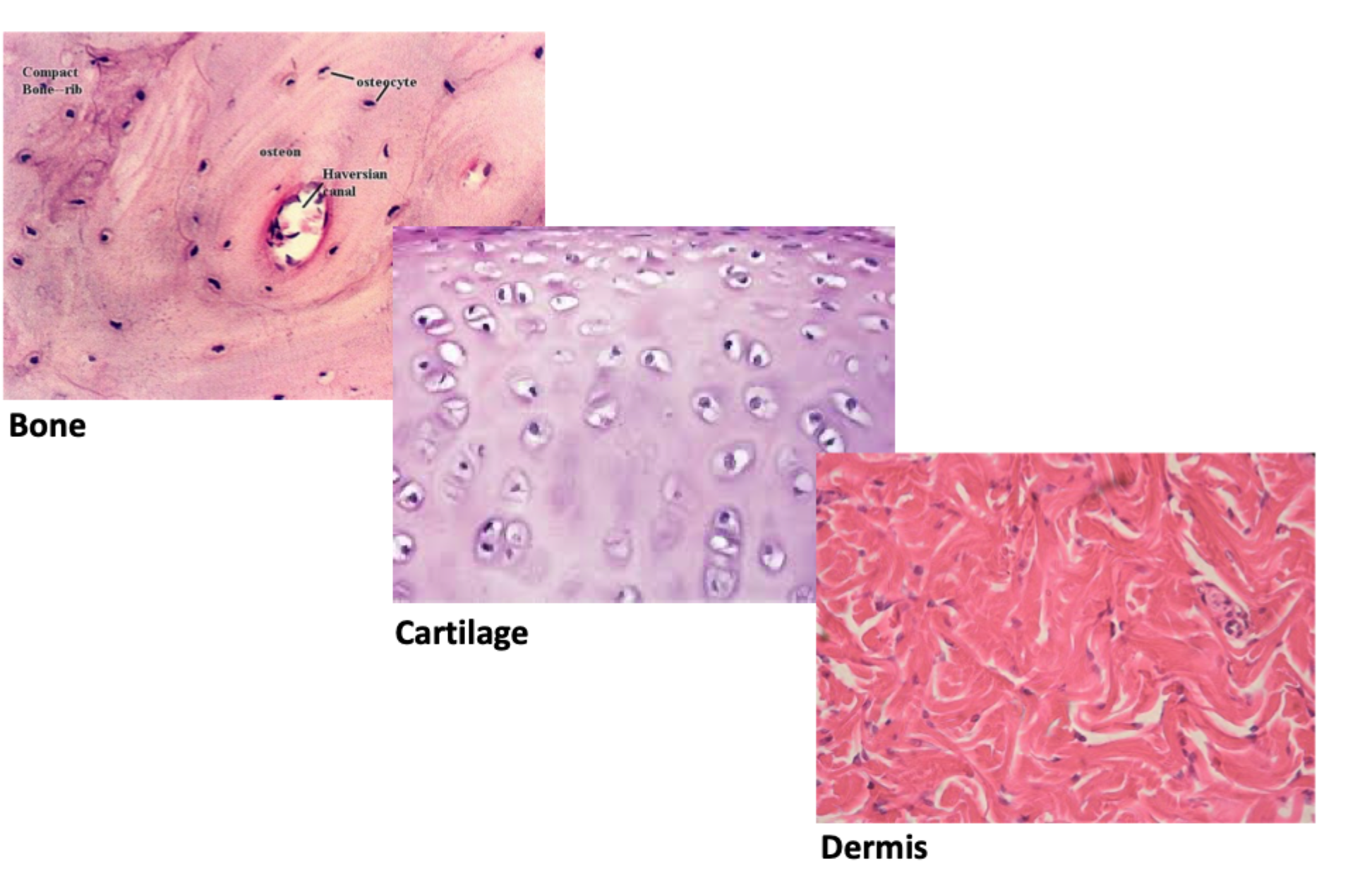
Hvad bestemmer forskelle i vævsstyrke mellem fx knogle, brusk og dermis?
Forskelle i ECM-sammensætning og organisering.
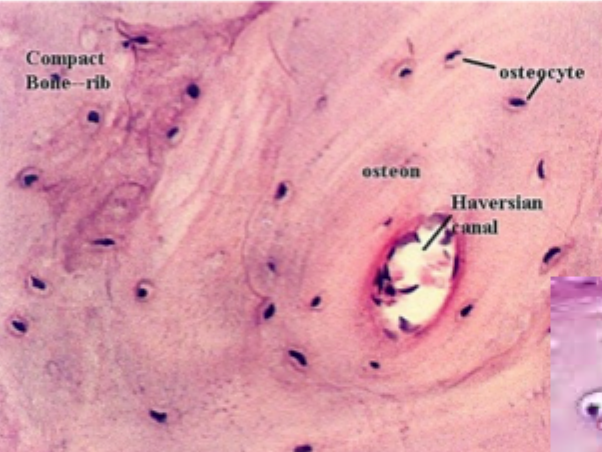
Hvorfor er knogle hårdt?
Fordi det har en ECM, der er stærkt organiseret og mineraliseret.
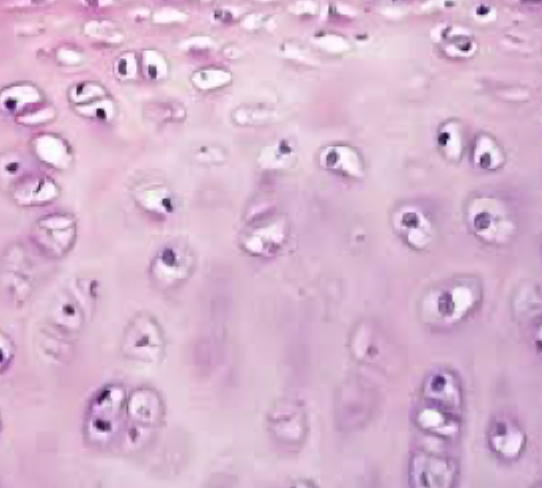
Hvorfor kan brusk modstå tryk?
Fordi det har meget vandbindende ground substance, især proteoglykaner/GAGs, som giver trykmodstand.
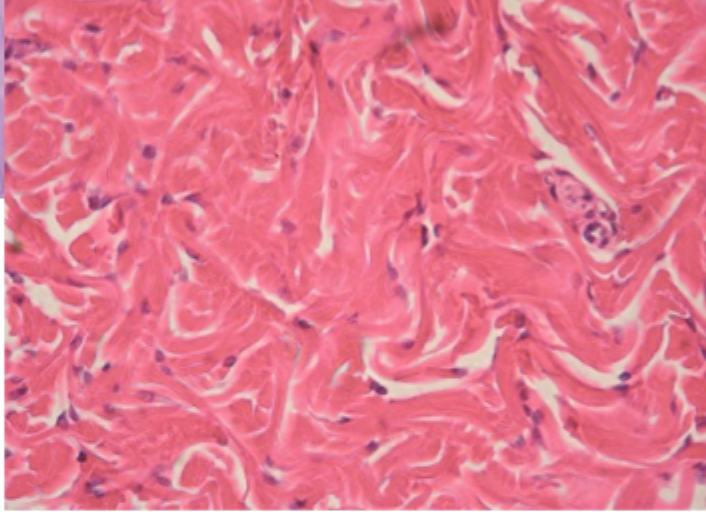
Hvorfor er dermis stærkt men mere fleksibelt end knogle?
Fordi ECM her især domineres af kollagenfibre organiseret uden mineralisering.
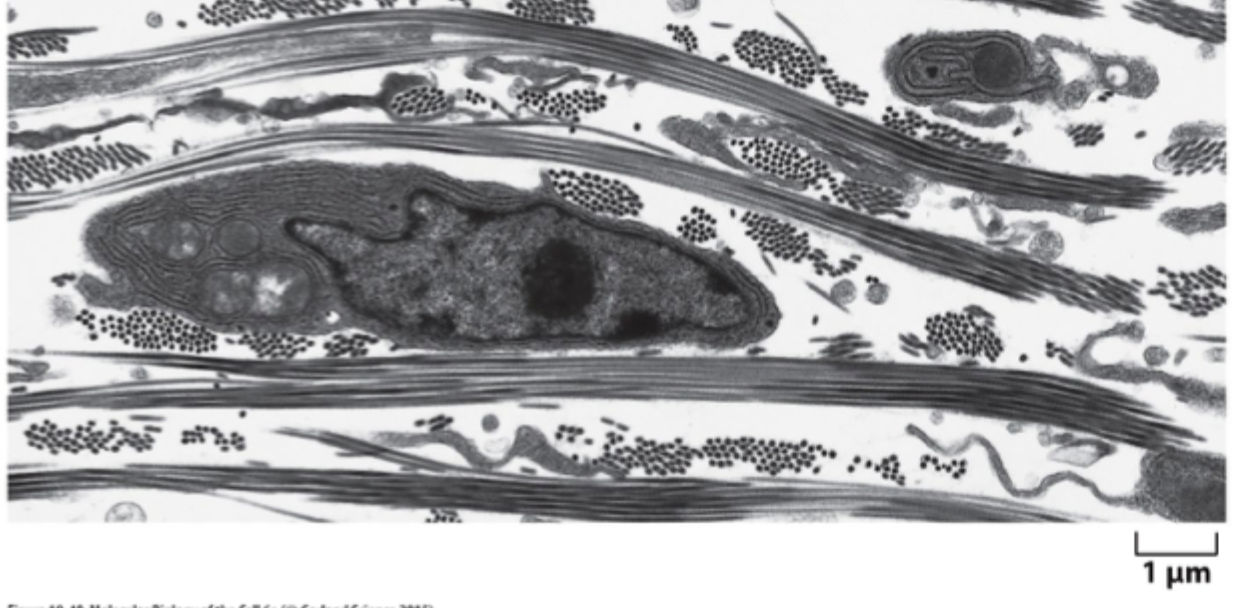
Hvilke tre hovedklasser af makromolekyler består ECM af?
GAGs/proteoglykaner, fibrøse proteiner og glycoproteiner.
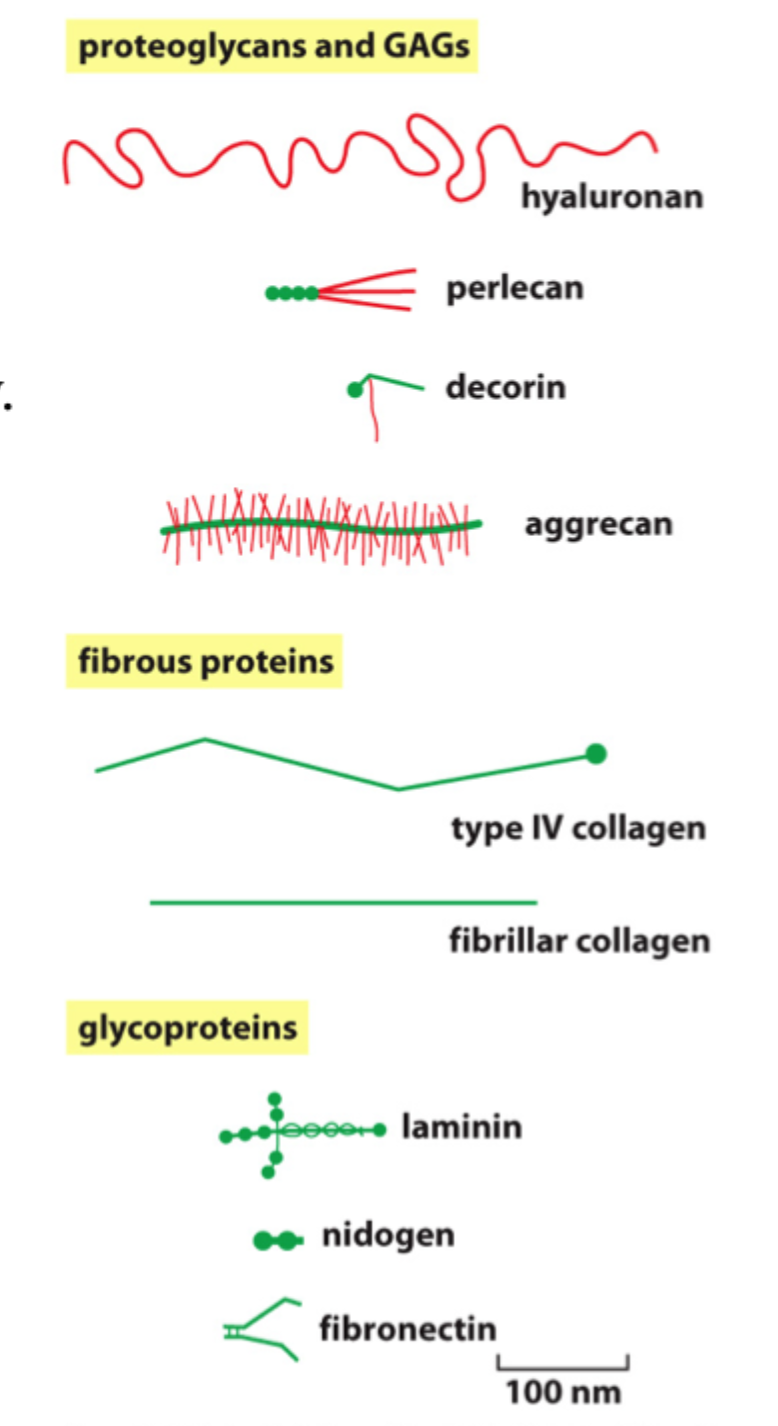
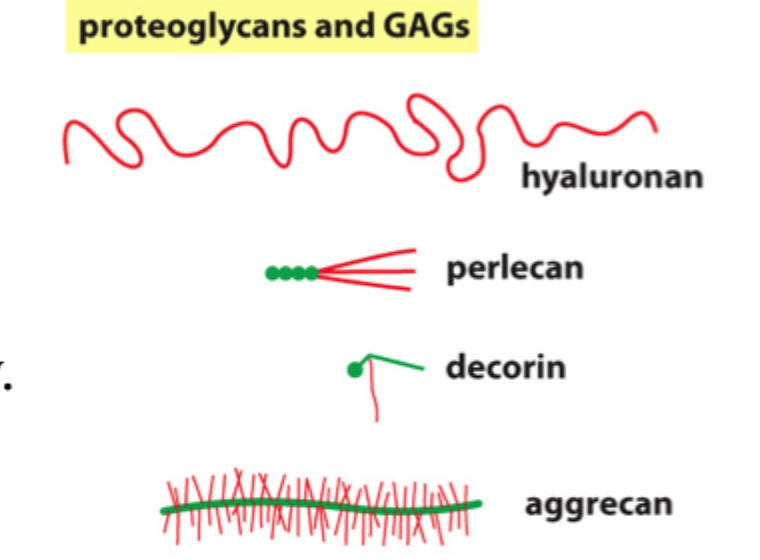
Hvad er glycosaminoglycans, GAGs?
Lange polysakkarider, som ofte er koblet til proteiner og danner proteoglykaner.
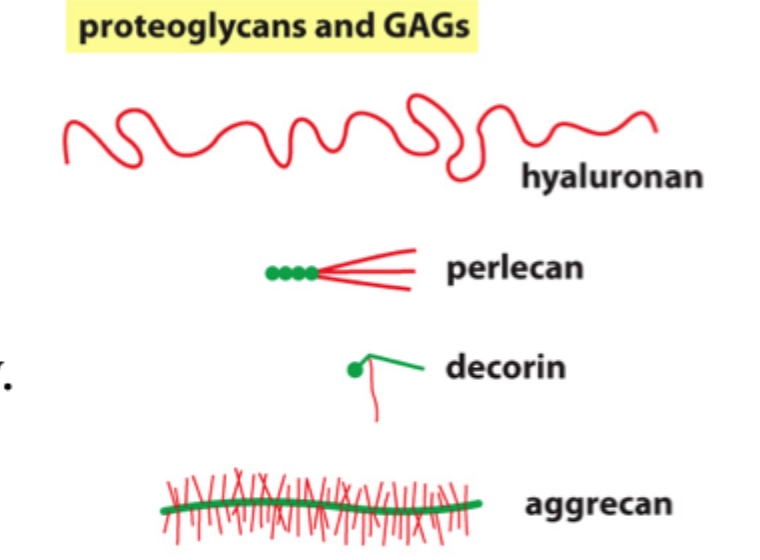
Hvad er hovedfunktionen af GAGs og proteoglykaner?
At danne den gel-lignende ground substance, som binder ioner og tiltrækker vand.
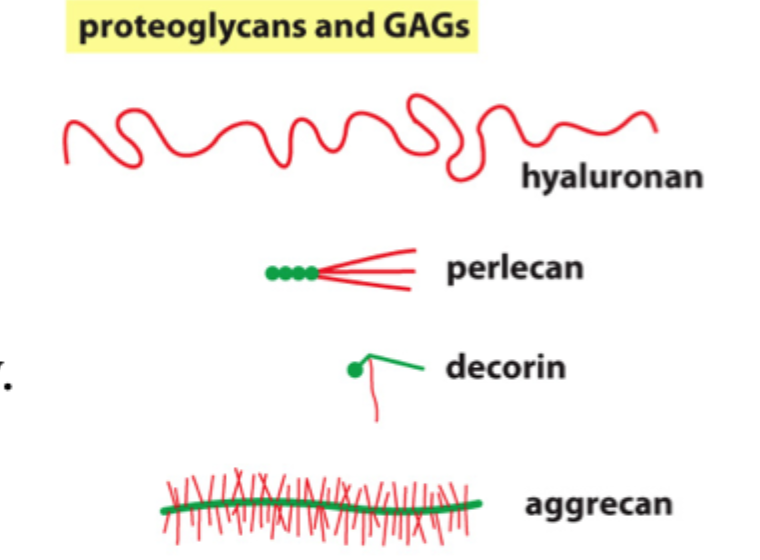
Hvorfor binder proteoglykaner meget vand?
Fordi deres GAG-kæder er stærkt negativt ladede og derfor tiltrækker kationer og vand.
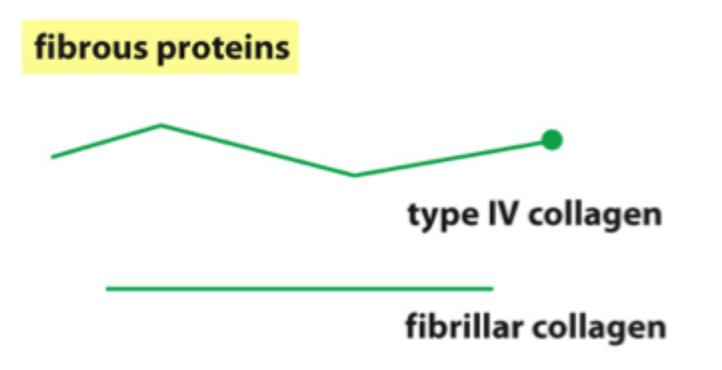
Hvad er hovedfunktionen af fibrøse proteiner i ECM?
At give trækstyrke og struktur, især via kollagen.
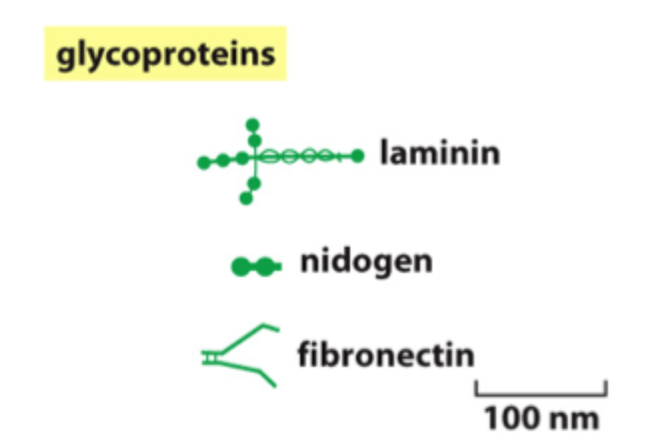
Hvad er hovedfunktionen af ECM-glycoproteiner?
At hjælpe med organisering, binding og kobling mellem ECM-komponenter og celler.
Hvad er forskellen på en GAG og et proteoglykan?
En GAG er polysakkaridkæden, mens et proteoglykan er et core-protein med én eller flere GAG-kæder bundet på.
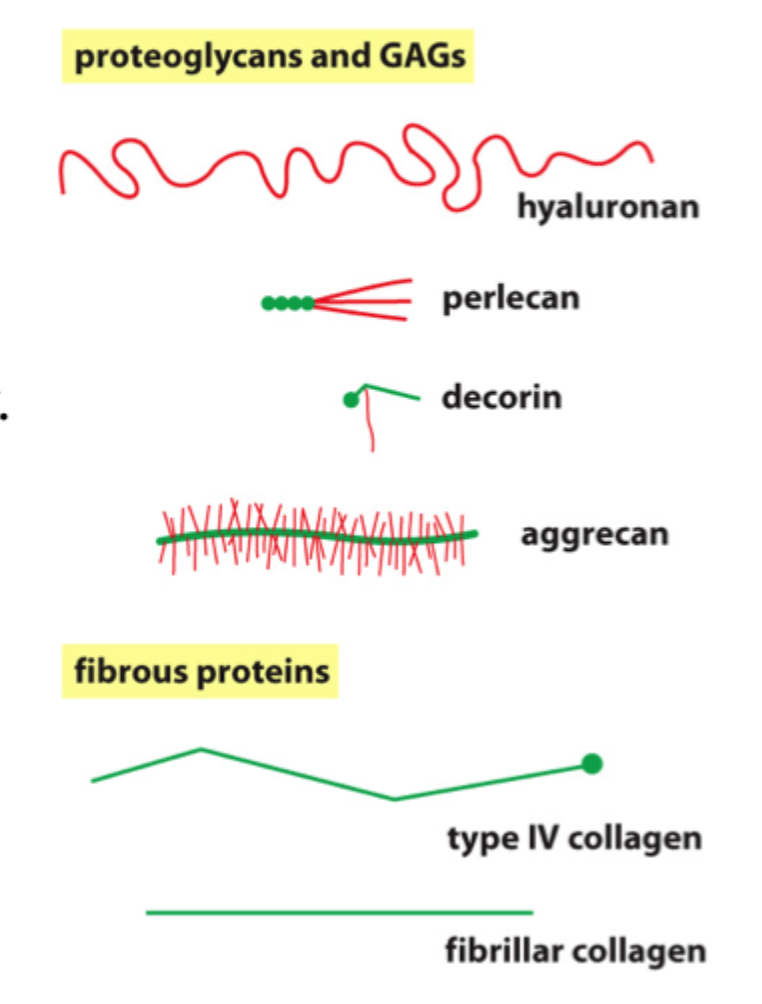
Hvad er hyaluronan særligt ved?
Det er en stor GAG, som ikke nødvendigvis er koblet til et core-protein som klassiske proteoglykane
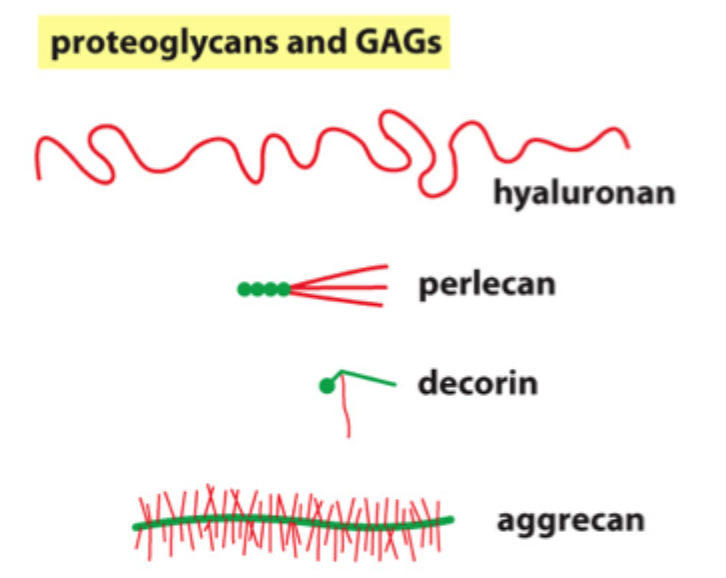
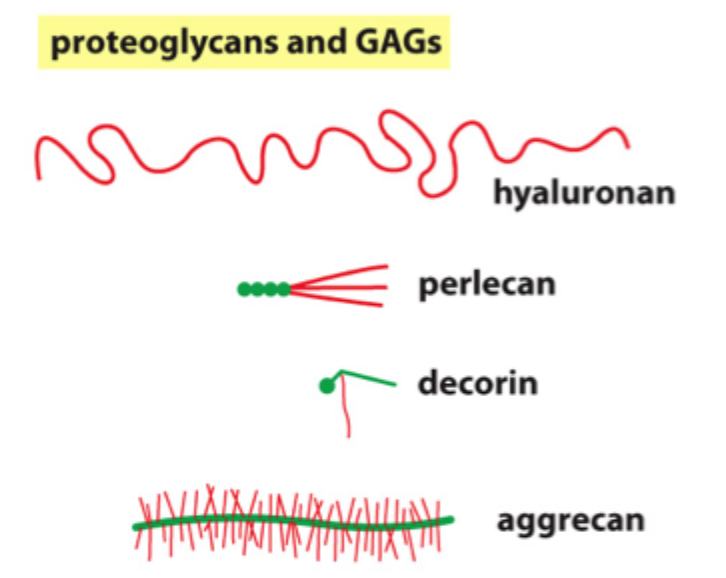
Hvad er hovedpointen med aggrecan, decorin og perlecan på sliden?
At forskellige proteoglykaner har forskellig størrelse og funktion, men alle bidrager til ECM’s fysiske egenskaber.
Hvad er de vigtigste proteiner i ECM?
Kollagener
Hvor stor en del af kroppens samlede proteinmasse udgør kollagen cirka?
Omkring 25 %.
Hvad er den grundlæggende struktur af et kollagenmolekyle?
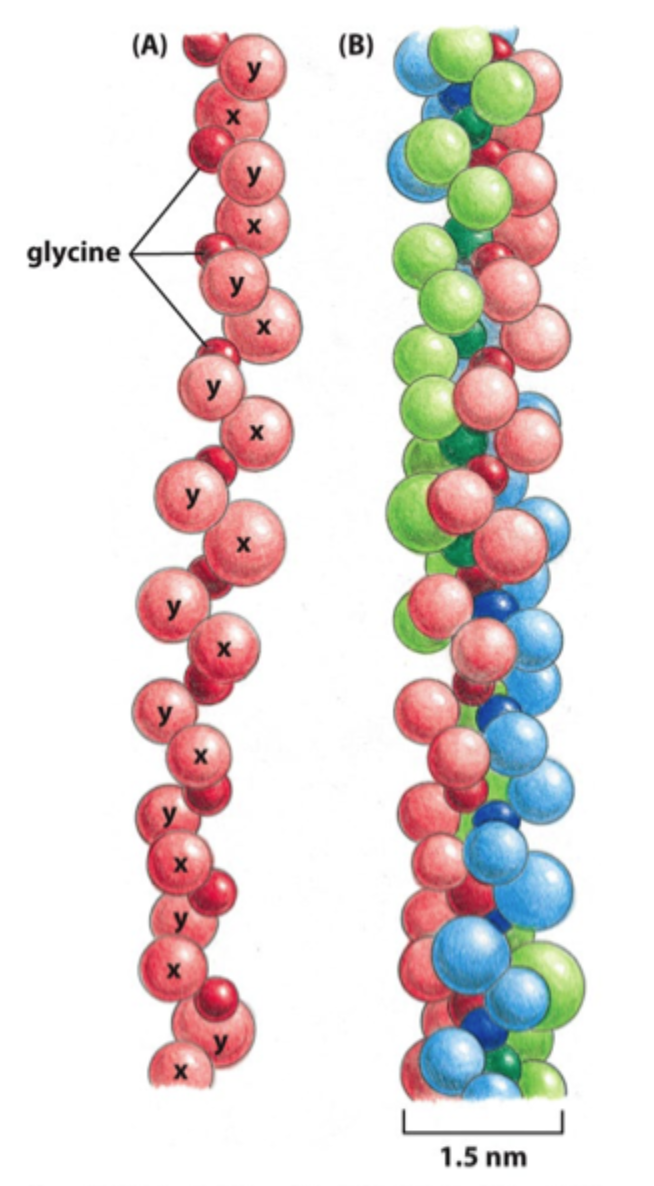
En triple helix bestående af tre α-kæder.
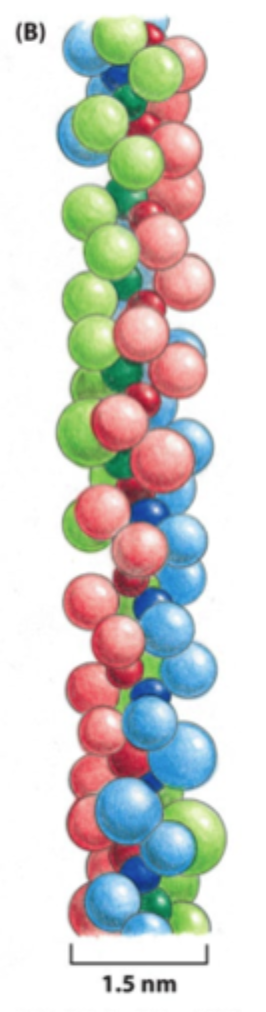
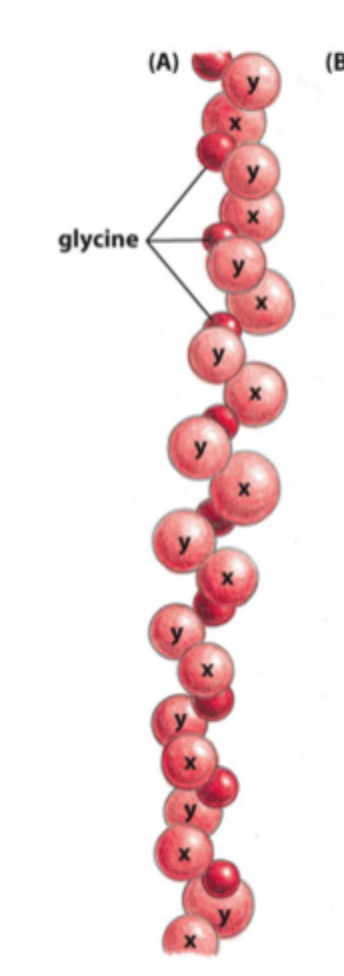
Hvad er særligt vigtigt i kollagens aminosyresekvens?
Meget glycin, fordi glycin er lille nok til at passe i midten af triple helixen.
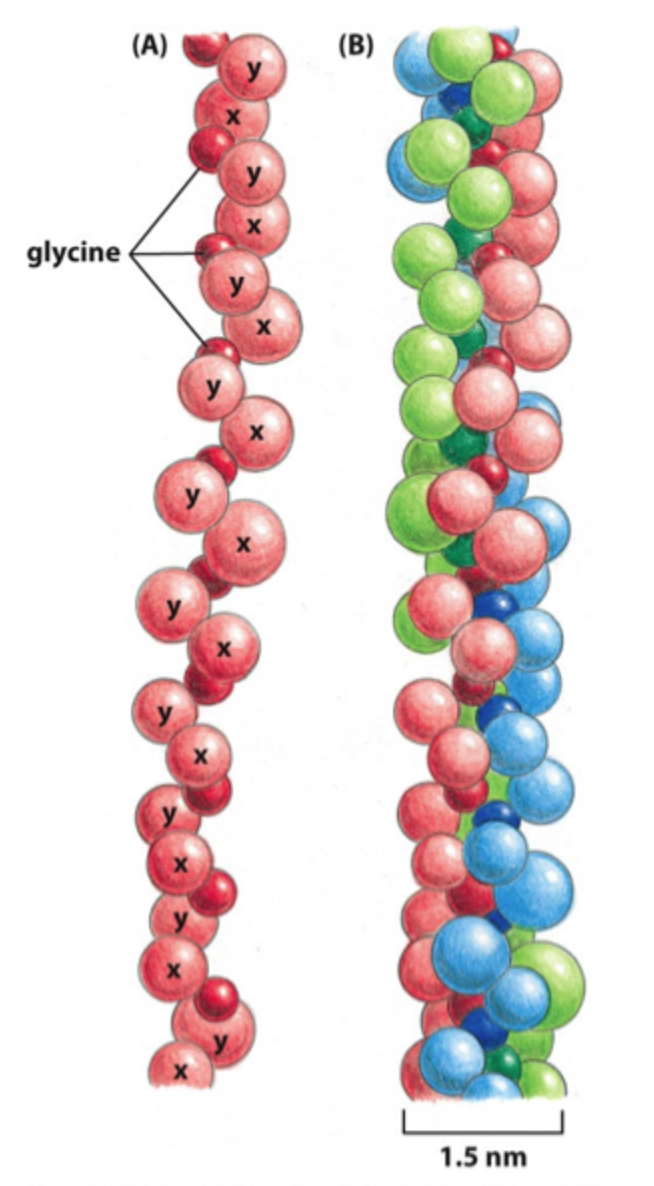
Hvad danner kollagenmolekyler først?
Kollagenfibriller
Hvad dannes ved sammenkobling af flere kollagenfibriller?
Kollagenfibre
Hvad er hovedfunktionen af kollagen i ECM?
At give mekanisk styrke, især mod træk.
Hvilken kollagentype er den klassiske fibrildannende type i fx hud, knogle og sener?
Type I kollagen.
Hvilken kollagentype er vigtig i brusk?
Type II kollagen.
Hvilken kollagentype danner netværk i basallamina?
Type IV kollagen.
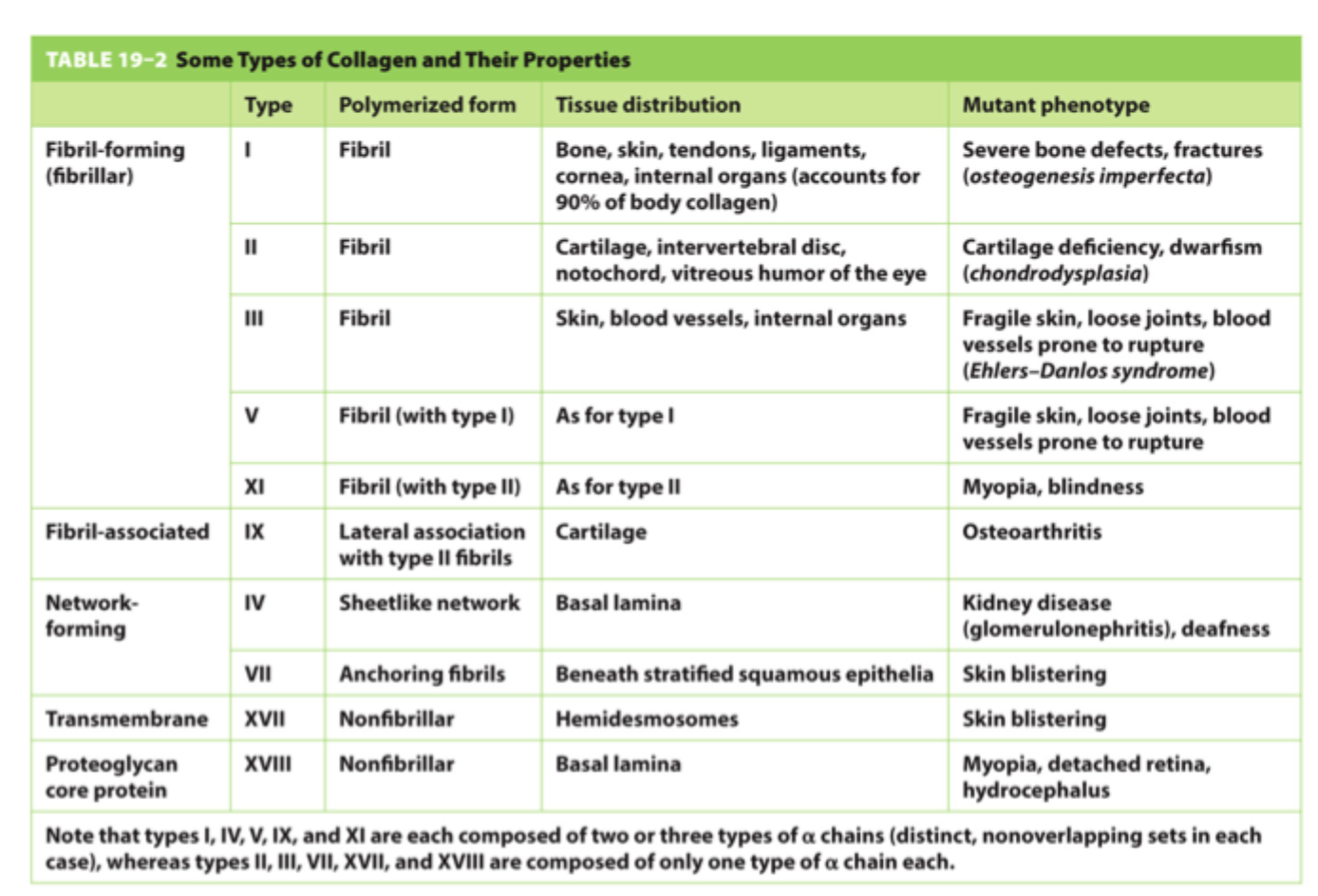
Hvad er hovedpointen med de mange kollagentyper?
At forskellige kollagener giver ECM forskellige mekaniske og strukturelle egenskaber i forskellige væv.
Er samme kollagentype organiseret ens i alle væv?
Nej, den samme kollagentype kan organiseres meget forskelligt afhængigt af vævet.

Hvordan er kollagen ofte organiseret i hud?
Mere uregelmæssigt, så vævet kan tåle træk fra mange retninger.
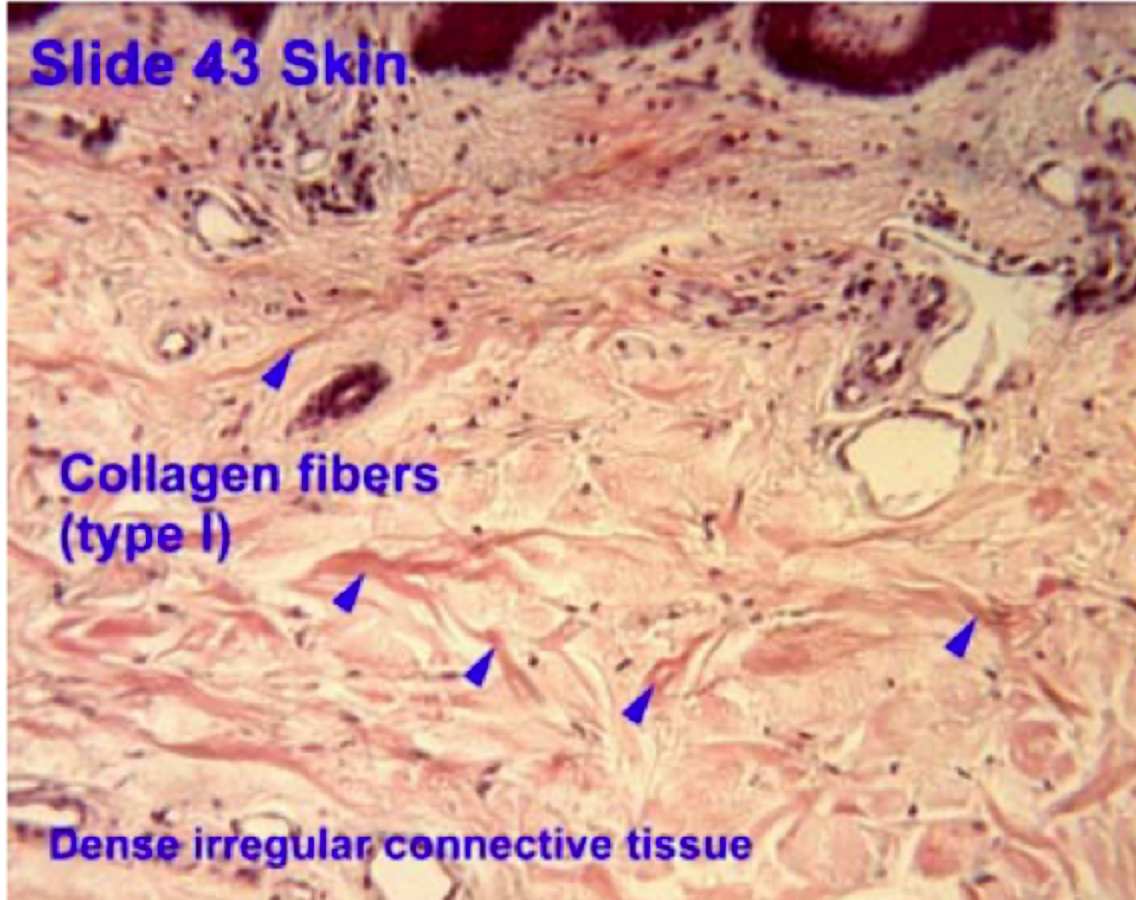
Hvordan er kollagen ofte organiseret i sener?
Meget parallelt, så vævet kan modstå træk i én bestemt retning.
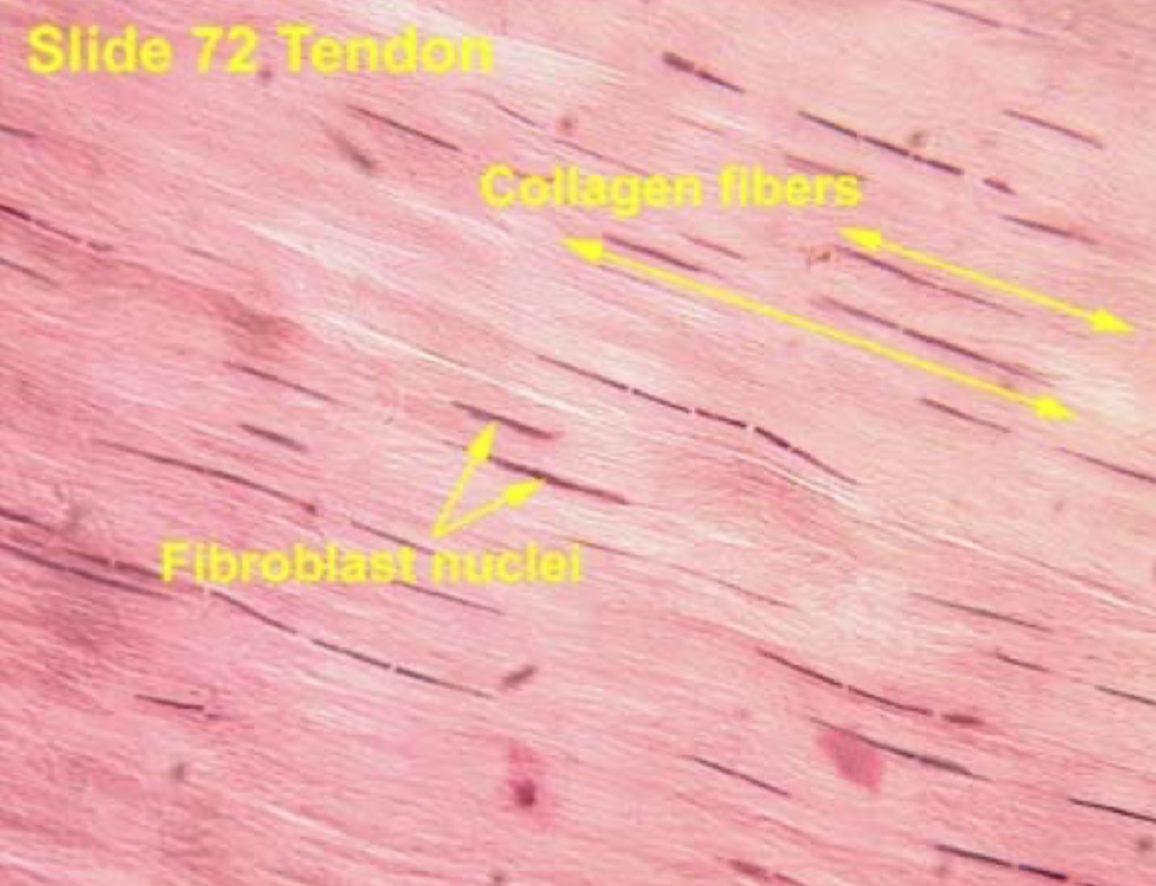
Hvordan kan celler påvirke kollagenfibrillers organisering?
Ved at styre, hvor fibriller dannes, udskille organiserende matrixproteiner og ved at trække i matrixen.
Hvorfor er celletræk vigtigt for ECM-organisering?
Fordi mekanisk tension kan rette og reorganisere kollagenfibriller.
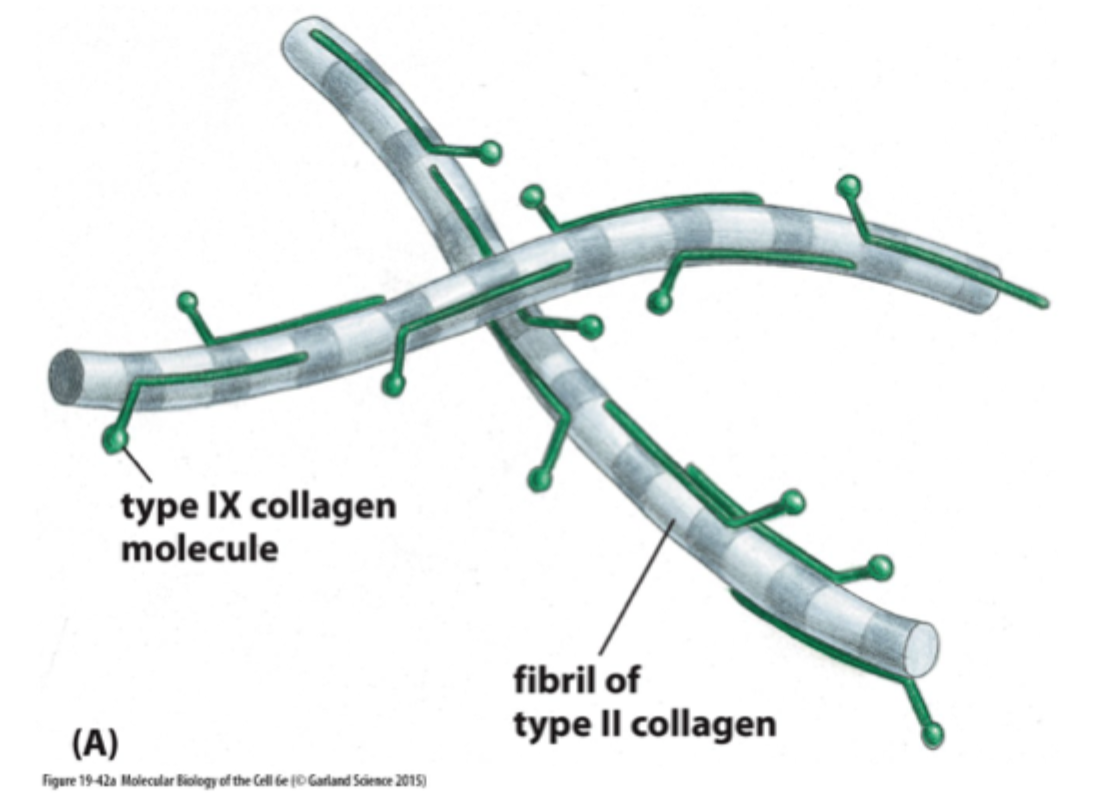
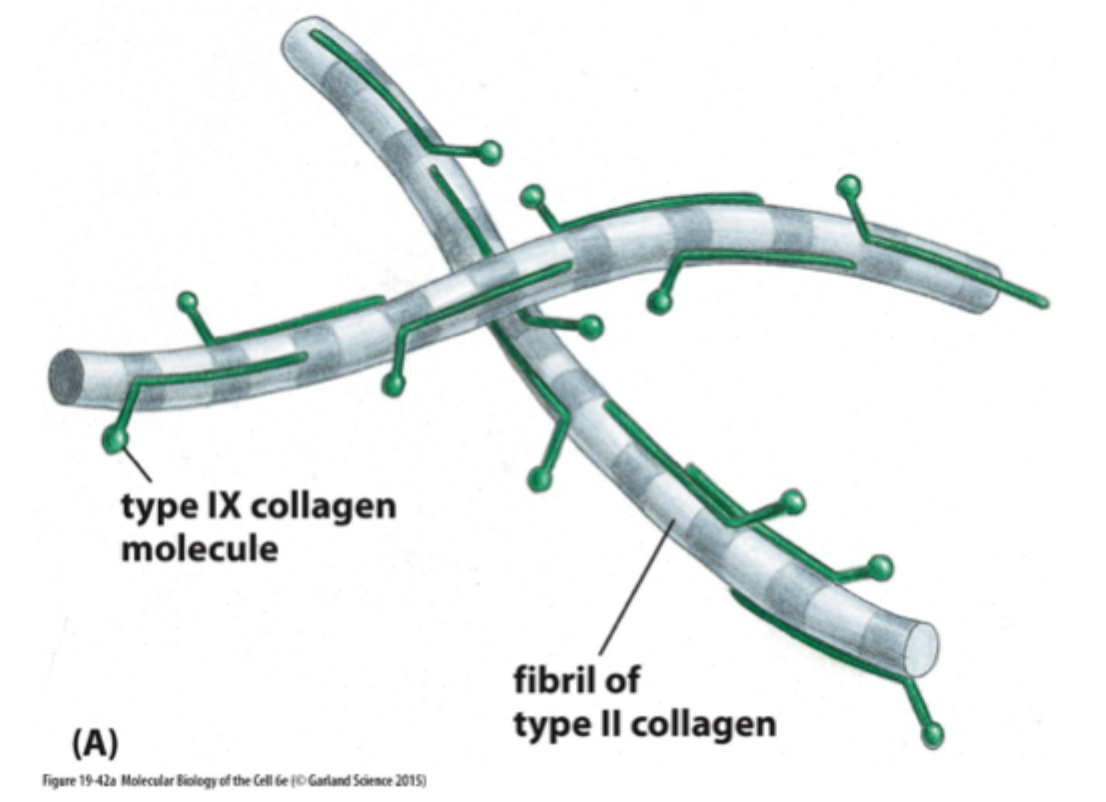
Hvad er pointen med type IX kollagen på figuren?
At nogle kollagener ikke primært danner fibriller selv, men hjælper med at modificere og organisere andre kollagenfibriller.
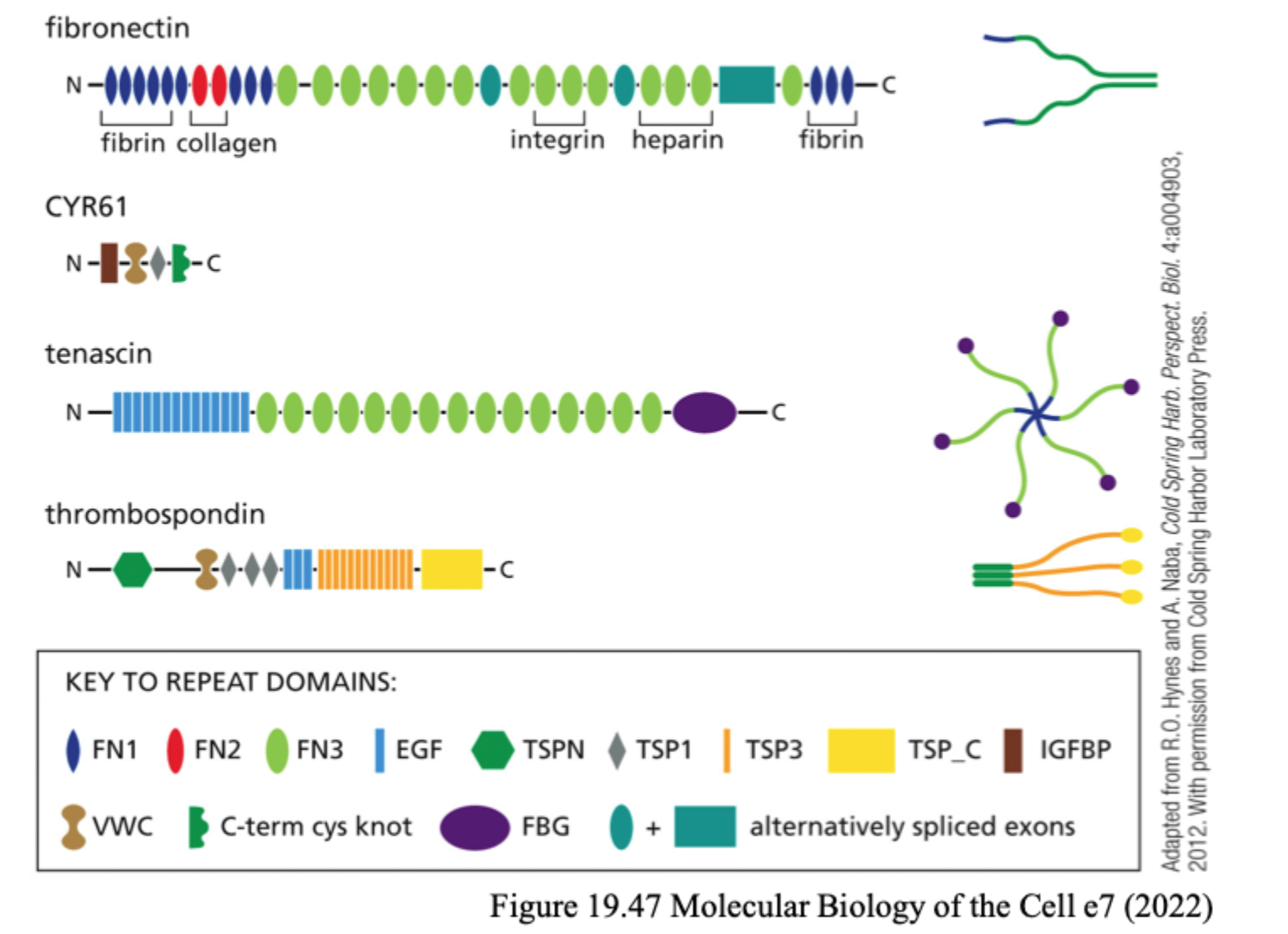
Hvad er fibronectin?
Et multidomæne-glycoprotein, som hjælper med at organisere ECM og koble celler til matrix.
Hvilke ting kan fibronectin typisk binde til?
Fx integriner, kollagen og heparin/heparansulfat.
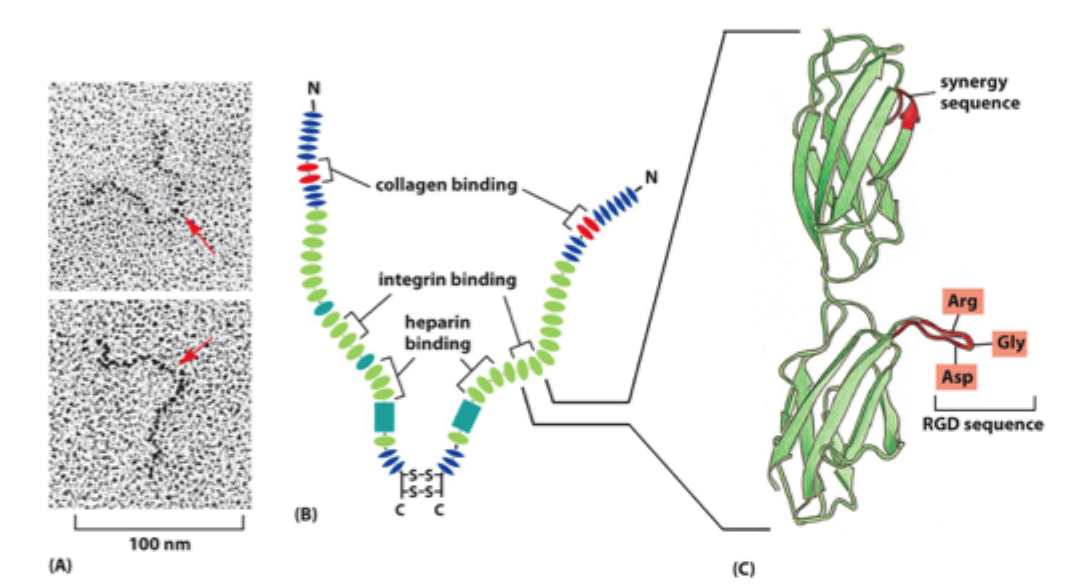
Hvorfor er fibronectin vigtigt som organiseringsmolekyle?
Fordi det har mange bindingsdomæner og derfor kan forbinde flere komponenter i ECM og celleoverfladen.
Findes fibronectin kun i ECM?
Nej, det findes både som en opløselig form i blodet og som en uopløselig fibrillær form (crosslinked dimer) i ECM.
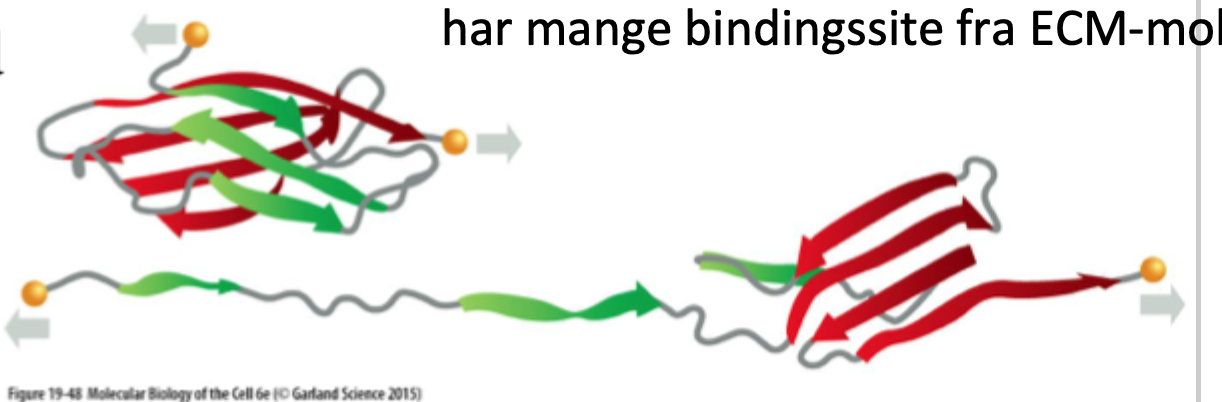
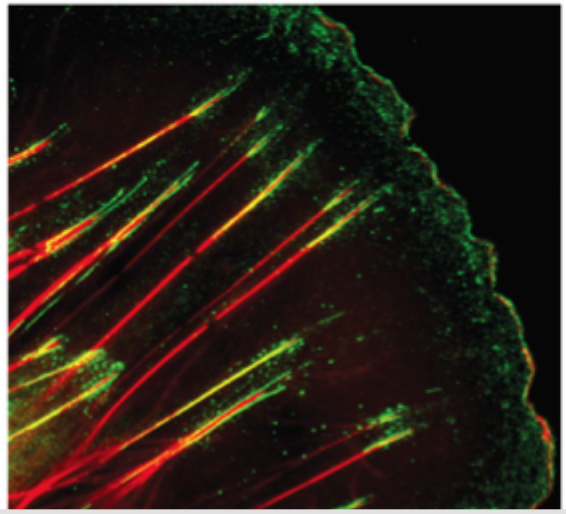
Hvad kræves for dannelse af fibronectin-fibriller i ECM?
Interaktion med celleoverfladen, især via integriner, og mekanisk tension.
Hvad er hovedpointen med fibronectin-sliden?
At ECM ikke kun er bygget af kollagen, men også kræver organiserende glycoproteiner, især fibronectin, for at blive opbygget korrekt.
Hvad er basal lamina?
En specialiseret del af ECM, som ligger tæt op ad cellers basale side, især under epithel, omkring muskelceller og ved visse filtrationsbarrierer.
Hvad er forskellen på ECM generelt og basal lamina?
ECM er det brede ekstracellulære netværk, mens basal lamina er en tynd, specialiseret og mere organiseret ECM-struktur.
Hvad er hovedfunktionerne af basal lamina?
Den giver vævsarkitektur, bestemmer cellepolaritet, påvirker overlevelse, proliferation og differentiering og kan guide migration.
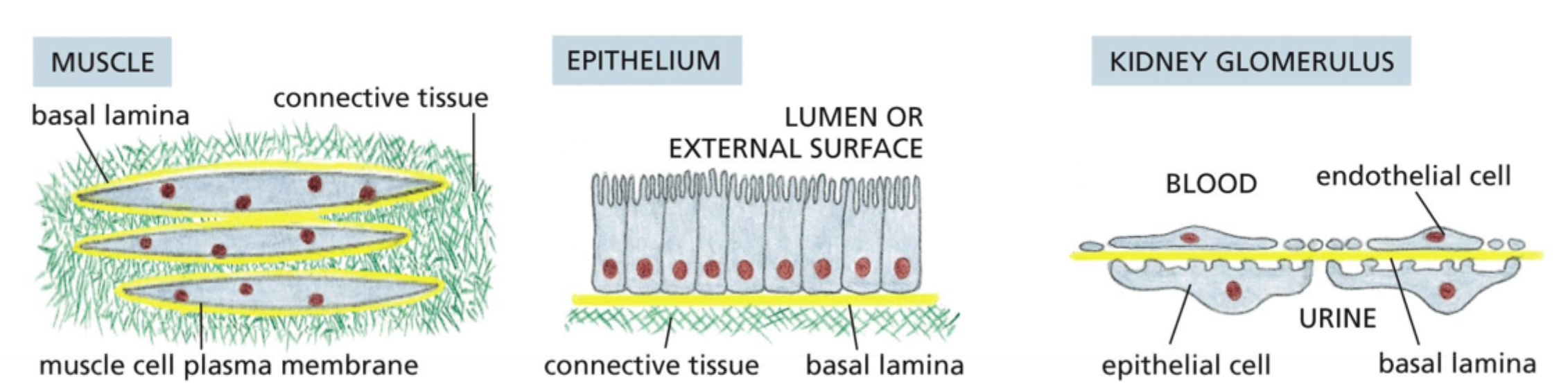
Hvor findes basal lamina typisk?
Under epithel, omkring muskelceller, Schwann-celler og i strukturer som fx nyrens glomerulus.
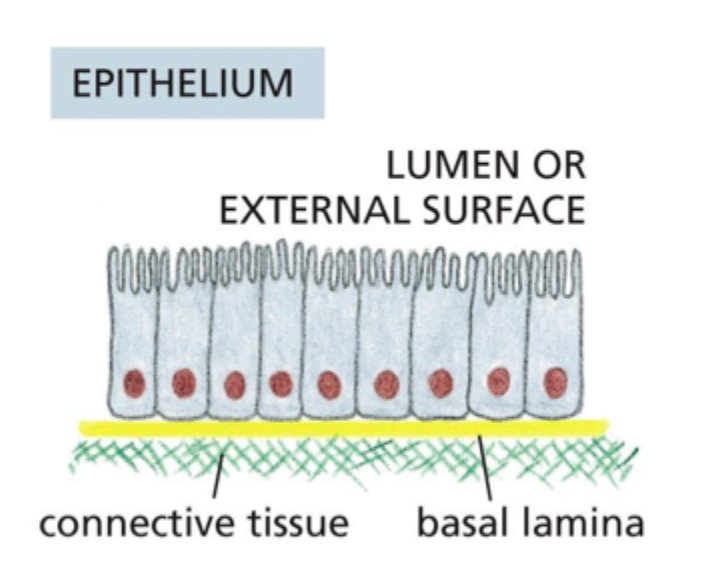
Hvorfor er basal lamina vigtig i epithel?
Den hjælper med at definere basal vs. apikal side og støtter epithelets organisering.
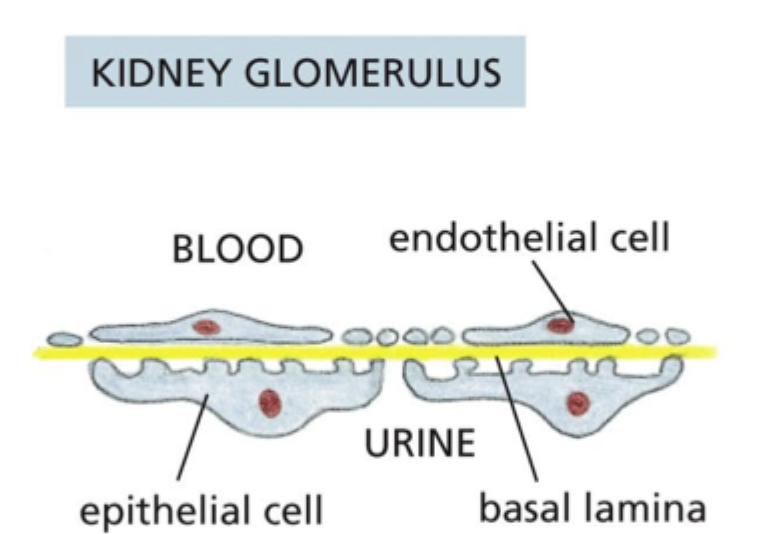
Hvad er basal lamina’s rolle i nyreglomerulus?
Den indgår i filtrationsbarrieren mellem blod og urin.
Hvad er pointen med at basal lamina er “tissue-specific organized”?
At den har fælles hovedkomponenter, men sammensætning og organisation varierer mellem væv.
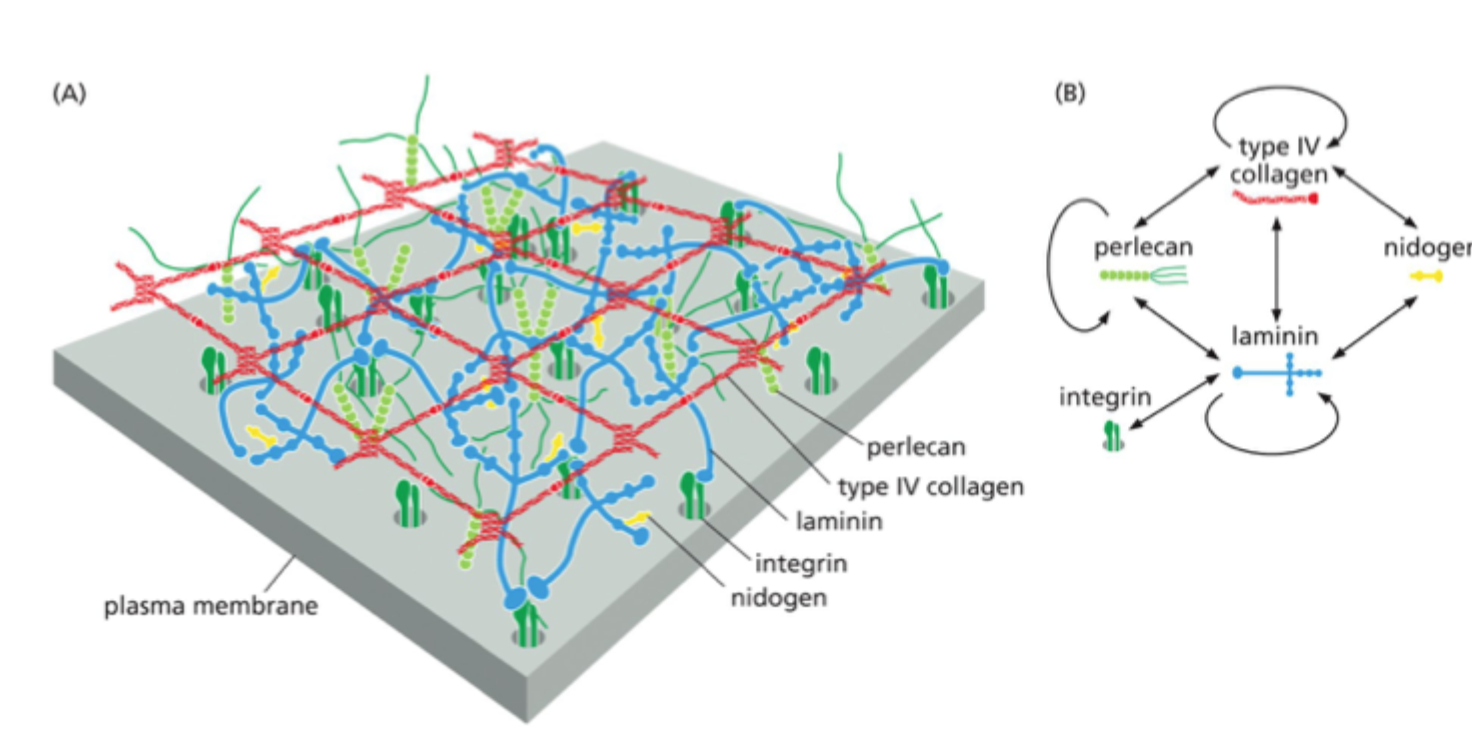
Hvad er de vigtigste komponenter i basal lamina?
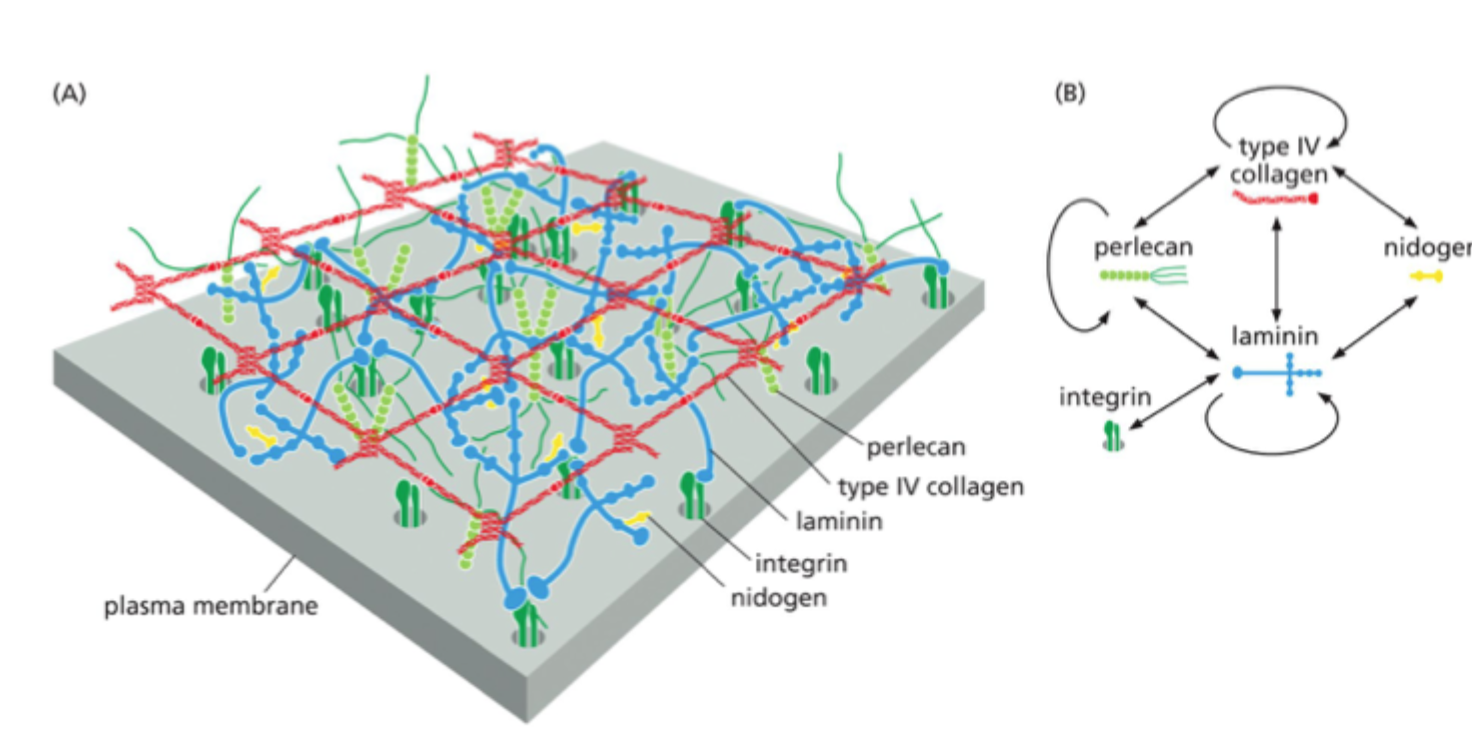
Glykoproteiner: Laminin, type IV kollagen, nidogen
Proteoglykan: perlecan.
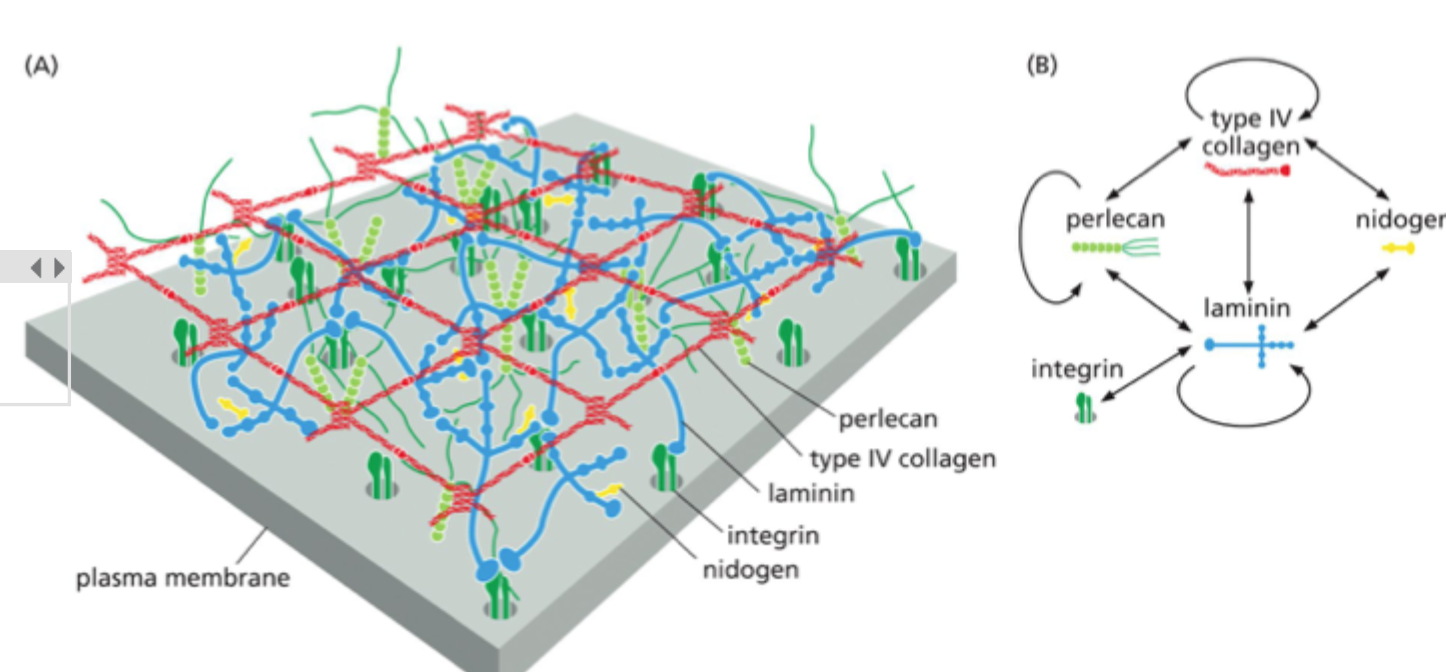
Hvilken komponent er central for organiseringen af basal lamina?
Laminin
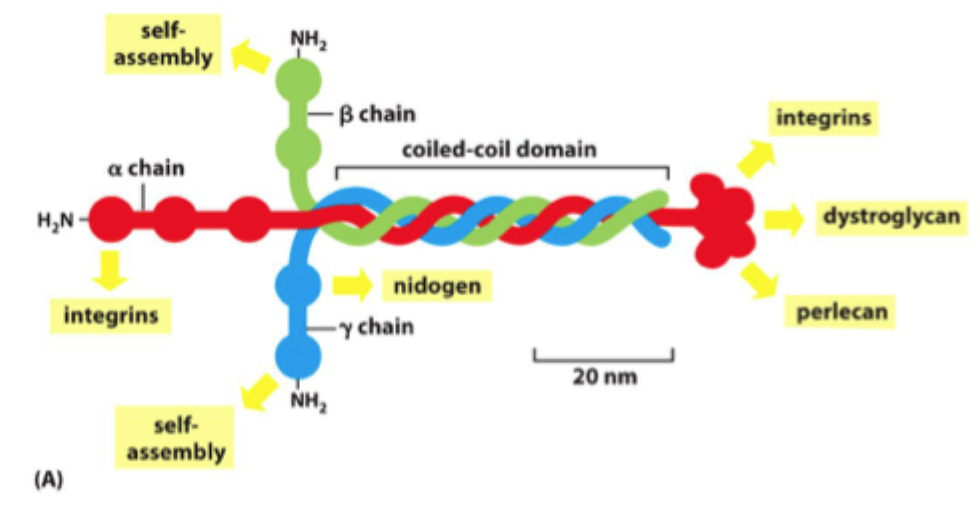
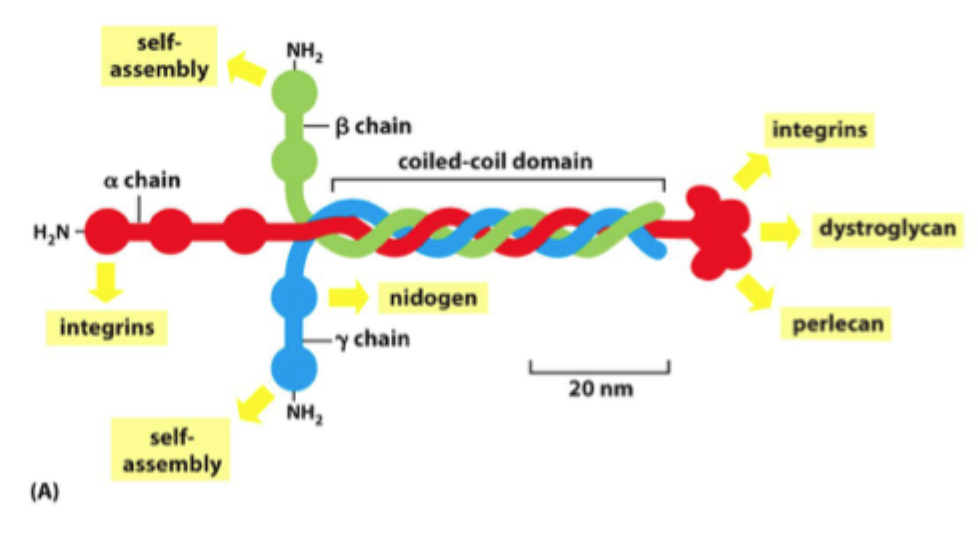
Hvad er laminin strukturelt?
Et trimerisk glycoprotein opbygget af en α-, β- og γ-kæde.
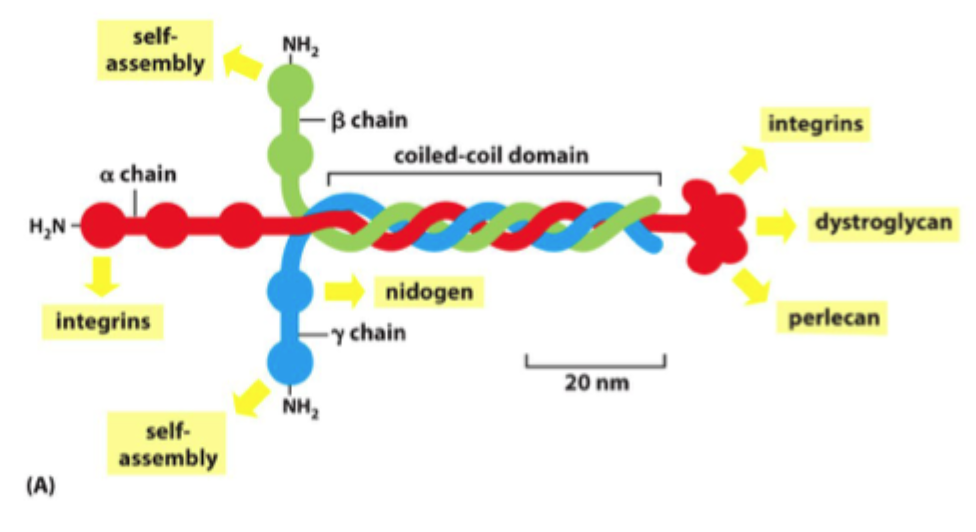
Hvorfor findes der mange typer laminin?
Fordi forskellige α-, β- og γ-kæder kan kombineres på flere måder og danne forskellige laminin-isoformer.

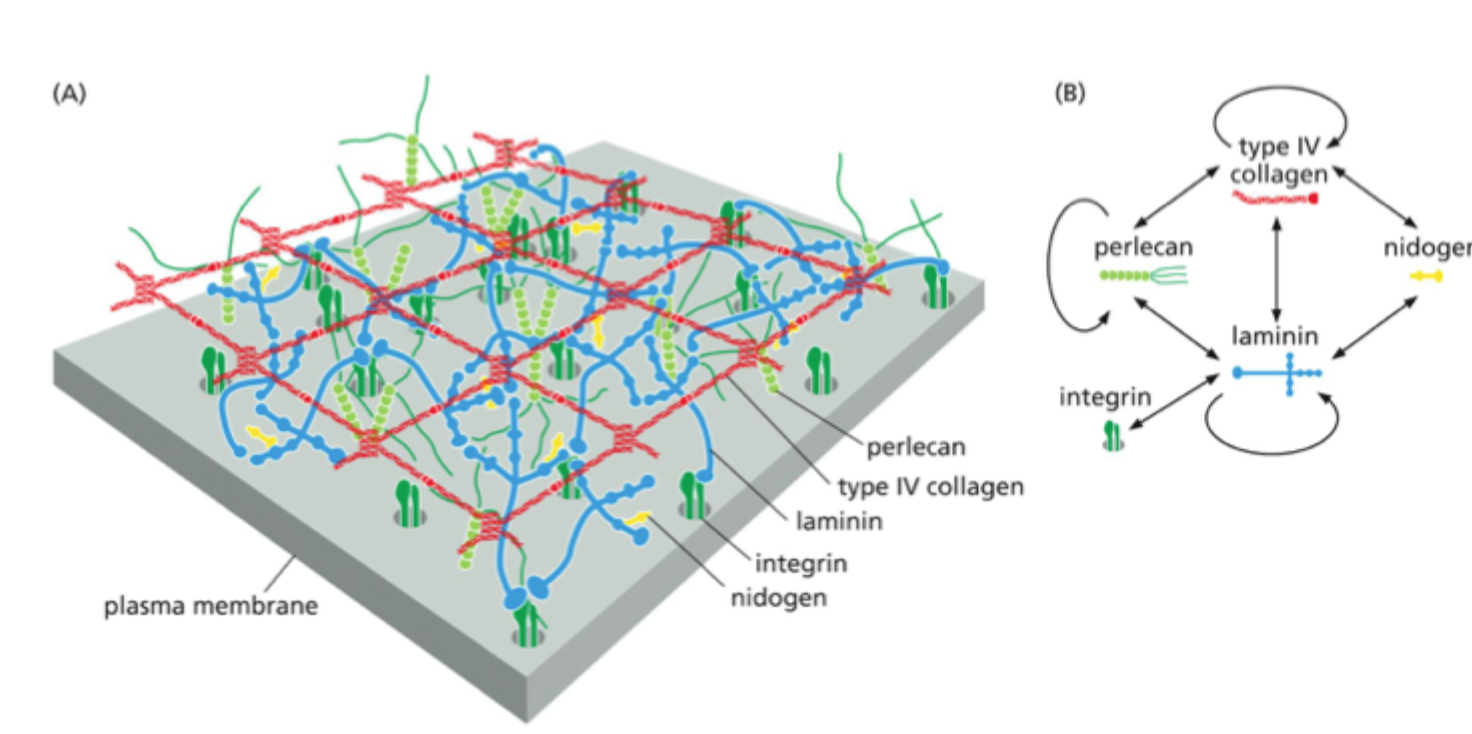
Hvad binder laminin til i basal lamina?
Det kan binde til andre lamininmolekyler, til perlecan, til nidogen og til celler via integriner eller dystroglycan.
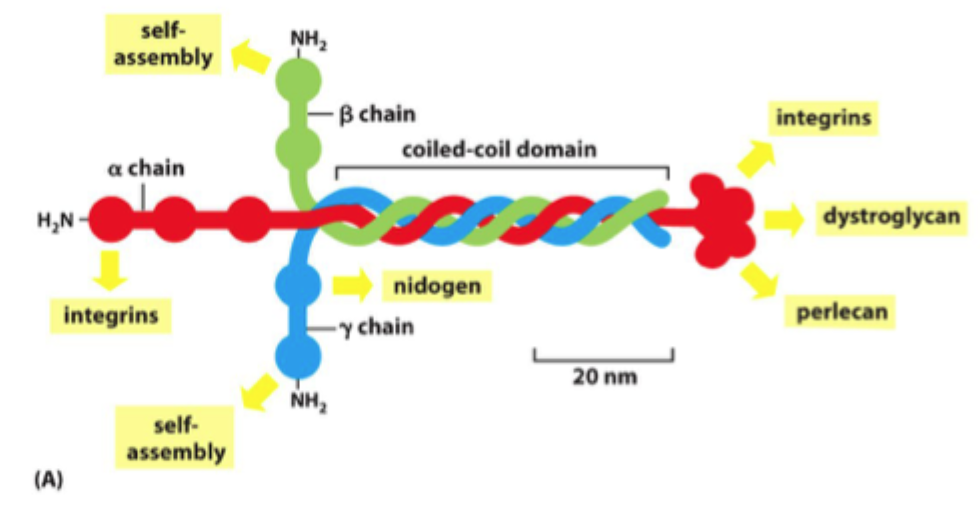
Hvad gør nidogen i basal lamina?
Det fungerer som en kobler mellem laminin-netværket og kollagen IV-netværket.
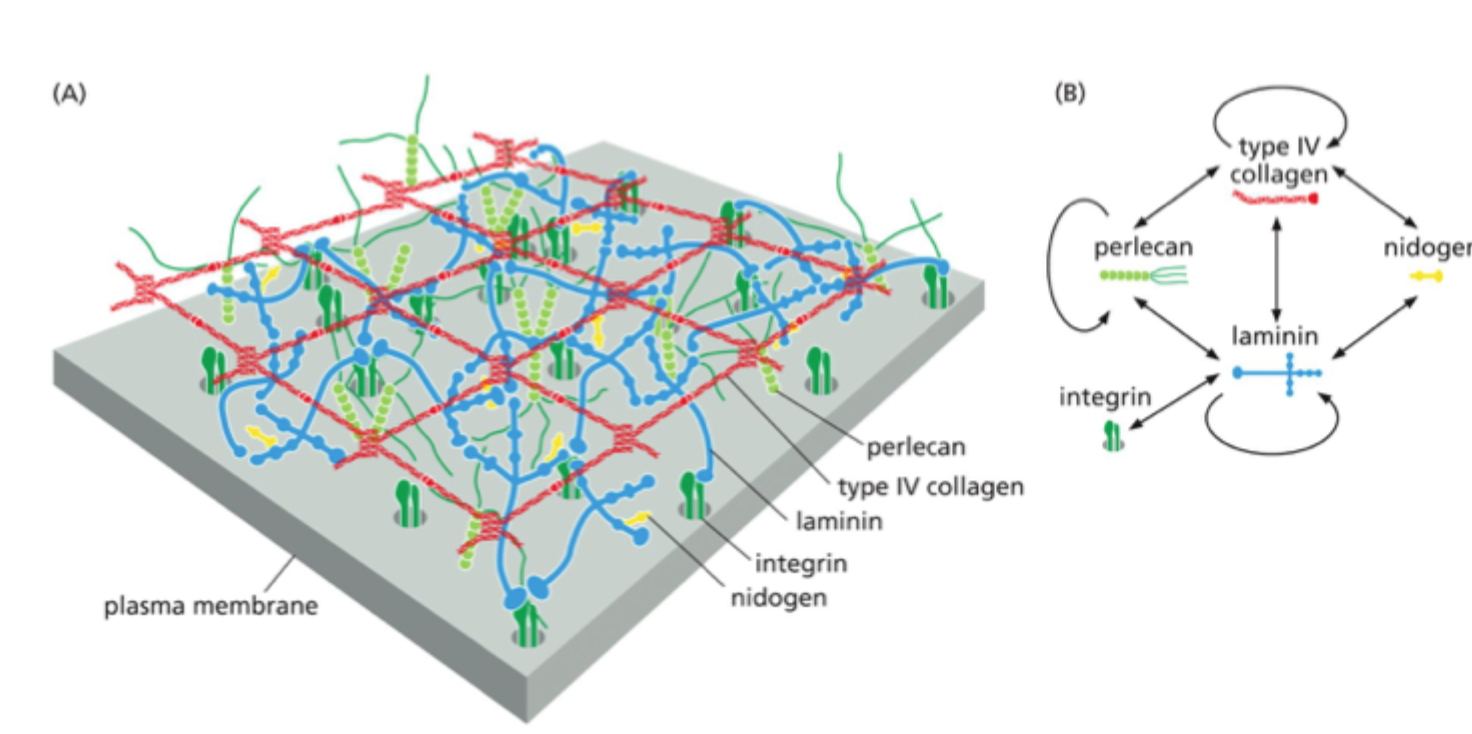
Hvad er rollen af type IV kollagen i basal lamina?
Det danner et netværk, som giver strukturel støtte, ikke klassiske fibriller som type I kollagen.
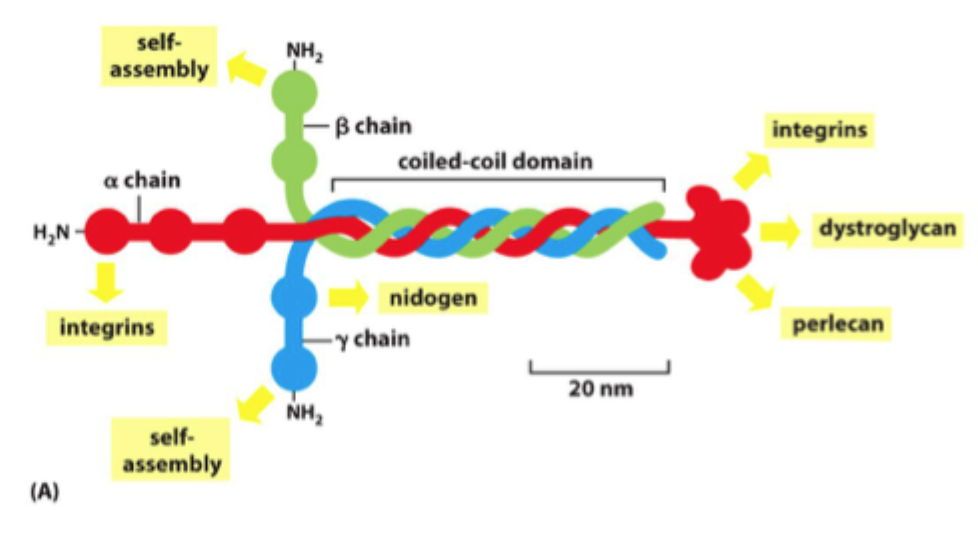
Hvad gør perlecan i basal lamina?
Det er et heparansulfat-proteoglykan, som bidrager til filtrering, hydrering og binding af signalmolekyler.
Hvorfor er basal lamina vigtig ved regeneration af den neuromuskulære junction?
Fordi den bevarer positionsinformation, så regenererende nerve og muskel kan finde tilbage til det oprindelige kontaktsted.
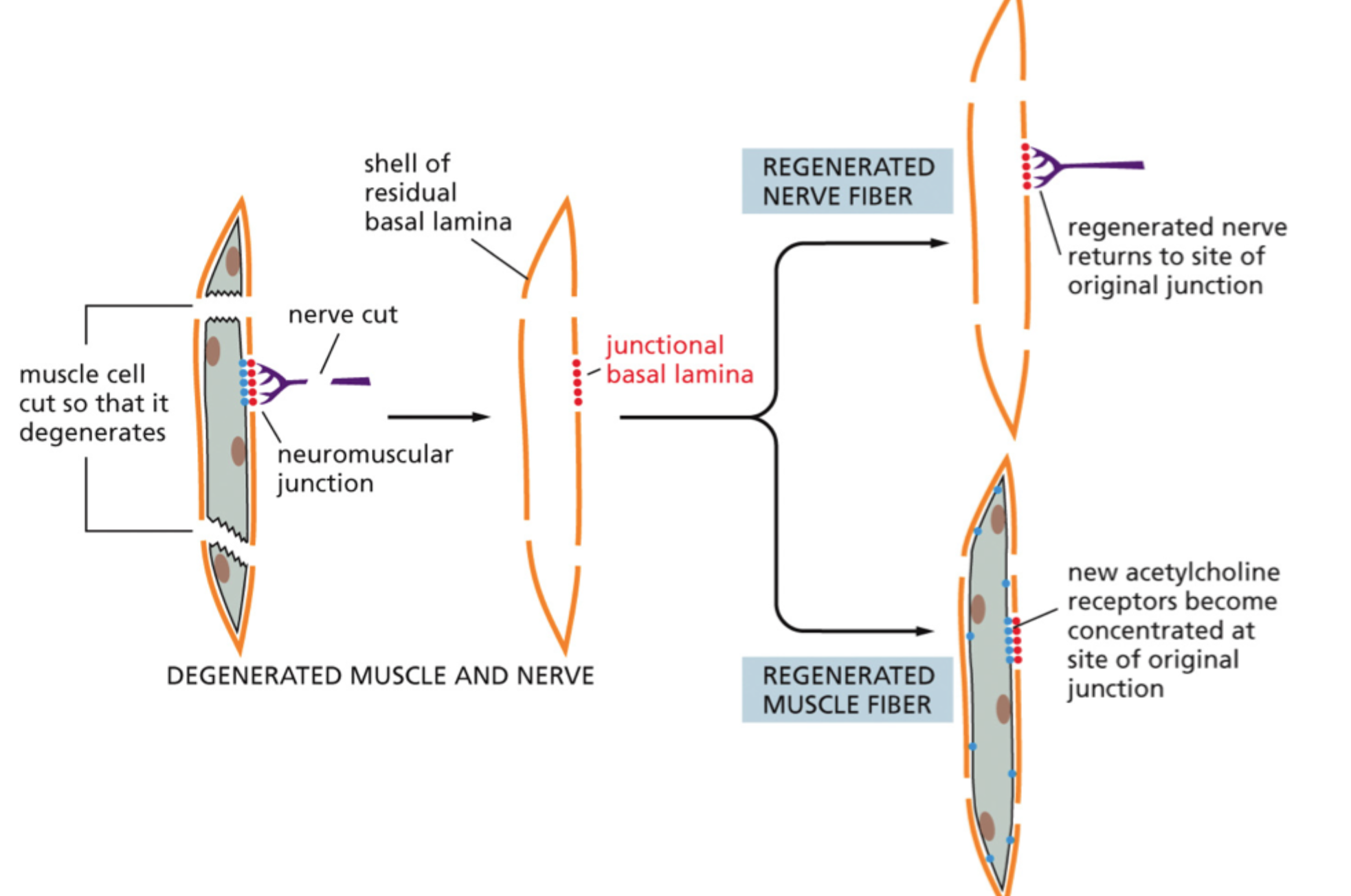
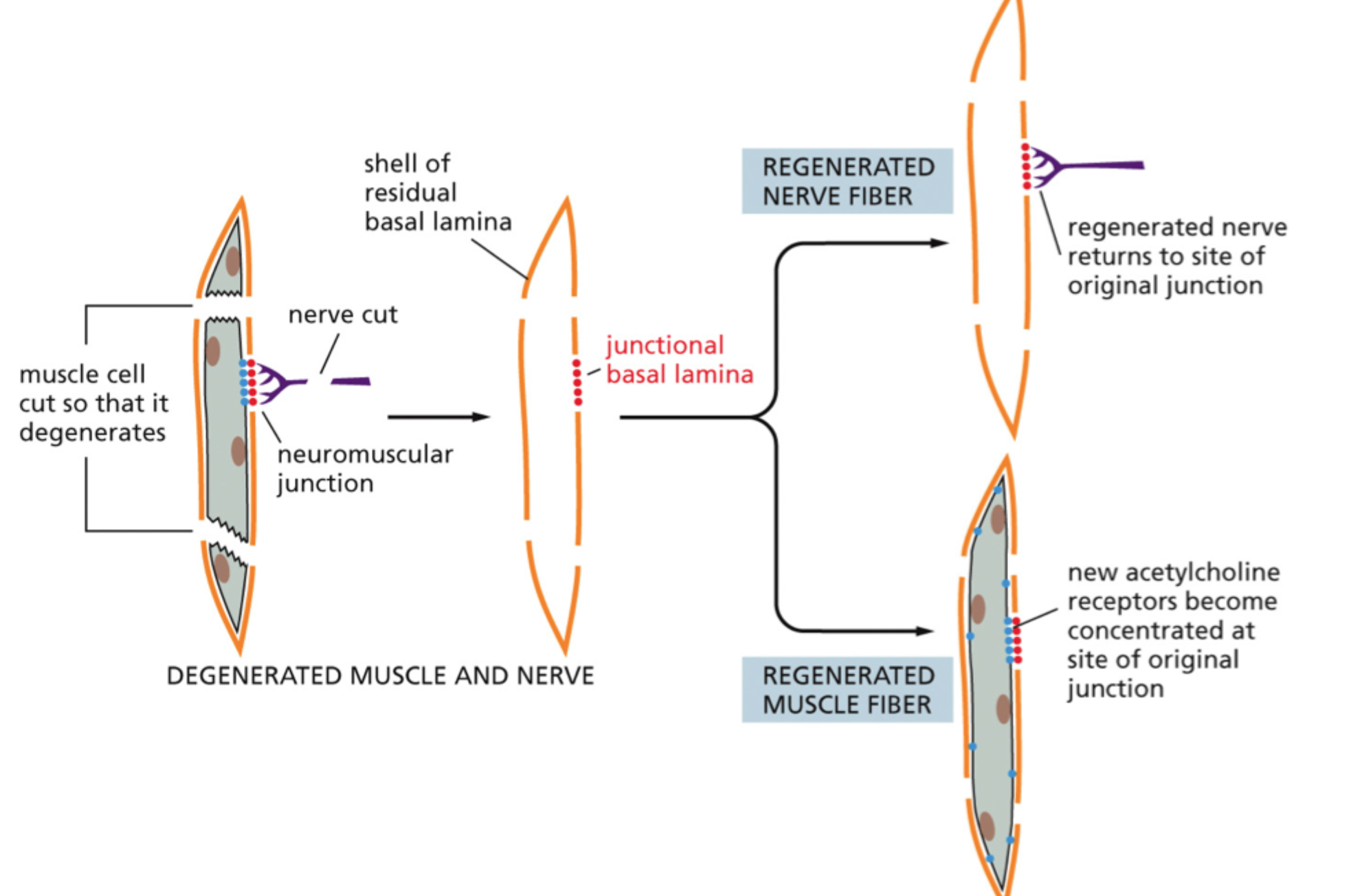
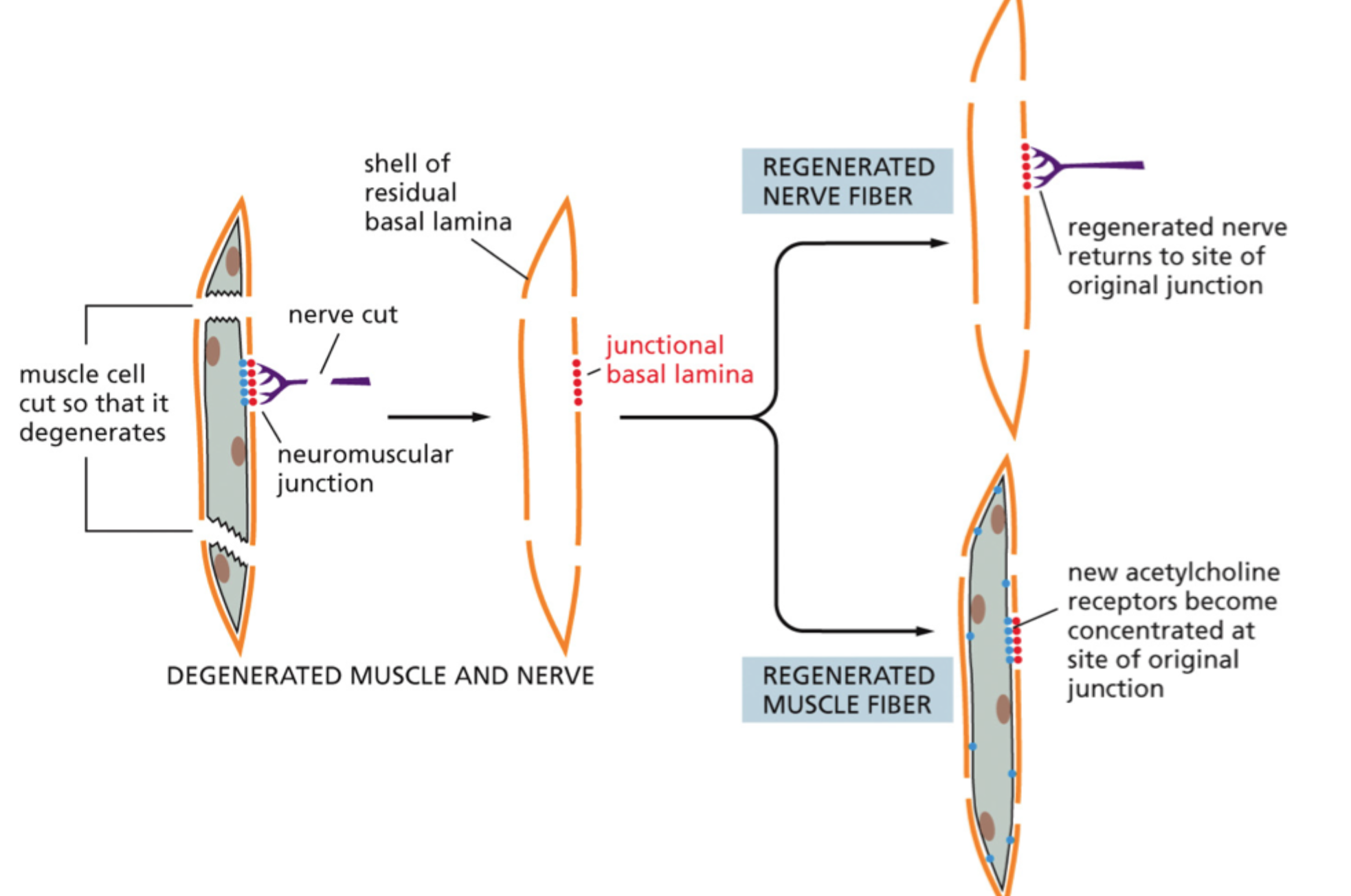
Hvad viser neuromuskulær junction-sliden som hovedpointe?
At rest-basal lamina kan fungere som en skabelon for regeneration.
Kan basal lamina altså gemme information om tidligere vævsstruktur?
Ja, den kan fungere som et strukturelt og funktionelt “memory template”.
Er ECM en statisk struktur?
Nej, ECM er dynamisk og remodelleres hele tiden.
Hvorfor skal ECM nedbrydes?
For at celler kan dele sig, ændre form og migrere gennem vævet.
Hvilke to hovedklasser af proteinaser nedbryder ECM?
Matrix metalloproteinases, MMPs og serinproteinaser.
Hvorfor skal ECM-nedbrydning være stramt reguleret?
For at undgå uspecifik vævsskade, så nedbrydning kun sker det rigtige sted og tidspunkt.
Hvordan reguleres ECM-nedbrydning?
Via proteasehæmmere, lokal aktivering og ofte ved at proteaser er lokaliseret til celleoverfladen.
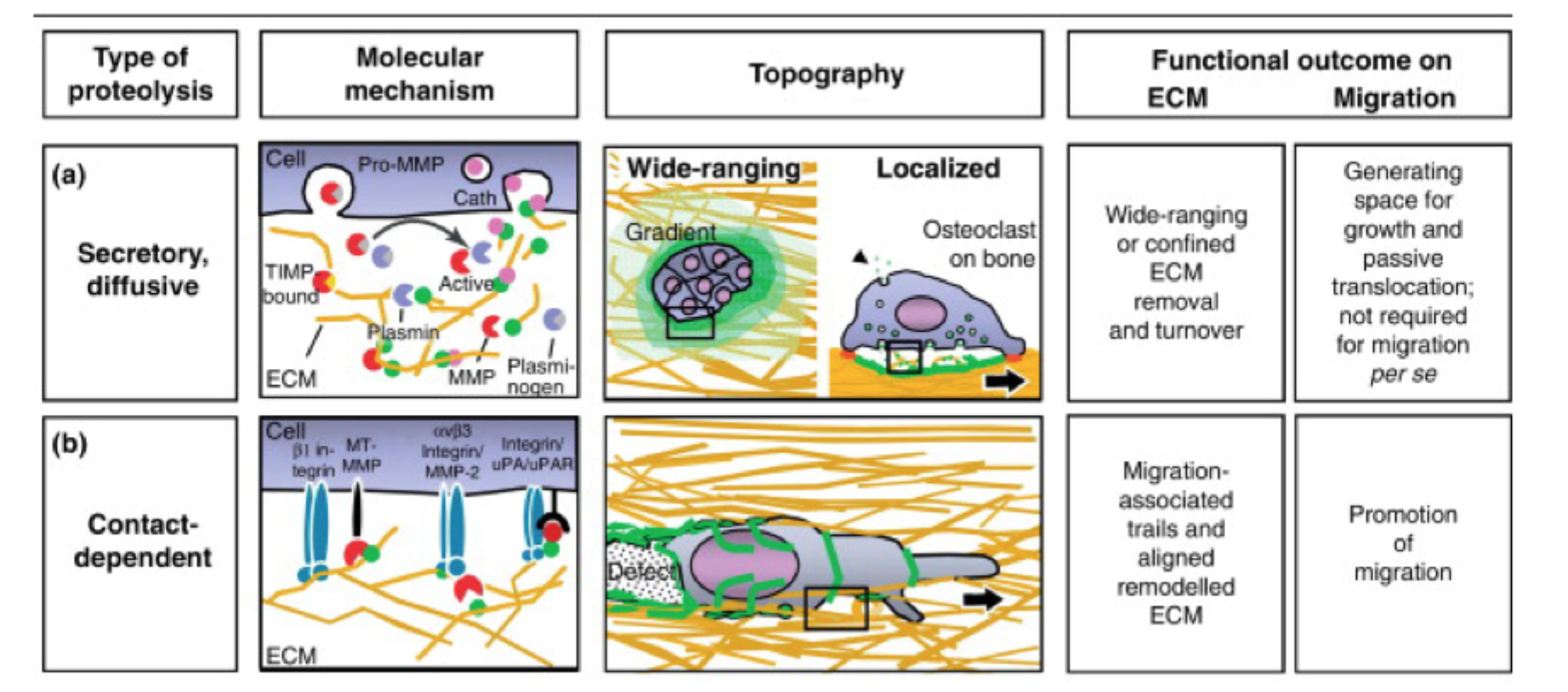
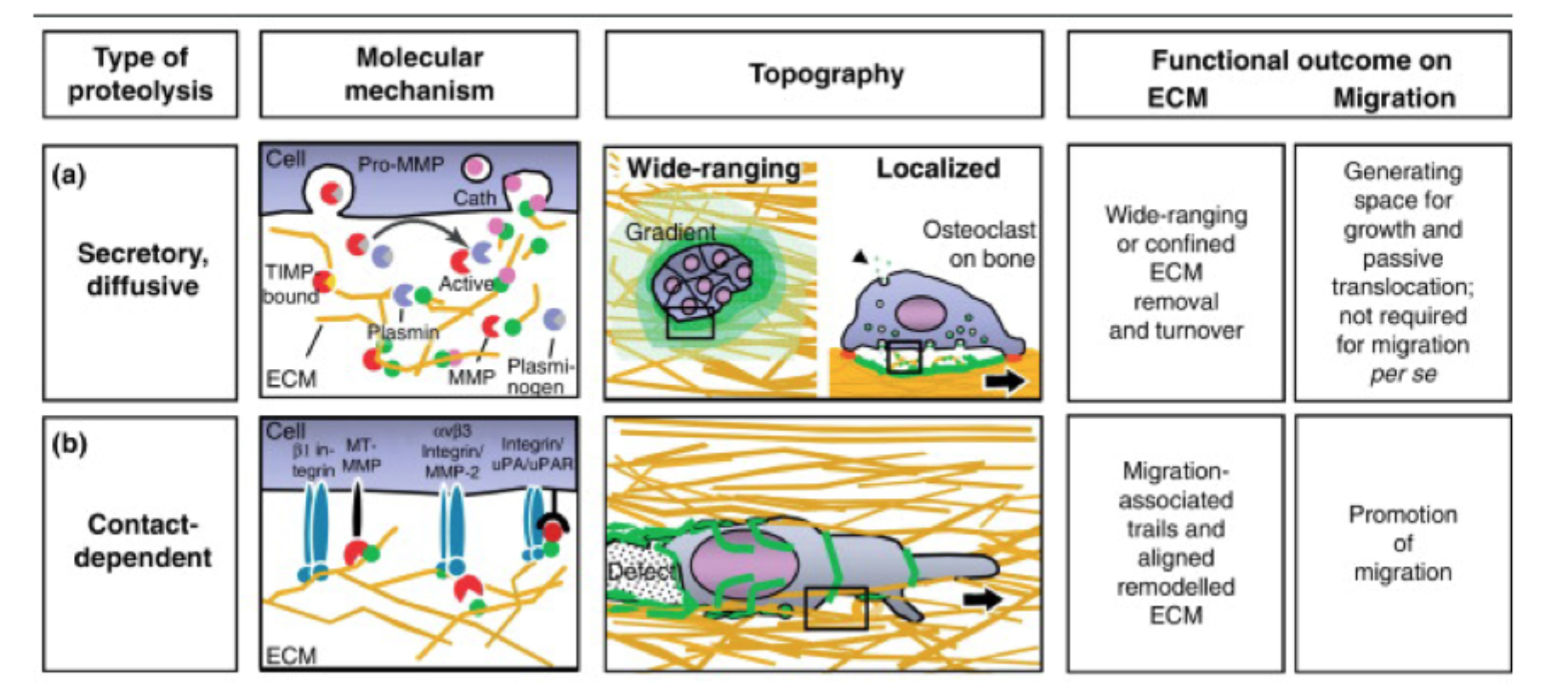
Hvad er hovedpointen med remodellering-sliden?
At celler ikke bare bevæger sig gennem ECM, men ofte åbner vej ved lokal nedbrydning af matrix.
Hvordan kan proteoglykaner påvirke vækstfaktorer?
De kan fungere som lokale reservoirs for vækstfaktorer.
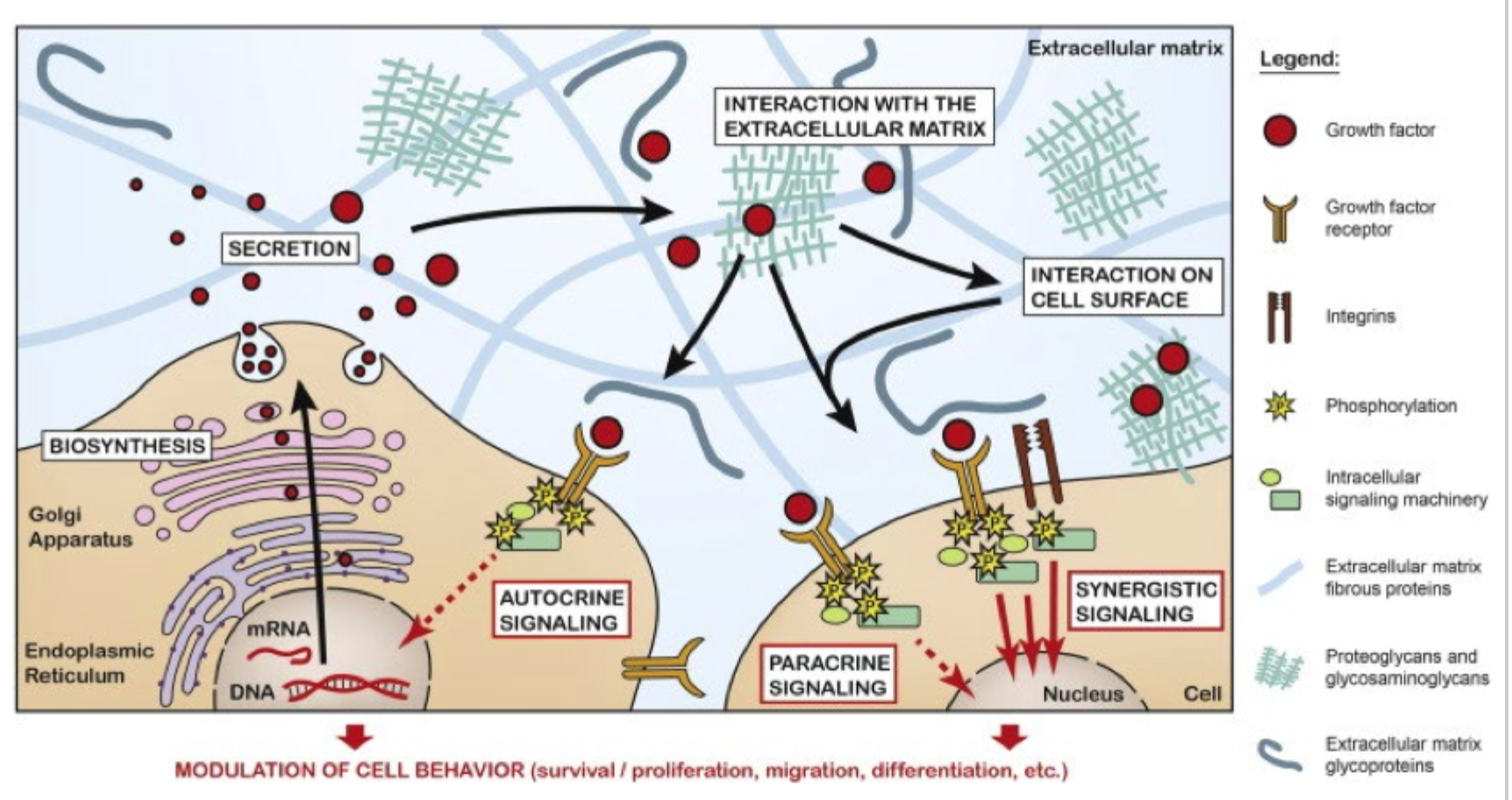
Hvad betyder det, at membranbundne proteoglykaner kan være co-receptorer?
At de hjælper receptorer med at binde eller præsentere signalmolekyler mere effektivt.
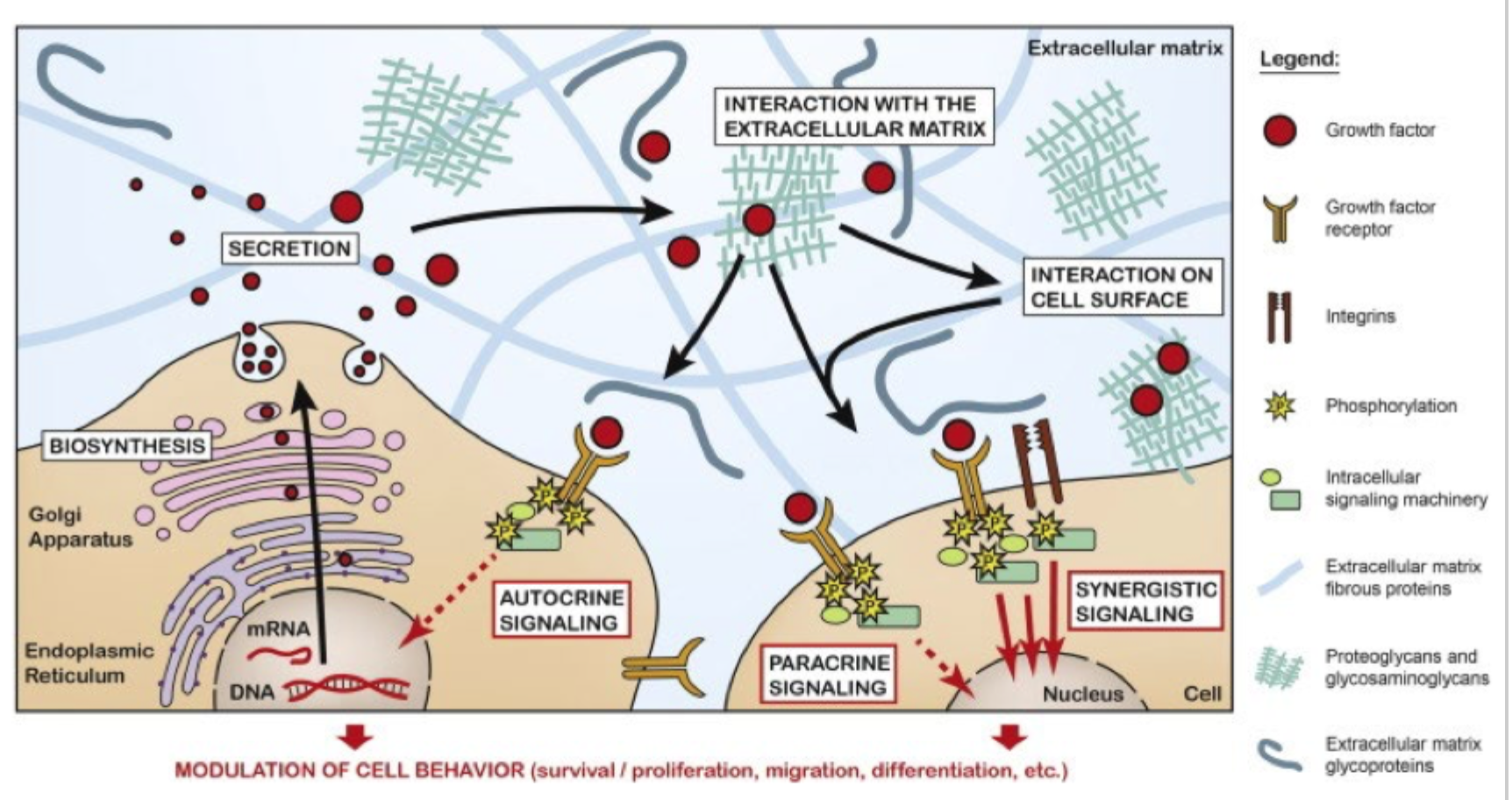
Kan ECM påvirke signalering ud over at være struktur?
Ja, ECM regulerer også signalmolekylers tilgængelighed, koncentration og aktivitet.
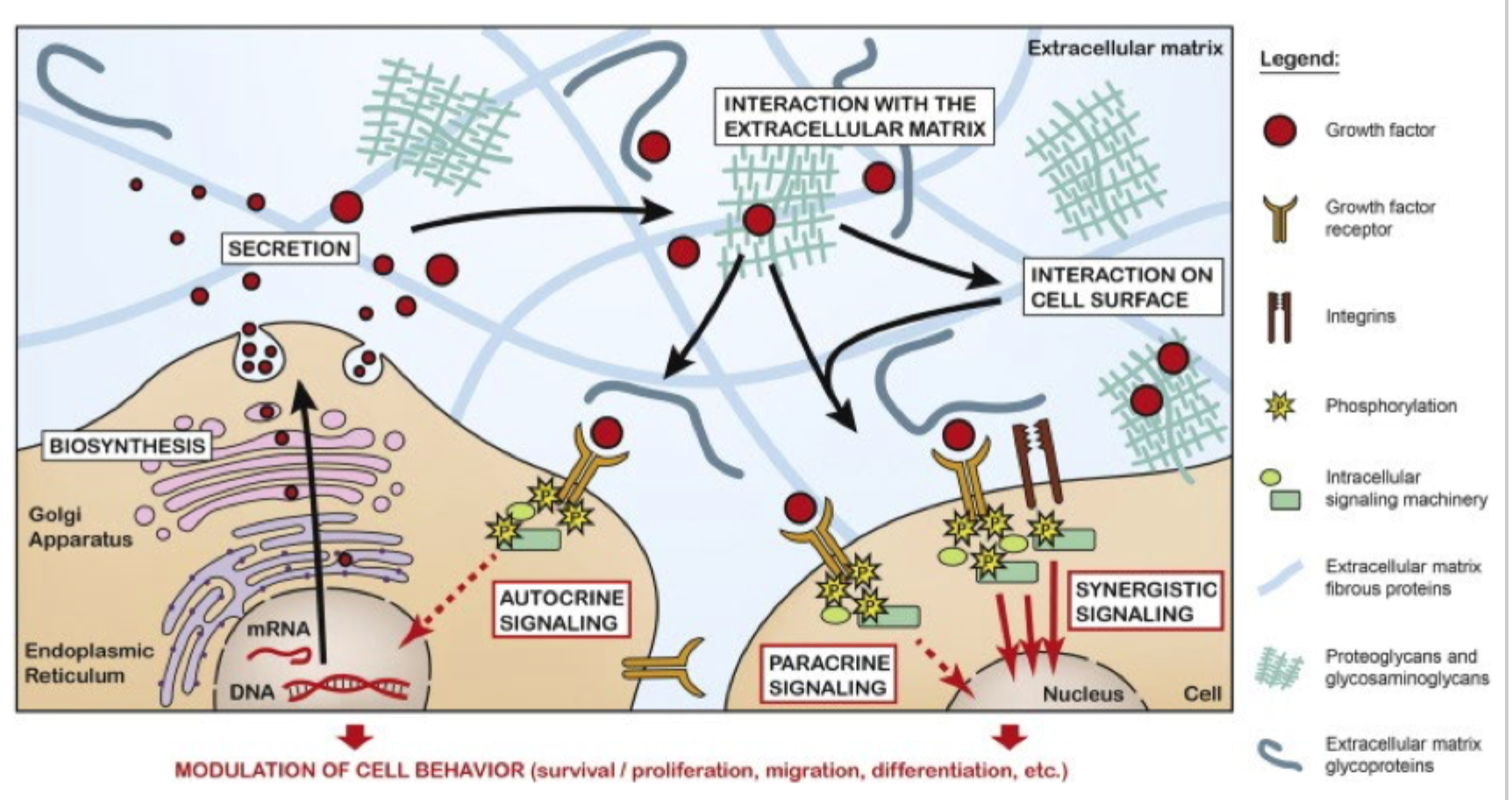
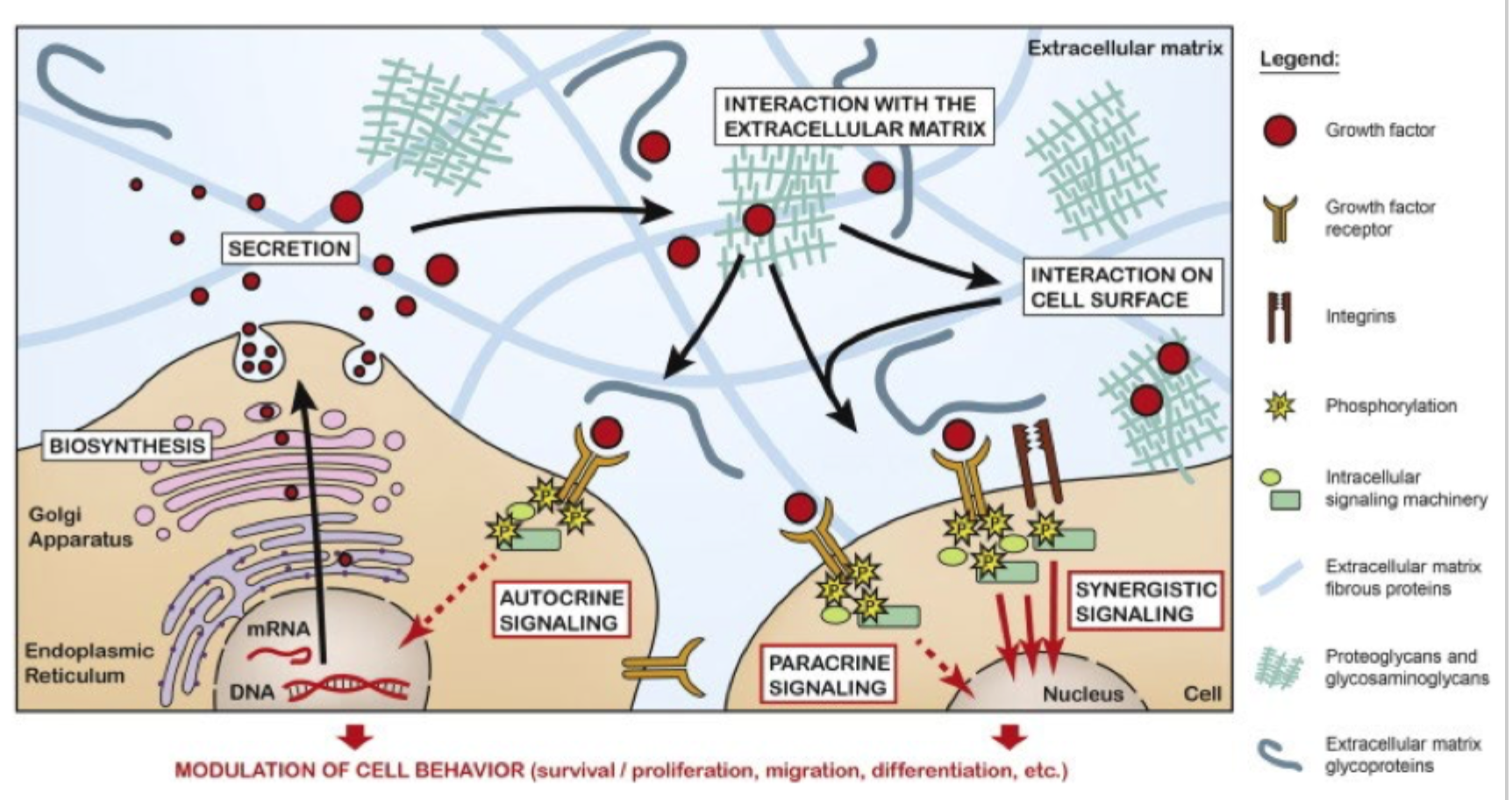
Hvad er pointen med fibronectin på den slide?
At ECM-glycoproteiner også kan interagere med vækstfaktorer og fremme deres funktion.
Hvordan påvirker matrix cellers adfærd?
Ved at binde til matrixreceptorer på celleoverfladen.
Hvilke to vigtige typer matrixreceptorer nævnes på sliden?
Transmembrane proteoglykaner og integriner.
Hvad er integriner?
Transmembrane heterodimere receptorer, som kobler ECM til cytoskelettet.
Hvad betyder det, at integriner forbinder ECM til cytoskelettet?
At mekaniske og kemiske signaler kan overføres mellem ydersiden og cellens indre.
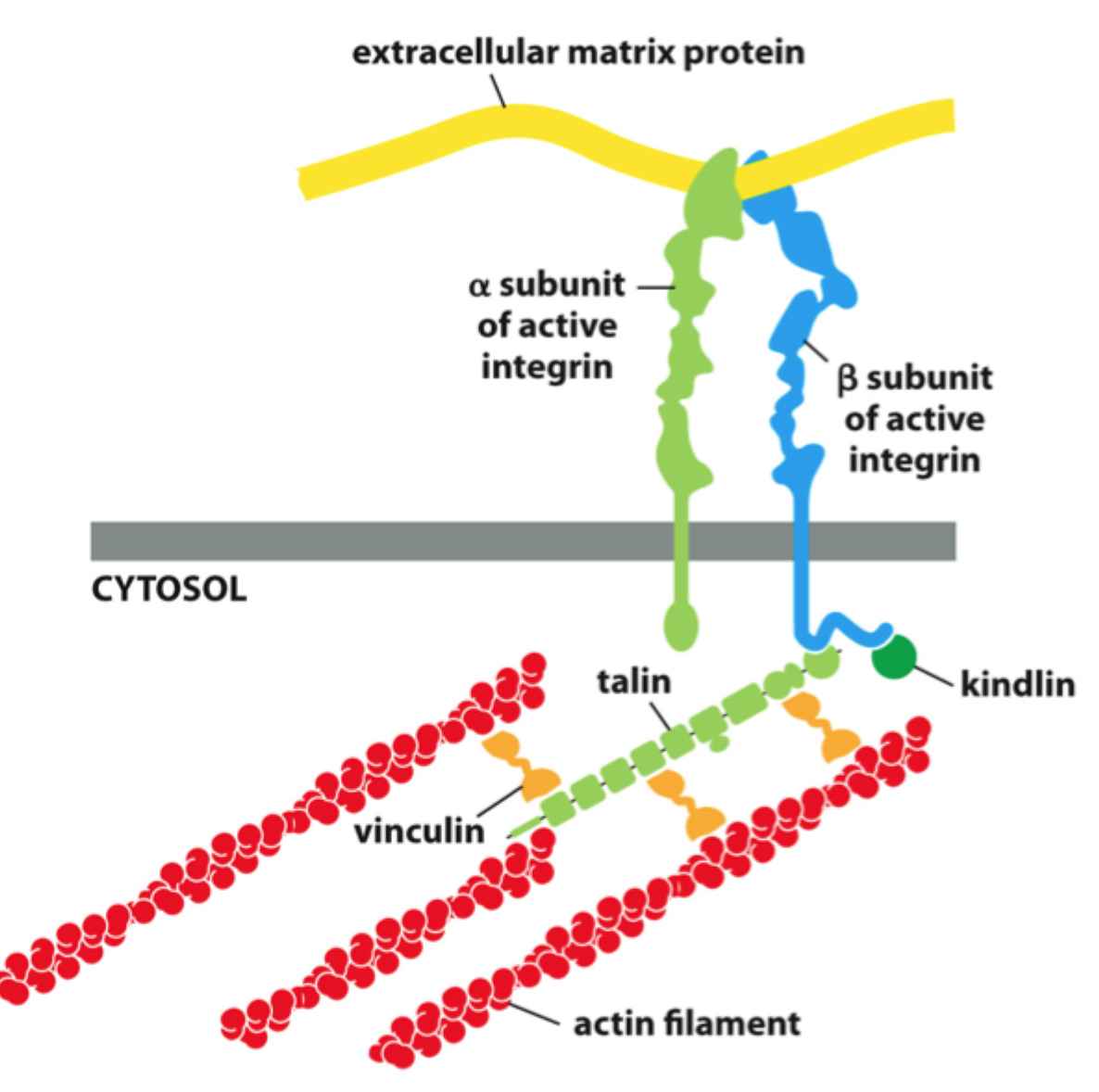
Hvilke adaptorproteiner er vigtige ved integrinforankring til aktin?
Især talin, kindlin og vinculin.
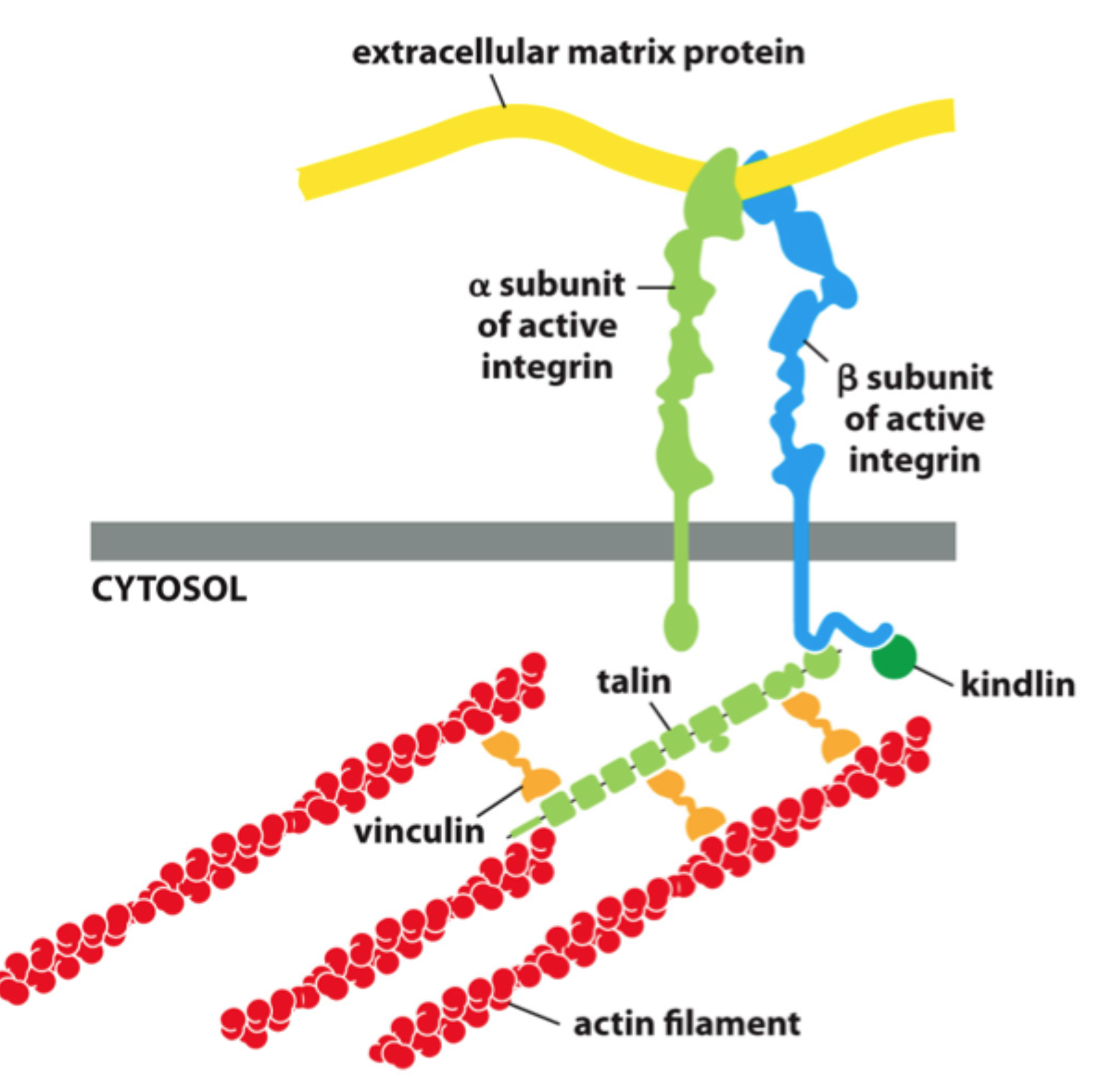
Hvad består et integrin af?
En α-subunit og en β-subunit.
Hvor mange forskellige α- og β-kæder findes der hos mennesker?
Ca. 18 α-kæder og 8 β-kæder.
Hvorfor findes der mange forskellige integriner?
Fordi forskellige α- og β-kæder kombineres til forskellige heterodimere med forskellige bindingsspecificiteter.
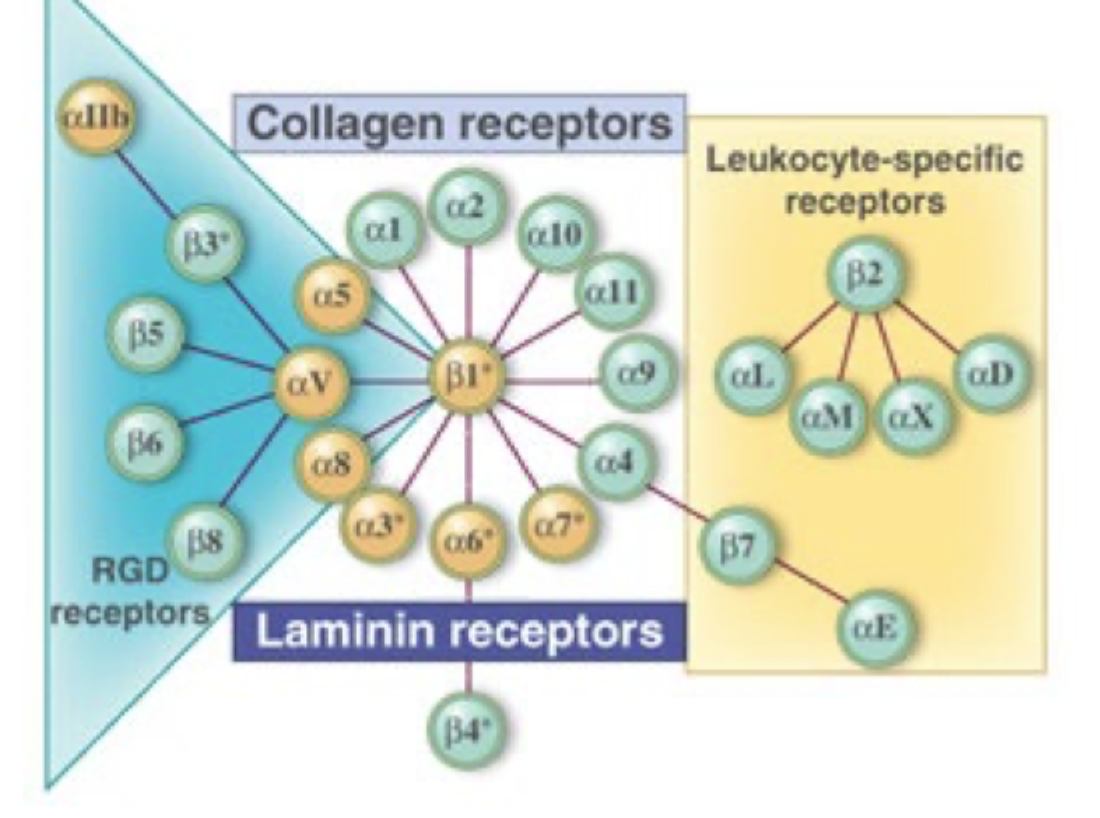
Hvilke ECM-molekyler binder integriner ofte til?
Fx laminin, fibronectin og kollagen.
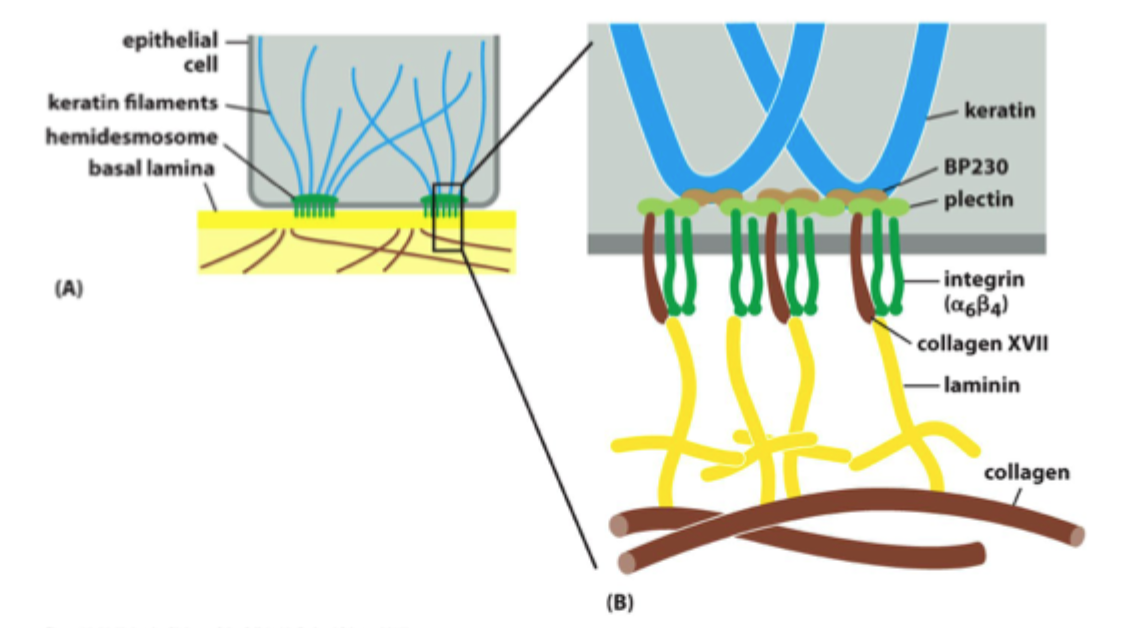
Hvad er særligt ved integriner i hemidesmosomer?
De kobler ikke primært til aktin, men til intermediære filamenter.
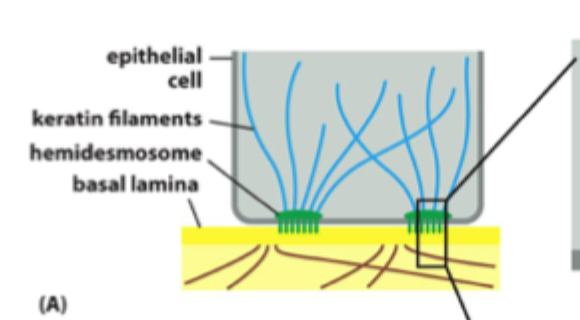
Hvilket integrin er klassisk for hemidesmosomer?
α6β4-integrin.
Hvad er pointen med hemidesmosom-figuren på integrin-sliden?
At nogle integriner er specialiseret til stærk forankring af epithel til basal lamina.
Hvorfor kan defekter i integriner give alvorlig sygdom?
Fordi integriner er afgørende for adhæsion, migration, udvikling og signalering.
Hvad kan ske, hvis leukocyt-integriner er defekte?
Hvide blodlegemer kan ikke binde og migrere normalt, hvilket giver immunproblemer, fx leukocyte adhesion deficiency.
Hvad kan ske ved defekter i integriner i epithel?
Man kan få hudblærer og svag epithelforankring.
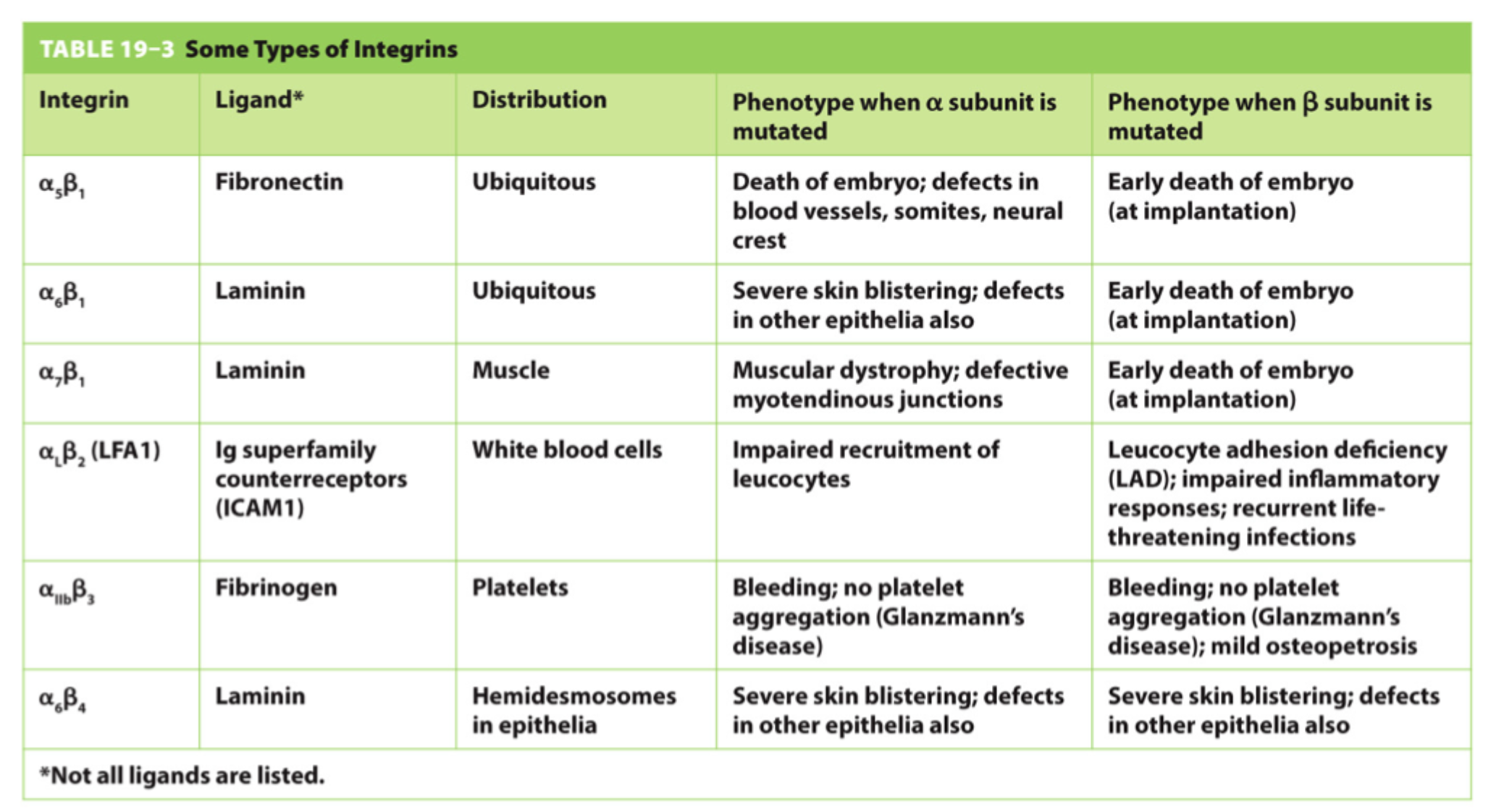
Hvad er hovedpointen med sygdomstabellen?
At den specifikke integrintype afgør, hvilke væv der rammes, og hvilken sygdom man får.
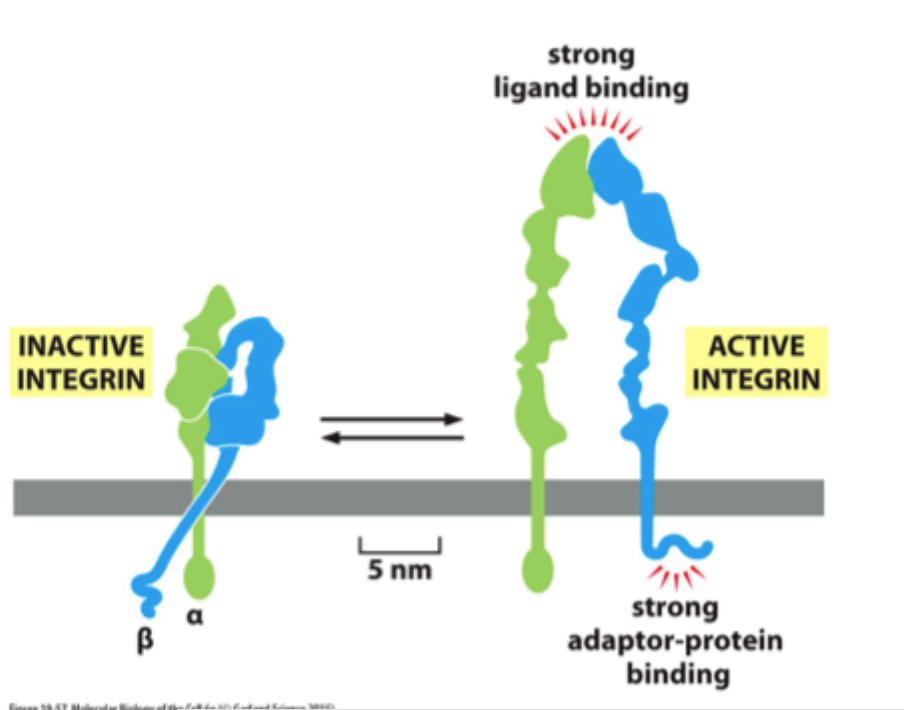
Kan integriner skifte form?
Ja, de kan skifte mellem inaktiv, bøjet form og aktiv, udstrakt form.
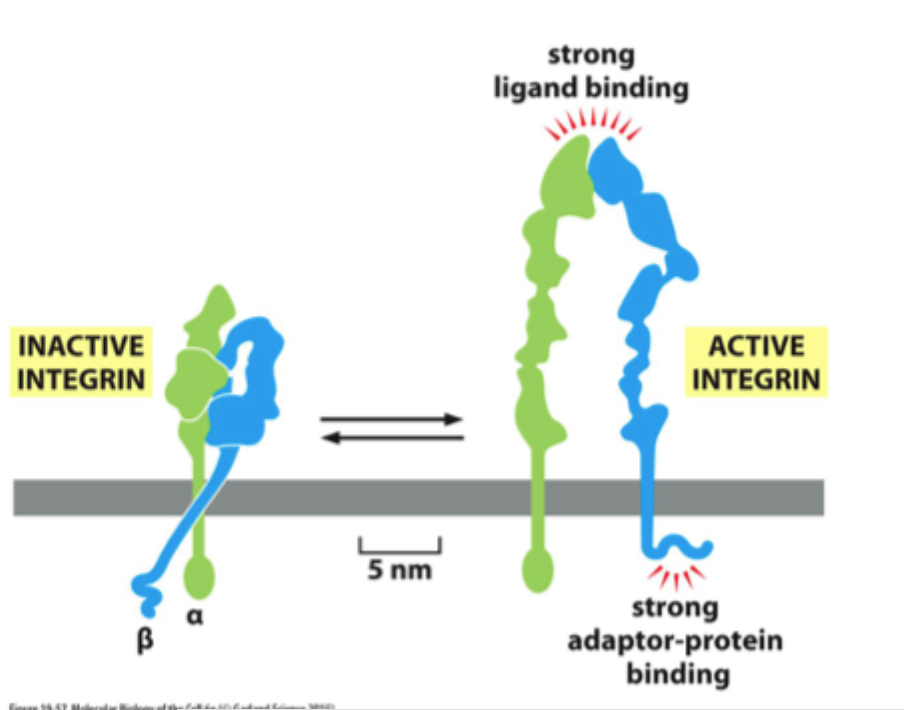
Hvad betyder den aktive form af integrin funktionelt?
Højere affinitet for ligand og bedre binding til adaptorproteiner intracellulært.
Hvad er inside-out signaling for integriner?
Intracellulære signaler ændrer integrinets konformation, så det bliver aktivt og kan binde ECM stærkere.
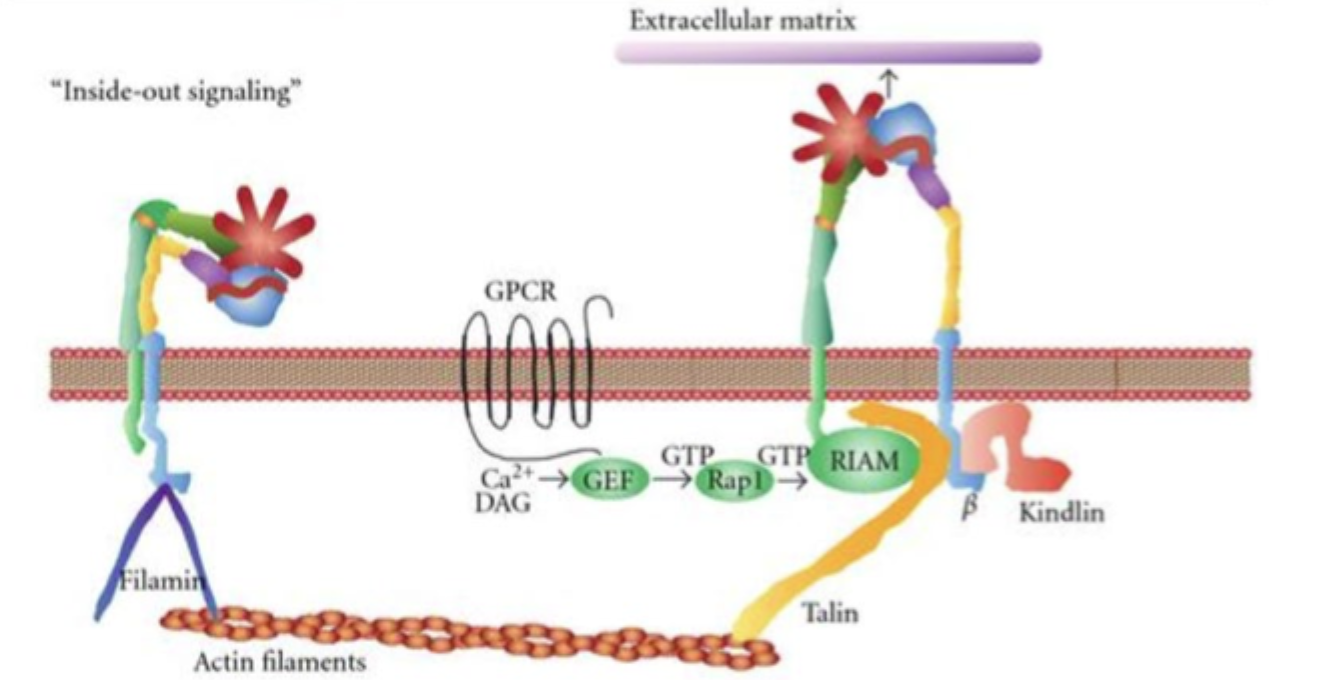
Hvad er outside-in signaling for integriner?
ECM-binding til integrinet udløser signaler ind i cellen og påvirker fx cytoskelet og genekspression.
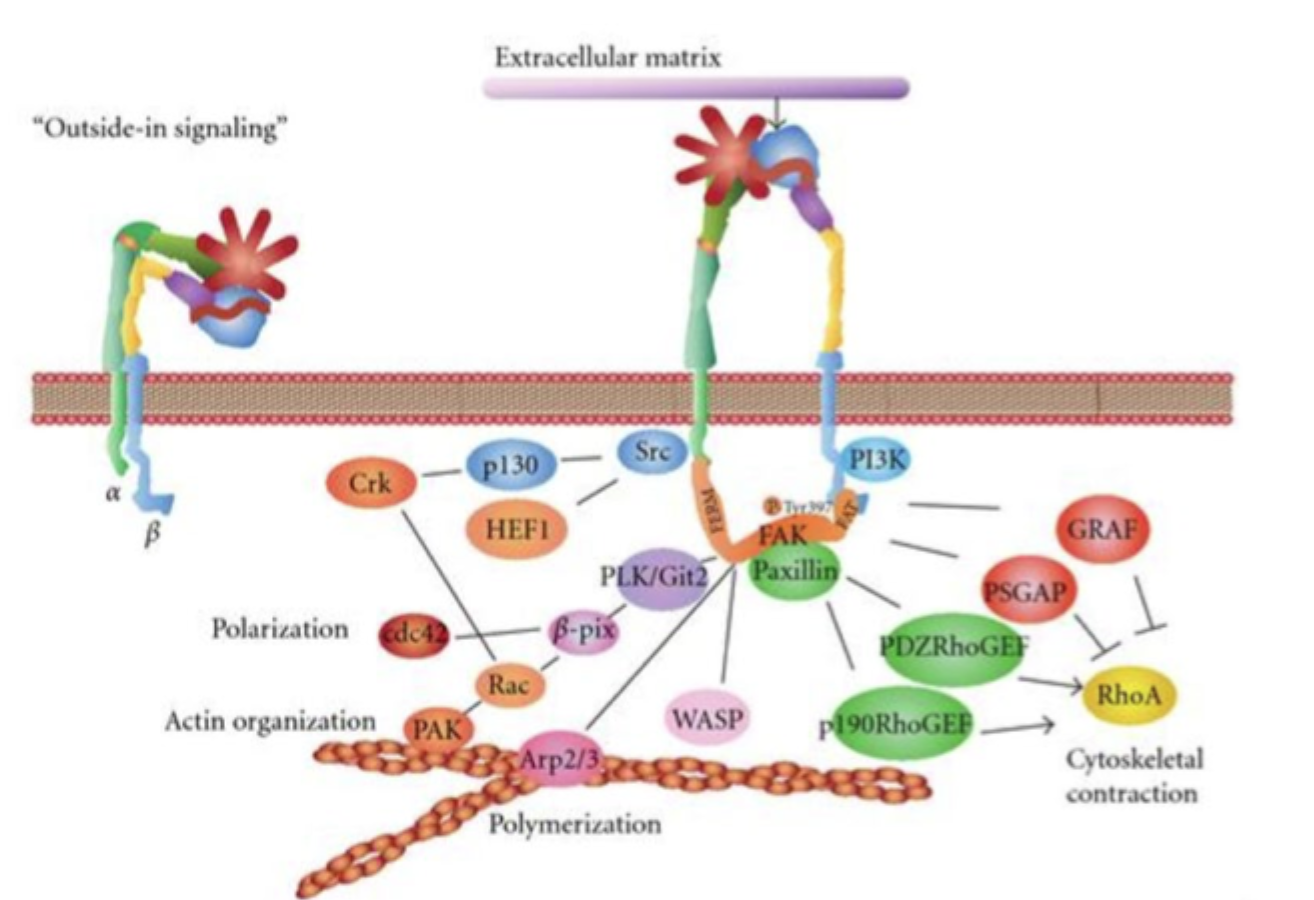
Hvilke proteiner er særligt vigtige for aktivering af integriner indefra?
Talin og kindlin.
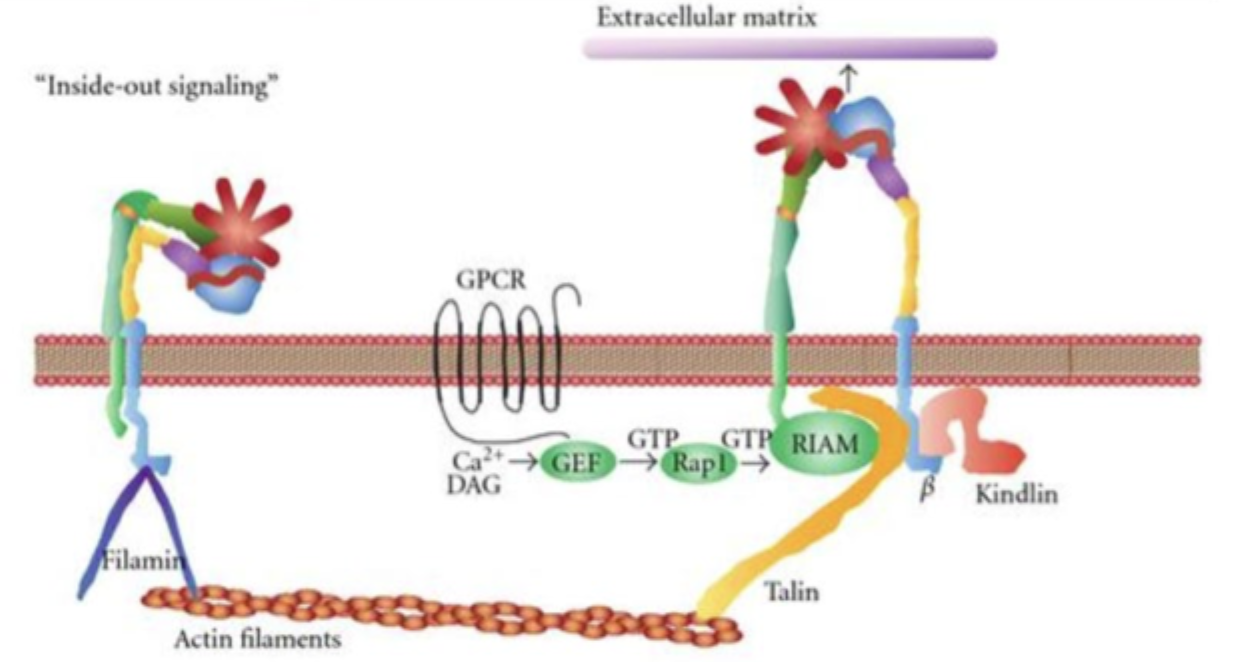
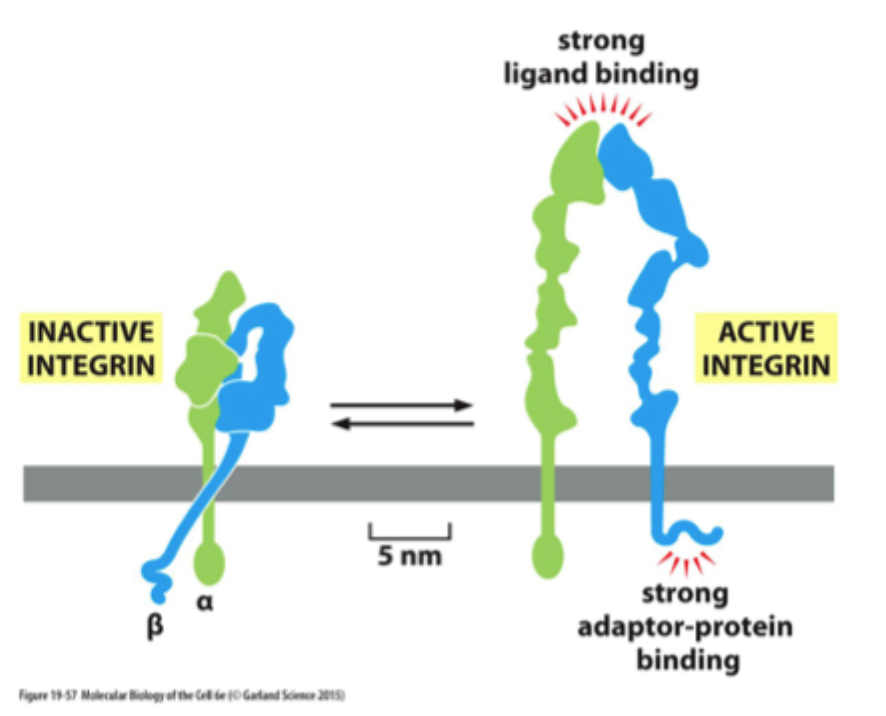
Hvorfor er denne figur vigtig?
Fordi den viser, at integriner ikke bare er lim, men regulerbare signalreceptorer.
Hvorfor giver ét aktivt integrin ikke nødvendigvis stærk adhæsion alene?
Fordi stærk adhæsion ofte kræver mange integriner samlet i klynger.
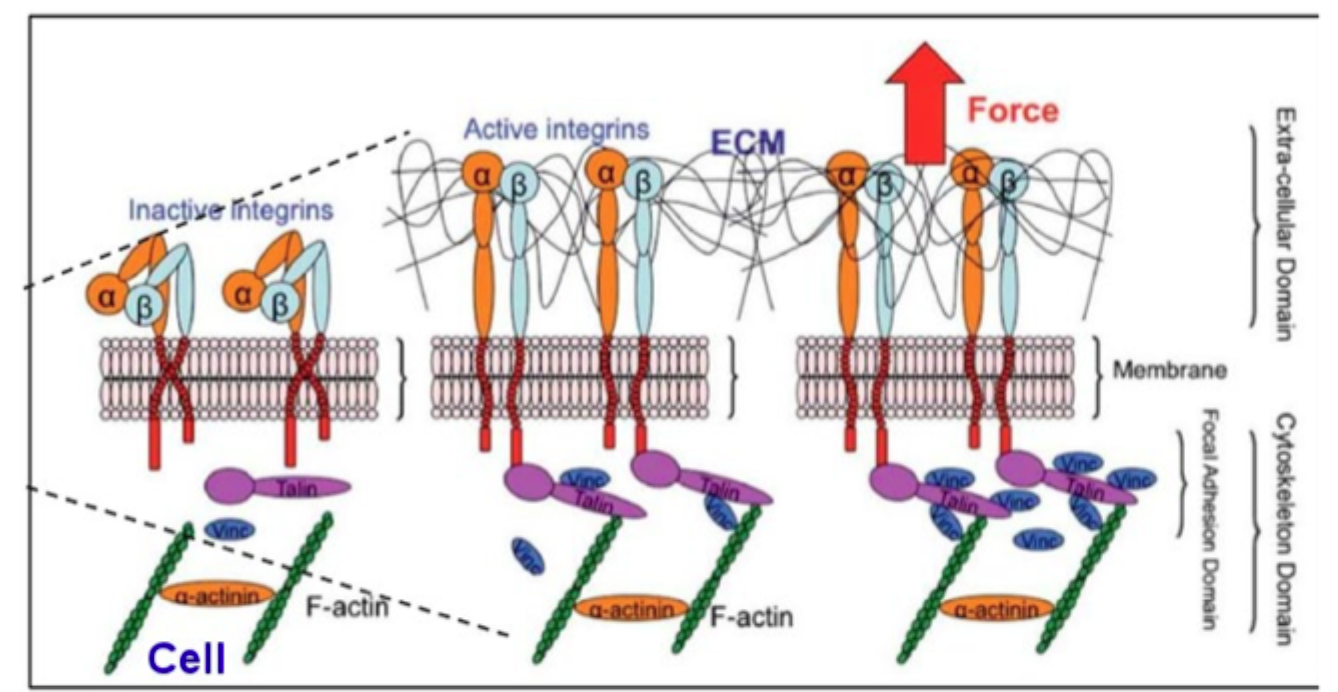
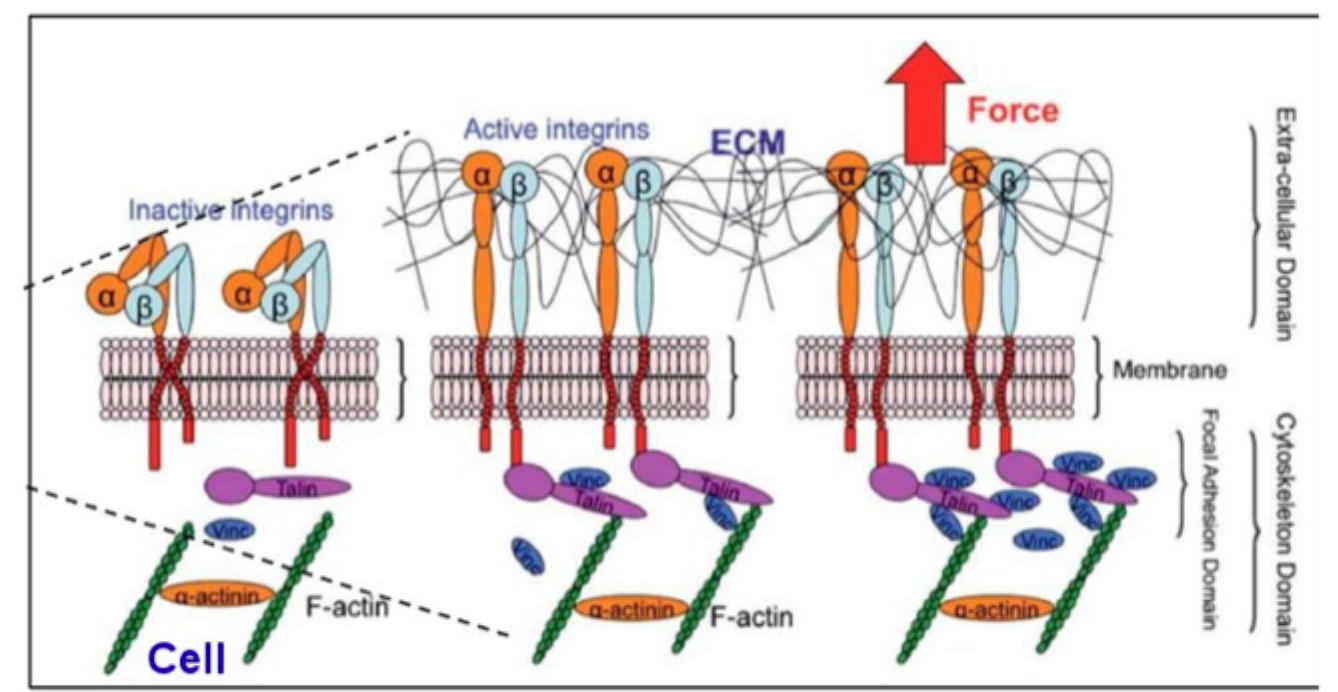
Hvad betyder integrin clustering?
At flere integriner samles i et område og danner stærkere og mere stabil kontakt med ECM.
Hvad sker der med aktin ved stærke integrin-baserede adhæsioner?
Aktinfilamenter organiseres og kobles tættere til adhesionsstederne.
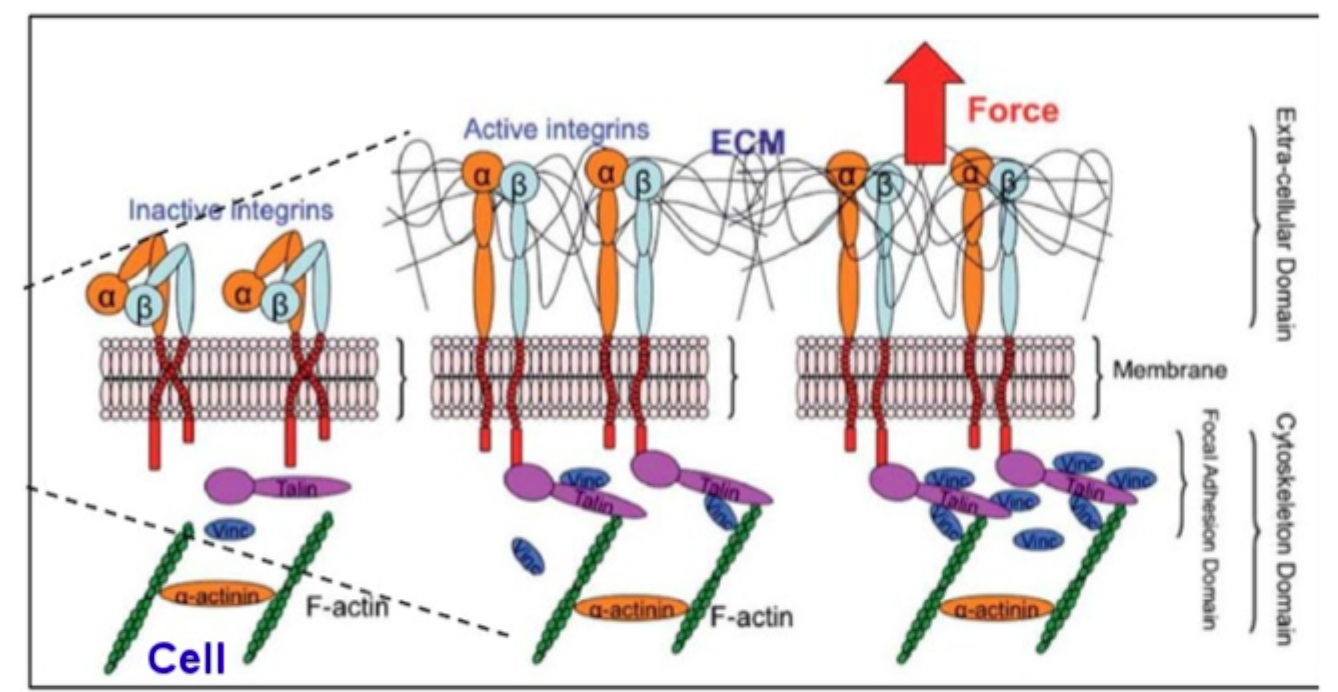
Hvad er hovedpointen med den sidste slide om integrin clusters?
At integriner både skaber mekanisk forankring og fungerer som platforme for signalering.
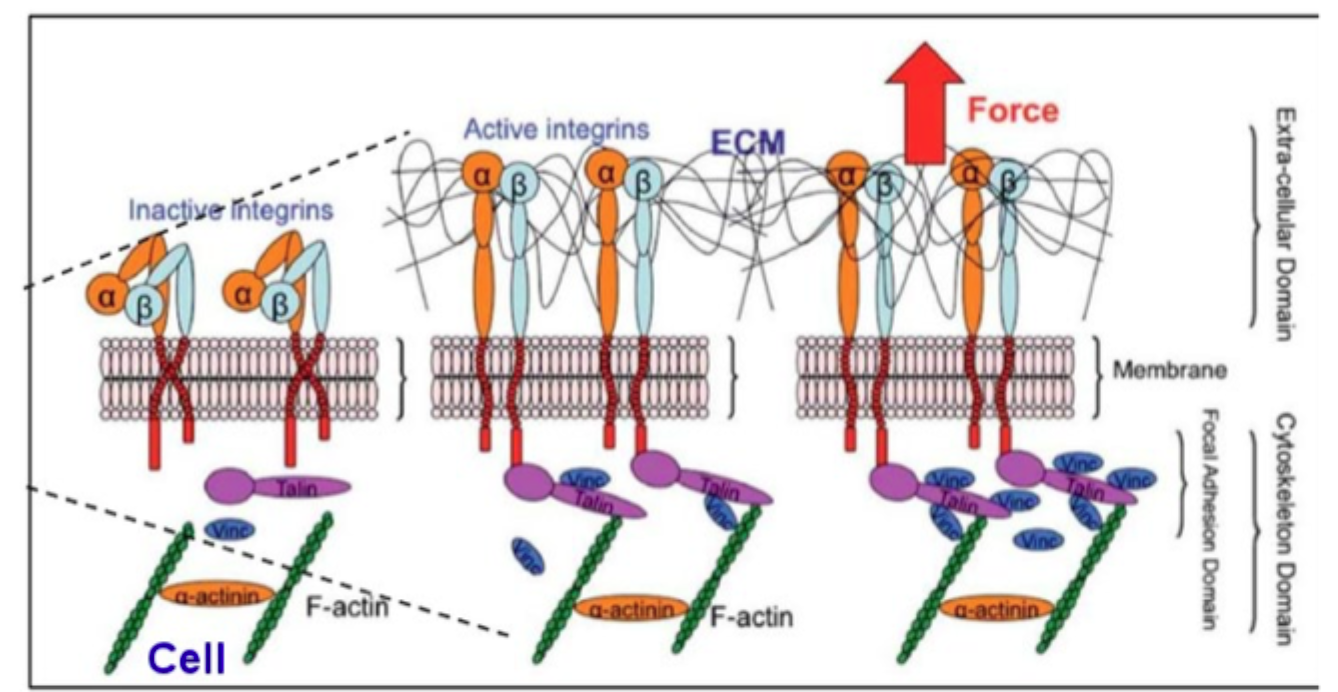
Hvorfor er matrixkontakt vigtig for mange cellers overlevelse og vækst?
Mange celler har anchorage dependence, altså behov for matrixkontakt for normal proliferation og overlevelse.