Derivati degli Idrocarburi - Alogenuri Alchilici
1/61
Earn XP
Description and Tags
Questi flashcards coprono i concetti chiave relativi agli alogenuri alchilici, le loro proprietà, nomenclatura, reattività e reazioni.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
62 Terms
Cosa sono i derivati degli idrocarburi?
sono composti organici che si formano dalla sostituzione di uno o più atomi di idrogeno di un idrocarburo con atomi o gruppi atomici diversi, detti gruppi funzionali.
Quali sono i tre tipi di derivati degli idrocarburi?
I tre gruppi principali dei derivati degli idrocarburi sono:
Derivati alogenati: (tra cui alogenuri alchilici) contenenti atomi di alogeno nel gruppo funzionale.
Derivati ossigenati: contenenti atomi di ossigeno nel gruppo funzionale (alcol, eteri, chetoni, e acidi carbossilici).
Derivati azotati: contenuti atomi di azoto nel gruppo funzionale (comprendono ammine e nitrili).
Questi gruppi di composti presentano diverse proprietà chimiche e fisiche a causa della presenza dei gruppi funzionali variabili.
Cosa sono e quel’è la formula molecolare generale degli alogenuri alchilici?
composti organici in cui uno o più atomi di alogeno appartenenti al gruppo funzionale sono legati a uno o più atomi di carbonio di un alcano.
la formula molecolare generale degli alogenuri alchilici è R-X, dove 'R' rappresenta la catena e 'X' è un atomo di alogeno.
Come si nomina un alogenuro alchilico secondo le regole IUPAC?
La nomenclatura di un alogenuro alchilico secondo le regole IUPAC inizia con l'indicazione del numero di posizione dell'alogeno, seguito dal nome dell'alogeno stesso e infine dal nome dell'alcano da cui deriva. Ad esempio: il cloroetano è nominato come 1-cloroetano se il cloro si trova sul primo carbonio.
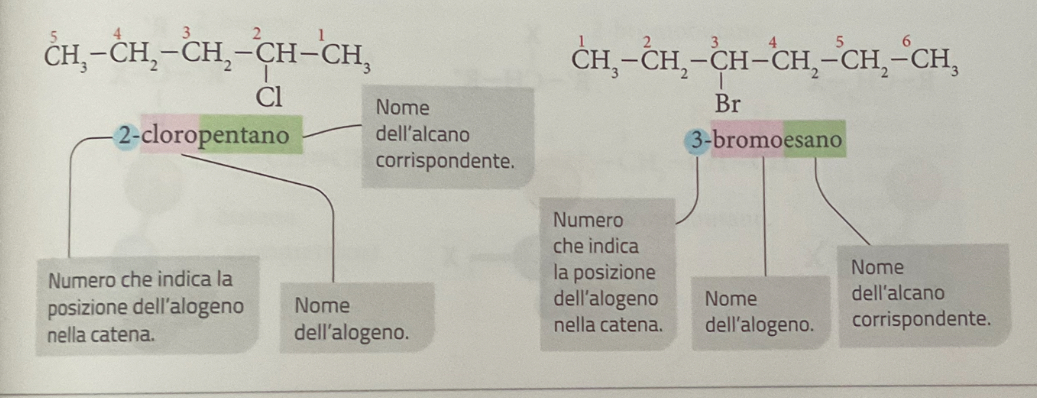
se nella catena è presente lo stesso sostituente più volte?
i numeri che ne indicano la posizione sono separati dalla virgola e il nome del sostituente inizia con i prefissi di/tri/tetra
se sono presenti sostituenti diversi?
devono essere denominati in ordine alfabetico, numerando la catena carboniosa piú lunga partendo dall’estremità più vicina al primo sostituente

Qual è la differenza tra alogenuri alchilici primari, secondari e terziari?
Primari: l'atomo di carbonio con l'alogeno è legato a un solo atomo di carbonio.
Secondari: l'atomo di carbonio con l'alogeno è legato a due atomi di carbonio.
Terziari: l'atomo di carbonio con l'alogeno è legato a tre atomi di carbonio.
quali sono le proprietà fisiche degli alogenuri alchilici?
punti di ebollizione più alti rispetto a quelli degli idrocarburi originali. questo accade perchè l’alogeno presente ha una massa atomica maggiore dell’idrogeno sostituito.
gli alogenuri alchilici sono reattivi?
sì, poichè l’alogeno è più elettronegativo del carbonio e il legame carbonio-alogeno è polarizzato.
cosa porta la reattività degli alogenuri alchilici?
porta due tipi di reazioni: la sostituzione nucleofila e l’eliminazione
descrivi il processo di sostituzione nucleofila
reazione tra alogenuro alchilico ed un nucleofilo, il quale sostituisce l’alogeno formando un alcol o un etere. questo processo avviene in uno di questi due meccanismi;
1 SN2, uno stadio che prevede la partecipazione dei due reagenti (sostituzione nucleofila biomolecolare)
2 SN1, due stadi che prevedono la partecipazione prima solo dell’alogenuro (sostituzione nucleofila monomolecolare)
descrivi il processo di eliminazione
reazione tra alogenuro alchilico e nucleofilo (base forte) dove il nucleofilo sottrae all’alogenuro vicino un atomo di idrogeno sotto forma di ione H+. si forma così un nuovo legame π tra i due carboni, oltre a quello già presente, l’alogenuro si stalla come anione X- e si crea così un alchene. questo processo avviene in uno di questi due meccanismi:
1 meccanismo E2, processo che avviene in uno stadio e porta ad un’eliminazione bimolecolare
2 meccanismo E1, processo che avviene in due stadi e porta ad un’eliminazione monomolecolare
definisci gli alcoli e la loro formula
composti con gruppo funzionale idrossido o ossidrile legato a un carbonio ibridato sp3.
R-OH
come si classificano gli alcoli?
in alcoli saturi e insaturi.
gli alcoli saturi sono composti formati da una catena carboniosa unita da legami semplici
gli alcoli insaturi sono composti nei quali sono presenti il gruppo ossidrile e un legame multiplo

quali sono le regole IUPAC di alcoli saturi e insaturi?
il nome degli alcoli saturi è costituito dal nome dell’alcano corrispondente in cui la desinenza -o è sostituita dal suffisso -olo.
il nome degli alcoli insaturi invece è costituito dal numero che indica la posizione del legame multiplo, seguito dal nome dell’idrocarburo insaturo e dal numero che indica la posizione del gruppo, seguito dal prefisso olo

quali sono le reazioni di sintesi degli alcoli?
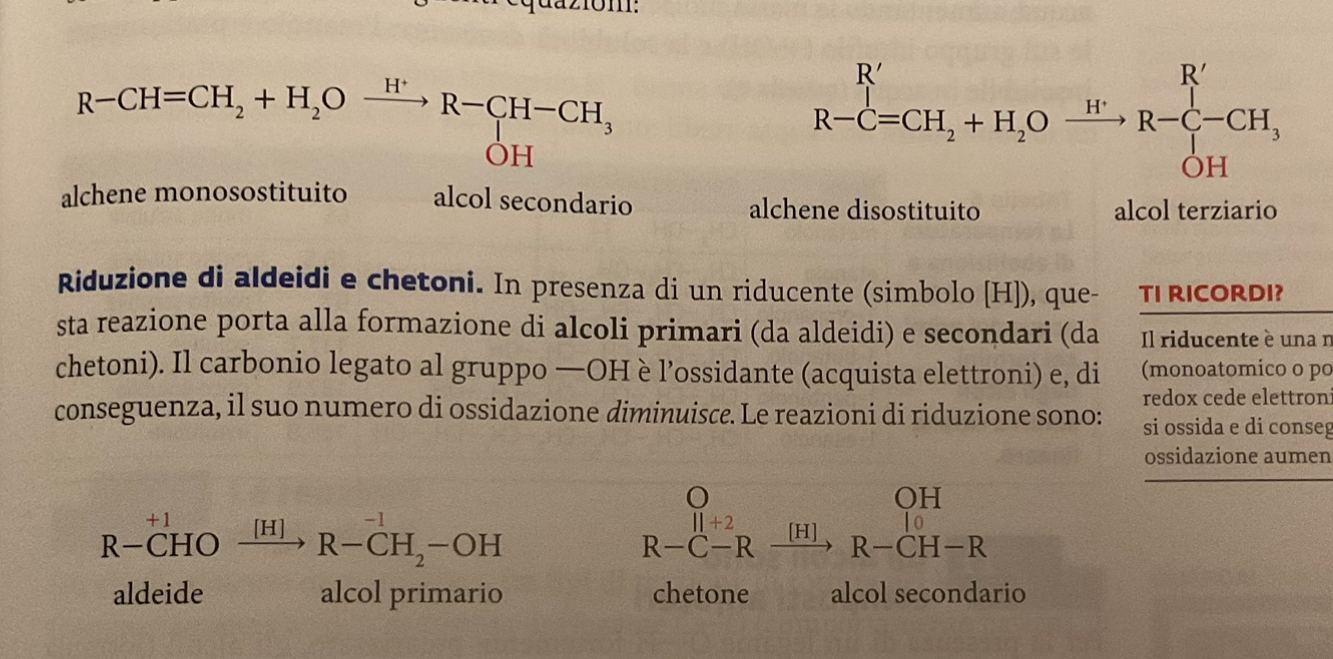
idratazione degli alcheni e riduzione di aldeidi e chetoni.
l’idratazione rompe il doppio legame e aggiunge uno ione H+. porta alla sintesi di un alcol secondario o terziario
la riduzione porta alla formazione di alcoli primari e secondari
descrivi le proprietà fisiche degli alcoli
1 leggera polarizzazione a causa della carica di OH-
2 solubili in H2O
3 di norma, a temperatura ambiente, se l’alcol in questione ha meno di 12 atomi di carbonio si trova allo stato liquido, se invece l’alcol presente più di 12 atomi di carbonio si trova allo stato solido
4 formano legami a idrogeno intermolecolari che determinano alti punti di ebollizione e la solubità in acqua che diminuisce all’aumentare della massa molecolare, tanto che l’esanolo è praticamente insolubile

perchè gli alcoli sono composti anfoteri?
perchè possono comportarsi sia da acidi rompendo il legame OH e rilasciando ioni H+, sia da basi, dato che O ha due elettroni liberi da donare
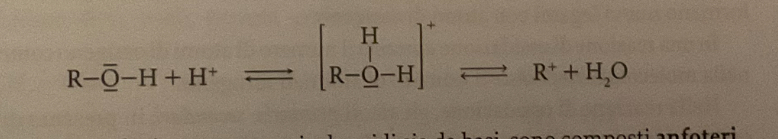
quali sono i due tipi di reazioni degli alcoli?
1 deidrogenazione, processo dove avviene la rottura del legame O-H e si formano sali e ioni
2 disidratazione, processo dove avviene la rottura del legame C-O e viene separata la molecola di H2O
definizione di polioni
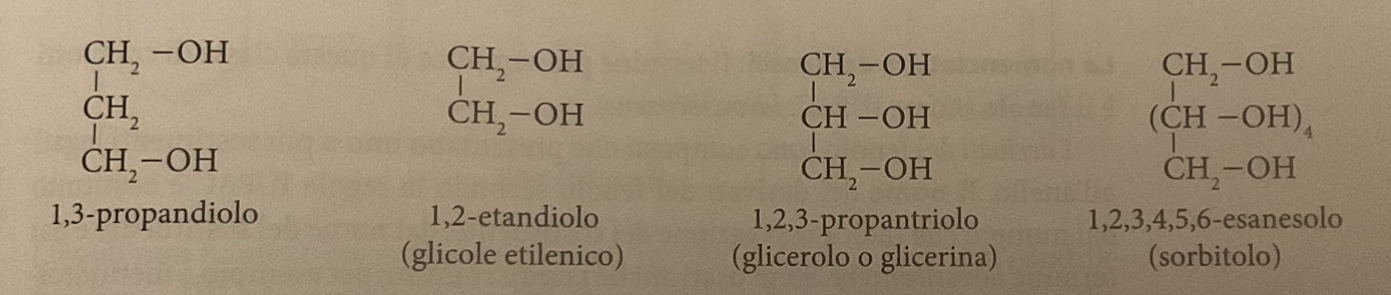
composti che derivano dagli alcani per sostituire due o piú atomi di carbonio con due o più gruppi ossidrili -OH
nome iupac dei polioni
numeri che indicano la posizione dei gruppi -OH più la radice del nome dell’alcano e dal suffisso -diolo/-triolo/-tetraolo/-pentaolo
definizione, formula e esempio di fenolo
sono composti organici con gruppo -OH legato all’anello benzenico. formula Ar-OH. il termine più semplice è il fenolo o ideossibenzene
nomenclatura derivati del fenolo
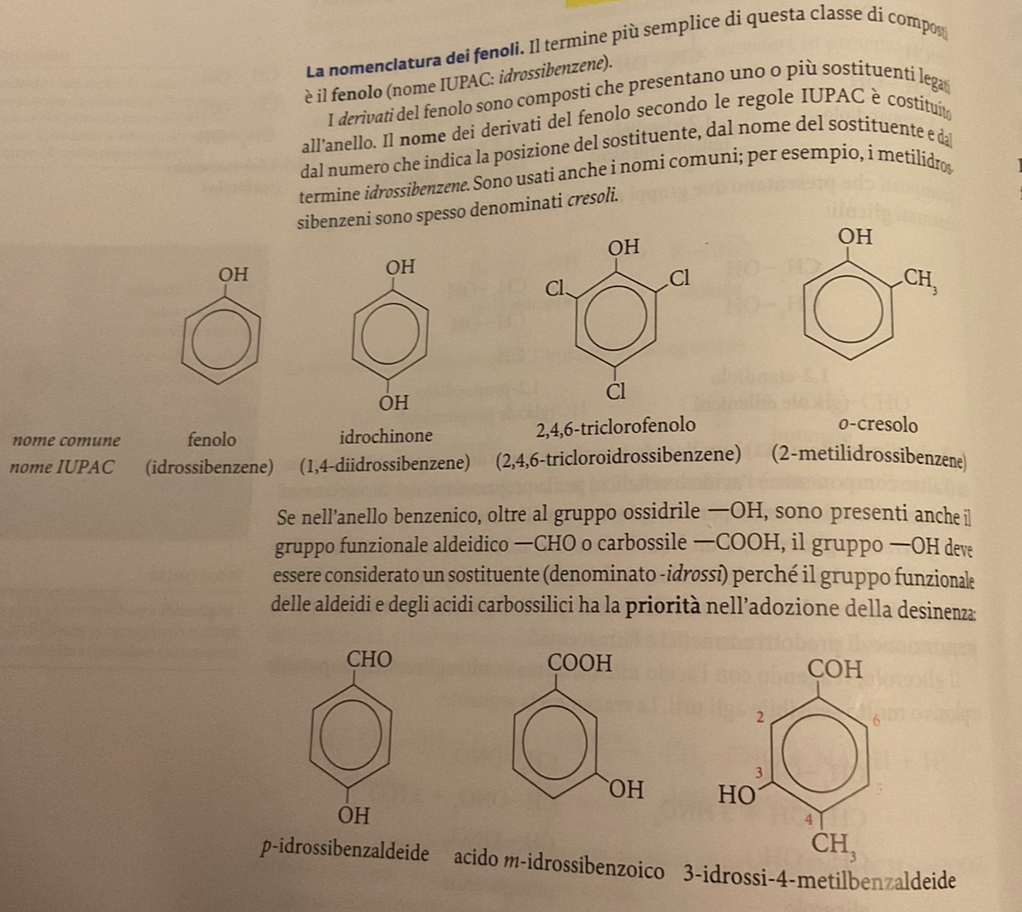
proprietà fisiche e chimiche dei fenoli
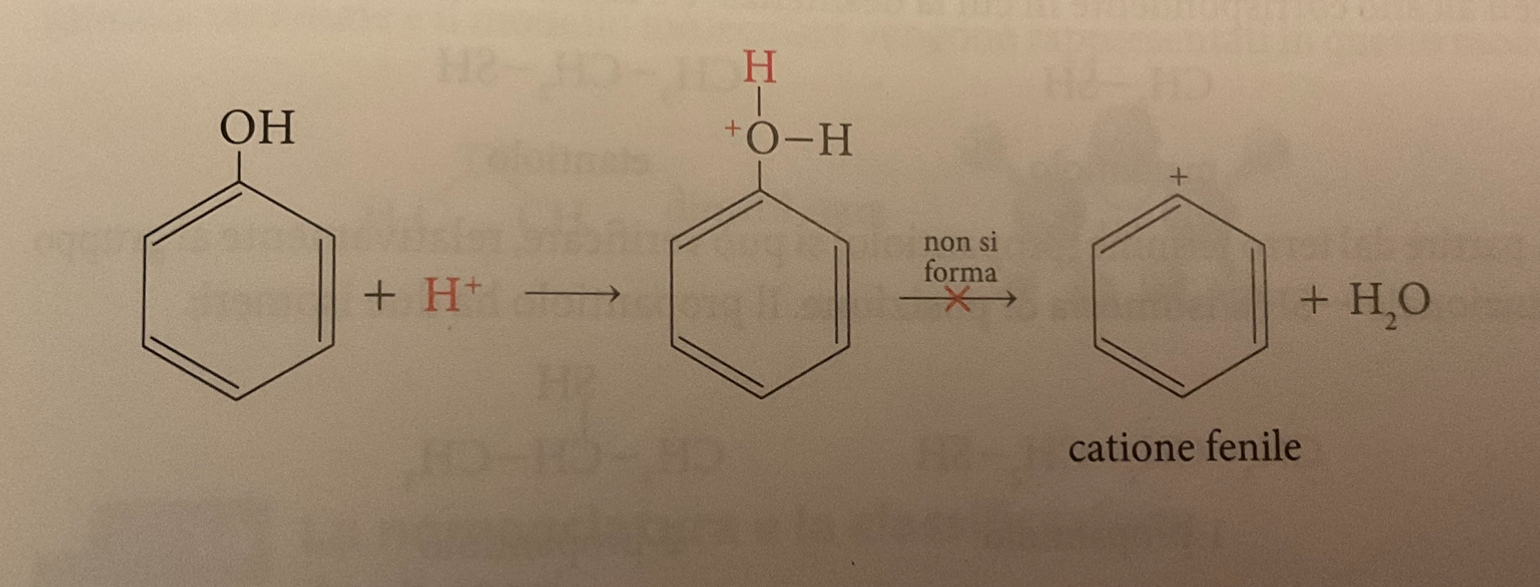
I fenoli sono solidi cristallini incolori. Non hanno un comportamento basico: in acqua si comportano da acidi di Brønsted-Lowry cedendo l’atomo di idrogeno del gruppo -OH sotto forma di ione H+; si formano così lo ione fenossido e lo ione ossonio.
definizione e formula dei tioli
I tioli sono composti caratterizzati dalla presenza del gruppo funzionale solfidrile -SH legato ad un atomo di carbonio ibridato sp³. La loro formula molecolare è R-SH.
nome iupac dei tioli
Il nome è costituito dall’alcano corrispondente con suffisso -tiolo.

eteri, definizione e formule generali
composti in cui un gruppo funzionale è un atomo di ossigeno legato a due gruppi organici, alchilici (Ar) o acrilici (R). le formule molecolari sono: R-O-R, Ar-O-Ar, R-O-Ar
denominazione (nome comune) degli eteri
si distinguono in simmetrici, se i gruppi legati all’ossigeno sono uguali, asimmetrici se son diversi
nomenclatura eteri
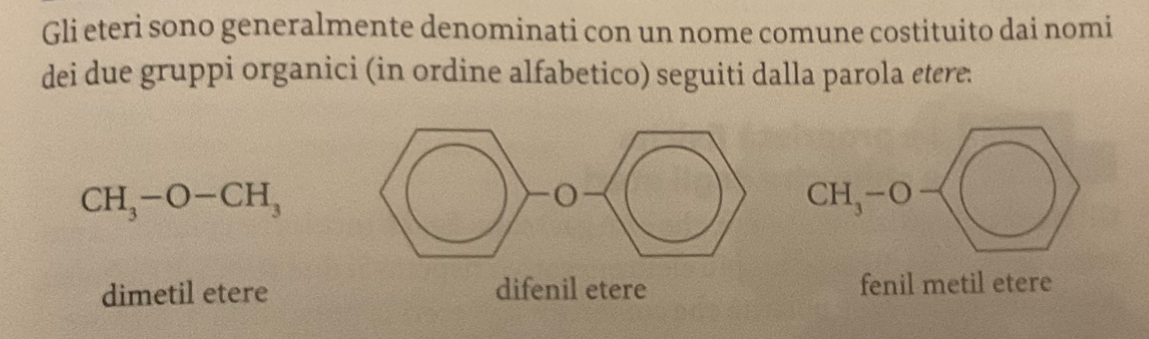
quali sono le reazioni di sintesi degli eteri?
1 la disidratazione interomolecolare di alcoli primari, che forma eteri simmetrici
2 sintesi di williamson, che forma eteri asimmetrici
proprietà fisiche e chimiche degli eteri
sono liquidi, incolori e volatili
definizione di aldeidi e chetoni
composti caratterizzati dalla presenza del gruppo carbonile (CO), il cui che C è ibridato in sp2 e legato a un atomo di ossigeno da un doppio legame C=O. sono fortemente aromatici (rilasciano odori)
formula molecolare e nomenclatura delle aldeidi
Nelle aldeidi il C del gruppo carbonile è sempre legato ad un H e ad un gruppo alchilico o arilico. Le formule molecolare generali sono R-CHO e Ar-CHO.
formula molecolare e nomenclatura dei chetoni
Nei chetoni il C del gruppo carbonile è legato a due gruppi alchilici o arilici, oppure uno alchilico e l’altro arilico. Le formule molecolari generali sono R-CO-R, Ar-CO-Ar e Ar-CO-R.
nomenclatura di aldeidi alifatiche e chetoni alifatici
1 : Il nome delle aldeidi alifatiche si ottiene sostituendo la desinenza -o del nome dell’alcano corrispondente con il suffisso -ale. Quando nella catena carboniosa sono presenti dei sostituenti la catena va numerata partendo dal carbonio del gruppo carbonile.
2 Il nome dei chetoni alifatici si ottiene sostituendo la desinenza -o del nome dell’alcano corrispondente con il suffisso -one.
reazioni di sintesi di aldeidi e chetoni
La sintesi più comune di aldeidi e chetoni avviene per ossidazione degli alcoli in presenza di un ossidante, in ambiente acido. Il tipo di prodotto dipende dalla struttura dell’alcol di partenza:
1 le ossidazioni degli alcol primari forma le aldeidi
2 le ossidazioni degli alcol secondari forma i chetoni
proprietà fisiche di aldeidi e chetoni
punti di ebollizione più alti degli idrocarburi ma più bassi degli alcani (con stessa massa molecolare). la loro solubità si abbassa all’aumentare della massa molecolare
reazioni di aldeidi e chetoni
1 Addizione nucleofila: in aldeidi e chetoni un nucleofilo attacca il carbonio del C=O e si ottiene un prodotto di addizione.
2 Ossidazione: le aldeidi si ossidano facilmente in acidi carbossilici.
3 Riduzione: aldeidi e chetoni si riducono ad alcoli: le aldeidi → alcoli primari, i chetoni → alcoli secondari.
4 I reattivi di Fehlimg e di Tollens
come si distinguono, in laboratorio, aldeidi e chetoni?
Tramite i reattivi di Tollens e di Fehling, test classici per riconoscere le aldeidi distinguendole dai chetoni, che non reagiscono.
Il reattivo di Tollens è una soluzione basica che contiene il complesso d’argento [Ag(NH₃)₂]⁺. In presenza di un’aldeide, l’aldeide si ossida (in ambiente basico) mentre lo ione argento Ag⁺ si riduce e si deposita sulle pareti della provetta formando la tipica patina o lo “specchio d’argento”. I chetoni in genere risultano negativi, anche se alcuni composti particolari possono dare comunque esito positivo.
Il reattivo di Fehling si prepara mescolando due soluzioni: Fehling A, che contiene CuSO₄ (ioni Cu²⁺), e Fehling B, che contiene tartrato sodio-potassico e NaOH. In ambiente basico, se è presente un’aldeide (o uno zucchero riducente), l’aldeide si ossida a carbossilato e il rame(II) Cu²⁺ si riduce a rame(I), formando un precipitato di Cu₂O di colore rosso mattone: questo è il segnale di positività del test. Anche qui i chetoni normalmente non reagiscono, salvo alcune eccezioni.
Definizione acidi carbossilici
composti organici caratterizzati dal gruppo funzionale carbossile -COOH costituito da due gruppi funzionali, il gruppo carbonile CO e il gruppo ossidrile OH
Distinzione: alifatici vs aromatici + formule
Si distinguono secondo il gruppo (alchilico o arilico) a cui è legato l’atomo di carbonio del carbossile in:
1 alifatici, in cui C è legato a un gruppo alchilico (R) e la formula molecolare generale è R-COOH, e
2 aromatici, in cui C è legato a un gruppo arilico (Ar) e la formula molecolare generale è Ar-COOH.
Nomenclatura acidi carbossilici
Il nome è costituito dal termine acido (all’inizio) e dal nome dell’alcano corrispondente in cui la desinenza -o è sostituita dal suffisso -oico; -ico nel nome comune (es. ACIDO pentanOICO). Parto a contare i carboni così da avere l’acido carbossile -COOH nella posizione più vicina a 1 (solitamente è sempre 1).
definizione e suddivisione acidi grassi
acidi carbossilici alifatici con numero pari di atomi di carbonio uguale o superiore a 12. sono divisi in:
1 saturi, solo legami semplici
2 insaturi, un legame doppio
3 polinsaturi, più legami doppi
reazioni di sintesi degli acidi carbossilici
La reazione più comune per la loro sintesi è l’ossidazione di alcoli primari e di aldeidi.
proprietà fisiche degli acidi carbossilici
1 A temperatura ambiente primi quattro termini sono allo stato liquido; i termini superiori allo stato solido. infatti la solubità diminuisce all’aumentare della massa molecolare
2 punti di ebollizione più alti di idrocarburi e alcoli
3 in acqua si comportano da acidi di Brønsted-Lowry, liberando l’idrogeno del gruppo OH-
reazioni degli acidi carbossilici
1 salificazione, la reattività degli acidi carbossilici è legata al gruppo ossidrile, che può cedere H e portare alla creazione di R-COO e alla formazione di sale
2 sostituzione nucleofila, si creano i derivati degli acidi carbossilici
definizione e formula degli esteri
derivati degli acidi carbossilici nei quali il gruppo ossidrile -OH è stato sostituito dal gruppo alcossilico -OR, a cui possono essere legati due gruppi alchilici: uno arilico e uno alchilico oppure due arilici. formula generale R-COO-R / Ar-COO-R
come avviene la creazione di un trigliceride?
tramite esterizzazione; perdita di 3 molecole di H2O da un estere e formazione legami O-C
definizione ammidi
le ammidi sono derivati degli acidi carbossilici dove il gruppo ossidrile OH è sostituito dal gruppo -NH2, -NHR o -NR2.
tipi di ammidi
esistono le ammidi:
1 primarie, che hanno come gruppo funzionale NH2
2 secondarie, che hanno come gruppo funzionale NHR
3 terziarie, che hanno come gruppo funzionale NR2
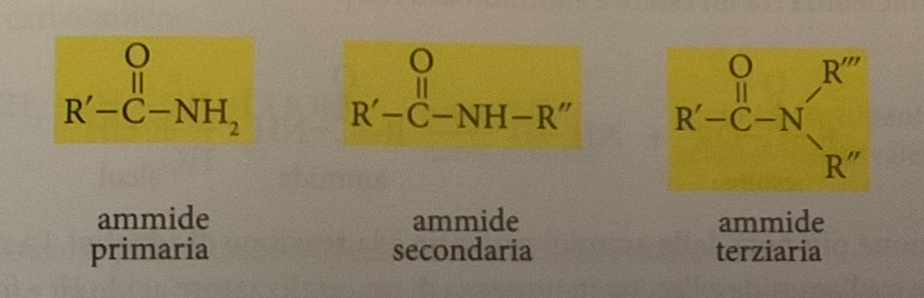
Legame ammidico/peptidico
Il legame carbonio-azoto è detto ammidico; quando si stabilisce tra gli amminoacidi delle proteine (ammidi più importanti), chiamato di legame peptidico.
cos’è l’urea
amminide prodotta dal metabolismo degli amminoacidi, è tossico.
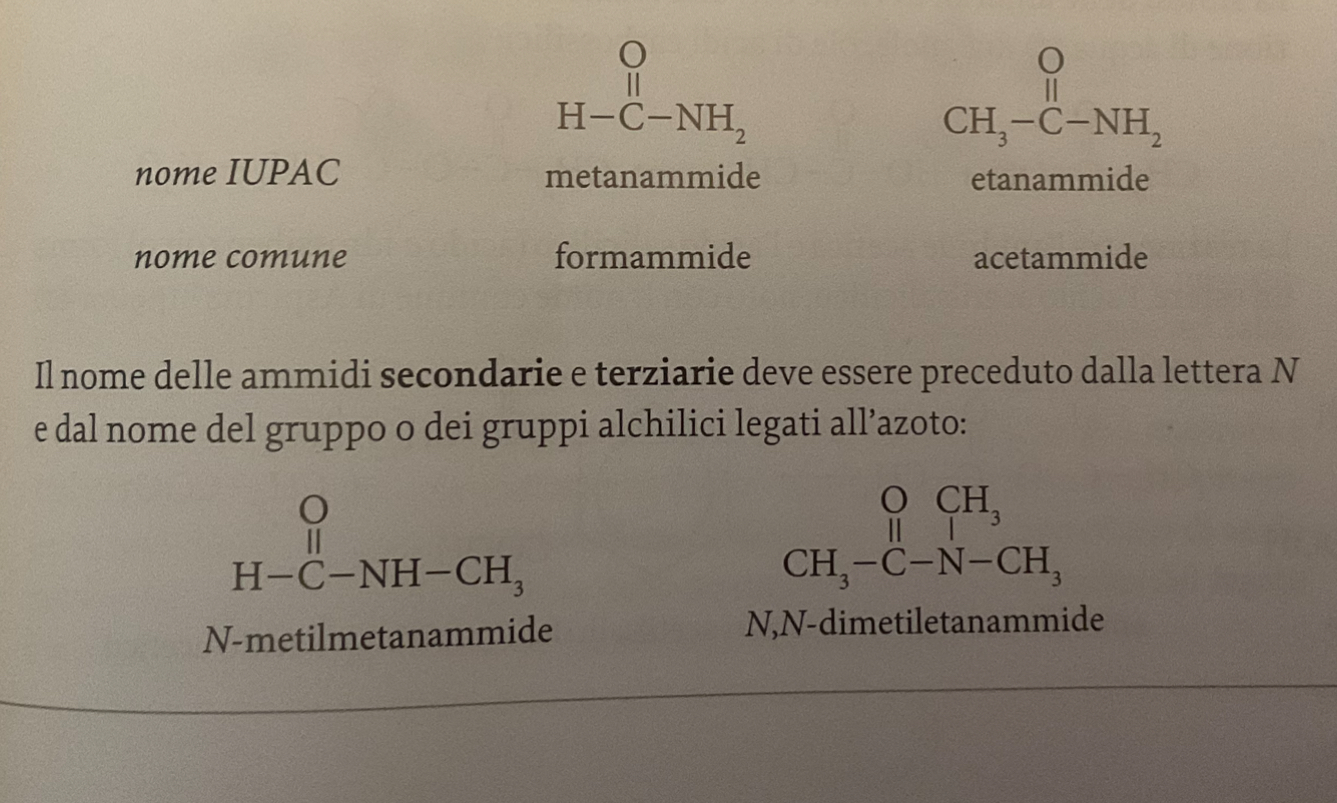
nomenclatura ammidi
Il nome delle ammidi primarie è costituito dalla radice del nome dell’acido corrispondente con il suffisso -ammide; quello delle secondarie e terziarie è preceduto dalla lettera N e dal nome del/dei gruppo/gruppi alchilici legati all’azoto.
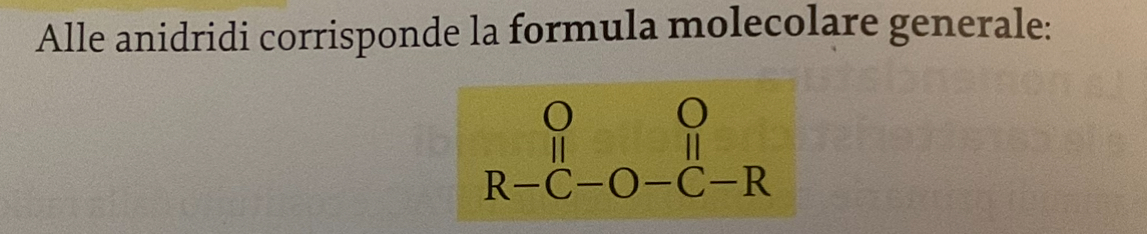
definizione e formula anidridi
composti derivati degli acidi carbossilici con gruppo funzionale —CO-O-CO—
definizione di acidi carbossilici polifunzionali
composti in cui sono presenti due o più gruppi funzionali
tipi di acidi carbossilici polifunzionali
1 idrosaccaridi, composto in cui sono presenti 1 o più gruppi ossidrile -OH e 1 o più gruppi carbossilici -COOH.
2 chetoacidi, composto in cui sono presenti un gruppo carbonile -CO e 1 o più gruppi carbossilici -COOH
3 acidi bicarbossilici, composti costituiti da due gruppi gruppi carbossilici alle estremità della catena carboniosa
definizione ammine
Sono composti organici derivati dell’ammoniaca, per sostituzione di uno o più atomi di idrogeno con uno o più gruppi alchilici.
definizione gruppo funzionale amminico
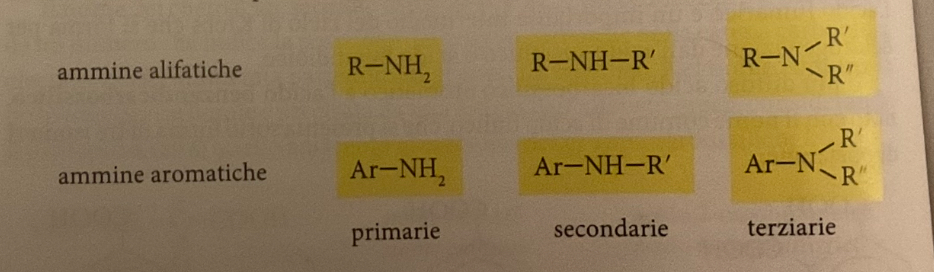
Il gruppo funzionale amminico è costituito da un atomo di azoto legato a un gruppo alchilico o arilico e da due H che possono essere sostituiti da gruppi alchilici o arilici.
classificazione gruppo funzionale amminico
Le ammine sono classificate in primarie, secondarie e terziarie, se all'atomo di azoto sono legati rispettivamente due atomi di idrogeno, un atomo di idrogeno e un gruppo alchilico, oppure due gruppi alchilici.
sintesi delle ammine
Le reazioni di sintesi delle ammine alifatiche sono: 1 l’alchilazione dell’ammoniaca (sostituzione nucleofila Sn2)
2 la riduzione delle ammidi (rompo il legame amminico e riduco).

nomenclatura delle ammine

proprietà ammine
1 a temperatura ambiente, metilammina ed etilammina sono allo stato gassoso, i termini superiori invece a quello liquido.
2 A parità di massa molecolare i punti di ebollizione delle ammine primarie e secondarie sono più alti rispetto agli idrocarburi e più bassi rispetti agli alcoli.
3 La solubilità diminuisce all’aumentare della massa molecolare.
4 Con un acido forte si comportano da basi di Lewis per la presenza di un doppietto elettronico libero sull’atomo di azoto; possono condividerlo con lo ione H+ ceduto dall’acido.
5 In acqua si comportano da basi di Brønsted-Lowry accettando un protone dall’acqua che agisce da acido.
6 Le ammine aromatiche sono meno basiche di quelle alifatiche e dell’ammoniaca perché il doppietto elettronico non condiviso dell’azoto è delocalizzato all’interno dell’anello benzenico e quindi meno disponibile ad accettare un protone.