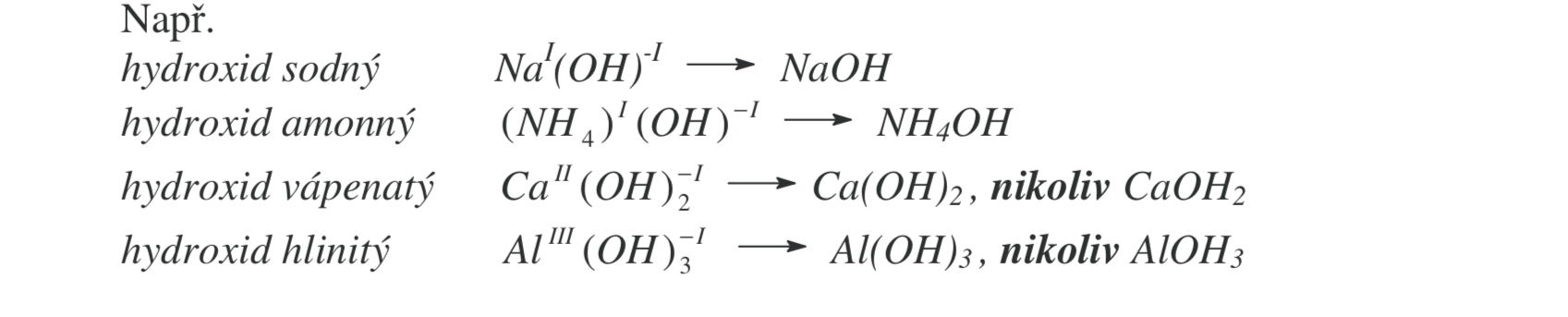Názvosloví
Obsah:
Názvosloví
- K zapamatování
- oxidů
- Hydroxidů
- Kyselin * Bezkyslíkaté kyseliny * Kyslíkaté kyseliny * Polykyseliny * Hydrogenkyseliny * Thiokyseliny
- Solí * Soli bezkyslíkatých kyselin * Soli kyslíkatých kyselin * hydrogensoli * Hydráty * Podvojné soli
\
\

NH3 = amoniak
PH3 = fosfan
ASH3 = arsan
CH4 = methan
SiH4 = silan
BH3 = boran
H2SO4 = kyselina sírová
H2SO3 = kyselina siřičitá
H2CO3 = kyselina uhličitá
Názvosloví oxidů
- Binární (dvouprvkové) sloučeniny s kyslíkem
- Oxidační číslo kyslíku je -2
Tvoření vzorce
Oxid dusičný - ičný=5
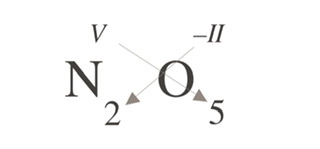
- křížové pravidlo
- Název tvořed slovem oxid + přídavným jménem odvozeným od prvku
\ # Názvosloví hydroxidů
- mají skupinu -OH (oxidační číslo -1)
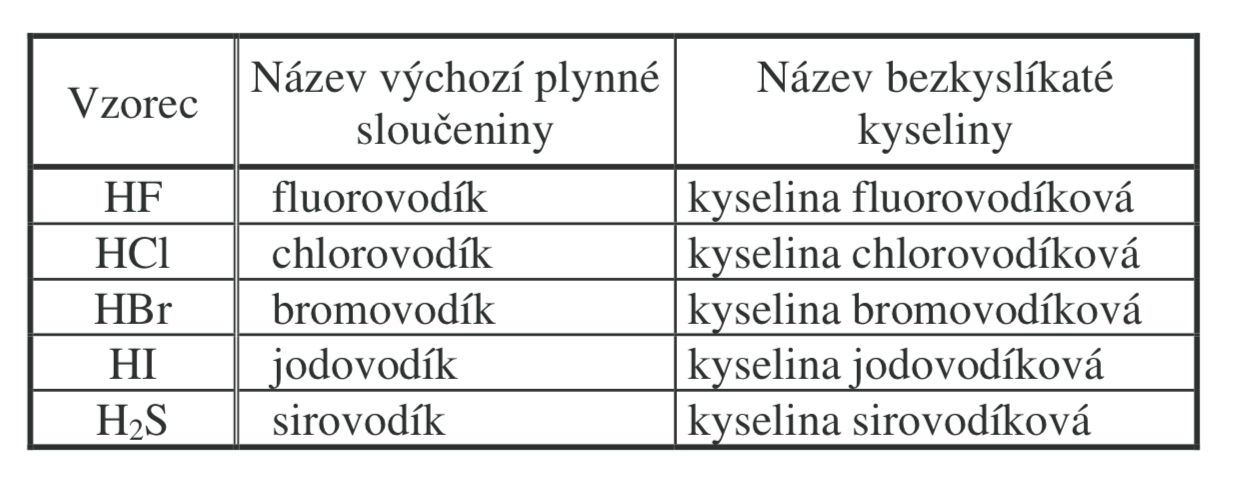
Bezkyslíkaté kyseliny
- H má oxidační číslo +1
Kyslíkaté kyseliny
- většinou tříprvkové sloučeniny (H, další prvek, O)
- Oxidační čísla H + prvek X = O
\

Polykyseliny
- více centrálních atomů
Zapamatovat:
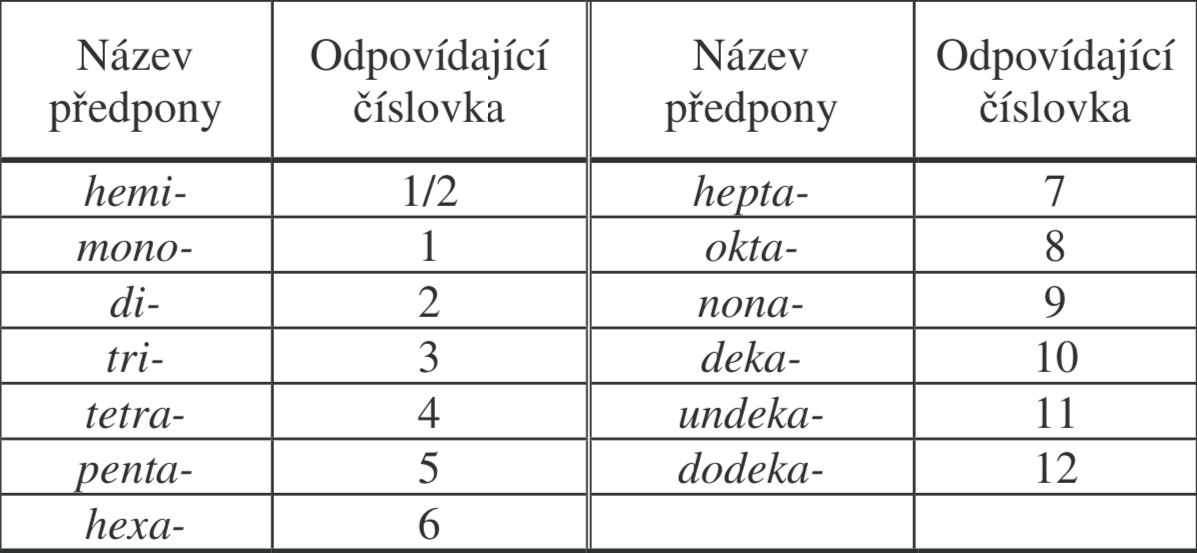
Např.
Kyselina tetrakřemičitá - má 4 x křemík
Hydrogenkyseliny
- Má víc vodíků
Např. Trihydrogen fosforitá
\
Thiokyseliny
- kyslík nahrazen sírou
Soli bezkyslíkatých kyselin
- Nemají kyslík

Tvoření názvu
- Podstatným jménem odvozeným od aiontu + koncovka -id (jodid, bromid)
- Přídavným jménem odvozeným od názvu prvku se zakončením podle oxidačního čísla
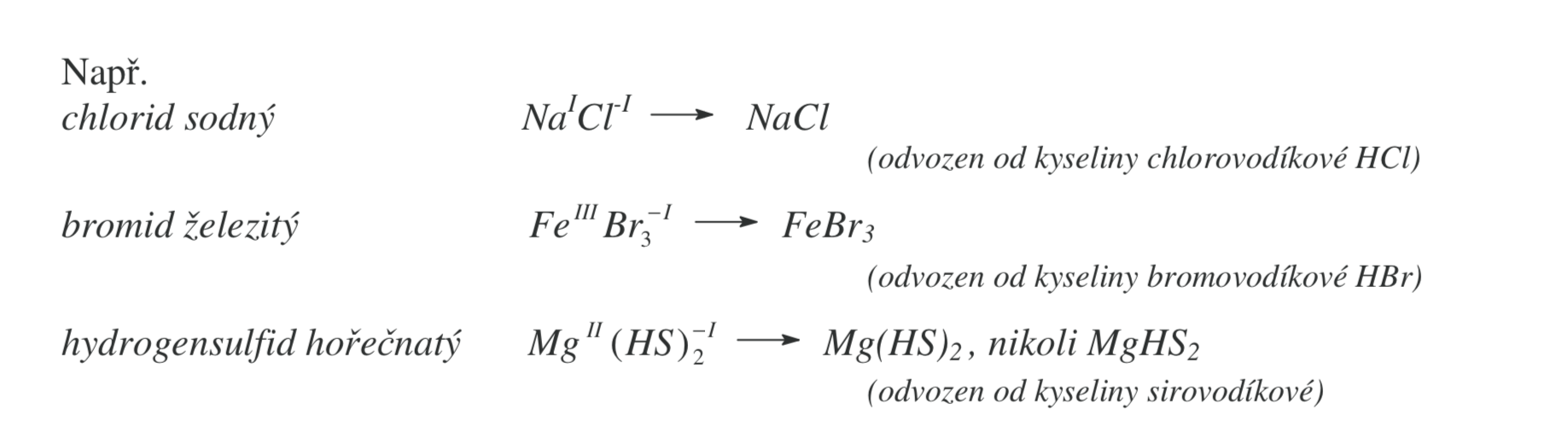 Soli kyslíkatých kyselin
Soli kyslíkatých kyselin
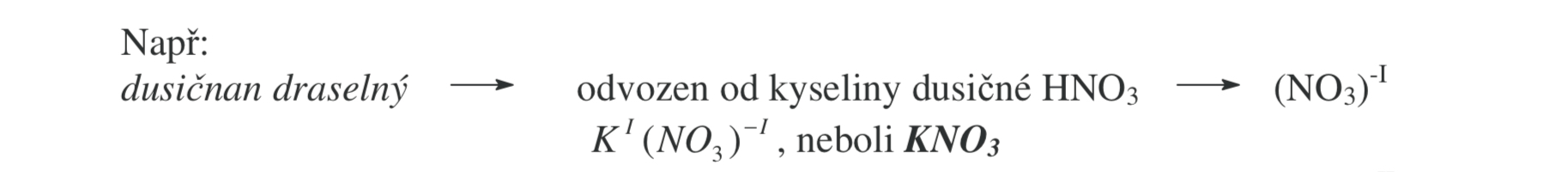
 Hydrogensoli
Hydrogensoli
- vzniká, pokud nejsou nahrazeny všechny vodíky
- Počet nenahrazených vodíků je vyjádřen před slovem hydrogen (dihydrogen, tetrahydrogen,…)
#  Hydráty
Hydráty
- Soli obsahující vázané molekuly vody
 Podvojné soli
Podvojné soli
- Obsahují dva anionty nebo dva kationty
- Kationty se řadí podle vzrůstající hodnoty oxidačního čísla
- Anionty se řadí abecedně