Kemi - sanoma
Kapitel 4
Materiens uppbyggnad
Sammanlagt innehåll
|
|---|
Atomens inre • Sid 164 - 167
Atommodellen
Allt är uppbyggt av atomer, atomer består av olika delar. Dessa är protoner (+), elektroner (-) och neutroner (neutrala). Protonerna är positivt laddade och ligger i atomkärnan tillsammans med neutronerna som är neutrala. Runt om atomkärnan finns det elektronskal, där finns även elektronerna som är negativt laddade. Atomnumret berättar hur många protoner det finns i atomkärnan. Kol har till exempel atomnummer 6 vilket betyder att det har 6 protoner i atomkärnan. Eftersom en atom är oladdad vet vi att det alltid finns lika antal elektroner och neutroner som protoner. Därför anger även atomnumret hur många elektroner det finns sammanlagt.
Det var Niels Bohr som presenterade denna atommodellen. Enligt hans modell ligger elektronskalen i bestämd avstånd från atomkärnan. K-skalet ligger närmast atomkärnan och efter det kommer skalen L, M, N osv. Elektronerna lägger sig i skalet som är närmast atomkärnan om den har plats. Det närmsta elektronskalet kan bara ha 2 elektroner medan de andra kan ha upp till 8 elektroner var. Eftersom det yttersta skalet bara kan hålla 8 elektroner, kallas det för ett fullt ytterskal/att den har ädelgasstruktur när den gör det.
Elektronerna i det yttersta skalet kallas valenselektroner. Det är antalet valenselektroner som ger ett grundämne dess egenskaper. Atomer med fulla ytterskal är stabila, de har ädelgasstruktur. Detta strävar alla atomer efter att bli. De kan uppnå detta genom att antingen ta emot eller ge bort elektroner beroende på hur många valenselektroner det finns. Atomer med flera valenselektroner tar emot elektroner från andra ämnen medan vissa men färre skickar bort sina elektroner. När en atom skickar iväg elektroner blir den till en positivt laddad jon eftersom de har fler protoner än elektroner. Om atomen istället tar emot elektroner omvandlas den till en negativt laddad jon då den har fler elektroner än protoner.
Atommassa
Atomer är väldigt små, men trots det finns det olika metoder för att räkna ut vad en atom väger. Atomer väger självklart väldigt lite och därför är det opraktiskt att väga det i kg, därför finns det en speciell enhet för atommassan, u. U kommer från enheten unit (engelska) som betyder enhet på svenska. Protoner och neutroner har samma massa, 1U. Elektronens massa är så liten att den inte ens går att räkna ut. 99.9% av atomens massa finns i kärnan där neutronerna och protonerna ligger. T.ex. en väteatom har atomnumret 1, den består alltså bara av en proton och har därför vikten 1U. En heliumatom (atomnummer 2) väger 4U, eftersom den har två protoner och därav två neutroner. En litiumatom med tre protoner och 4 neutroner väger då 7U. 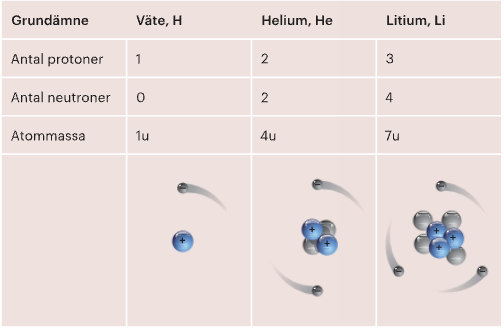
Isotoper
Det är antalet protoner i atomen som bestämmer vilket grundämnet är. I ett grundämne har alla atomer samma antal protoner, fast antalet neutroner kan variera. Dessa är alltså olika varianter av samma grundämne och kallas för isotoper, de är samma grundämne fast de har olika atommassa.
Grundämnet väte finns i 3 olika isotoper. Vanligt väte är den vanligaste isotopen och har inga neutroner, den kan även kallas för protium. Deuterium/tungt väte har en proton och en neutron. Deuterium väger alltså dubbelt så mycket som vanligt vete, dvs. 2U. Tritium/super tungt väte har en proton och tre neutroner och väger därför tre gånger så mycket som vanligt väte, 3U.
Periodiska systemet • 168 - 174
I det periodiska systemet sorteras ämnena utifrån antalet protoner.
Periodiska systemet visar ämnenas egenskaper
År 1869 uppfann Dimitrij Mendelejev periodiska systemet. Under denna tid hade man bara upptäckt 63 olika grundämnen. Han hade suttit och antecknat varenda grundämne på en enskild liten lapp och sorterade dem efter deras atommassa. Sedan dess har det periodiska systemet utvecklats mycket, idag känner vi till över 100 olika.
Alla grundämnen finns i periodiska systemet
Periodiska systemet är en karta över alla grundämnen som vi känner till. Grundämnena är sorterade i vågräta rader efter deras atomnummer, det vill säga antalet protoner. En oladdad atom har lika många protoner och elektroner, alltså anger atomnumret även det.
Elektronerna är fördelade i flera elektronskal, när det första fylls hamnar elektronerna i nästa osv. Atomer med lika antal elektronskal hamnar i samma rad i periodiska system. Alltså hamnar atomer med lika många valenselektroner under varandra (lodrätt).
Perioder och grupper
Det periodiska systemet är uppbyggt av perioder och grupper. Vågräta rader kallas perioder, i period 1 finns väte o helium som båda endast har ett elektronskal. Ämnet längst till vänster har alltid en enda valenselektron, och ämnet längst till höger har alltid fullt ytterskal. I period 2 finns åtta grundämnen, och alla de har två elektronskal. Periodens nummer anger alltså hur många elektronskal grundämnena har.
Lodräta kolumner kallas grupper. Grundämnena i en grupp har samma antal valenselektroner. Undantaget är helium som har två, med de övriga ämnen i grupp 18 har 8 valenselektroner. Antalet valenselektroner har stor betydelse för ämnenas egenskaper och alla grundämnen i en grupp har därför liknande egenskaper, de bildar en grundämnesfamilj.
Massantalt ger antal protoner och neutroner
Bortsett från protonerna finns även neutroner i atomkärnan. Protonerna och neutronerna är de tyngre partiklarna i atomen, därför är atommassan ett ungefär mått på hur många protoner och atomer det finns. Atommassan är sällan ett heltal, det beror på att det finns varianter av samma grundämne med olika antal neutroner (isotoper). Atommassan är medelvärdet av de olika isotoperna.
Exempel
Natriums atommassa är 22,99. Nästan alla natriumatomer har 11 protoner och 12 neutroner, det blir 23 kärnpartiklar. Men ett litet antal natriumatomer har 11 protoner och 11 neutroner, alltså bara 22 kärnpartiklar. Därför är atommassan lite mindre än 23.
Metaller och icke-metaller
Grundämnena delas upp i två huvudgrupper: metaller och icke-metaller
De flesta metaller har 1-3 valenselektroner och lämnar därför ifrån sina elektroner vid kemiska reaktioner. Metallerna finns till vänster i det periodiska systemet.
Icke-metaller tar upp elektroner då de oftast har 4 - 6 valenselektroner. Icke-metallerna ligger till höger av periodiska system, men undantag för väte.
Vissa få grundämnen har både metalliska och icke-metalliska egenskaper. De kallas halvmetaller och finns på gränsen mellan de två huvudgrupperna.
Alkalimetaller
Alkalimetallerna är grupp 1. De innehåller grundämnen med en valenselektron. I deras grupp finns, förutom väte, sex mjuka metaller som kallas alkalimetaller. De reagerar lätt med andra ämnen som till exempel syre och vatten. Vid reaktioner lämnar alkalimetallerna ifrån sig en elektron och får på så sätt fullt ytterskal. De vanligaste alkalimetallerna är litium, natrium och kalium. Alkalimetaller är metaller men går inte att använda till vardagsföremål eller byggnader, de är för mjuka och reagerar väldigt lätt med andra ämnen.
Halogener
Halogener är grupp 17, de har 7 valenselektroner. Eftersom de saknar en elektron för att få fullt ytterskal, reagerar de lätt med metaller som lämnar ifrån elektroner. Halogener finns ofta i salter, till exempel koksalt, natriumklorid, som båda bildas när halogenen klor reagerar med alkalimetallen natrium.
Ädelgaser
Grupp 18 är ädelgaser, de har antingen 2 eller 8 valenselektroner vilket innebär att de har fully ytterskal
(→ deltar därför inte i kemiska reaktioner). När övriga grundämnen reagerar och får ett fullt ytterskal, säger man att de har fått ädelgasstruktur. Ädelgaser används bland annat i belysning och ballonger.
Övergångsmetaller
Grupp 3 - 12 är övergångsmetaller. De är tunga metaller med höga smält- och kokpunkter. De har hög hållfasthet + bra mekaniska egenskaper. Det beror på att det finns starka bindingar mellan atomerna, förutom kvicksilver (Hg) som är flytande.
Övergångsmetaller används främst för att tillverka bilar,båtar, flygplan, byggnadskonstruktioner, ledningar, möbler och verktyg. De används nästan överallt.
Joner • 175 - 179
Atomer bildar joner
Atomer har alltid lika många protoner och elektroner, därför anses de oladdade. Men i en jon finns det olika antal protoner och elektroner, och är därmed laddade partiklar.
Atomer bildar joner eftersom de strävar efter ädelgasstruktur. I det periodiska systemet är det främst ämnena längst till vänster och ämnena längst till höger (bortsett från ädelgaserna) som bildar joner.
Metallerna till vänster i det periodiska systemet lämnar ifrån sig och bildar positiva joner (fler protoner än elektroner). Icke-metallerna längst till höger tar upp elektroner och bildar då negativa joner (fler elektroner än protoner). Väte är ett undantag då det är en icke-metall som bildar positiva joner.
Metaller bildar positiva joner
Atomer med få elektroner i sitt yttersta skal skickar enkelt iväg elektronerna. Detta gör grupperna till vänster i det periodiska systemet, eftersom då blir skalet innanför fullt, sedan det yttersta. Då bildas positiva joner eftersom det finns fler protoner än elektroner.
Atomerna i grupp 1 har en valenselektron i det yttersta skalet, därför lämnar de ifrån sig den för att uppnå ädelgasstruktur. Detta gör att grundämnet blir en positiv jon med laddningen 1+. Om en natriumjon (atomnummer 11) hade skickat iväg en elektron för att få fullt ytterskal, hade det bara funnits 10 elektroner och 11 protoner kvar. Laddningen skrivs då som 1⁺, vilket blir Na⁺.
Atomerna i grupp 2 har två valenselektroner som skickas bort, detta innebär att laddning blir 2+. Detta betyder att metallerna som t.ex beryllium och magnesium bildar Be²⁺ och Mg²⁺.
Atomerna i grupp 3 har tre valenselektroner i deras yttersta skal, genom att ge iväg dem så bildas joner med laddning 3+. T.ex aluminium ingår i grupp 3 och bildar aluminiumjoner, Al³⁺.
Negativa joner
Atomer med många valenselektroner kan istället ta upp elektroner för att uppnå ädelgasstruktur. Detta är vad ämnena längst till höger, vid ädelgaserna gör. de bildar alltså negativa joner genom att ta emot elektroner (fler elektroner än protoner).
Atomer i grupp 17 fyller på sitt yttersta skal då de bara saknar en valenselektron. Den nya elektronen gör att jonladdning blir 1-. Fluor och Klor bildar alltså F⁻ och Cl⁻.
Atomerna i grupp 16 fyller på med 2 valenselektroner för att uppnå ädelgasstruktur. Atomerna syre, O, och svavel, S, bildar O²⁻ och S²⁻. Men i grupp 16 finns både icke-metaller och metaller, vilket reagerar annorlunda och därför gäller inte denna regel hela vägen. Icke-metallerna fyller alltså på med elektroner medan metallerna avger dem för att uppnå ädelgasstruktur.
Positiva och negativa joner bildas samtidigt
Elektroner finns ju inte bara sådär, utan de är alltid bundna till atomer. Detta innebär att när en atom avger en elektron, måste det finnas en annan som tar upp den. Därför bildas alltså både positiva och negativa joner samtidigt.
Kemiska bindningar • Sid 180 - 185
Atomer kan få ädelgasstruktur på flera sätt
Det finns 3 sätt för atomerna att uppnå ädelgasstruktur. Det första sättet är att ge bort eller ta emot valenselektroner så att atomer får ett fullt ytterskal (sker när jonen bildas). Det andra sättet är att atomen släpper iväg valenselektronerna så de inte längre är bundna till en enskild atom. Det tredje sättet är att två atomer “delar” på samma atomer så att de båda kan räkna dem som sina egna.
Dessa tre sätt leder alltid till en kemisk bindning mellan atomerna. Bindningen är en attraktionskraft mellan atomerna, de dras alltså mot varandra. Bildningen består inte av materia, utan bara energi.
Valenselektronerna deltar i kemiska reaktioner
Valenselektroner är de som deltar i kemiska reaktioner, detta beror på att de sitter längst ut och därför enklare kommer i kontakt med andra atomer. När atomerna ibland stöter ihop hjälper valenselektroner till att skapa nya bindningar som håller atomerna samman.
Valenselektroner hamnar på nya platser i ämnet som bildas efter en kemisk reaktion. De ingår även i de bindningar som inte fanns tidigare. Ämnenas egenskaper beror ju på valenselektronerna, därför får det nya ämnet ofta helt andra egenskaper än det som de är uppbyggda av. Detta förklarar till exempel varför socker inte har någon egenskap från kol, väte och syre, vilket är det de består av.
Den typen av bindning som skapas mellan de reagerande atomerna beror på vilka atomslag som är inblandade. Det finns alltså tre sätt för valenselektronerna att skapa starka bindningar.
Metall + icke-metall:
När en valenselektron hoppar från en atom till en annan. Metallatomerna bildar positiva joner då de ger bort elektronerna och icke-metallerna bildar negativa joner när de tar emot elektroner.
Positiva och negativa joner dras till varandra pga. deras motsatta laddning och då uppstår något, detta kallas jonbindning. Den kemiska föreningen kallas jonförening.
Jonföreningar kallas för salter och är väldigt vanliga. I salt är det samma mängd positiva laddningar som negativa laddningar, ingen elektron har tagits bort eller lagts till. Elektronen bara hoppar från en atom till en annan. Jonbindning är en stark kemisk bindning och därför har salter ofta hårda kristaller med höga smältpunkter.
Ex: Natrium + klor → Natriumklorid
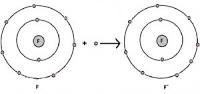
Metall + Metall:
Lättrörliga atomer som bildar ett “block” av hela metallstycken (“vilse” atomer). I en bit metall sitter atomernas valenselektroner löst, de kan alltså röra sig fritt i hela metallbiten. Detta gäller både rena metaller och legeringar. Därför är metallatomerna “inbäddade” i ett moln, vilket skapar något som kallas metallbindning. Elektronmolnet är liksom lim som håller ihop metallerna.
Att valenselektronerna rör sig fritt i metallen gör även att de är bra på att leda elektrisk ström och värme. Därför är alla metaller bra ledare. Denna rörlighet bidrar även till att metallerna reflekterar ljus (har metallglans).
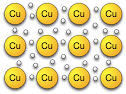
Icke-metall + icke-metall:
En valenselektron från varje atom “delar” på elektronerna vilket kopplar ihop atomerna. Eftersom icke-metallerna vill ta upp elektronerna kan ämnena inte binda med jon- eller metallbindning. De får alltså samsas om elektroner vilket bildar en molekylbindning. Två elektroner, en från varje atom skapar ett elektronpar som blir gemensamt för atomerna, de båda räknar det som sina egna.
Denna bindning kan kallas molekylbindning, elektronparbindning och kovalent bindning.
Två elektroner som ingår i en molekylbindning brukar ritas som ett streck mellan atomerna, H-H. Om det är en dubbelbindning har man två streck och om man har en trippelbindning så är det tre streck.
Ex: Väte + väte → Vätgas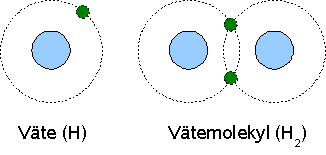
Salter är uppbyggda av joner • Sid 232 - 239
Salter är fasta ämnen som bildar kristaller
Det finns flera slags salt än koksalt, till exempel marmor, salmiak, gips och krita. Salter har olika egenskaper och används till olika saker, från bakning till gödsel.
Men det alla salter har gemensamt är att de är fasta ämnen som bildar kristaller. Detta beror på att de är uppbyggda av joner i jonbindningar. Jonbindningar är en stark bindning vilket gör att salter har hög smältpunkt. Vanligt koksalt måste värmas till ca 801ºC.
Salter kan bildas på fler sätt
Salter kan bildas på flera sätt, men det är alltid positiva och negativa joner som reagerar med varandra. Detta betyder att det finns lika många plusladdningar som minusladdningar, därför är salt alltid oladdat, även fast det består av elektriskt laddade joner.
Kopparsulfat är en salt med blågröna kristaller. Saltet är uppbyggt av kopparjoner, Cu²⁺ och negativa sulfatjoner SO₄²⁻.
Om man blandar en syra och en bas, naturaliseras alltid ämnet och det bildas salt. I en lösning av syra och vatten finns det positiva vätejoner och negativa joner. Vad de negativa jonerna är beror på vilken syra det är.
Saltsyra HCl ger negativa kloridjoner Cl⁻
Svavelsyra H₂SO₄ ger negativa sulfatjoner SO₃²⁻
Salpetersyra HNO₃ ger negativa nitratjoner NO₃⁻
Kolsyra H₂CO₃ ger negativa karbonatjoner CO₃²⁻
Dessa negativa syror ovan är de negativa joner från syran som bildar salter tillsammans med de positiva jonerna från basen. Salters namn bestäms utifrån de joner som ingått. Man börjar alltid namnet med den positiva jonen och slutar med den negativa jonen: t.ex kopparsulfat.
Salter kan bildas på flera sätt. Man kan t.ex lägga en bit zink i saltsyra, då löses zinken och det bildas zinkjoner samtidigt som saltsyran sönderdelas och bildar negativa kloridjoner + vätgas. Zinkjonerna och kloridjonerna bildar sedan jonföreningen zinkklorid (=salt).
Ett salt kan också bildas när en metalloxid reagerar med en syra. Detta kan ske t.ex när kopparoxid reagerar med svavelsyra (=kopparsulfat).
Salter kan alltså bildas på tre sätt:
- Vid neutralisation
- När en metall löses i syra
- När en metalloxid löses i syra
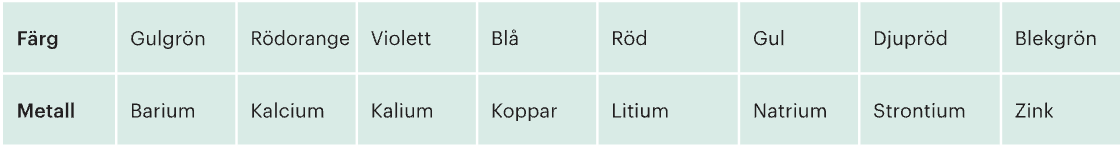
Metallsalter används i fyrverkerier
I fyrverkerier finns metallsalter, det är bl.a metalljonerna i saltet som skapar färgerna i fyrverkerierna. Färgen påverkas av många faktorer, men om man värmer metallsalter i en låga kan det skapas olika färger.
Natriumklorid - vanligt koksalt
Vanligt salt som används till matlagning har det kemiska namnet natriumklorid och består av natriumjoner och kloridjoner.
Koksalt finns förutom i mat, även i havet. För att framställa vanligt salt kan man fånga upp havsvatten i bassänger och låta resten av vattnet avdunsta. Saltet som då blir kvar innehåller inte bara natriumjoner, men även joner av magnesium, kalium och kalcium. När sådant salt säljs kallas det havssalt. Det natriumet som finns i koksalt är nödvändigt för vår kropp, men ökad konsumtion kan leda till hälsorisker, till exempel högt blodtryck.
Koksalt används även på vägar efter att det har snöat, detta beror på att en blandning av vatten och koksalt har lägre fryspunkt än vanligt vatten.
Kalciumjoner bildar olika salter
Även fast kalk finns i flera former, innehåller alla former alltid kalciumjoner. Kalciumkarbonat är ett salt som i huvudsak består av kalk, krita och marmor. Dessa bergarter kan såklart se olika ut beroende på vilka andra mineraler som ingår. Marmor används bland annat som byggnadssten för att framställa cement.
I skelettet finns kalciumfosfat. Kalciumfosfat innehåller precis som kalciumkarbonat, kalciumjoner vilket gör skelettet hårt o vitt.
Gips består av kalciumsulfat och är även salt. När man gipsar till exempel en bruten arm dränker man gipsbindor i gips och vatten. När detta sen torkar blir gipset hårt vilket gör att armen hålls stilla tills den har läkt.
Vatten löser många salter
De flesta salter är lättlösliga i vatten, detta beror på att vattenmolekylerna har en positiv och negativt laddad sida. Syreatomen i en vattenmolekyl drar alltså till sig elektronerna från de båda väteatomerna, inte tillräckligt för att det ska bildas joner. Men tillräckligt mycket för att vattenmolekylen ska få en negativ sida vid syreatom och en positiv sida vid väteatomerna.
Därför är vatten bra på att lösa salter, olika laddningar dras ju till varandra och de negativa och positiva delarna från saltet drar i sig till de negativa och de positiva delarna i vattnet. Alltså bryts jonbindningen.
Detta fenomen har en stor betydelse för livet på jorden. Vatten kan alltså transportera salt till växterna och näringsämnen i kroppen. Havet som livet uppstod i, had en salthalt på ca. 3,5% och fostervattnet man utvecklas i hade 2%.
Mineraler bygger upp vår jord
Jorden är uppbyggd av en stor mängd mineraler som kemiskt sett är salter. Dessa bildar tillsammans bergarter. Flera salter är lättlösta i vatten, men inte alla. Annars hade vi inte haft någon mark att gå på.
Mineralerna som bygger upp berg & sten är salter, fast de är mer svårlösliga i vatten. Men även om de är svårlösliga, kan de genom tusentals år börja lösa, detta kan bero på starka vindar, vatten eller temperaturförändringar. Det kan även ha lösts upp kemiskt. Vattnet som faller som regn över berg och stenar är surt. Det reagerar sedan med berget vilket gör att det sker en kemisk vittring.
Salter har speciella egenskaper
Salt i fast form kan inte leda ström eftersom alla joner sitter fast i kristallen och inte kan flytta på sig. Däremot så kan en saltlösning leda ström då jonerna rör sig.
Salt i smält form kan också leda ström, men detta är ovanligt eftersom det kräver en väldigt hög temperatur för att få salt i smält form.
Salt kan användas som reagens
Salter kan även bilda fällningar. Om man doppar en lösning som innehåller silverjoner i en koksaltlösning så grumlas blandningen av ett vitt ämne. Efter ett tag kommer det vita falla till botten. Silverjonerna Ag⁺ har bildat ett svårlösligt salt med kloridjonerna Cl⁻ → det har bildats en fällning. Fällningen består då av AgCl. Man kan alltså använda silverjoner för att få reda på om det finns kloridjoner i en lösning. Silverjoner är en reagens på kloridjoner.
När metaller reagerar med syre, inträffar en kemisk process som kallas oxidation. I det här fallet avger metallen sina valenselektroner till syremolekylerna. Detta resulterar i bildandet av positiva metalljoner och negativa syrejoner. Dessa joner binds sedan tillsammans för att bilda en kemisk förening som kallas metalloxid.
För att ta ett exempel, låt oss titta på reaktionen mellan järn och syre:
\[ 4Fe + 3O_2 \rightarrow 2Fe_2O_3 \]
- #O
Här reagerar järn (Fe) med syre (O₂) för att bilda järnoxid (Fe₂O₃). Varje järnatom förlorar elektroner och blir till järnjoner (Fe³⁺), medan syremolekylerna får elektroner och blir till syrejoner (O²⁻). Dessa joner binds sedan samman för att bilda järnoxiden.
Denna process är vanligtvis vad vi ser när metaller rostar eller oxiderar när de utsätts för syre i luften under lång tid.
När metaller reagerar med syre för att bilda metalloxider, bildas vanligtvis en typ av kemisk bindning som kallas jonbindning.
I en jonbindning avger en atom valenselektroner för att bilda positiva joner (katjoner), medan en annan atom tar emot dessa elektroner för att bilda negativa joner (an joner). I fallet med metall-oxid-reaktioner, avger metallen valenselektroner för att bilda positiva joner, medan syret tar emot dessa elektroner för att bilda negativa joner. Dessa positiva och negativa joner attraherar varandra och bildar starka bindningar som håller samman föreningen, vilket resulterar i en jonbindning.