Präanalytik und Untersuchungsmaterialien
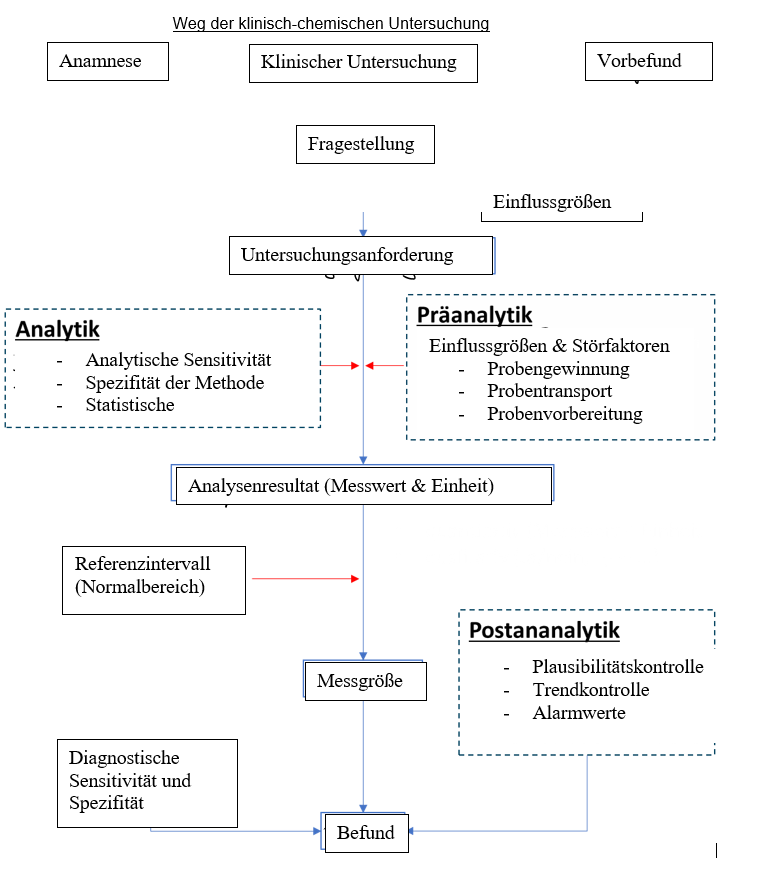
Präanalytische Phase
- Ärztliche Fragestellung
- Testauswahl
- Laboranforderung
- Patientenidentifikation
- Probenentnahme
- Transport
- Untersuchungsmaterial/-identifikation
- Probenannahme/-beurteilung
- Probenaufbereitung
- Probenaliquotierung
\
Einflussgrößen/Störfaktoren/Einflussfaktoren
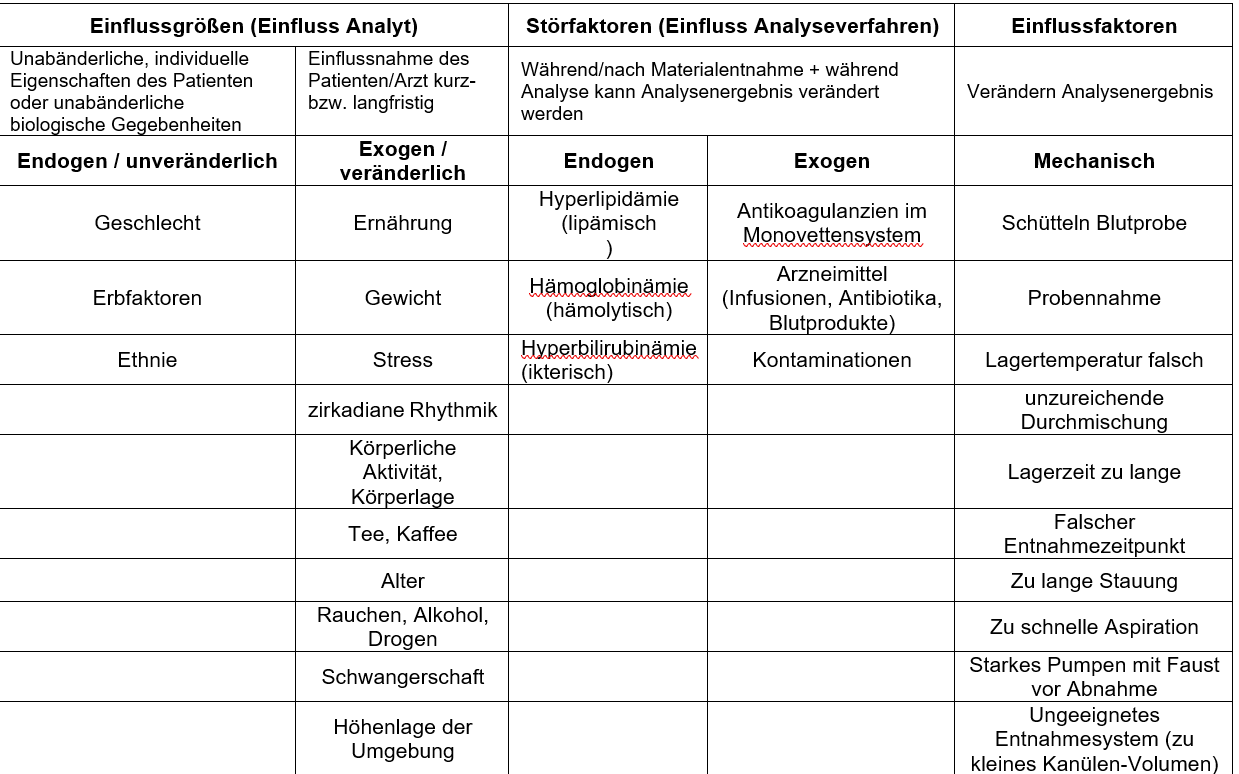
Einflussgrößen
- können Laborbefund verfälschen
- führen in vivo zu Veränderung der Konzentration/Aktivität /Beschaffenheit des Analyten in Probe
- unabhängig vom Analysenverfahren
- unterschieden werden:
* unveränderliche, unbeeinflussbare Einflussgrößen •
* Geschlecht - Creatinkinase (bei Männern höher aufgrund höherer Muskelmasse)
* Erbfaktoren - Personen mit Blutgruppe 0 = niedrigeren von Willebrand-Faktor
* Ethnie - Schwarzafrikaner haben signifikant niedrigere Leukozytenanzahlen
* veränderliche, beeinflussbare Einflussgrößen
* Ernährung - vegetarische Ernährung kann zu Abnahme von Creatin führen, wenn Eigensynthese nicht mehr ausreicht
* Alkohol - 2-4h nach Konsum Erhöhung von Harnsäure und Lactat, Glukose ist erniedrigt
* diagnostische Maßnahmen - intramuskuläre Injektion erhöht Creatinkinase- und Myoglobinwert
Störfaktoren
- Sind immer auf Analytik bezogen
- endogene Störfaktoren können physikalisch-chemischen Eigenschaften einer Probe beeinflussen und führen zu Messergebnis, das nicht der in vivo-Konzentration entspricht
- unterschieden werden:
\
a) körpereigene Störfaktoren (endogen)
hämolytische Proben:
- Erythrozyten wurden zerstört und Hämoglobin ist ausgetreten
- weitere Stoffe treten aus: Kalium, Transaminasen, Laktatdehydrogenasen
→ führen zu verfälschten Untersuchungsergebnissen durch:
- Einfluss der Stoffe auf Nachweisreaktionen
- Stoffe nehmen selbst an Reaktion teil und führen zu falsch positiven Ergebnissen
- Ursachen hämolytischer Proben:
* Alterung der Erythrozyten, hämolytische Anämie
* Thermische oder osmotische Schädigung
* Toxine (z.B. Arsen, Überdosierung Vit. K bei Neugeborenen)
* Parasiten, bakterielle Toxine
* Mechanische Überbeanspruchung (z.B. künstliche Herzklappen)
\
ikterische Proben:
- Ikterus: Gelbsucht
- abnorme Erhöhung des Bilirubins
- Bilirubin = Abbauprodukt des Hämoglobins
- bewirkt in pathologischer Konzentration eine dunkelgelbe - braune Verfärbung von Körperflüssigkeiten/Haut
- Interferenzen durch optische Veränderung der Probe bei verschiedenen Messverfahren
- Ursachen ikterischer Proben:
* prähepatisch z.B. Transfusionszwischenfälle
* intrahepatisch z.B. Leberschäden
* posthepatisch z.B. Abflussbehinderungen
\
lipämische Proben:
- weißliche Trübung des Blutserum bzw. -plasmas verursacht durch Fette
- Interferenzen bei optischen Messungen
- negativer Effekt auf Affinität von Antikörpern, wichtig bei Antigen-Antikörper-Reaktionen
\
- Ursachen lipämischer Proben:
* Fettstoffwechselstörungen
* Nahrungsaufnahme
* Blutentnahme an nicht nüchternen Patienten
\
b) Körperfremde Störfaktoren
- Infusionen
- Antikoagulanzien im Monovettensystem
- Kontaminationen (z.B. Bakterien, Pilze)
\
Einflussfaktoren
- beeinflussen Analysenergebnis
a) mechanisch:
- zu lange Stauung
- Starkes Pumpen vor der Abnahme
- Zu schnelles aspirieren
- Schütteln
b) Probennahme
- Ungeeignete Entnahmesysteme (Kanülenvolumen zu gering)
- Falscher Entnahmezeitpunkt
- Unzureichende Durchmischung
- Kontamination
c) Lagerung
- Falsche Temperatur
- Zu lange Lagerzeit
\
\
- Blut
- Gewebe und Organe
- Urin
- Abstriche
- Stuhl
- Liquor
\
\
| Untersuchungsmaterial | Serum | Plasma | Plasma | Plasma | Plasma | Plasma |
|---|---|---|---|---|---|---|
| Zusätze | keine | EDTA | Citrat | Heparin (Lithium) | Heparin (NH+) | Natriumfluorid |
| Farbe | weiß/braun | rot/lila | grün | orange | blau | gelb |
| Untersuchungen | klinisch-chemischimmunologischinfektionsserologisch | BBDiff (Blutausstrich)HbA1cBG | allg. Gerinnungsparameter (PTT, Quick, Fibrogen, D-Dimere) | z.B. Metallanalytik | Glukosebestimmung | |
| Wirkung der Zusätze | ||||||
| Hinweis |
\
\
Untersuchungsmaterialien
- Blut
- Gewebe und Organe
- Urin
- Abstriche
- Stuhl
- Liquor
Urin
| Gewinnungsart | Zeitpunkt | Geeignet für | Ungeeignet für |
|---|---|---|---|
| Mittelstrahlurin | 1.Morgenurin | Bakteriologie, Teststreifen, (Sediment), chem. Nachweise | |
| 2.Morgenurin | Teststreifen, Sediment, Glukose, Proteine, chem. Nachweise, Hormone | Nitrit | |
| Postprandial (2h nach KH-reicher Mahlzeit) | Glukose | Bakterien, Sediment | |
| Spontanurin | Notfallnachweise, Toxikologie | Bakterien, Sediment | |
| Sammelurin | Definierte Sammelperiode | Chem. Bestimmungen, Hormone | |
| Blasenpunktions- /Katheterurin | Bakteriologie, Teststreifen, Sediment, chemische Nachweise |
Mittelstrahlurin:
- Sammeln des Urins in sterilem Gefäß
- Erste & letzte Fraktion verwerfen
- Harnstrahl darf nicht unterbrochen werden
24h-Sammelurin
- Sammeln des Urins in entsprechenden Sammelbehälter
- Sammlung beginnt nach 1. Morgenurin & endet nach 1.Morgenurin
- Eliminierung tageszeitlicher Schwankungen einzelner Parameter
- Für mikrobiologische Untersuchungen ungeeignet
Blasenkatheterurin:
- Entnahme direkt aus Blase durch Katheter
- Erste 200 ml verwerfen
- Vorwiegend mikrobiologische Fragestellung
Blasenpunktionsurin:
- Nach 24 Uhr Blase nicht entleeren
- Morgens 0,5 l Tee trinken
- 2-3h später suprapubische Blasenpunktion
- Für mikrobiologische Fragestelllungen
Urintauchkulturen:
- nach Gewinnung der Probe wird Nährboden vollständig mit Probe bedeckt
- überflüssigen Urin abfließen lassen
- für mikrobiologische Fragestellungen
\
Blut
Vollblut
- enthält korpuskuläre (Erythrozyten, Leukozyten, Thrombozyten) und flüssige Bestandteile
- → Vollblut = Blutzellen + Serum + Gerinnungsfaktoren
\
Plasma
- Vollblut + Antikoagulanzien
- gerinnt nach der Abnahme nicht
- durch Zentrifugation werden zelluläre Bestandteile von dem flüssigen Überstand getrennt
- → Plasma = zellfreier, flüssiger Bestandteil des Vollblutes inkl. Gerinnungsfaktoren
\
Serum
- Vollblut ohne Zusätze
- nachdem die Gerinnung abgeschlossen ist, wird das Serum durch Zentrifugation gewonnen
- Blutkuchen und flüssige Bestandteile werden separiert
- → Serum = zellfreier, flüssiger Bestandteil ohne Gerinnungsfaktoren
\
Vorteile Plasma:
- höhere Ausbeute
- Zeitgewinn
- keine Störung durch Nachgerinnung
- bessere Darstellung des in vivo-Status
\
Nachteile Plasma:
- Störungen durch Fibrinogen
- Störungen durch Antikoagulantien
- Kontamination durch Kationen
\
Abnahme erfolgt:
- Venös/arteriell oder kapillar
\
venöse Blutabnahme
Bedingungen:
- möglichst zwischen 7.00 – 9.00 Uhr
- nüchtern (12-14h Nahrungskarenz) à nicht immer erforderlich
- vor Blutabnahme 5-10 min ruhig sitzen/liegen
- veränderliche Einflussgrößen beachten
- bei Medikamenteneinnahme im Tal abnehmen
\
Technik:
- am liegenden Patienten empfohlen (bei Verlaufskontrolle gleiche Position)
- weitlumige Punktionskanülen
- Stauungszeit 30 Sekunden
- zu starke Aspiration vermeiden
\
keine Blutentnahme
- an geröteten. geschwollenen, infizierten Hautstellen
- in der Nähe von Ödemen
- an vernarbten Venen
- am Infusionsarm
- aus Katheter
\
Reihenfolge der Blutentnahme !
- Blutkulturen (Sterilität)
- Vollblut ohne Zusätze
- Citratblut für Gerinnungsuntersuchungen (wenn kein Serum gefordert, dann erste Fraktion verwerfen
- Heparinblut
- EDTA-Blut für hämatologische Untersuchungen
- Citratgepuffertes NaF für Glukose-, Laktat, Pyruvat
\
Stuhl
- bakterielle, virologische oder klinisch-chemische Untersuchung
- ungewöhnliche Beimengungen gezielt entnehmen
- haselnussgroße Menge
- Lagerung bei 4° um Vermehrung der Bakterien zu vermeiden
Liquor
- wichtig zur Diagnose von Erkrankungen des ZNS
- zeitgleich muss immer eine Serum-Monovette mit abgenommen werden →wichtig für die Beurteilung best. Parameter
- Polycarbonat- und Glasröhrchen sind wegen Adsorption von IgG ungeeignet
Monovettenarten
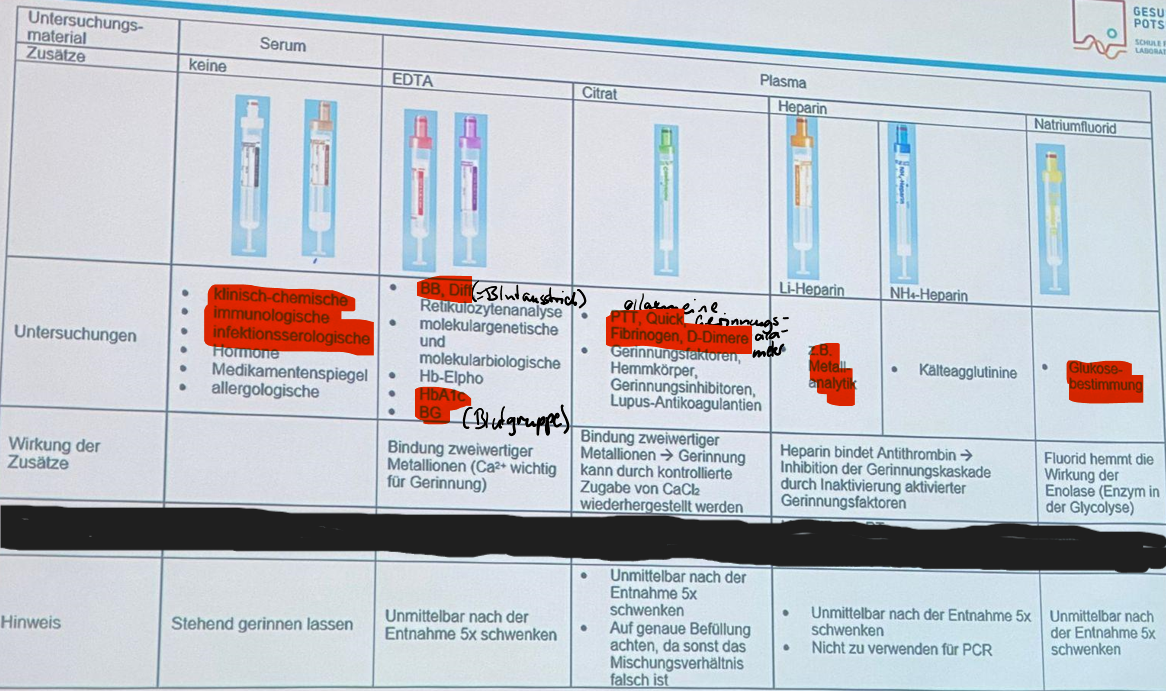
\