8. Metabolismo, respiración celular y fotosintesis (TANS)
8.1 Metabolismo El metabolismo es la suma de todas las reacciones químicas que ocurren en un sistema (por ejemplo, una célula o un organismo). Las enzimas son responsables de coordinar y controlar los procesos metabólicos.
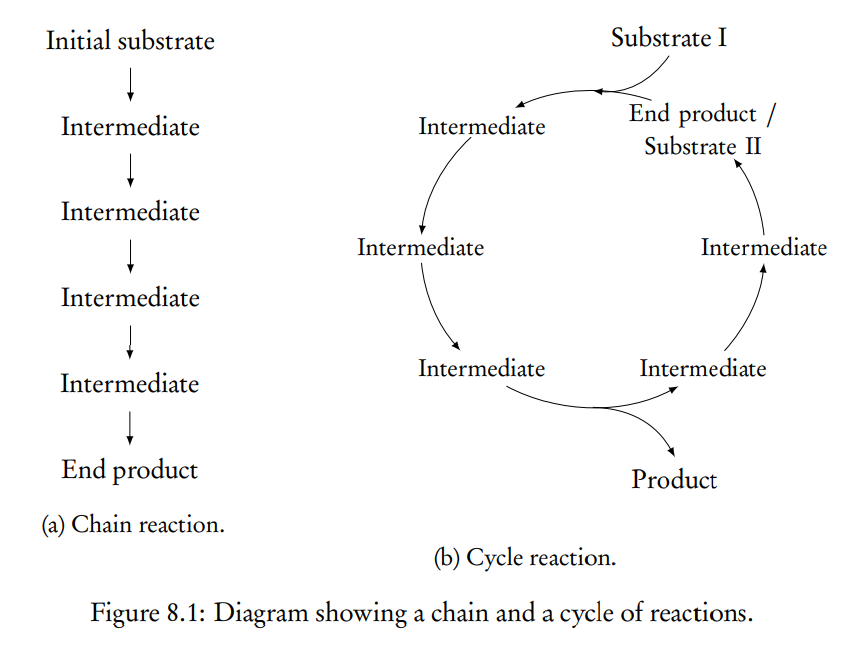
8.1.1 Vías metabólicas: cadenas y ciclos Varias vías metabólicas consisten en cadenas de reacciones (por ejemplo, la glucólisis), donde el sustrato inicial y el producto final no necesariamente interactúan o se parecen entre sí. Otras vías metabólicas consisten en ciclos de reacciones (por ejemplo, el ciclo de Krebs), donde un sustrato del ciclo se regenera constantemente a partir de otros intermediarios involucrados en el mismo ciclo. Muchas vías metabólicas incluyen ambos tipos de reacciones.
8.1.2 Enzimas y energía de activación de las reacciones El modo en que las enzimas catalizan y, por lo tanto, aceleran las reacciones es el siguiente: antes de que una molécula del reactivo pueda participar en la reacción, debe adquirir energía (también conocida como energía de activación), que ayuda a romper los enlaces moleculares dentro del reactivo. Cuando se forman nuevos enlaces tras la descomposición del reactivo, se libera energía (ver Figura 8.2).
Las enzimas reducen la energía de activación de las reacciones que catalizan debilitando los enlaces moleculares del reactivo, facilitando así que la reacción ocurra.
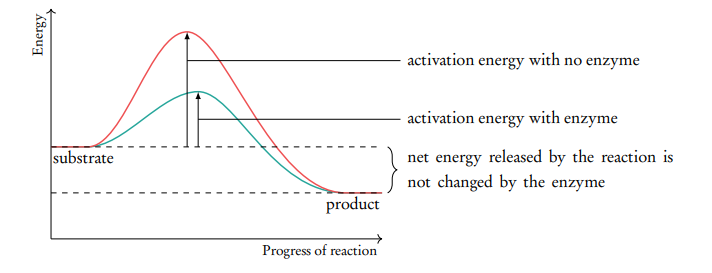
Figura 8.2: Gráfico que muestra la reducción en la energía de activación en presencia de enzimas, así como el hecho de que la energía liberada por la formación de nuevos enlaces permanece sin cambios. La reacción mostrada es exotérmica, lo que significa que libera más energía de la que requiere como energía de activación (lo opuesto sería una reacción endotérmica).
8.1.3 Inhibición competitiva vs. no competitiva Inhibición competitiva Un inhibidor competitivo compite directamente por el sitio activo de la enzima al unirse a él. Evita que el sustrato se una hasta que el inhibidor se disocia. El inhibidor debe tener una estructura molecular muy similar a la del sustrato para poder encajar en el sitio activo y unirse a él. La inhibición competitiva puede ser reversible o irreversible. Aumentar la concentración de sustrato generalmente puede reducir el efecto inhibidor, ya que el inhibidor es desplazado con mayor facilidad por las muchas moléculas de sustrato.
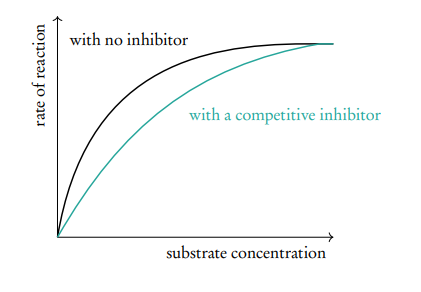
En el ciclo de Krebs, la succinato deshidrogenasa actúa sobre el sustrato succinato, eliminando un átomo de hidrógeno y convirtiéndolo en otro intermediario. El malonato actúa como un inhibidor competitivo, ralentizando de manera efectiva el ciclo de Krebs.
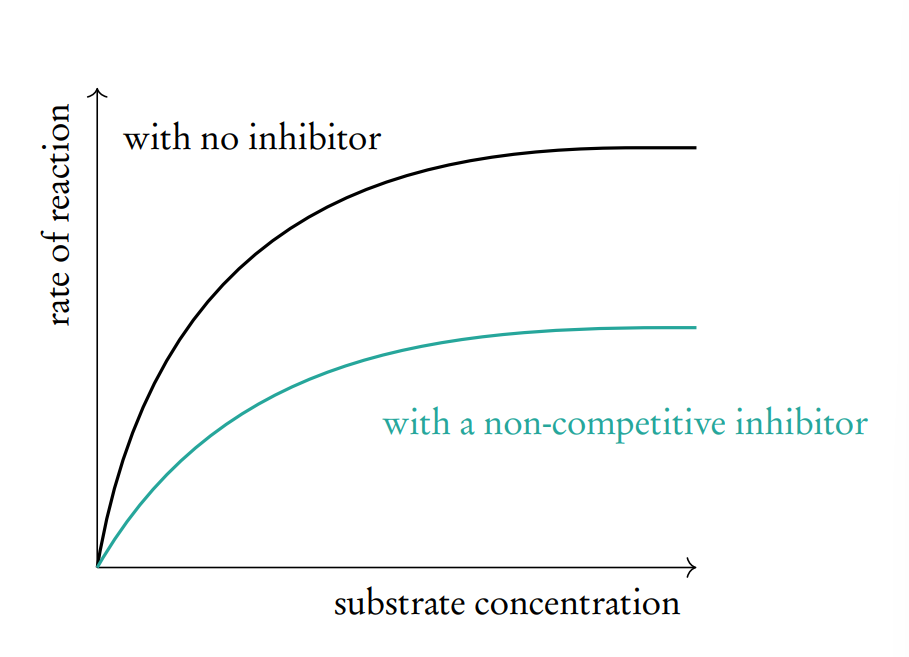
Inhibición no competitiva Un inhibidor no competitivo se une a la enzima en un sitio diferente al sitio activo (también conocido como sitio alostérico). La unión del inhibidor en el sitio alostérico provoca un cambio conformacional en la enzima (incluido el sitio activo), volviéndola no funcional y ralentizando la reacción. La inhibición no competitiva es usualmente, pero no siempre, reversible; sin embargo, a diferencia de la inhibición competitiva, aumentar la concentración de sustrato no reduce el efecto inhibidor (aunque haya más moléculas de sustrato, estas no pueden unirse al sitio activo no funcional).
El gas nervioso (Sarin) se une de manera alostérica a la enzima respiratoria acetilcolinesterasa, cambiando la forma del sitio activo de la enzima. El sustrato ya no puede unirse, y esta interrupción puede resultar en un bloqueo de la vía respiratoria, lo cual puede ser letal, ya que este proceso es irreversible.
8.1.4 Inhibición por el producto final La inhibición por el producto final, también llamada inhibición por retroalimentación, ocurre cuando el producto de la última reacción en una vía metabólica (cadena o ciclo) inhibe la enzima que cataliza la primera reacción. La enzima inhibida se llama enzima alostérica. Las enzimas alostéricas tienen tanto un sitio activo como un sitio alostérico. El producto final se une al sitio alostérico y cambia la forma del sitio activo, inhibiendo la enzima. Este proceso es reversible, por lo que cuando el producto final se desliga, la reacción continúa. Este es un método eficiente de controlar la tasa metabólica. Si la concentración del producto es demasiado alta, la inhibición por el producto final detiene la vía, produciendo menos desechos.
8.2 Respiración celular
8.2.1 Respiración celular: una reacción redox La respiración celular es la liberación controlada de energía, en forma de ATP, a partir de compuestos orgánicos en las células. La respiración celular es una reacción redox, que implica la oxidación y reducción de los transportadores de electrones NAD+ y FAD en diferentes etapas de este proceso metabólico. Los transportadores de electrones transfieren energía química a través de reacciones redox. La oxidación es la pérdida de electrones e hidrógeno, mientras que la reducción es la ganancia de electrones e hidrógeno.
8.2.2 Glucólisis: de la glucosa al piruvato
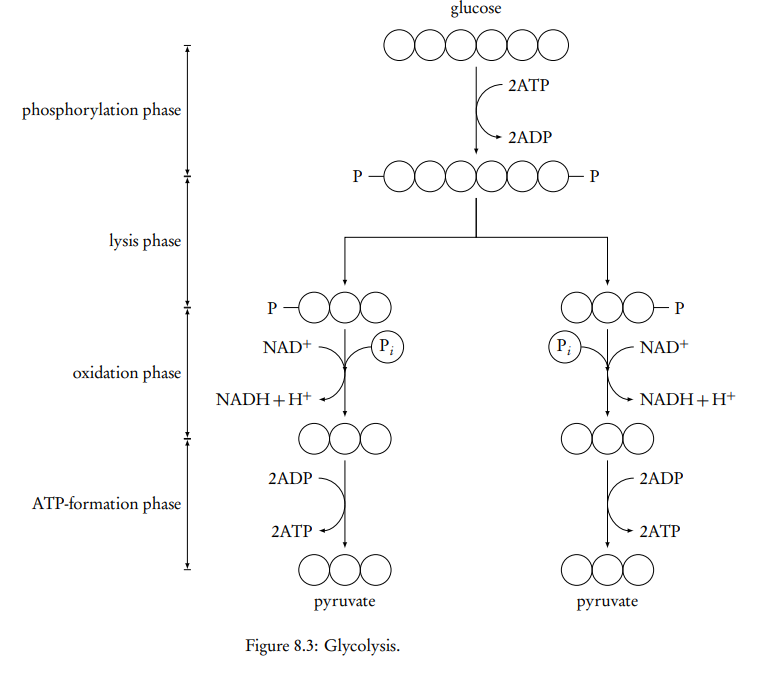
La glucólisis es una vía de reacciones en cadena catalizada por enzimas en el citoplasma de la célula que convierte una glucosa en dos piruvatos. No utiliza oxígeno, por lo que ocurre en la respiración celular aeróbica y anaeróbica (tanto en procariotas como en eucariotas). Se divide en cuatro fases principales:
Fase de activación/fosforilación
Se utilizan dos moléculas de ATP para comenzar la glucólisis. Un fosfato de cada ATP fosforila la molécula de glucosa para formar la molécula intermedia fructosa bifosfato.
Fase de lisis
Este intermedio de 6 carbonos se divide en dos azúcares de 3 carbonos, cada uno con un grupo fosfato, ya que es muy inestable.
Fase de oxidación
Se eliminan dos átomos de hidrógeno por NAD+ de cada molécula de 3 carbonos (oxidación). La energía liberada por esta oxidación se utiliza para enlazar otro grupo fosfato libre a cada molécula de 3 carbonos. Los átomos de hidrógeno son transportados por un transportador de electrones (formando NADH + H+).
Fase de formación de ATP
El piruvato se forma eliminando dos grupos fosfato de cada molécula de 3 carbonos y fosforilando ADP (produciendo 4 moléculas de ATP). Dado que inicialmente se utilizaron 2 ATP en la fase de activación, la glucólisis produce los siguientes productos netos:
2 × ATP
2 × piruvato
2 × NADH + H+
8.2.3 Reacción de enlace y ciclo de Krebs: respiración celular aeróbica
Si el oxígeno está disponible para la célula, las moléculas de piruvato pasan por la reacción de enlace y el ciclo de Krebs para generar una cantidad mucho mayor de ATP. A continuación, se describen ambos procesos.
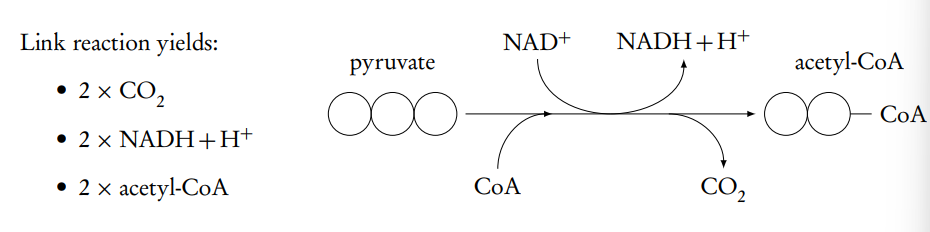
Reacción de enlace
El piruvato entra en la matriz de la mitocondria mediante transporte activo. En la matriz, cada piruvato pasa por los siguientes pasos:
Oxidación por NAD+
Descarboxilación
Unión con coenzima A (CoA) para formar acetil-CoA
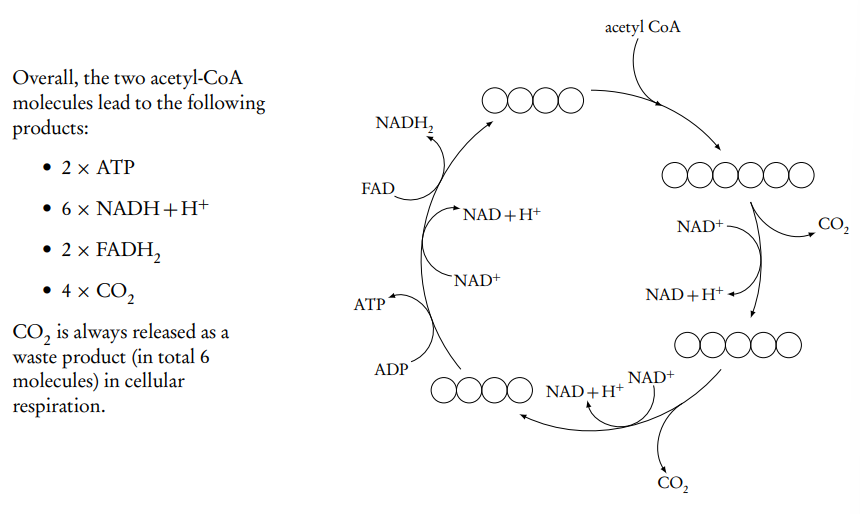
Ciclo de Krebs
Ocurre en la matriz de la mitocondria.
El acetil-CoA se combina con un compuesto de 4 carbonos, formando un intermedio de 6 carbonos (todos los productos mencionados a continuación se duplican, ya que entran dos moléculas de acetil-CoA en el ciclo).
El intermedio de 6 carbonos sufre una descarboxilación oxidativa, resultando en una molécula de 5 carbonos, CO2 y NADH + H+.
Otra descarboxilación oxidativa ocurre, resultando en una molécula de 4 carbonos, CO2 y NADH + H+.
El intermedio de 4 carbonos sufre una fosforilación a nivel de sustrato, liberando un grupo fosfato para fosforilar una molécula de ADP. El intermedio resultante es luego oxidado, esta vez por FAD → FADH2.
La molécula de 4 carbonos resultante es la misma que el intermedio inicial que se combina con el acetil-CoA al inicio del ciclo.
8.2.4 Cadena de transporte de electrones y quimiósmosis: producción de ATP
Mediante la glucólisis y el ciclo de Krebs, se producen varios transportadores de electrones ricos en energía. NADH + H+ y FADH2 son responsables de transportar hidrógeno y electrones (ricos en energía) desde la matriz mitocondrial hacia la membrana interna de la mitocondria. NAD+ permite la producción de 3 moléculas de ATP y FAD la producción de 2 moléculas de ATP al ingresar a la cadena de transporte de electrones. A continuación, se describe los eventos que tienen lugar en la membrana interna de la mitocondria, que conducen al mayor rendimiento de ATP: la cadena de transporte de electrones y la quimiósmosis.
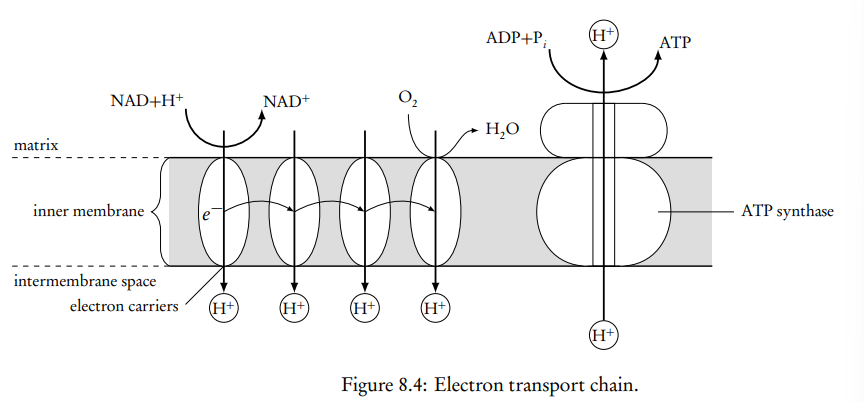
Cadena de transporte de electrones y quimiósmosis:
Los transportadores de electrones están ubicados en la membrana interna de la mitocondria, cada uno puede recibir electrones en diferentes niveles de energía.
NADH + H+ y FADH2 se oxidan, liberando electrones a los transportadores y H+ en la matriz.
Los electrones "saltan" de un transportador a otro, y cada salto libera algo de energía a medida que el electrón pasa a una posición energéticamente más favorable.
La energía liberada permite que los iones de hidrógeno en la matriz sean bombeados al pequeño espacio intermembrana, contra su gradiente de concentración.
Al final de la cadena de transportadores, los electrones desenergizados regresan a la matriz y se unen con oxígeno e hidrógeno, formando agua como producto de desecho.
En el espacio intermembrana, los iones de hidrógeno se acumulan en alta concentración. Esto crea tanto un gradiente químico de hidrógenos (alto en el espacio intermembrana y bajo en la matriz) como un gradiente eléctrico (más positivo en el espacio intermembrana y más negativo en la matriz), formando así el gradiente electroquímico.
La ATP sintasa es una enzima que se encuentra incrustada en la membrana interna de la mitocondria. Con el gradiente electroquímico de H+ apuntando hacia la matriz, los iones H+ ingresan naturalmente en la ATP sintasa. Cuando esto sucede, la enzima puede usar la energía liberada por los H+ al entrar en un estado más favorable energéticamente (yendo a la matriz) para unir ADP con Pi y formar ATP. Con los transportadores de electrones cargados generados a partir de una molécula de glucosa, la ATP sintasa tiene suficiente energía para generar una gran cantidad de moléculas de ATP, entre 36 y 38.
8.2.5 Mitocondria: Respiracion célular
Las mitocondrias son comúnmente conocidas como la "central energética" de la célula. Este orgánulo es donde ocurren la reacción de enlace, el ciclo de Krebs, la cadena de transporte de electrones y la quimiósmosis, lo que lo convierte en esencial para proporcionar a la célula la energía necesaria para satisfacer sus demandas funcionales. La estructura de las mitocondrias es muy ventajosa para las diversas funciones que debe acomodar. La Figura 8.5 es un diagrama anotado:
Habilidad: Anotación de un diagrama de una mitocondria para indicar las adaptaciones a su función.
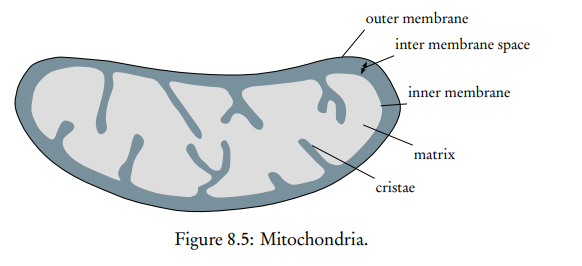
Figura 8.5: Mitocondrias.
Membrana externa: separa el contenido de la mitocondria del resto de la célula.
Membrana interna: contiene la cadena de transporte de electrones y la ATP sintasa, que llevan a cabo la fosforilación oxidativa.
Espacio intermembrana: este pequeño espacio entre las membranas mitocondriales permite la rápida acumulación de protones (H+) necesaria para que ocurra la quimiósmosis.
Crestas: regiones tubulares rodeadas de membranas que aumentan el área de superficie para la fosforilación oxidativa y la cadena de transporte de electrones.
Matriz: fluido interno similar al citosol que contiene las enzimas necesarias para el ciclo de Krebs y la reacción de enlace.
8.3 Fotosíntesis
La fotosíntesis es el proceso que utilizan las plantas para producir sus propias sustancias orgánicas (más comúnmente glucosa) utilizando la energía luminosa del Sol y sustancias orgánicas simples.
La fotosíntesis involucra múltiples reacciones que pueden categorizarse en dependientes de la luz e independientes de la luz. Las reacciones dependientes de la luz producen compuestos intermedios que se utilizan posteriormente en las reacciones independientes de la luz para producir "combustibles" orgánicos para la planta.
8.3.1 Cloroplastos: el sitio de la fotosíntesis
Los cloroplastos, orgánulos que son exclusivos de las células vegetales y de las algas eucariotas, son el lugar donde ocurren las reacciones de la fotosíntesis. Su estructura ha evolucionado para cumplir su función, como se puede ver en el diagrama anotado en la Figura 8.6.
Habilidad: Anotación de un diagrama de un cloroplasto para indicar las adaptaciones a su función.
Membrana externa
Membrana interna
Estroma (con ribosomas 70s)
Grana
Tilacoide
Lamela
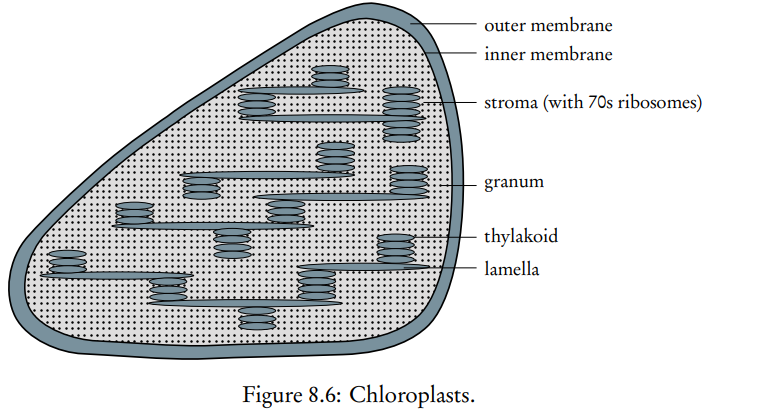
Figura 8.6: Cloroplastos.
Tilacoides: las pequeñas estructuras en forma de disco aumentan la superficie para la absorción de luz por los fotosistemas I y II.
Espacio tilacoide: el pequeño espacio dentro de los tilacoides permite una acumulación más rápida de protones para crear un gradiente electroquímico para la quimiósmosis.
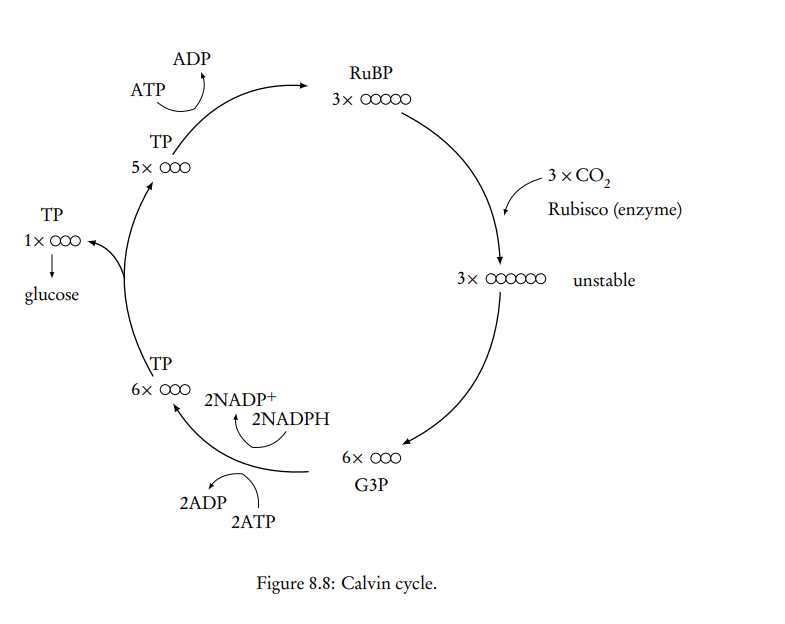
Estroma: sustancia similar al citosol donde se encuentran todas las enzimas necesarias para el ciclo de Calvin.
Doble membrana: aísla las partes funcionales de las enzimas dentro de los cloroplastos del citosol circundante.
Lamela: conecta los gránulos y aumenta aún más la superficie para la absorción de luz.
Quimiósmosis es el movimiento de iones a través de una membrana semipermeable, a lo largo de su gradiente electroquímico.
A través de la glucólisis y el ciclo de Krebs, se producen varios transportadores de electrones ricos en energía. NADH + H+ y FADH2 son responsables de transportar hidrógeno y electrones (ricos en energía) desde la matriz mitocondrial hacia la membrana interna de la mitocondria. NAD+ permite la producción de 3 moléculas de ATP y FAD la producción de 2 moléculas de ATP al ingresar a la cadena de transporte de electrones. A continuación, se describe los eventos que tienen lugar en la membrana interna de la mitocondria, que conducen al mayor rendimiento de ATP: la cadena de transporte de electrones y la quimiósmosis.
Cadena de transporte de electrones y quimiósmosis
Los transportadores de electrones están ubicados en la membrana interna de la mitocondria, cada uno puede recibir electrones en diferentes niveles de energía.
NADH + H+ y FADH2 se oxidan, liberando electrones a los transportadores y H+ en la matriz.
Los electrones "saltan" de un transportador a otro, y cada salto libera algo de energía a medida que el electrón pasa a una posición energéticamente más favorable.
La energía liberada permite que los iones de hidrógeno en la matriz sean bombeados al pequeño espacio intermembrana, contra su gradiente de concentración.
Al final de la cadena de transportadores, los electrones desenergizados regresan a la matriz y se unen con oxígeno e hidrógeno, formando agua como producto de desecho.
En el espacio intermembrana, los iones de hidrógeno se acumulan en alta concentración. Esto crea tanto un gradiente químico de hidrógenos (alto en el espacio intermembrana y bajo en la matriz) como un gradiente eléctrico (más positivo en el espacio intermembrana y más negativo en la matriz), formando así el gradiente electroquímico.
La ATP sintasa es una enzima que se encuentra incrustada en la membrana interna de la mitocondria. Con el gradiente electroquímico de H+ apuntando hacia la matriz, los iones H+ ingresan naturalmente en la ATP sintasa. Cuando esto sucede, la enzima puede usar la energía liberada por los H+ al entrar en un estado más favorable energéticamente (yendo a la matriz) para unir ADP con Pi y formar ATP. Con los transportadores de electrones cargados generados a partir de una molécula de glucosa, la ATP sintasa tiene suficiente energía para generar una gran cantidad de moléculas de ATP, entre 36 y 38.