Idealni Plini - zapiski
Idealno in Realno Obnašanje Plinov
Tipi Enačb Stanja
Kakšen Termodinamski Sistem Obravnavamo?
Obravnavajo se preprosti, zaprti, enofazni in enosestavinski sistemi.
Termodinamsko stanje je opisano z dvema neodvisnima intenzivnima spremenljivkama.
Enačbe Stanja
Enačba stanja je termodinamska relacija, ki opisuje stanje snovi pri danih fizikalnih pogojih, kot so tlak, volumen, temperatura ali notranja energija.
Običajni Tipi Enačb Stanja
Prva enačba stanja:
Kalorični enačbi stanja: ,
Temperaturno-entropijske (Gibbsove) enačbe stanja: ,
Zakoni Obnašanja Idealnih Plinov
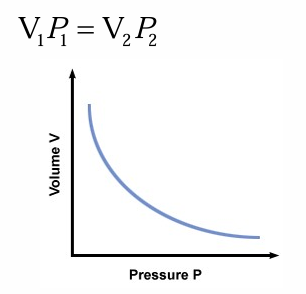
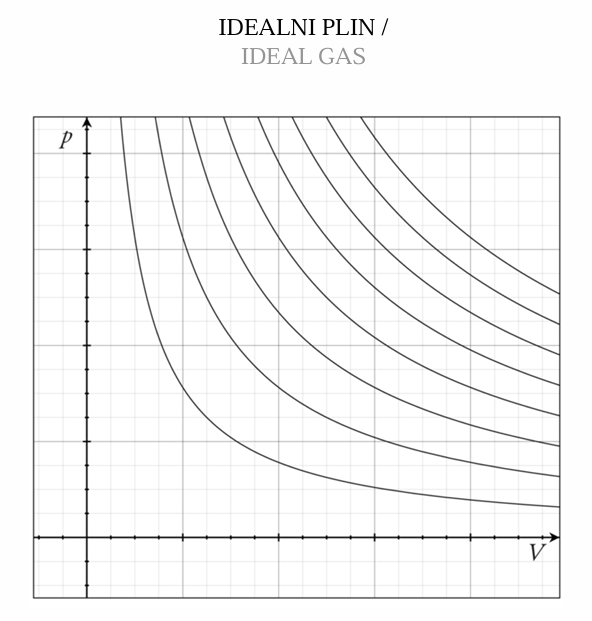
Robert Boylov zakon (1662): Volumen določene mase plina je obratno sorazmeren s tlakom pri konstantni temperaturi.
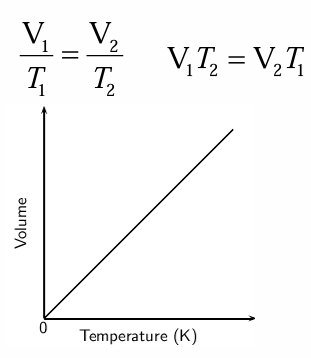
Jacques Charlesov zakon (1780): Volumen plina določene mase pri določenem tlaku je premo sorazmeren absolutni temperaturi plina.
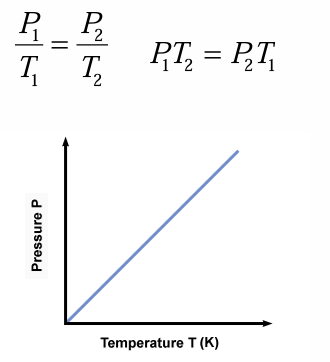
Joseph Louis Gay-Lussacov zakon (1800-1802): Tlak plina določene mase in volumna je premo sorazmeren absolutni temperaturi plina.
Amadeo Avogadrov zakon (1811): Enaki volumni vseh plinov pri enaki temperaturi in tlaku imajo enako število molekul.
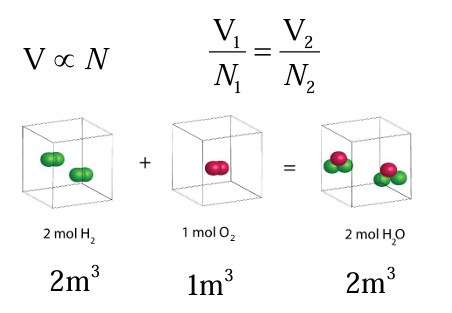
Splošna plinska enačba:
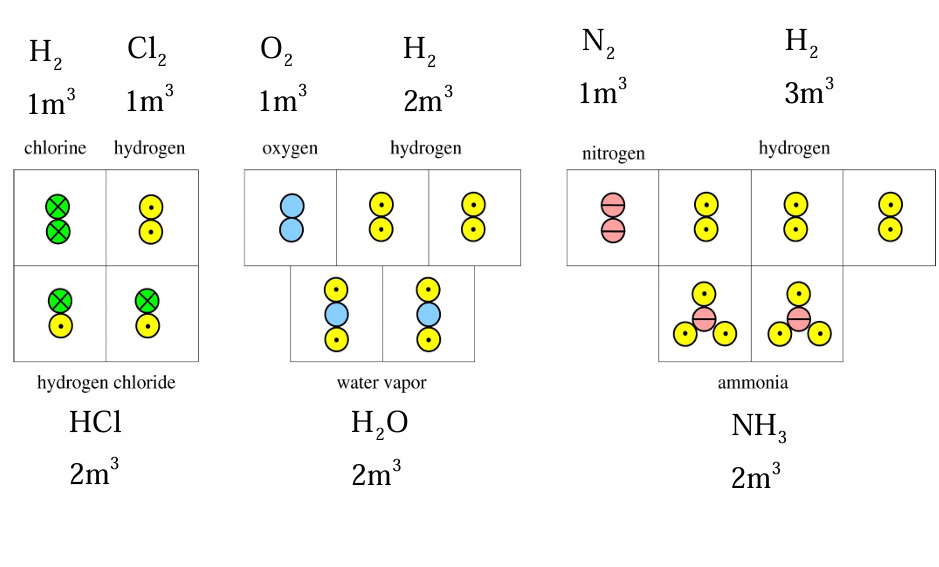
Izpeljava Splošne Plinske Enačbe
Spremembe glede na zakone idealnega obnašanja plinov:
Boyleov zakon:
Gay-Lussacov zakon:
Charlesov zakon:
Kombinacija idealnih plinskih zakonov:
Clapeyronova izpeljava iz empiričnih zakonov
Kombinacija Idealnih Plinskih Zakonov
R - specifična plinska konstanta
Nekatere vrednosti za R:
(vodna para):
He (helij):
(vodik):
Definicije Vseh Uporabnih Enačb Stanja Za Idealne Plina
Idealni plin je snov za katero velja spodnji izraz:
P - absolutni tlak
v - specifični volumen
R - specifična plinska konstanta
T - absolutna temperatura
- univerzalna plinska konstanta =
M - molska masa
Izrazi:
(gostota)
(število molov)
Izpeljava Enačbe Stanja Za Idealne Plina
Iz statistične termodinamike, s predpostavkami:
Molekule plina so točke brez volumna.
Molekule si izmenjujejo gibalno količino na podlagi idealnih trkov.
Kinetična energija je enakomerno razdeljena po vseh prostostnih stopnjah molekule.
Temperatura je sorazmerna s povprečno kinetično energijo molekul.
Enačba Stanja Realnega Plina
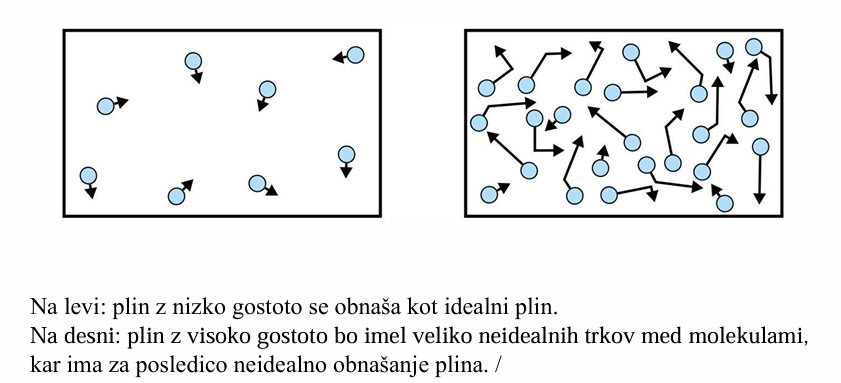
Plin z nizko gostoto se obnaša kot idealni plin.
Plin z visoko gostoto ima veliko neidealnih trkov med molekulami, kar povzroča neidealno obnašanje.
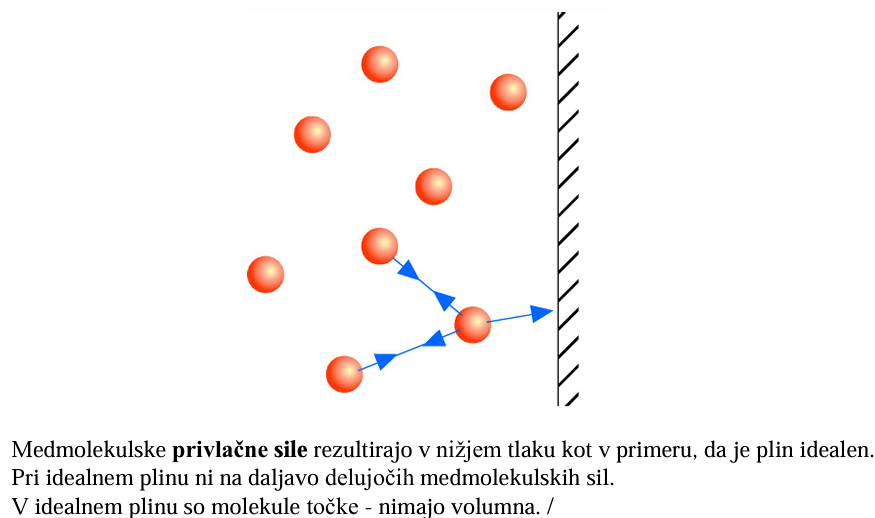
Medmolekulske privlačne sile povzročajo nižji tlak kot pri idealnem plinu.
V idealnem plinu ni medmolekulskih sil.
Molekule v idealnem plinu so točke - nimajo volumna.
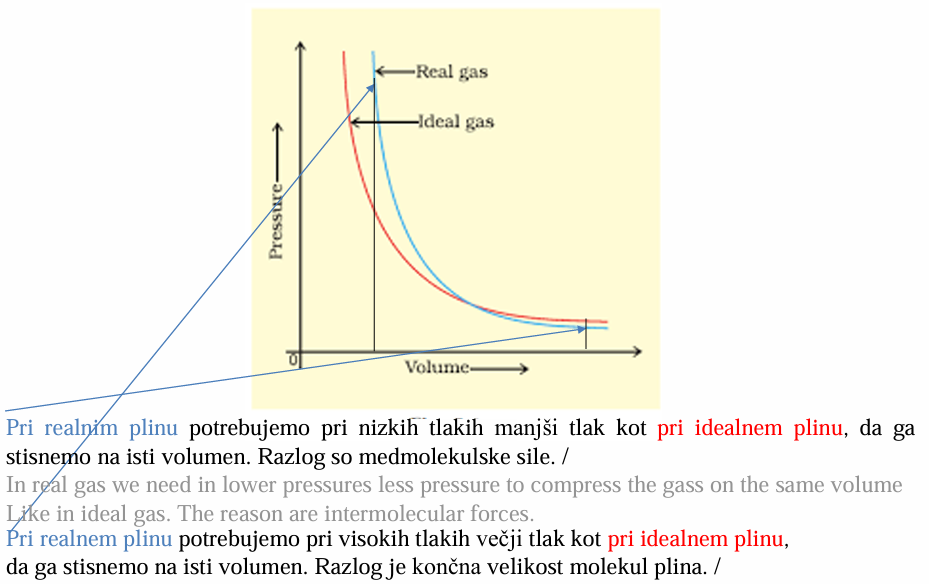
Pri realnem plinu potrebujemo pri visokih tlakih večji tlak kot pri idealnem plinu, da ga stisnemo na isti volumen zaradi končne velikosti molekul plina.
Pri realnem plinu potrebujemo pri nizkih tlakih manjši tlak kot pri idealnem plinu, da ga stisnemo na isti volumen zaradi medmolekulskih sil.
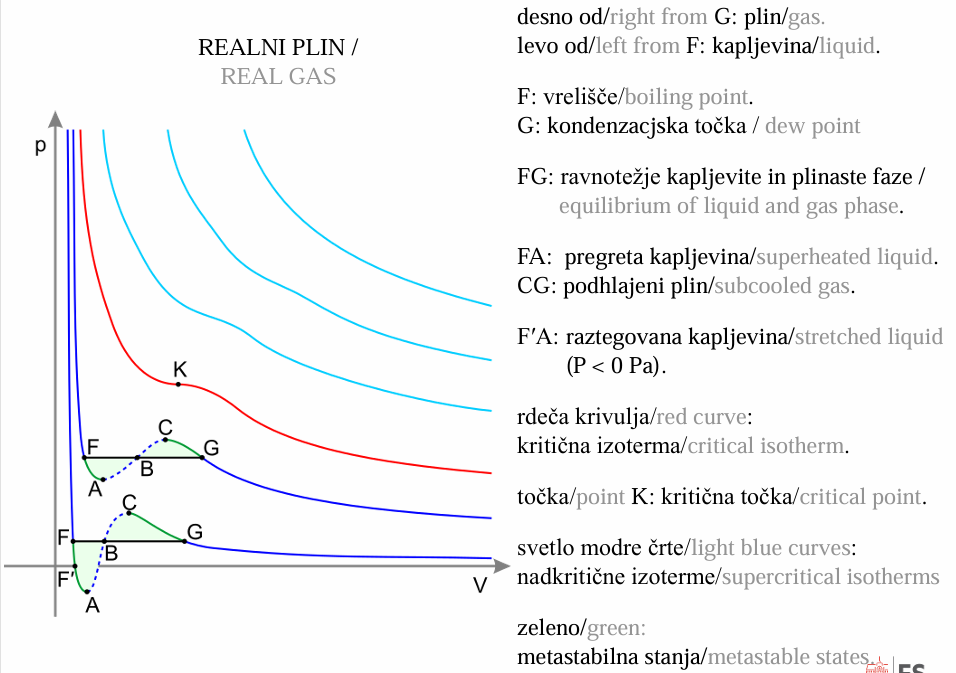
Realni Plin
Desno od G: plin
Levo od F: kapljevina
F: vrelišče
G: kondenzacijska točka
FG: ravnotežje kapljevite in plinaste faze
FA: pregreta kapljevina
CG: podhlajeni plin
F′A: raztegovana kapljevina
Rdeča krivulja: kritična izoterma
Točka K: kritična točka
Svetlo modre črte: nadkritične izoterme
Zeleno: metastabilna stanja
Debela črna pika označuje kritično točko v grafu P-v-T za propan. Pri temperaturah in tlakih nad kritično vrednostjo Tc in Pc kapljevite in plinaste faze ne razlikujemo.
Kritična točka je točka v P-v-T prostoru, definirana z najvišjo možno temperaturo in najvišjim možnim tlakom pri katerem lahko opazujemo kapljevito in plinasto fazo.
V kritični točki so vse snovne lastnosti plina enake vsem snovnim lastnosti kapljevine.
- kritična temperatura
- kritični tlak
- kritični specifični volumen
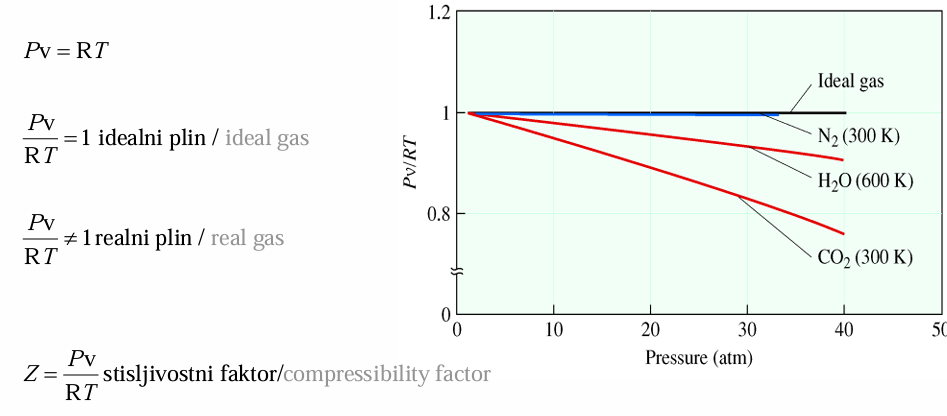
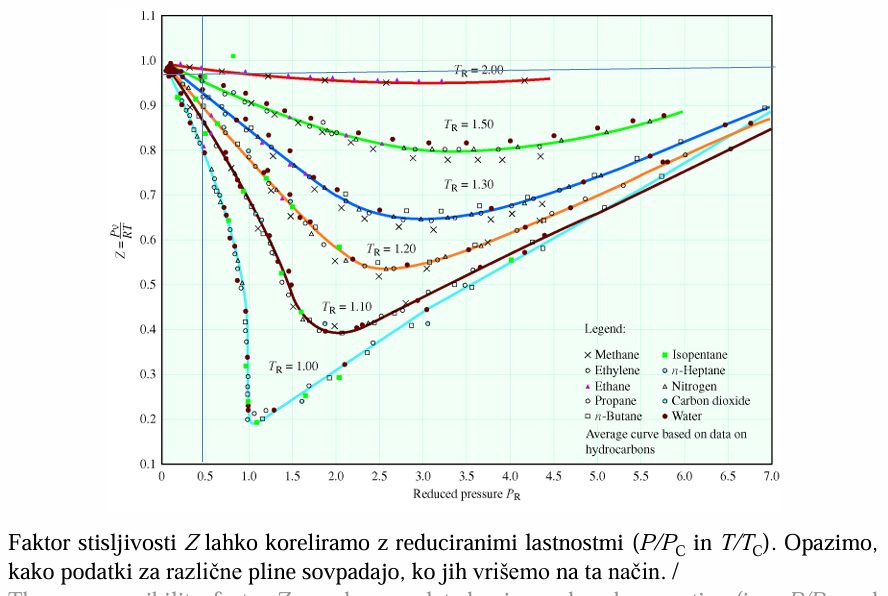
Odstopanja od vedenja idealnega plina se kažejo v odstopanju stisljivostnega faktorja od vrednosti 1.
idealen plin:
realni plin:
Stisljivostni faktor je odvisen samo od kritične temperature in tlaka.
Reducirane lastnosti plina: ,
Primer 3: Določanje stisljivostnega faktorja za kisik
Podatki: ,
,
,
(Iz grafa)
Veljavnost izračuna z idealnim plinom:
Če je lahko računamo z idealnim plinom!
Neidealno Obnašanje Plinov
Van der Waalsova enačba stanja:
Korekcija zaradi privlačnih sil.
Korekcija specifičnega volumna zaradi končnega volumna molekul.
Preurejena oblika: Koeficienti v van der Waalsovi enačbi stanja:
Druge Enačbe Stanja
Dieterici, Redlich-Kwong, Beatie-Bridgeman, Benedict-Webb-Rubin, Virial
Virusna oblika enačbe stanja:
Primer 4: Izračun tlaka pare
Podatki: ,
Izračun iz enačbe za idealni plin:
Izračun iz van der Waalsove enačbe: IzrazP = \frac{R T}{v} \rightarrow xy\alphaV = \frac{1}{V} (\frac{\partial V}{\partial T})P = \frac{1}{T}\betaT = - \frac{1}{V} (\frac{\partial V}{\partial P})T = \frac{1}{P}cV = (\frac{\partial u}{\partial T})VcP = (\frac{\partial h}{\partial T})PcV = \frac{3}{2}RcP = \frac{5}{2}RcV = \frac{5}{2}RcP = \frac{7}{2}RcV = 3RcP = 4R\gamma=\frac{Cp}{Cv}\gamma=1.667\gamma=1.4\gamma=1.33du = c_V dTdh = c_P dTdU = T dS - P dVdH = T dS + V dP\Delta S = \int{1}^{2} \frac{Cv}{T} \,dT + \int{1}^{2} \frac{R}{V}dV\Delta s = \int \frac{c dT}{T} + R ln(\frac{v2}{V1})T V^{\gamma-1}=const.P V^n = const.n = 1n = 0V = const.$$ ,n = +
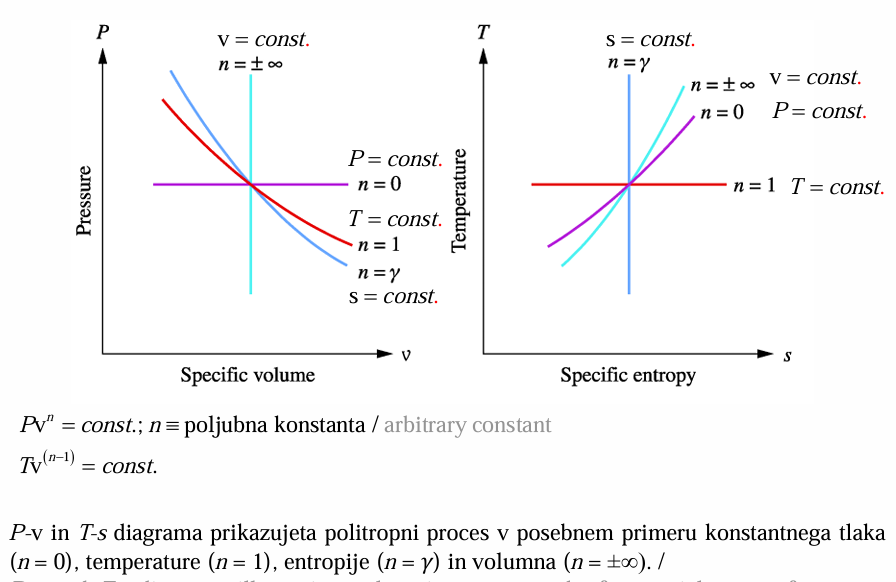
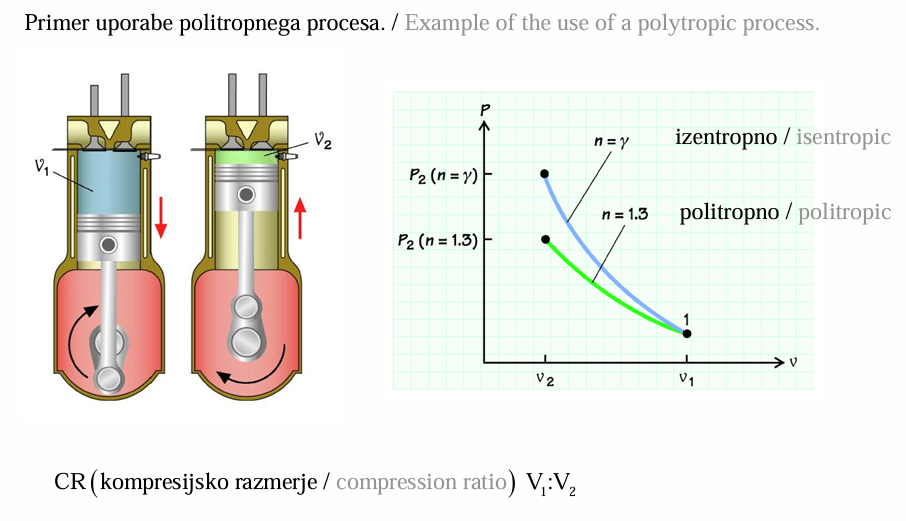
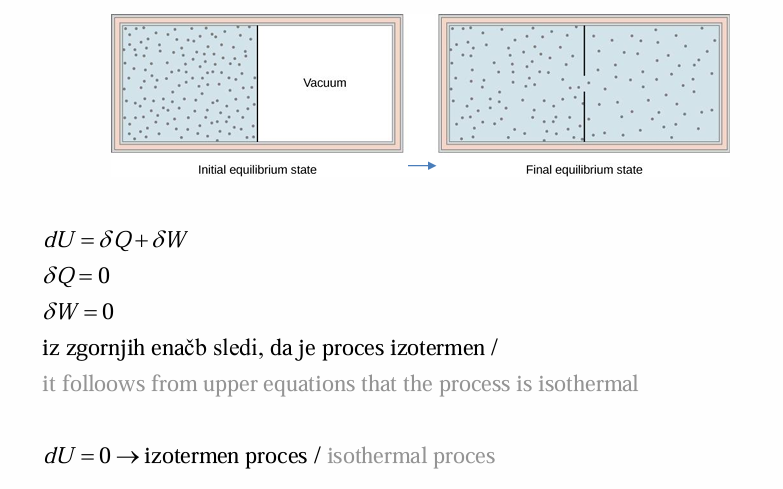
Ekspanzija Idealnega Plina V Prazen Prostor
Adiabatno raztezanje v prazen prostor je nepovračljiv proces, zato se entropija spreminja.
V this range of we K can c 1 alcu e la m te j daj velja: / w 0.95 Z .05 V t m ob oč u lahko računamo z idealnim plinom! / v p p i r th v ideal rimerih / i primer / : gas! in cases first case 0 R Z T Z
1 1