Азот и его соединения.
Общие свойства
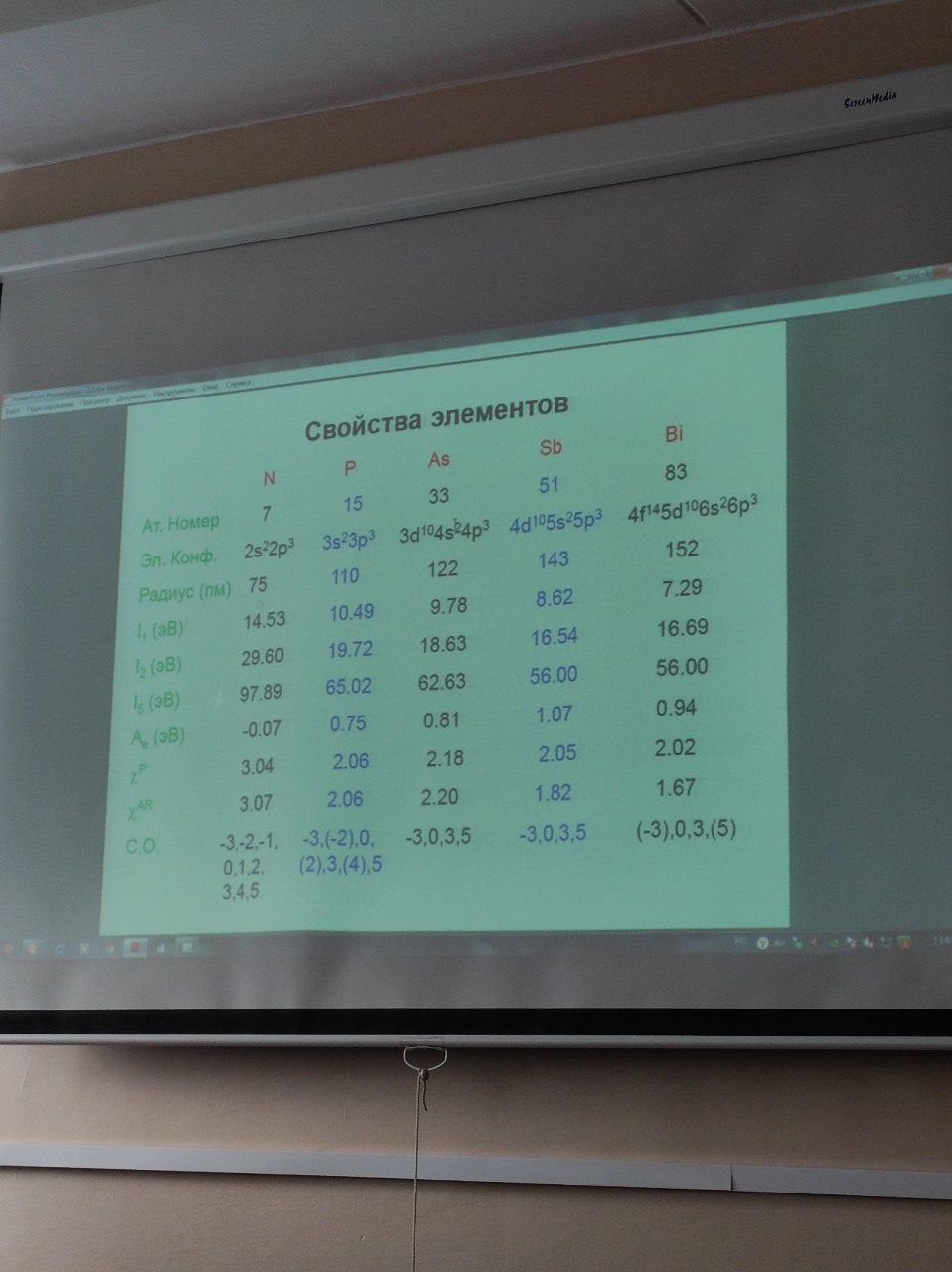
N: 1s2 2s2 p3
Характерные степени окисления: -3, 0, +1, +2, +3, +4, +5.
В природе он находится в свободном состоянии. Содержание азота в атмосфере 78%.
В связанном виде: NaNO3 – чилийская селитра.
В природе существует только два процесса получения связанного азота: это образование NO в грозовых разрядах и деятельность некоторых микроорганизмов.
Огромное народохозяйственное значение имеет проблема получения связанного азота. В настоящее время – это получение аммиака, из которого получают все другие соединения азота.
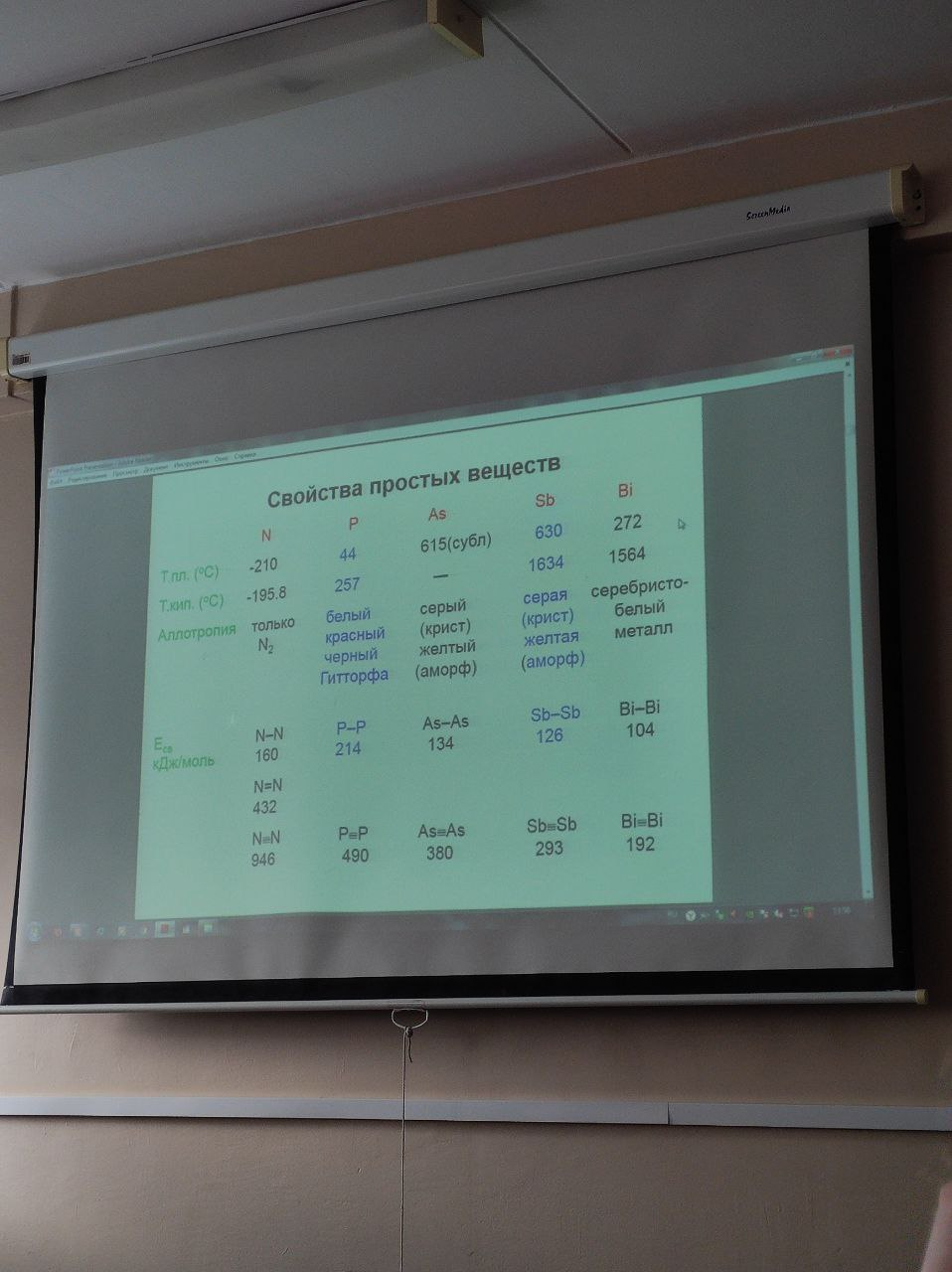
Азот – безцветный газ без вкуса и запаха. tкип = - 196С. Молекула азота – двухатомная, связь между атомами азота осуществляется тремя р-электронами: одна σ-связь и две π-связи. Есвязи= 941кДж/моль. Благодаря высокой энергии связи молекула очень прочная, поэтому азот так широко распространен в природе.
При стандартных условиях реагирует только с литием, при высокой температуре может реагировать со многими металлами.
3Mg + N2 = Mg3N2 (нитрид магния).
Электроотрицательность достаточно высокая: F > O > N.
В соединениях с фтором и кислородом проявляет положительную степень окисления.

Реакции:
С Ме при нагреве
3Mg + N2 = Mg3N2 (500C)
2Ti + N2 = 2TiN (800C)
2Al + N2 = 2AlN (900C)
N2+O2 = 2NO (разряд или 2000С)
Получение азота в лаборатории:
2NaN3 = 2Na + 3N2(t)
2NH4NO2 = N2 + 4H2O (t)
Применение:
Синтез аммиака
охлаждение
создание инертной атмосферы
охлаждение
Промышленное получение азота

Аммиак
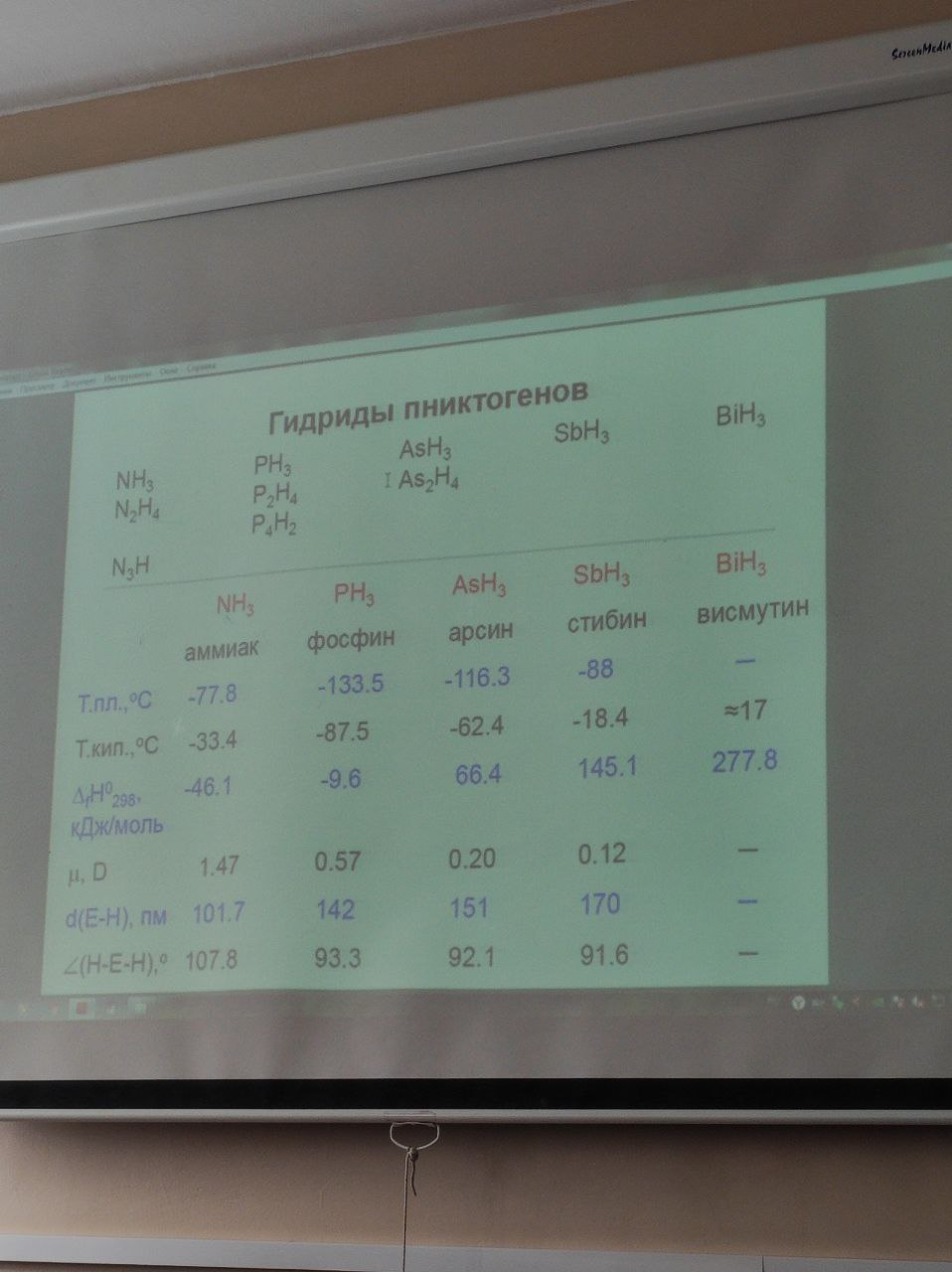
Аммиак – газ с неприятным резким запахом, хорошо растворим в воде.
tкип = -33 .
NH3 + H2O ↔ NH3*H2O – гидрат аммиака.
NH3·H2O ↔ NH4 + + OH-
Kосн. = 1,8*10-5 слабое основание.

Получение аммиака
Mg3N2 + 6H2O = 2NH3 + 3Mg(OH)2
2NH4Cl (тв) + Ca(OH)2 = 2NH3 + CaCl2 + 2H2O
KNO3 + 4Zn + 7KOH + 6H2O = NH3 + 2K2[Zn(OH)4]
Процесс Боша-Габера
N2 + 3H2 = 2NH3 (равновесие смещено влево)
Р - 200 атм для увеличения выхода
Т = 450C; кат Fe3O4 + Al2O3 + K2O + SiO2 для увеличения скорости
В отсутствие катализатора реакция идет очень медленно, катализатором является металлическое железо, промотированное оксидами алюминия и калия. Процесс обратимый, для смещения равновесия в сторону образования аммиака процесс ведут при повышенном давлении – 30 мПа. Прямая реакция – экзотермическая, поэтому значительное повышение температуры ведет к увеличению скорости обратного процесса, но при низкой температуре скорость прямой реакции тоже слишком низкая.
Направление окисления NH3 (В окислительно-восстановительных реакциях является восстановителем)
4NH3 + 5O2 = 4NO + 6H2O (кат Pt/Rh быстро)
4NH3 + 3O2 = 2N2 + 6H2O без катализатора
2NH3 + 2O2 =NH4NO3 + H2O (кат Pt/Rh медленно)
выбор условий: поток газов через катализатор.
Взаимодействие с кислотами с образованием солей аммония:
NH3 + HCl = NH4Cl (хлорид аммония)

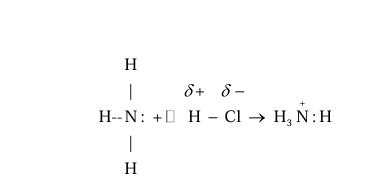
Ион аммония построен по типу донорно-акцепторной связи. Соли аммония при нагревании разлагаются:
NH4Cl = NH3 + HCl
NH4H2PO4 = NH3 + H3PO4
Если соль аммония, образована кислотой, в которой кислотный остаток является окислителем, то при нагревании происходит окислительно восстановительная реакция:
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
NH4NO3 = N2O + 2H2O (может сопровождаться взрывом).
NH4NO2 = N2 + 2H2O
Аммиак с солями d-элементов может давать комплексные соединения: Ni(NO3)2 + 5NH4OH = [Ni(NH3)4]NO3 + 5H2O + NH4NO3 (зелёный синий)
Гидразин (N2H4)
1)Бесцветная жидкость растворимая в воде
Т пл = 2С ; T кип = 114С
2) Получение
2NH3 + NaOCl = N2H4 + NaCl + H2O (катал Mn2+)
3) Основание
N2H4 + H2O = N2H5+ + OH- pK1 = 6.01 Равновесие
N2H5 + H2O = N2H6 2+ + OH- pK2 = 14 Равновесие
4) Окисление и разложение
N2H4 + O2 = N2(газ) + 2H2O(газ) (t)
3N2H4 = N2 + 4NH3
5)Сильный восстановитель
N2H5Cl + KIO3 + HCl = N2 + KCl + ICl + 3H2O
Гидроксиламин(NH2OH)
1)Бесцветные кристаллы нерастворимые в воде Т пл = 33С
2)Получение
6H+ + HNO3 + 6e = NH2OH + 2H2O (электролиз)
3)Основание
NH2OH + H2O = NH3OH+ + OH- pK=7.18
4)Разложение
3NH2OH = NH3 + N2 + 3H2O
5)Восстановитель
2NH2OH2 + I2 = N2 + 2HI + 2H2O
6)Окислитель
[NH3OH]Cl + FeCl2 + 2HCl = NH4Cl + FeCl3 +H2O

Оксокислоты

Азотистая кислота (HNO2)
1) Получение HNO2
Ba(NO2)2 + H2SO4 = 2HNO2 + BaSO4(осадок)
N2O3 + H2O = 2HNO2
3HNO2 = 2NO + HNO3 + H2O медленно
2)NO+NO2+H2O=2HNO2
Red/Ox свойства
HNO2 + Br2 + H2O = 2HBr + HNO3
HNO2 + FeCl2 + HCl = FeCl3 + NO + H2O
2HNO2 + 2SnCl2 + 8HCl = 3H2O + 2H2SnCl6 + N2O
NaNO2 + Zn + 5NaOH + 5H2O = 3Na[Zn(OH)4] + NH3
в свободном виде не существует, а только в растворе
Кд=5*10^-4 слабая к-та
структурная формула в виде 2 таутомерных форм
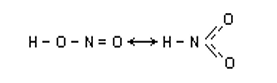
может быть как оx так и red
5NaNO2 + 2KMnO4 + 3H2SO4 = 2MnSO4 + 5NaNO3 + K2SO4 + 3H2O
2NaNO2 + 2KI + 2H2SO4 = 2NO + I2 + Na2SO4 + 2H2O + K2SO4

Азотная кислота
1)Безводная HNO3 медленно разлагается при н.у
4HNO3 = 4NO2 + 2H2O + O2 (слегка окрашена из-за присутствия NO2)
2)HNO3 + реагирует почти со всеми металлами (искл на слайде)
8Fe + 30HNO3 (очень разб) = 8Fe(NO3)3 + 3NH4NO3 + 9H2O
Sn + 4 HNO3 (k) = SnO2 + 4NO2 + 2H2O
3)Безводная HNO3 реагирует с неметаллами (s,se,Te,I)
6S + 6HNO3(б/в) = H2SO4 + 6NO2 + 2H2O
4)Концентрированная HNO3 пассивирует некоторые металлы (Al,Cr,Fe,Ni,Ti)
Непассивирующиеся металлы любой активности реагируют с азотной
концентрирванной кислотой с выделением диоксида азота
4HNO3(конц.) + Zn = Zn(NO3)2 + 2NO2 + 2H2O
5)Получение HNO3
4HNO3 + 5O2 = 4NO + 6H2O
NO + O2 = NO2 (NO2 = N2O)
NO2 + H2O = HNO3 + HNO2
HNO2 = NO + NO2 + H2O
3NO2 + H2O = 2HNO3 + NO
HNO3(конц.) – сильный окислитель
Эта кислота будет реагировать по-разному с различными металлами, но
водород не будет выделяться:
Mg – активный металл
4Mg + 10HNO3(очень разб.) = NH4NO3 + 4Mg(NO3)2 + 3H2O
Fe – металл средней активности
8Fe + 30HNO3(разб.) = 3N2O (N2) + 8Fe(NO3)3 + 15H2O
Cu – малоактивный металл:
3Cu + 8HNO3(разб.) = 2NO + 3Cu(NO3)2 + 4H2O
Нитраты хорошо растворяются в воде, являются сильными окислителями.
3KNO3 + 8Al + 5KOH +18Н2О = 3NH3 + 8K[Al(OH)4]
окислители в кислой среде и расплаве
MnO2 (тв) + 2KOH(ж) + KNO3(ж) = K2MnO4 + KNO2 + H2O
Нитраты щелочных и щелочно-земельных разлагаются до нитритов:
2NaNO3 = 2NaNO2 + O2
4NaNO2 = 2Na2O + 2N2 + 3O2 (температура > t пл.)
Нитраты большинства тяжелых металлов (кроме ртути и серебра):
2Cu(NO3)2 = 2CuO + 4NO2 + O2
2AgNO3 = 2Ag + 2NO2 + O2
Cd(NO3)2 = 2CdO + 2NO2 + O2

Азотистоводородная кислота(HN3)
1)Слабая кислота Т пл = -80С; Т кип = 36С
2)Окислитель
Cu + HN3 = Cu(N3)2 + N2 + NH3
3)Получение
2NaNH2 + N2O = NaN3 + NaOH + NH3
NaN3 + H2SO4 = Na2SO4 + 2HN3 (газ)

Red/Ox способность кислот и солей
1) В кислой среде Ox св-ва выраженны сильнее, чем в щелочной
2) В кислой среде восстановительные св-ва в отрицательных с.о. выраженны слабее, чем в щелочной
3) В кислой среде диспропорционируют все с.о. с образованием N2, HNO3, NH4 +
4) В щелочной среде NO и N2O4 сопропорционируют
2NO + N2O4 + 4 OH- = 4 NO2 - + 2H2O

Оксиды азота
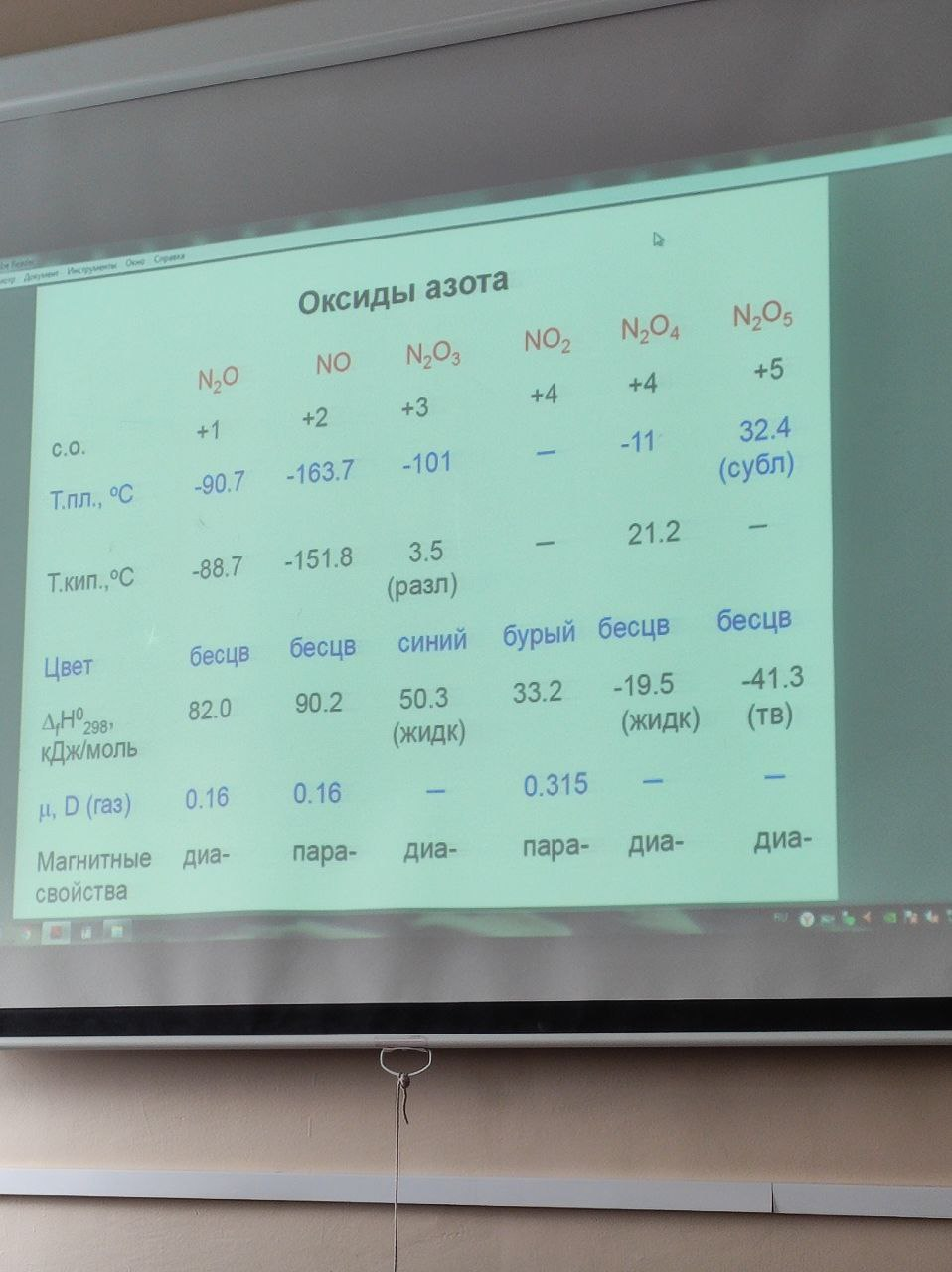
1)Закись азота(веселящий газ N2O)
несолеобразующий, бесцветный (безвредный)
NH4NO3 = N2O + 2H2O (250C) - получение
NH2OH + HNO2 = N2O + 2H2O - получение
C + 2N2O = CO2 + 2N2
поддерживает горение
N2O= 2N2+O2
2)Монооксид азота 2 (NO)
Несолеобразующий
NH3+5O2 = 4NO+5H2O(Pt)
Лабораторное получение
3Cu+8HNO3(разб)=3Cu(NO3)2+2NO+4H2O
2KNO2+2KI+2H2SO4 = 2NO+I2+2H2O+K2SO4
Промышленное получение
4NH3 + 5O2 = 4NO + 6H2O (1000С катализатор)
3)Азотистый ангидрид, оксид азота 3 (N2O3)
Газ, в жидком состоянии- синяя подвижная жидкость, солеобразующий оксид
NO+NO2 =N2O3 - равновесие
N2O3+H2O=HNO2(азотистая кислота) - равновесие
4)Оксид азота NO2 + N2O4
2NO + O2 = 2NO2(бурый газ)
димеризуется
2NO2=N2O4 равновесие (t = -11)
T=+22 жидкость, при Т+11 - твердое бесцветное вещество
Солеобразующий оксид
3) Cu + 4HNO3 (конц) = Cu(NO3)2 + 2NO2 + 2H2O
NO2 + H2O = HNO3+HNO2(азотная и азотистая кислота) - диспропор
2NO2+2NAOH= NaNO3 + NaNO2 + H2O - солеобразующий оксид
2C + 2NO2 = 2CO2 + N2

Применение соединений азота:
Синтез аммиака, азотная кислота, азотные удобрения. Азот – инертный газ (неактивный), используется для создания инертной атмосферы.
Токсическое действие
Азот относится к элементам жизни. В организме человека содержится до 7,2% азота.
Токсическое действие: большинство соединений обладают токсичностью, поражают верхние дыхательные пути и глаза. При поражении глаз возможна слепота. Оксид азота (II) вызывает разложение озонового слоя:
O3 + NO = NO2 + O2