Mešanice plinov – zapiski
UPORABA
Praktične teme vključujejo: razumevanje različnih načinov opisovanja sestave mešanice, določitev termodinamskih lastnosti idealne plinske mešanice in razumevanje razlik med idealno in realno mešanico plinov.
Izrednega pomena sta tudi povezava s predhodnimi temi (enaestavinske ali večstave pline) in realne aplikacije (npr. procesiranje materialov: jeklena talina v vakuumu, degasiranje aluminijeve taline, nastanek plinov med zgorevanjem).
V realnih pogojih so pomembni tudi razlaga o neidealnem vedenju mešanic (Soave/van der Waals) ter načini izračuna z uporabo zakonskih pravil o neidealnih plinih.
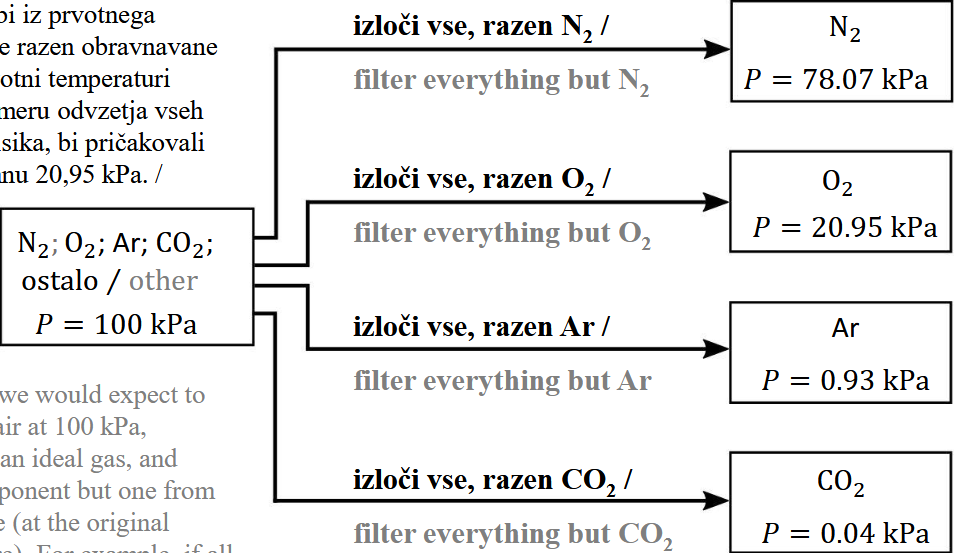
Daltonov zakon delnih tlakovi / Dalton’s Law of Partial Pressures
Zakon pravi: tlak mešanice plinov je vsota delnih tlak v komponent:
$P = \sum{k=1}^n Pk$
Delni tlak komponente k je povezan z njenim molskim deležem in skupnim tlakom:
$Pk = Xk P$ (pri pretirano enakih pogojih T in P za vse komponente)
Intenzivni in ekvivalenčni pomen: delni tlak v mešanici je tlak, ki bi ga ta plin ustvaril, če bi bil prisoten sam v istem prostoru pri isti temperaturi in tlaku.
Amagatov zakon delnih volumnov / Amagat’s Law of Partial Volumes
Koncept: volumen mešanice je vsota delnih volumov komponent, kjer vsak delni volumen "$V_k^*$" predstavlja volumen, ki bi ga komponenta zavzela, če bi bila sama pri isti temperaturi in tlaku kot mešanica:
$V = \sum{k=1}^n Vk^*$
Ta zakon opisuje volumne lastnosti in se pogosto uporablja za primerjavo z Daltonu, ki opisuje tlake.
Uporabo: prevalenca v idealnih plinskih mešanicah: ko je obnašanje plinsko‑idealno, so ti volumni medsebojno kompatibilni s preslikavo med $V_k^*$ in dejanskim volumenom mešanice pri T, P.
Gibbs–Daltonov zakon idealnih mešanic plinov / Gibbs–Dalton’s Law of Ideal Gas Mixtures
Ključna ideja: ekstenzivne lastnosti mešanice, ki so določene z množino molov komponent, so additivne:
Vse ekstenzivne lastnosti mešanice so ohranjene s seštevanjem deležev posameznih komponent:
$U = \sum{k=1}^n Nk U_k(T)$,
$H = \sum{k=1}^n Nk H_k(T)$,
$S = \sum{k=1}^n Nk S_k(T, P)$,
$V = \sum{k=1}^n Nk \bar{V}_k(T, P)$,
kjer je $\bar{V}_k$ parcialni volumen component.
Molske deleže za mešanico: $Xk = Nk / N$ in za intenzivne lastnosti mešanice: $g{ ext{mix}}(T,P) = \sumk Xk gk(T,P)$, kjer $g_k$ so lastnosti posameznih plinov pri isti $T, P$.
Ključna posledica: pri idealni mešanici vsak plin prispeva k lastnostim mešanice v skladu s svojimi molnimi deleži, in mešanica deluje kot superpozicija neodvisnih plinov.
Lastnosti idealne plinske mešanice / Properties of Ideal Gas Mixtures
Molarni volumen mešanice:
$V_m = \dfrac{RT}{P}$ (za popolnoma idealno mešanico; enotno za vse komponente pri isti $T,P$)
Delni tlak komponente:
$Pk = xk P$, kjer $x_k$ je molski delež komponente in $P$ skupni tlak mešanice.
Molarne lastnosti mešanice so utežene z molnimi deleži in lastnostmi komponent.
Praktični pomen: karakterizacija mešanic z enostavnimi pravili usmerja načrtovanje procesov (npr. kompresija, segrevanje, razmislek o toploti in delu).
Neidealno obnašanje mešanic plinov / Non-ideal Behaviour of Gas Mixtures
V realnih pogojih plini ne sledijo popolnoma idealnemu vedenju; pomemben je vlaganje v faktor kompresibilnosti $Z$ ali pravilne eq. st. za zmes.
Primer: Soave ali Redlich–Kwong equation of state (EoS) se uporablja za opis realnih plinov in mešanic.
Van der Waalsova mešanica plinov (mixing rules):
Podatki za mešanico: $a{ ext{mix}}$ in $b{ ext{mix}}$, ki popravita priljubljene privlačne sile in prostornino molekul.
Glavne formule (za mešanico):
$P = \dfrac{RT}{Vm - b{ ext{mix}}} - \dfrac{a{ ext{mix}}}{Vm^2}$,
$a{ ext{mix}} = \sumi\sumj xi xj a{ij}$, z $a{ij} = \sqrt{ai a_j}$,
$b{ ext{mix}} = \sumi xi bi$,
Posebej: $ai$ in $bi$ so komponentni vrednosti; za čiste pline obstajajo parametri $ai$, $bi$.
Napredne zadeve: eksperiment oziroma simulacije za realne pline uporabljajo komercialne EoS ali izračun Z (compressibility factor) za mešanice, da primerjajo z idealnim napovedovanjem.
Povezava s praktičnimi problemi in realnim svetom
Zgodbe iz uvoda/ motivacije: jeklena talina v vakuumu, degasiranje aluminijeve taline, nastanek različnih plinov med zgorevanjem.
Medicinski in industrijski primeri: kisik obogati plinske zmesi v respiratorjih; plinske mešanice v industriji privedejo do prilagoditev tlakov, volumnov in toplote v procesnih operacijah.
Pomembnost razumevanja razlik med idealnim in realnim vedenjem mešanic, saj vpliva na natančnost napovedi tlakov, volumnov in toplotnih zahtev.
Opombe za učenje
Razumevanje definicij in odnosov med količinami (molne, masne) je ključno za pravilno interpretacijo rezultatov iz primerov.
Pri reševanju problemov vedno razmislite, ali je opmerkingen z idealnimi plini ali z neidealnimi korekcijami (EoS, faktor Z).
V realnih postopkih je pomembno oceniti, katere lastnosti in pogoji (T, P) dominirajo pri izračunih: volumen, tlak, temperatura, toplota in delo.
Primeri 1–6 ponazarjajo širok razpon tehnik izračuna: od osnovnih definicij do neidealnih primerov in primerov znotraj industrijskih procesov.