7. NIER
H33. ORGANISATIE URINAIRE SYSTEEM
1) Geef de functionele regio’s van een nefron en bespreek de clearance van een stof in de nier, met als voorbeeld de creatinine clearance.
De functionele regio's van een nefron
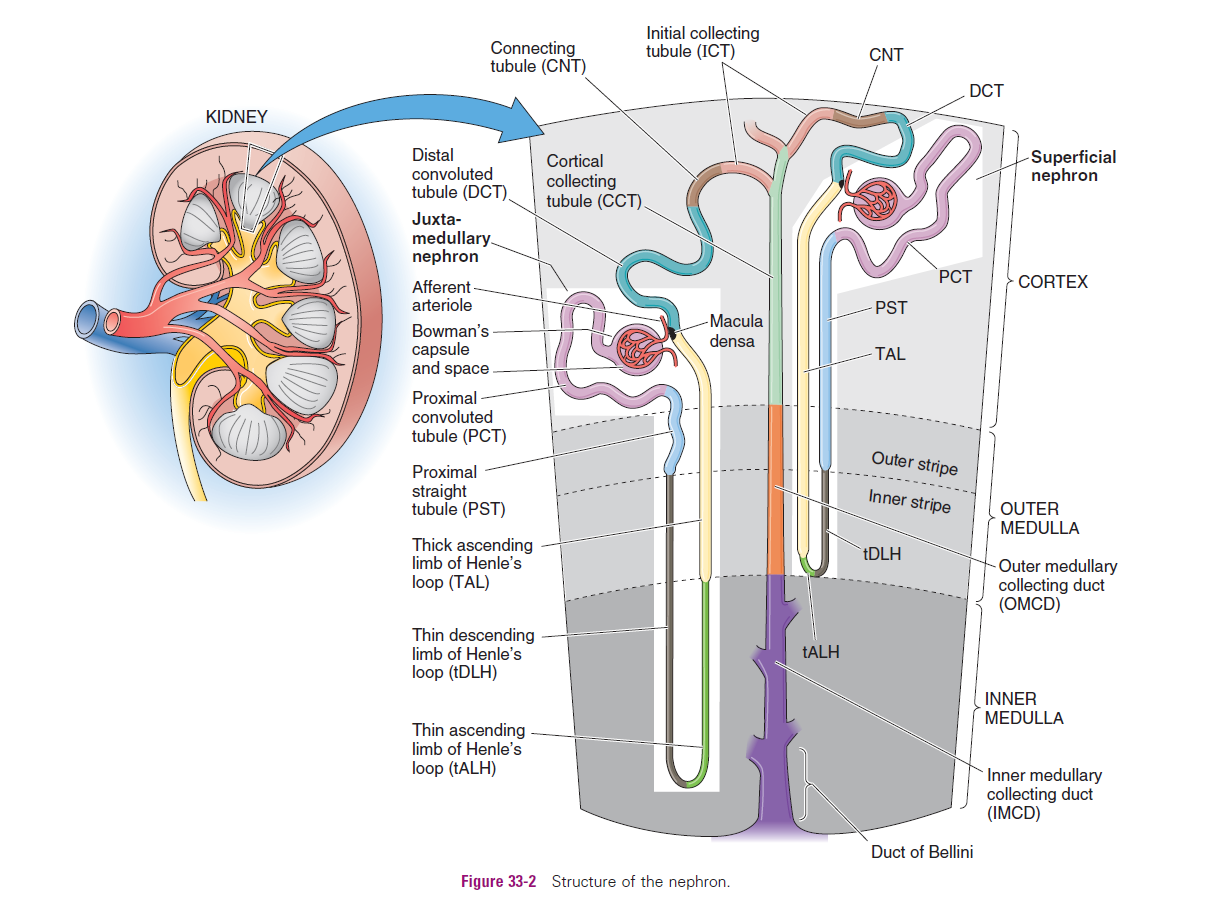
Het nefron is de functionele eenheid van de nier en bestaat uit de volgende regio's:
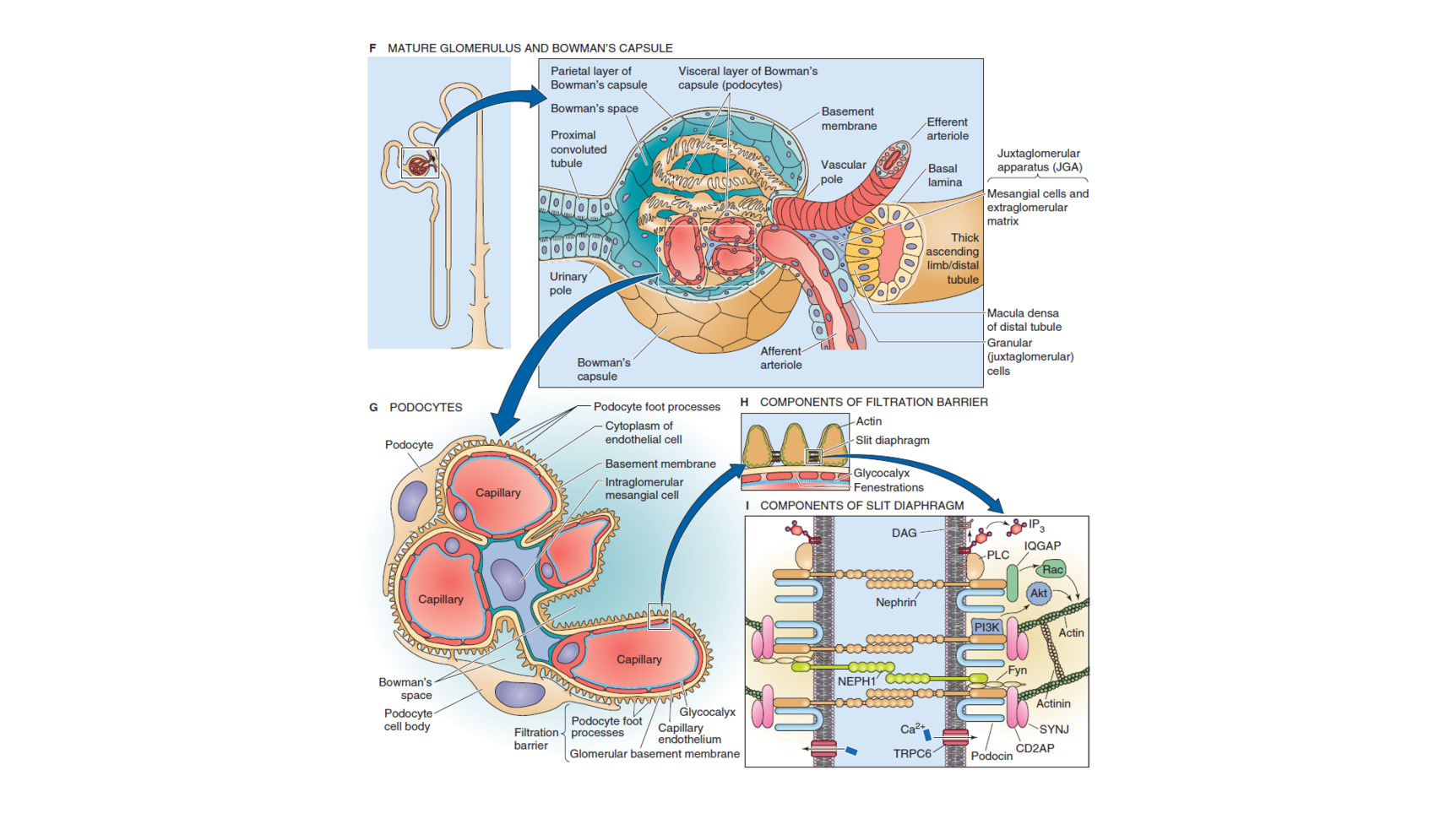
Corpusculum Renale (Glomerulus + Capsule van Bowman): Dit is de plaats waar het bloed wordt gefilterd om een ultrafiltraat (pre-urine) te vormen. Het vormt de barrière die bloedcellen en grote eiwitten tegenhoudt, maar water en kleine opgeloste stoffen doorlaat. De snelheid waarmee dit gebeurt, noemt men de Glomerular Filtration Rate (GFR).
Proximale tubulus (Contorta + Recta): In dit deel worden de essentiële nutriënten (zoals glucose en aminozuren) vanuit het filtraat terug in het bloed opgenomen (gereabsorbeerd).
Lus van Henle: Deze lus bestaat uit een dalend en een stijgend deel. In de dalende lus wordt voornamelijk water gereabsorbeerd, terwijl in de stijgende lus zouten via actief transport worden teruggehaald uit het filtraat. De "concentratiemachine", cruciaal voor het opbouwen van de osmotische gradiënt in het merg.
Distale tubulus: Hier vindt een hormoon-gereguleerde opname plaats van water en zouten (bijvoorbeeld beïnvloed door het Atrial Natriuretic Peptide, ANP). Tevens vindt hier de secretie van overtollig kalium (K+) plaats.
Verzamelbuis (Collecting tubule/duct): Dit laatste deel is primair verantwoordelijk voor de opname van water, sterk gereguleerd door het anti-diuretisch hormoon (ADH), en speelt eveneens een rol in de uitscheiding van K+.
Renale clearance van een stof
Clearance is de functionele maat voor de uitscheidingscapaciteit van de nier voor een specifieke stof. Het definieert het volume bloedplasma dat per tijdseenheid volledig van een bepaalde stof wordt 'geklaard' of gezuiverd en vervolgens in de urine terechtkomt. Clearance vertelt je niet hoeveel gram van een stof wordt verwijderd, maar hoeveel milliliter plasma er volledig "schoon" is gemaakt.
In de nier werkt het precies zo:
Er stroomt bloed door de nier met een bepaalde concentratie afvalstoffen:
De nier haalt daar een deel uit en stopt dat in de urine:
Clearance () is het aantal milliliters plasma dat de nier per minuut volledig heeft kunnen zuiveren om die hoeveelheid in de urine te krijgen.
Creatinine clearance als maat voor nierfunctie
Om de daadwerkelijke werking van de nieren (de GFR) te berekenen in de klinische praktijk, gebruikt men vaak de creatinine clearance (). Creatinine is een uitstekende endogene (lichaamseigen) merker omdat het een vast afbraakproduct is van phosphocreatine uit de spieren; de aanmaak is dus relatief constant en afhankelijk van de spiermassa.
Bij een gezond persoon ligt de normale waarde van de creatinine clearance (en dus de GFR) rond de 125 ml per minuut.
EXTRA — verband clearance en GFR
: stof wordt alleen gefiltreerd
C_x < GFR: netto reabsorptie; plasma wordt niet volledig schoongemaakt omdat de nier de stof weer terug het bloed in haalt
C_x > GFR: netto secretie; nier haalt méér van de stof uit het plasma dan er via de glomerulus alleen gefiltreerd kon worden
H34. GLOMERULAR FILTRATION (GF) EN RENAL BLOOD FLOW (RBF)
1) Bespreek de parameters die de glomerulaire filtratie rate (GFR) bepalen, inclusief formule, en de re-absortie in het peritubulaire systeem.
Parameters en de GFR formule
De Glomerular Filtration Rate (GFR) wordt bepaald door de wet van Ernest Starling;
doorlaatbaarheid van het bloedvat ()
netto ultrafiltratiedruk () = druk die filtratie bevordert - druk die filtratie tegenwerkt
Uitgebreid wordt dit geschreven als:
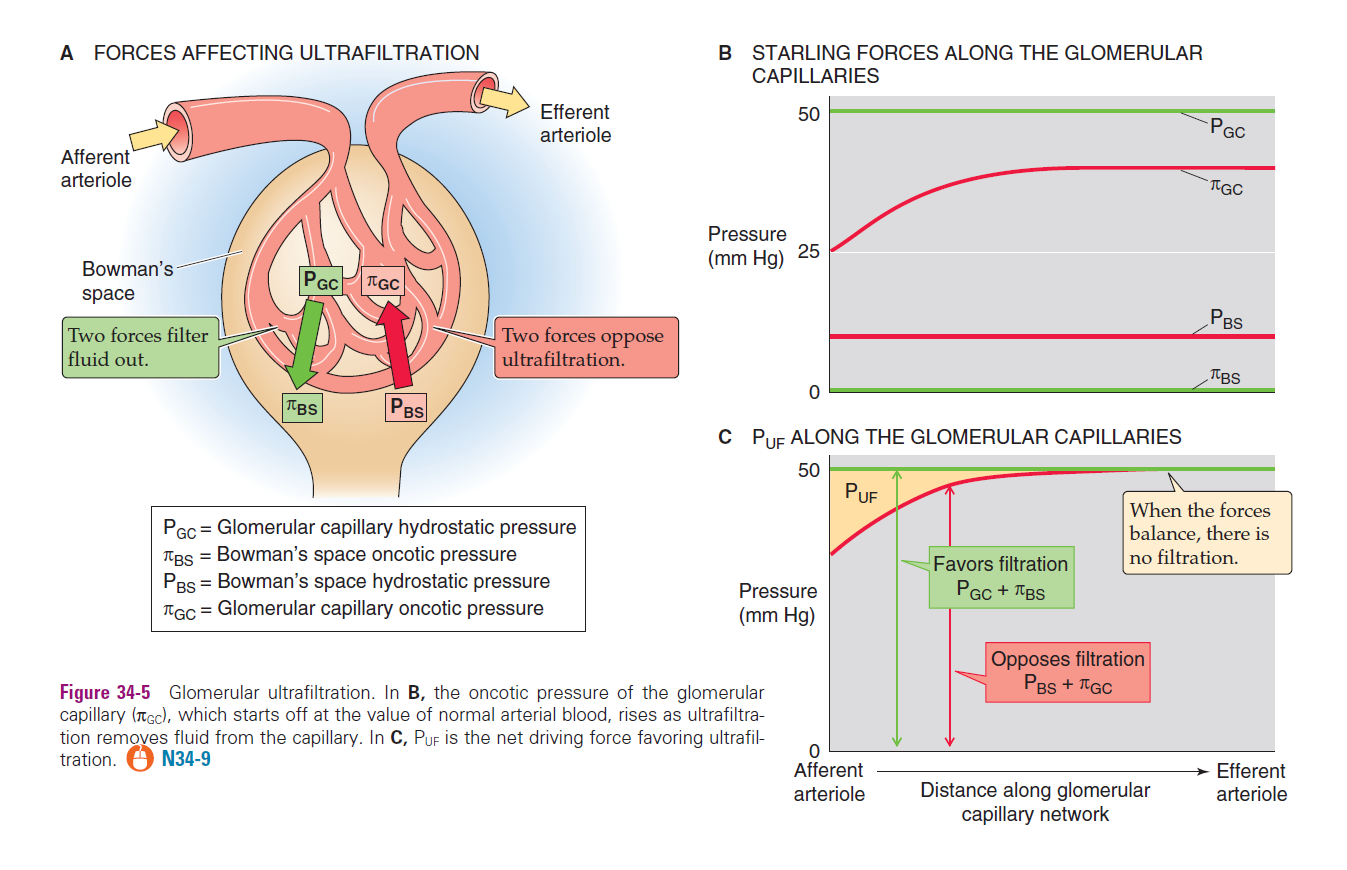
(hydrostatische druk capillair) = bloeddruk in de glomerulaire capillair
(hydrostatische druk Bowman) = tegendruk in het kapsel van Bowman
en (oncotische drukken) = osmotische gradiënt veroorzaakt door eiwitten; omdat eiwitten normaal niet worden gefilterd, is er geen eiwit in het kapsel van Bowman, waardoor verwaarloosbaar (nul) is
(filtratiecoëfficiënt) = doorlaatbaarheid; bedraagt ongeveer 12,5 ml/min per mmHg, wat resulteert in een normale GFR van zo'n 125 mL/min
De fysieke filter zelf is opgebouwd uit gefenestreerd capillair endotheel, een negatief geladen basale membraan (dat eiwitten afstoot) en podocyten met "slit pores".
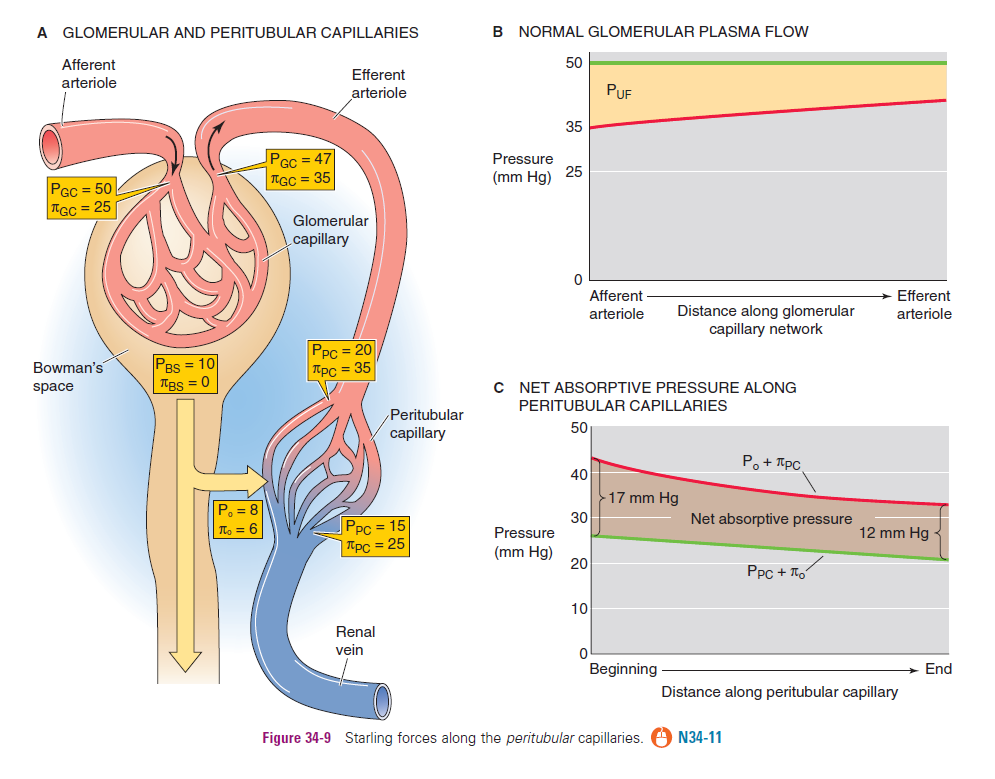
Re-absorptie in het peritubulaire systeem
Het peritubulaire capillaire netwerk, dat zich stroomafwaarts van het efferente arteriole bevindt, volgt exact dezelfde wetmatigheid van Starling voor de uitwisseling van vocht.
De netto druk () is hier echter in tegengestelde richting, waardoor de krachten niet langer in het voordeel van filtratie werken, maar juist zorgen voor de absorptie (opname) van water en oplosbare stoffen in de bloedbaan.
Werking;
De hydrostatische druk () is daar nu heel laag (omdat het bloed al door twee weerstandsvaten is gegaan, afferent arteriool en efferent arteriool; weerstand in serie)
De oncotische druk () is daar heel hoog (omdat we in de glomerulus juist veel water zijn kwijtgeraakt, maar de eiwitten hebben gehouden; “zuigkracht” die stoffen vanuit interstitium terug in het bloed trekt)
EXTRA — samenvatting
Hydrostatische druk — “traptreden”
Deze druk neemt af naarmate we verder van het hart komen, maar in de nier gebeurt dit niet geleidelijk. Het gaat in schokken door de enorme weerstand van de arteriolen.
Vóór afferente arteriool: hoge systeemdruk (± 100 mmHg)
In de glomerulus: druk wordt hoog gehouden (± 60 mmHg) doordat de "uitgang" (efferente arteriool) nauw is
Na efferente arteriool: De druk keldert pas echt. In de peritubulaire capillairen is hij nog maar ± 13 mmHg
Oncotische druk — concentreren en verdunnen
Glomerulus: water gaat eruit, eiwitten blijven → stijgt in het bloed
Peritubulaire capillairen: water komt terug uit de tubulus het bloed in → wordt weer verdund en daalt
Volledige verloop
Glomerulair netwerk; bloed vs. kapsel van Bowman → wint van → netto filtratie (vloeistof verlaat het bloed)
Peritubulair netwerk; bloed vs. interstitium → wint van → netto reabsorptie (vloeistof keert terug in het bloed)
2) Bespreek de renale plasma flow (RPF) inclusief mechanisme van regulatie en effect ervan op de glomerulaire filtratie rate (GFR).
Renale Plasma Flow en de relatie met GFR
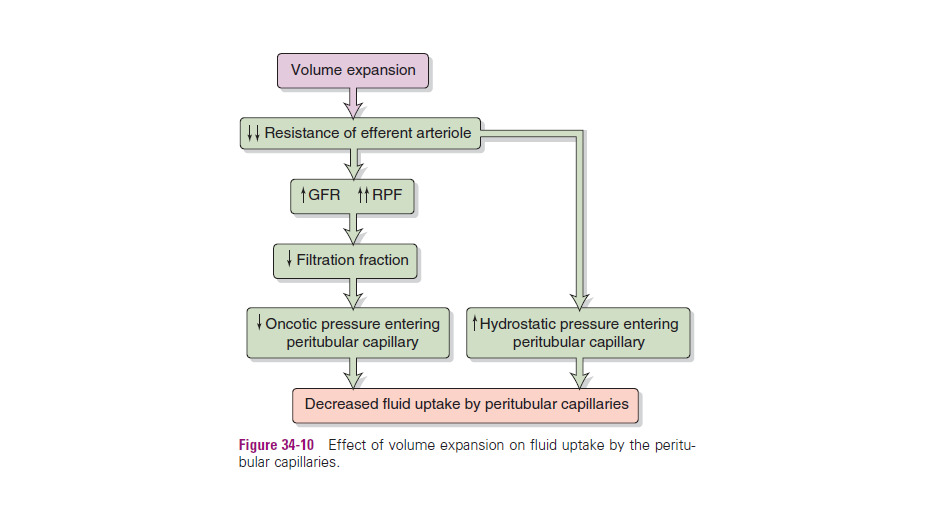
De GFR is sterk afhankelijk van de bloedtoevoer in de glomerulaire capillairen en is dus direct gekoppeld aan de Renal Plasma Flow (RPF).
RPF vertegenwoordigt het plasmagedeelte van het bloed dat de nier passeert, berekend met de formule: (Renal Blood Flow). De RBF bedraagt ongeveer 20% van de totale cardiac output.
De verhouding tussen de effectief gefilterde hoeveelheid en de plasma flow is de filtratiefractie: .
Mechanismen van regulatie en effect op de GFR
Zowel de GFR als de RPF worden fundamenteel gereguleerd door de systemische bloeddruk en door wijzigingen in de weerstand (vasoconstrictie of vasodilatatie) van de afferente en efferente arteriolen.
Myogene autoregulatie: Gladde spiercellen rond de glomerulaire capillairen treden op als druksensoren en passen zelfstandig de diameter aan.
Tubuloglomerulaire feedback (Renine-Angiotensine): De "macula densa" cellen in het juxtaglomerulair apparaat detecteren de natriumconcentratie in het filtraat ter hoogte van de distale tubulis. Een te lage natriumwaarde triggert juxtaglomerulaire cellen om renine vrij te stellen. Dit leidt (via angiotensine II) tot vasoconstrictie (RAAS), voornamelijk van de efferente arteriole, wat de GFR beïnvloedt.
Orthosympatisch zenuwstelsel: De nier wordt enkel door het orthosympatisch stelsel geïnnerveerd. Vrijstelling van noradrenaline veroorzaakt vasoconstrictie, wat leidt tot een afname van de GFR.
Atrial Natriuretic Peptide (ANP): Dit hormoon wordt bij een hoge bloeddruk door de atria van het hart vrijgesteld en veroorzaakt vasodilatatie van zowel de afferente als efferente arteriolen, wat resulteert in een toename van de GFR.
H35. NA-TRANSPORT
1) Bespreek mechanisme en functie van Na transport in de proximale tubule (inclusief glucose als voorbeeld) en de connecting/cortical collecting tubule (inclusief regulatie door aldosterone).
Mechanisme en functie van Na-transport in de proximale tubule (en glucose)
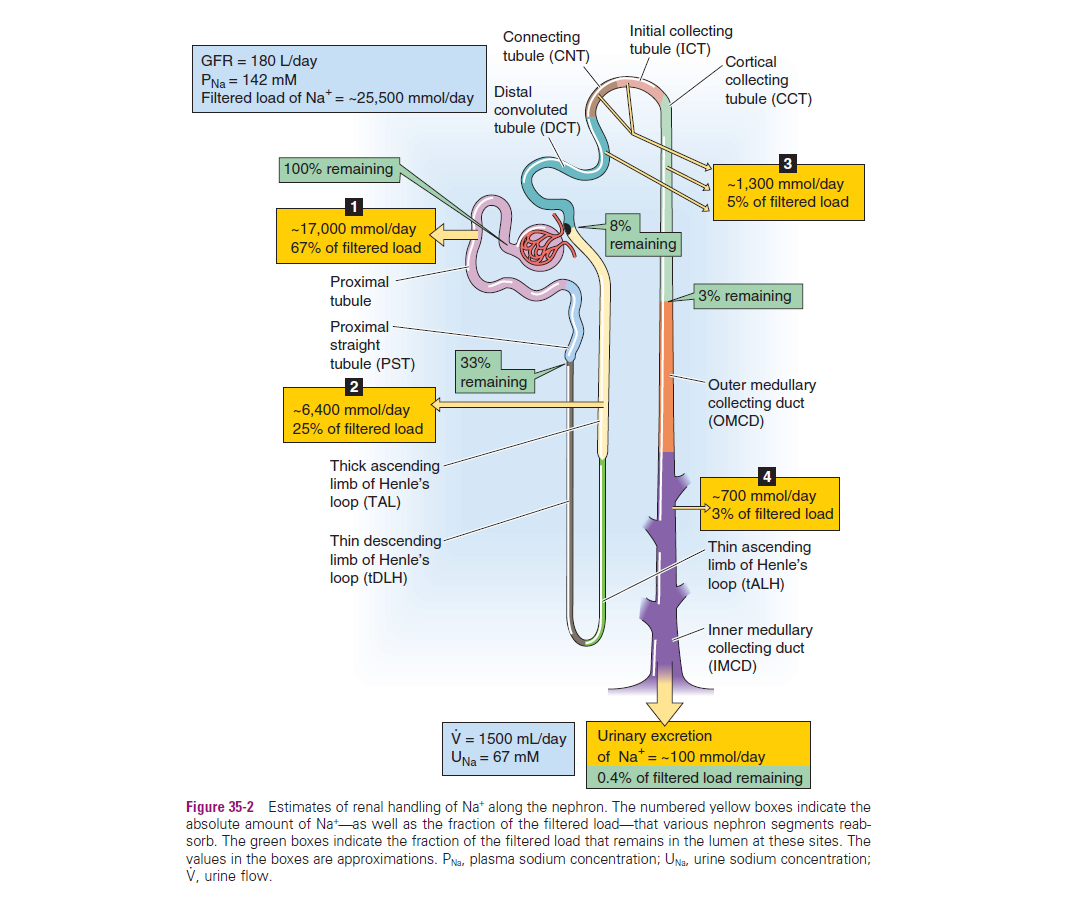
Functie: Het transport van natrium is hier primair gericht op het terug opnemen (absorberen) van essentiële nutriënten uit het ultrafiltraat (pre-urine). Daarnaast is het cruciaal voor de regulatie van het extracellulaire vloeistofvolume en osmolaliteit, aangezien water (via osmose) de reabsorptie van natrium volgt.
Mechanismen: Het transport omvat een combinatie van actieve en passieve processen:
Actief transport: Dit vereist energie en gebeurt tegen de gradiënt in via de Na-K-ATPase pomp, en via gekoppeld transport (symporters en antiporters) aan de luminale zijde.
Passief transport: Dit gebeurt via diffusie (volgens de gradiënt) en osmose/solvent drag.
Routes: Het transport is hoofdzakelijk transcellulair (door de epitheelcel heen via Na-gemedieerd transport). In het eerste deel van de tubule vindt er ook paracellulair transport plaats, waarbij er sprake is van een passieve "backleak" van Na vanuit het interstitium terug naar het lumen (tot wel 1/3 van het gereabsorbeerde Na).
Voorbeeld Glucose (SGLT):
In een gezonde nier wordt glucose in de proximale tubule volledig (100%) gereabsorbeerd via de Sodium-glucose transporter (SGLT), waarbij de opname van glucose direct gekoppeld is aan de actieve opname van natrium.
Er is echter een transportlimiet. Bij een plasmaconcentratie boven de 200 mg/dl geraken de transporters verzadigd en komt glucose in de urine terecht.
Omdat glucose een osmotisch deeltje is, houdt het water vast in het tubulaire lumen. Hierdoor daalt de waterreabsorptie, wat leidt tot een pathologische osmotische diurese (bijvoorbeeld bij niet-gecontroleerde diabetes).
Na-transport in de connecting/cortical collecting tubule en Aldosterone
Mechanisme (ENaC): In de connecting en cortical collecting tubule (CCT) gebeurt de Na-reabsorptie specifiek via de epithelial Na channels (ENaC). Dit zijn spanningsongevoelige natriumkanalen.
Functie en Regulatie door Aldosterone
Aldosterone is een mineraalcorticoïd (een steroïdhormoon uit de bijnier) waarvan de afgifte onder meer gestimuleerd wordt door Angiotensine II.
Omdat het een steroïdhormoon is, beïnvloedt het lokaal de gen-expressie in de cel. Aldosterone stimuleert direct de synthese van nieuwe ENaC-kanalen en verhoogt tevens de activiteit van de Na/K-ATPase pompen.
Het uiteindelijke resultaat is een sterke toename in de reabsorptie van natrium (en dus water) uit het filtraat.
Naast het terughalen van natrium, stimuleert aldosterone tegelijkertijd ook de secretie (uitscheiding) van kalium (K+) naar de urine.
Klinische noot: Cortisol kan ook de ENaC-kanalen stimuleren, maar wordt normaal gesproken geïnactiveerd door het enzym 11b-HSD2. Bij een remming van dit enzym of een zeer hoge cortisolconcentratie ontstaat er excessieve Na- en waterreabsorptie.
H38. URINE CONCENTRATIE
1) Geef formule voor de water clearance en bespreek het mechanisme voor de concentratie van urine in de lus van Henle en inner medullary collecting duct (inclusief regulatie door AVP of anti-diuretisch hormoon).
EXTRA — korte inleiding
Je bloed moet precies de juiste verhouding tussen water en zout hebben;
Te veel water gedronken? Bloed wordt te waterig. De nier moet het extra water eruit halen en wegspoelen. Dit noemen we positieve water clearance (je loost "vrij water").
Te weinig gedronken/gezweet? Bloed wordt te zout. De nier moet water uit de "urine-in-wording" terugzuigen naar het bloed. De urine die overblijft is heel zout en geconcentreerd. Dit noemen we negatieve water clearance.
Je nier heeft een heel slim systeem om dit te regelen;
Stap 1: De Zoutpomp (Lus van Henle)
In het niermerg (het binnenste deel van de nier) wordt het weefsel extreem zout gemaakt. De Lus van Henle pompt namelijk continu zout naar buiten, maar laat daar geen water door.
Het resultaat: Het weefsel rondom de buisjes is een "zoutwoestijn" geworden die heel hard aan water kan zuigen.
Stap 2: De Kraan (De verzamelbuis & ADH)
De urine komt nu in de laatste buis (de verzamelbuis). Hier wordt beslist: laten we het water doorlopen naar de blaas, of zuigen we het terug naar het bloed?
Dit wordt geregeld door het hormoon ADH:
Geen ADH: De wanden van de buis zijn "waterdicht". Al het water stroomt gewoon door naar je blaas. Je plast veel en lichte urine.
Wel ADH: ADH maakt kleine gaatjes (aquaporines) in de wand. Omdat de "zoutwoestijn" uit stap 1 zo hard aan water zuigt, ontsnapt het water uit de buis, terug je lichaam in. Je plast heel weinig en donkere urine.
Formule voor de water clearance
De nier reguleert de osmolariteit en het volume van het bloedplasma door urine te concentreren of te verdunnen. Hiervoor worden twee berekeningen gebruikt:
1. Osmolaire clearance ()
: urine-osmolariteit
: urinedebiet (volume/tijd)
: plasma-osmolariteit
2. Water clearance ()
Negatieve waarde: De nier produceert urine die geconcentreerder is dan het plasma. Er wordt zuiver water aan de urine onttrokken (reabsorptie).
Positieve waarde: Er wordt zuiver water aan het bloedplasma onttrokken, wat resulteert in verdunde urine.
Grenswaarden: De urine-osmolaliteit varieert van ~30 mOsm (bij 20 L urine/dag) tot maximaal ~1200 mOsm (bij 0,5 L urine/dag).
Concentratiemechanisme in de lus van Henle
Het "counter-current" effect zorgt voor een osmolaire gradiënt in het interstitium van de medulla, wat de drijvende kracht is voor waterreabsorptie.
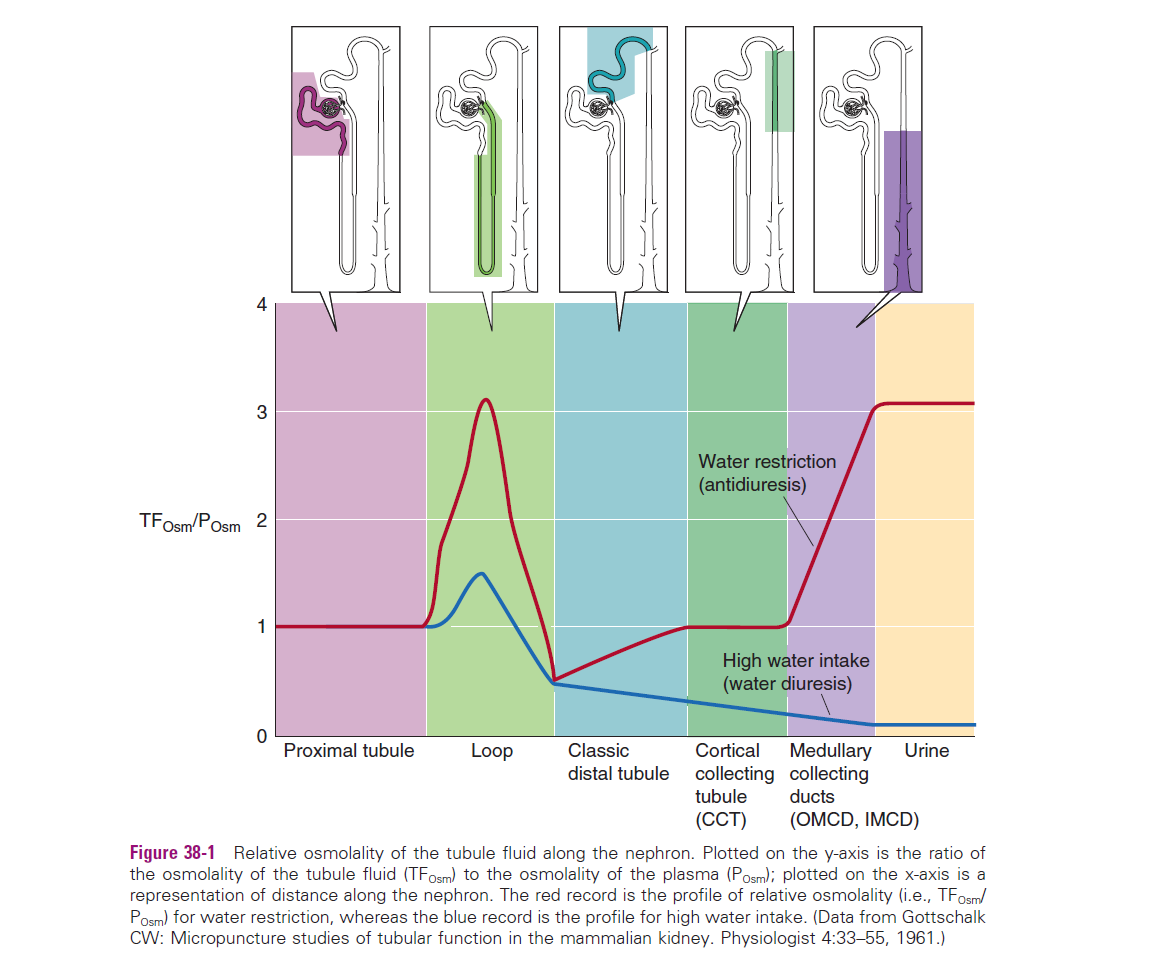
1. Dalende lus (Thin Descending Limb - tDLH)
Permeabiliteit: Zeer permeabel voor water door de expressie van Aquaporine 1 (AQP1).
Transport: Geen actief transport. Water wordt passief gereabsorbeerd door de hoge osmolariteit in het interstitium van de medulla.
Resultaat: Ongeveer 15% van het water in de urine wordt hier gereabsorbeerd, wat leidt tot concentratie van de tubulaire vloeistof (hypertone urine).
2. Dunne stijgende lus (Thin Ascending Limb - tALH)
Permeabiliteit: Impermeabel voor water (H2O).
Transport: Passief NaCl-transport naar het interstitium (reabsorptie). Dit gebeurt omdat de NaCl-concentratie in het lumen groter is dan in het interstitium.
Ureum: Er vindt actieve secretie van ureum plaats in het lumen, wat de osmolariteit reguleert.
3. Dikke stijgende lus (Thick Ascending Limb - TAL)
Permeabiliteit: Impermeabel voor water.
Transport: Actieve reabsorptie van NaCl (en K+). Dit gebeurt via Na-K-2Cl symport (apicaal) en NaK-ATPase (basaal).
Resultaat: Verdunning (dilutie) van de tubulaire vloeistof. De actieve opname van NaCl bouwt de osmolariteit in het interstitium op (tot een gradiënt van 200 mOsm).
Concentratie in de Inner Medullary Collecting Duct en regulatie door ADH
De finale concentratie van de urine wordt distaal gereguleerd in de verzamelbuizen.
Regulatie door ADH (Vasopressine):
ADH reguleert de expressie van waterkanalen (Aquaporine 2 - AQP2) in de apicale wand van de corticale en medullaire verzamelbuizen.
ADH stimuleert daarnaast de inbouw van ureum transporters (UT) in de medullaire verzamelbuizen.
Effect van ADH:
Toename ADH: Meer aquaporines zorgen voor meer waterreabsorptie, wat resulteert in geconcentreerde urine (antidiurese).
Afname ADH: Minder waterreabsorptie resulteert in verdunde urine (diurese).
Rol van Ureum: Ureum wordt gereabsorbeerd uit de inner medullary collecting duct naar het interstitium. Dit draagt aanzienlijk bij aan de hoge osmolariteit op het diepste punt van de lus (tot 1200 mOsm). Een hoog proteïne dieet (meer ureum) kan de urine hierdoor sterker concentreren.
H39. ROL NIER BIJ ZUUR-BASE BALANS
1) Geef de rol en werkingsmechanisme van de nier bij de regulatie van het zuur-base evenwicht.
De rol van de nier bij het zuur-base evenwicht
De nieren werken samen met chemische buffers in het bloed om de zuurtegraad van het lichaam strikt te reguleren, pH ± 7.4. Een plasma-pH onder de 6.9 of boven de 7.8 is immers dodelijk. In ons lichaam is de belangrijkste buffer de bicarbonaatbuffer;
Longen: Regelen -kant (ademhaling)
Nieren: Regelen -kant (bicarbonaat)
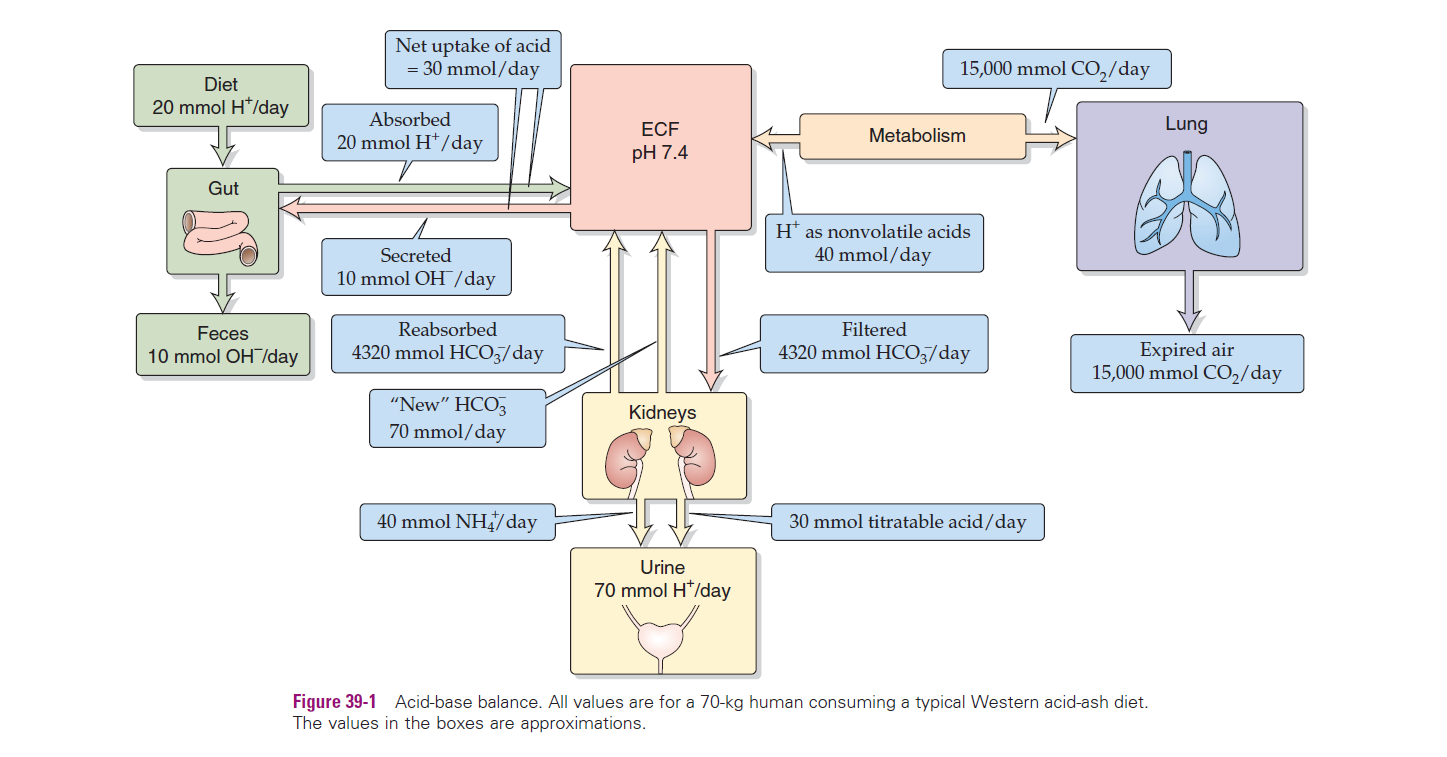
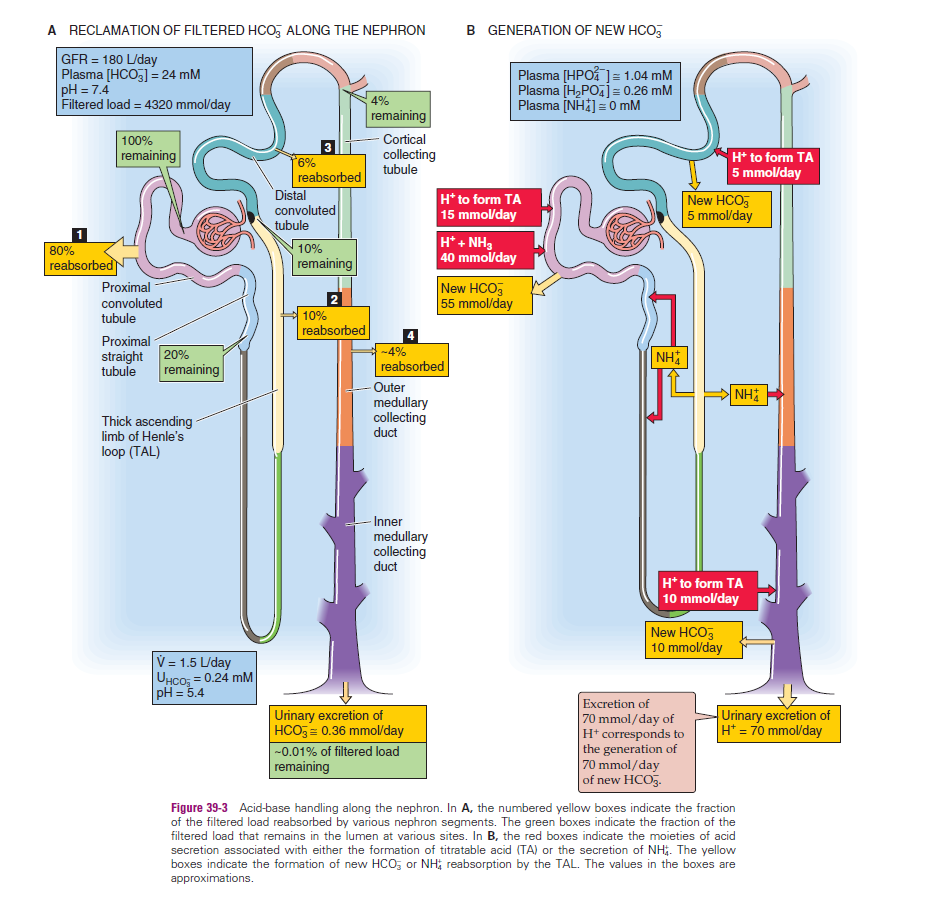
Het lichaam produceert dagelijks metabolische zuren. De specifieke taak van de nier is om dagelijks ongeveer 70 mmol ionen uit te scheiden via ongeveer 1,5 liter urine.
Tegelijkertijd genereert de nier dagelijks ongeveer 70 mmol nieuw bicarbonaat () om de verbruikte buffers in het bloedplasma weer aan te vullen.
Het fysiologische probleem en de oplossing
Indien de nieren 70 mmol vrije ionen zouden oplossen in 1,5 liter water, zou dit een extreem lage en weefselbeschadigende pH van ongeveer 1.3 opleveren.
De nieren kunnen urine fysiologisch echter maar aanzuren tot een minimale pH van 4.4.
Het werkingsmechanisme is daarom sterk afhankelijk van specifieke buffermechanismen in het tubulaire lumen om de ionen te binden, zodat ze veilig in de urine kunnen worden uitgescheiden zonder de pH-limiet te overschrijden.
Werkingsmechanismen voor excretie en generatie
De nier gebruikt drie primaire mechanismen om dit zuur in de urine te bufferen en uit te scheiden:
Titreerbare zuren: ionen worden uitgescheiden door ze in het tubulaire lumen te binden aan aanwezige titreerbare zuren, zoals fosfaat, urinezuur (uric acid) en creatinine. De effectiviteit en mate van deze uitscheiding is afhankelijk van de actuele pH van de pre-urine.
Ammonium excretie: De nier maakt actief ammoniak () aan, voornamelijk in de proximale tubulus. Dit wordt in het lumen gesecreteerd waar het een ion bindt om ammonium () te vormen. Dit ammonium wordt vervolgens met de urine uitgescheiden. Verdere reabsorptie en secretie van deze moleculen vindt nog plaats in de lus van Henle en de medullaire verzamelbuis. Ongeveer 5% van het opgenomen gaat overigens via het hepatorenaal mechanisme naar de lever.
Excretie van carboxylaten: Het uitscheiden van organische anionen zoals carboxylaten (bijvoorbeeld acetoacetaat of beta-hydroxybutyraat, beter bekend als ketonbodies) helpt eveneens bij de zuureliminatie. Dit mechanisme wordt extra belangrijk bij ernstige metabole verzuring, zoals bij keto-acidose, waarbij grote hoeveelheden van deze ketonlichamen in de urine terechtkomen. Via ditzelfde actieve secretiemechanisme ontdoet de nier zich ook van diverse medicijnen (farmaca).
H40. CONTROLE ZOUT-WATER BALANS
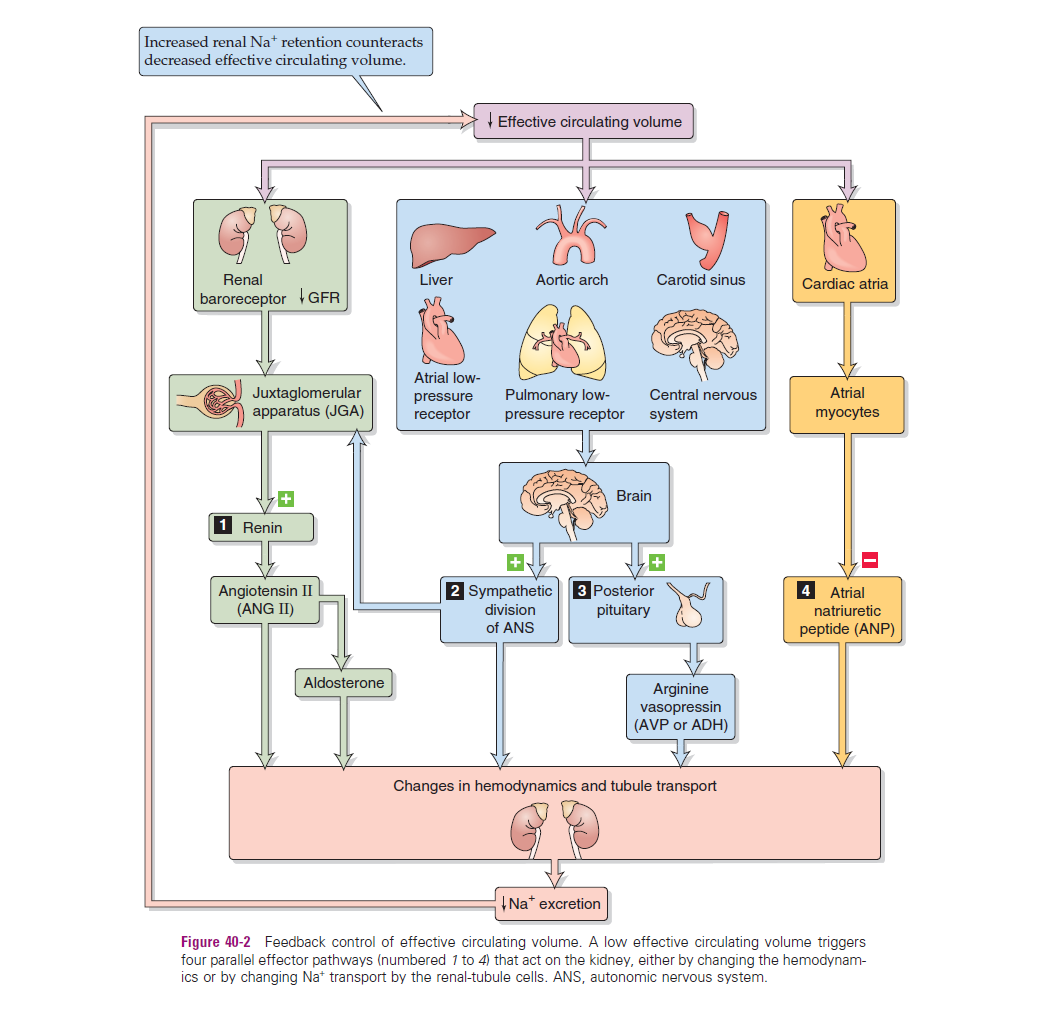
1) Bespreek de mechanismen in de nieren die de osmolariteit en het volume van het effectief circulerend volume (bloedplasma) in balans houden.
Sensoren voor de zout- en waterbalans
De nieren regelen de homeostase van het bloedplasmavolume en de osmolariteit aan de hand van twee soorten sensoren;
1. osmolariteit-sensoren: detecteren de osmolariteit van het bloedplasma in het centraal zenuwstelsel
in hypothalamus
vrijzetting ADH (door neurohypofyse) → opsparen water + dorst
2. volume-sensoren: meten verandering in bloedplasmavolume
"high pressure" baroreceptoren
in sinus caroticus + arcus aortae
bewaken de arteriële bloeddruk; bij daling van de bloeddruk (en dus volume) neemt hun vuurfrequentie af → RAAS activatie → vasoconstrictie
"low pressure" baroreceptoren detecteren veranderingen in het bloedplasmavolume
in rechteratrium
detecteren de veneuze return
veel volume: stimulatie van de Bainbridge-reflex → hartslag omhoog + vrijzetting van ANP (zie ook H23-H25.)
weinig volume: signaal naar de hypothalamus om ADH vrij te zetten (volumebehoud)
De vier effectormechanismen in de nier
Deze sensoren sturen de renale adaptatie aan via vier primaire effectorwegen;
1. Het Renine-Angiotensine-Aldosteron pad
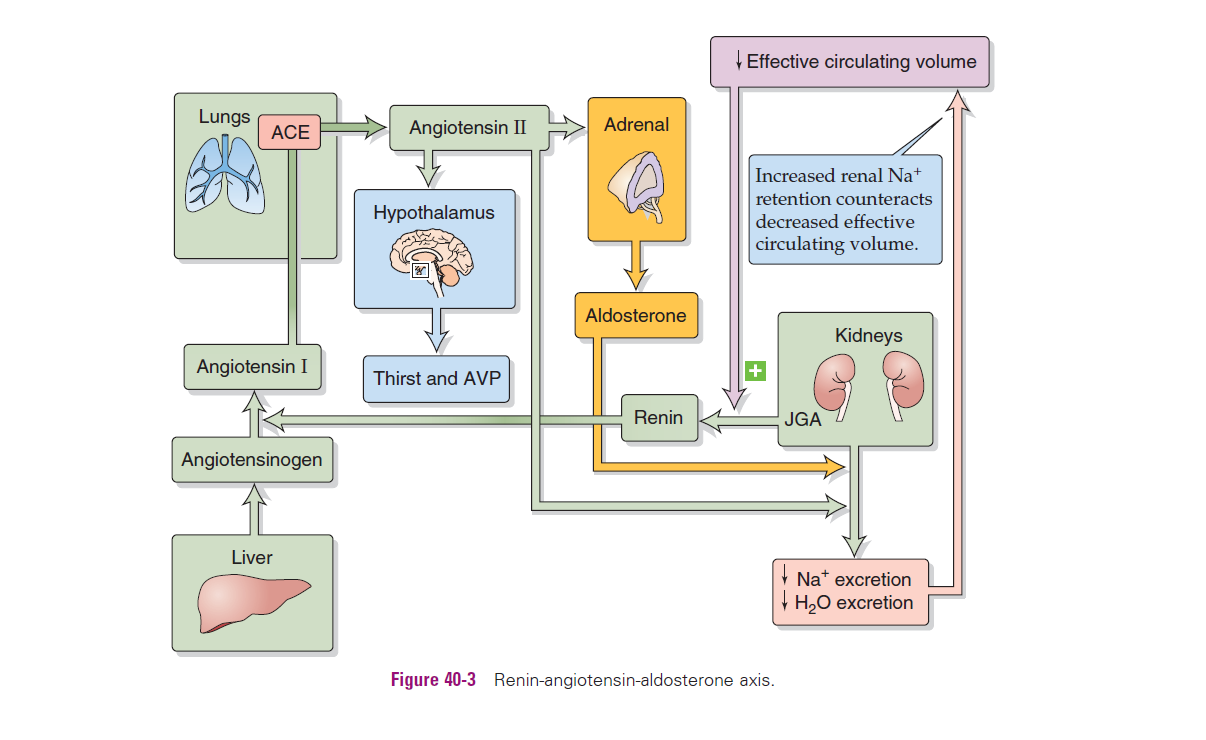
Dit hormoonsysteem is sterk betrokken bij de natriumreabsorptie.
Aldosteron stimuleert de synthese van epitheliale natriumkanalen (ENaC) in de cortical collecting tubule (CCT).
Deze toename in ENaC leidt tot extra Na-reabsorptie, wat op zijn beurt resulteert in een toename van het extracellulaire vloeistofvolume (ECF) en een stijging van de bloeddruk.
2. De orthosympatische divisie van het autonoom zenuwstelsel
De orthosympatische stimulatie heeft een direct effect: het veroorzaakt vasoconstrictie (waardoor de Glomerular Filtration Rate of GFR daalt) en het stimuleert direct de Na+-reabsorptie.
Indirect stimuleert het orthosympatisch zenuwstelsel ook de verdere vrijstelling van renine.
3. Regulatie van AVP / ADH
Zowel de osmoreceptoren als de baroreceptoren (via de hypothalamus-hypofyse as) sturen de afgifte van Arginine-Vasopressine (AVP), ook gekend als het anti-diuretisch hormoon (ADH).
Dit hormoon wordt vrijgesteld vanuit de achterste kwab van de hypofyse (posterior lobe pituitary gland) en is cruciaal voor de reabsorptie van water en dus het behoud van het volume en de osmotische waarde.
4. Atrial Natriuretic Peptide (ANP)
Dit peptide wordt vrijgesteld door de atria van het hart, specifiek wanneer er een volumetoename is (“stretch”). Bij een daling in het volume wordt de afscheiding van ANP logischerwijs verminderd.
Heeft tegengestelde werking aan RAAS; het doet bloeddruk, bloedvolume en [Na] dalen;
Nieren: stimuleert natriurese (Na excretie) and diurese (waterexcretie) doordat GFR toeneemt (afferente arteriool: vasodilatatie; efferente arteriool: vasoconstrictie) → verminderd bloedvolume
Cardiovasculair: vasodilatatie → verminderde weerstand → verminderde bloeddruk
Endocrien: inhibeert vrijzetting van:
renine (nier)
aldosteron (bijnier)
ADH (aanmaak hypothalamus, vrijzetting neurohypofyse)