hoof 4
FACULTEIT WETENSCHAPPEN
ALGEMENE CHEMIE
Prof. dr. Isabel Van Driessche
Prof. dr. Klaartje De Buysser
1. Chemische Vergelijkingen en Balancering
Definitie: Een chemische vergelijking is een kwalitatieve en kwantitatieve weergave van een chemisch proces. Het toont welke stoffen reageren en in welke verhouding ze dit doen.
Wet van Lavoisier (Behoud van Massa): Massa kan niet worden gecre'eerd of vernietigd. Dit impliceert dat het aantal atomen van elk element constant blijft voor en na de reactie.
Balanceringstechnieken:
Trial-and-error: Aanpassen van co'effici'ebnten tot de atoombalans klopt.
Indeling in fracties: Soms nuttig om met fracties te werken (bijv. ) om vervolgens de hele vergelijking te vermenigvuldigen.
Toestandsaanduidingen:
(solid): vaste stof.
(liquid): zuivere vloeistof.
(gas): gasfase.
(aqueous): opgelost in water (gehydrateerde ionen of moleculen).
2. Stoichiometrische Berekeningen
De Mol (): De centrale eenheid in de chemie. deeltjes (Getal van Avogadro).
Basisformules:
Massa naar mol: waarbij de massa in gram is en de molaire massa in .
Concentratie (Molariteit): (in of ).
Beperkend Reagens en Overmaat:
Het beperkend reagens is de reactant die theoretisch als eerste opgebruikt is. Dit bepaalt de maximale productvorming.
Berekening: Deel de beschikbare hoeveelheid mol () door de stoichiometrische co'effici'ebnt van de stof. De kleinste waarde wijst op het beperkende reagens.
3. Reactierendement
Theoretische Opbrengst: De hoeveelheid product bij 100% omzetting van het beperkende reagens.
Actuele Opbrengst: De werkelijk gemeten hoeveelheid product na afloop van het experiment.
Rendementsverliezen: Veroorzaakt door evenwichten, zijreacties, onzuiverheden in reagentia of verlies tijdens filtratie/kristallisatie.
Formule:
4. Classificatie van Chemische Reacties
4.1 Combinatie en Ontleding
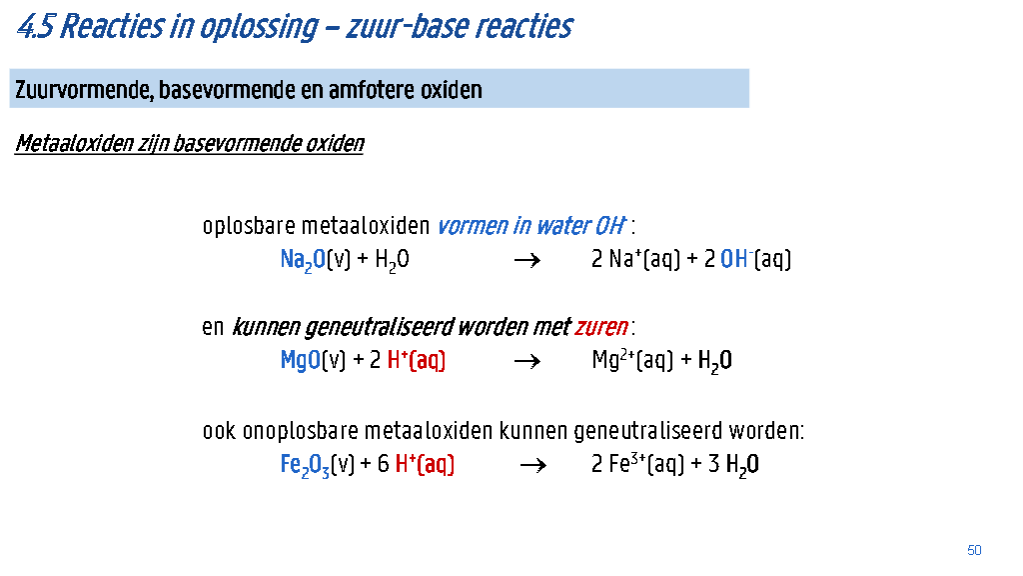
Synthese: . Bijv. de vorming van metaaloxiden: .
Ontleding: .
Thermolyse: Door warmte, bijv. .
Elektrolyse: Door elektrische energie.
4.2 Uitwisselingsreacties (Metathese)
Neerslagreacties: Wanneer twee goed oplosbare zouten in oplossing een onoplosbaar zout vormen.
Voorbeeld: .
Netto-ionenvergelijking: Alleen de reagerende ionen worden genoteerd: . De en ionen zijn toeschouwerionen.
4.3 Verbrandingsreacties
Reactie met zuurstof (), waarbij veel energie vrijkomt in de vorm van warmte.
Volledige verbranding van koolwaterstoffen levert altijd en op: .
5. Oplosbaarheid in Water
Oplosbaarheidsregels (Belangrijkst):
Oplosbaar: Alkalimetalen, , , , .
Meestal oplosbaar: (behalve met ).
Meestal onoplosbaar: (behalve met Groep 1 of ).
6. Titrimetrie
Volumetrische Analyse: Kwantitatieve bepaling van een onbekende concentratie via een bekende standaardoplossing.
Equivalentiepunt: Het moment waarop de stoichiometrische hoeveelheden van titrant en analiet exact met elkaar overeenkomen (bijv. bij een zuur-base titratie).
Indicator: Een hulpstof die van kleur verandert bij een specifieke pH, wat dient om het eindpunt (visueel punt) te markeren.
7. Empirische en Moleculaire Formules
Massapercentage: .
Empirische Formule: De eenvoudigste verhouding (bijv. ).
Moleculaire Formule: De werkelijke structuur (bijv. ). De factor wordt bepaald door: .