6. EXTRA
REPROGRAMMERING
Tijdens de embryonale ontwikkeling vinden er 2 golven van epigenetische resetting plaats. Dit betekent dat de epigenetische signatuur tijdens deze golven wordt gereset of grotendeels gewist, zodat de genexpressie wordt geïnstalleerd die nodig is voor;
(i) het ondersteunen van de pre-implantatie embryonale ontwikkeling (eerste golf) en
(ii) tijdens de geslachtscelvorming om de correcte vorming van PGCs en latere gametogenese toe te laten (tweede golf).
IN VIVO — natuurlijk
Een voorbeeld van deze in vivo ‘epigenetische reprogrammering’ of ‘resetting’ is dat de methylatiegroepen van vele genen verdwijnen. Dus tijdens die twee stadia (embryo’s en PGCs) is de methylatie minimaal en spreken we dus van hypomethylatie.
IN VITRO — kunstmatig
In vitro reprogrammering kan ook gebeuren. Dit is dan meestal in de context om een gedifferentieerde cel te ‘resetten’ of te ‘transformeren’ naar zijn embryonale status (analoog als de eerste golf). Gedifferentieerde cellen (somatische cellen) bezitten elk hun eigen specifieke functie, dus gepaard gaande met hun eigen specifieke genexpressie. Bedoeling is om bij het klonen of bij de aanmaak van bepaalde stamcellen, een gedifferentieerde cel te transformeren naar pluripotente stamcellen, door bvb de methylaties op het DNA van de gedifferentieerde cel te verminderen, en dus de specifieke genexpressie uit te schakelen en te vervangen door ‘embryonale’ genexpressie. Dit laatste is kenmerkend voor pluripotente stamcellen (zoals embryonale stamcellen) die kunnen uitgroeien tot eender welk type gedifferentieerde cel van ons lichaam.
AFBEELDING
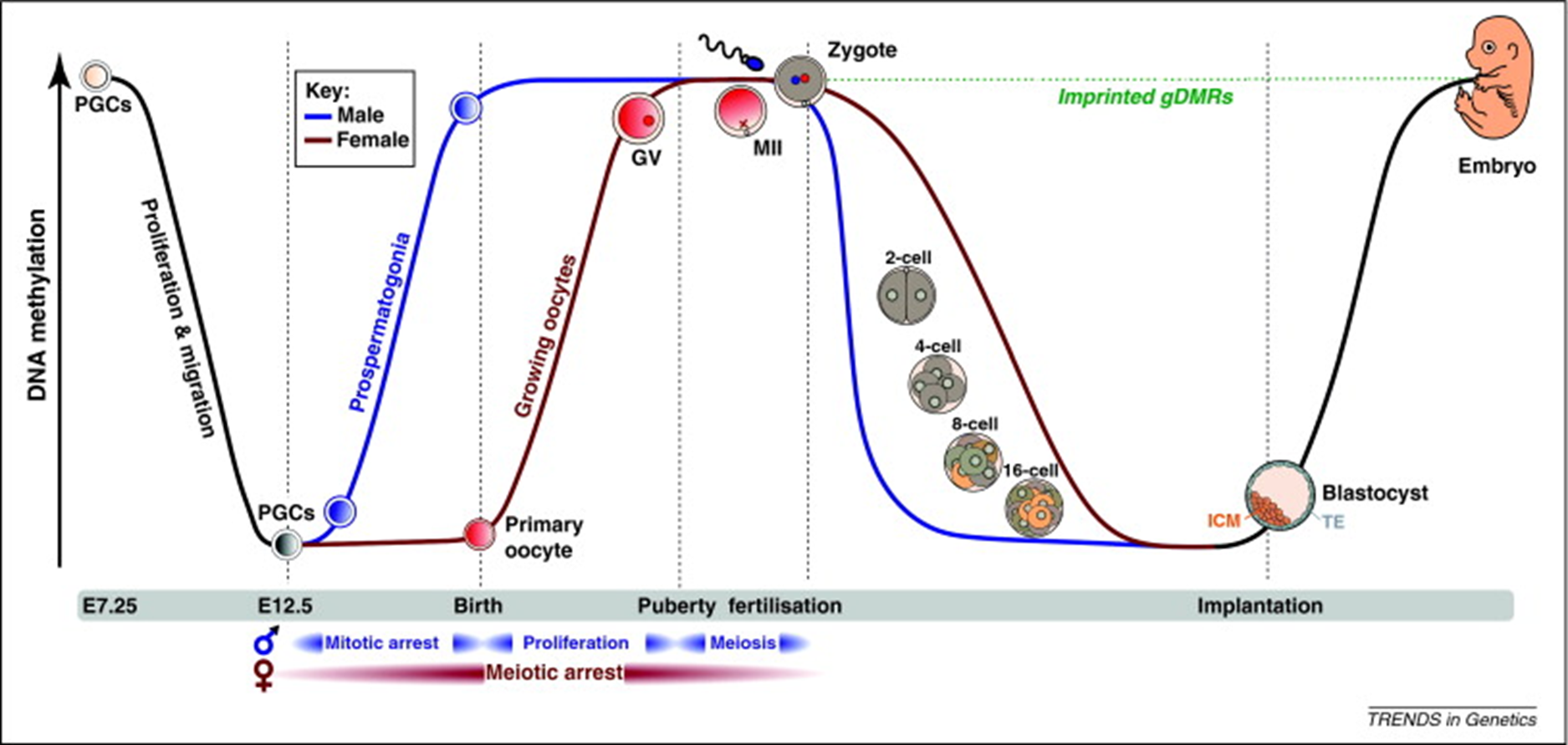
minder methylatie → meer genexpressie
blastocyst, PGC
meer methylatie → minder genexpressie
cellen moet enkel eigen functie uitvoeren
somatische cellen, zaadcellen …
MORFOLOGISCHE SCORINGSPARAMETERS EICELLEN
Een normale rijpe eicel wordt gekenmerkt door de aanwezigheid van een eerste poollichaam, een helder en kleurloos cytoplasma met dus middelmatige granulatie, en de afwezigheid van inclusies. Mogelijke abnormaliteiten kunnen zijn;
een abnormaal groot poollichaam
een gefragmenteerd poollichaam
aanwezigheid van inclusies
abnormale (vb. ovale) vormen van de eicel
een dunnere zona pellucida
granules in de perivitelliene ruimte
Maar dit zijn allemaal abnormaliteiten die weinig invloed hebben op de zwangerschapskans. Andere abnormaliteiten zoals;
een centrale grote granulevlek,
de afwezigheid van een eerste poollichaam (=onrijpe eicel)
aanwezigheid van clusters smooth endoplasmatisch reticulum,
een reuze eicel,
een abnormale spoelfiguur,
hebben wel een nadelige invloed op de zwangerschapskans, en worden meestal niet gebruikt voor bevruchting. Een voorbeeld is totaal chaotisch georganiseerde metafase II spoelfiguren die vaak teruggevonden worden in patiënten die enkel onrijpe eicellen produceren na hormoonstimulatie.
EICELACTIVATIEMECHANISME
Voor een succesvolle eicelactivatie vervullen zowel de zaadcel als de eicel een cruciale rol. Na het binnenkomen van de zaadcel, komt er een eiwit vrij uit de zaadcelkop, het fosfolipase C zeta (PLC), een enzym dat de klieving veroorzaakt van fosfatidylinositol-difosfaat (PIP2) in inositoltrifosfaat (IP3) en diacylglyceryl (DAG).
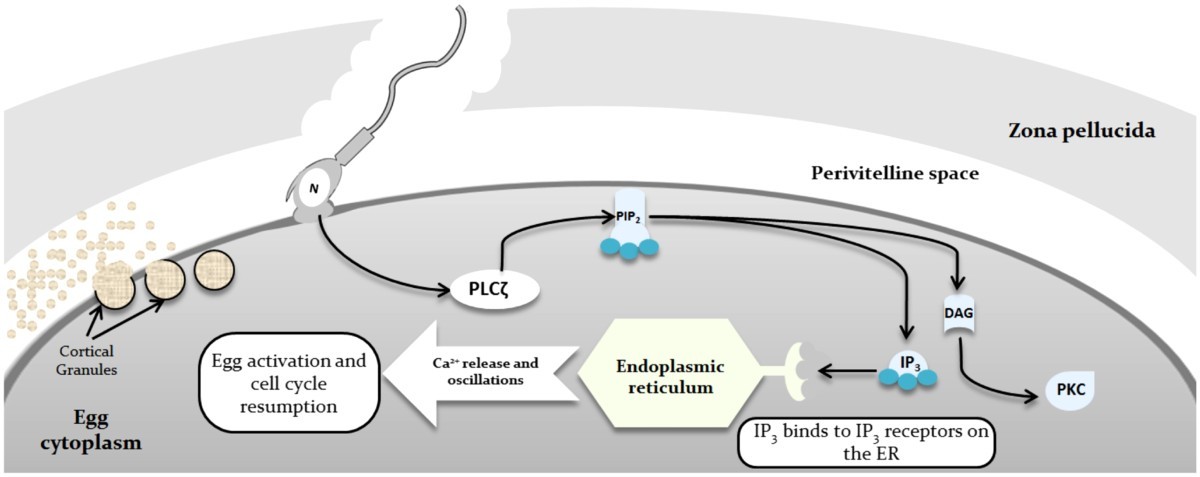
IP3 zal vervolgens binden op zijn receptor (IP3R) die zich bevindt in het ER van de eicel. Deze receptor functioneert als calcium opslag binnen de eicel, en bij het binden van IP3 zal calcium vrijgelaten worden vanuit het ER in het cytoplasma van de eicellen. Via pompen komt er terug calcium binnen in het ER van de eicel en worden de opslagplaatsen opnieuw gevuld, waarbij IP3 dan zorgt voor verdere calcium stijgingen in het cytoplasma van de eicel, de zogenaamde serie van calcium oscillaties die een specifiek patroon vertonen.

De calcium oscillaties duren tot aan het begin van de pronuclei (= voorkernen) vorming in de eicel, en zijn dus cruciaal voor het begin van de bevruchting. De calcium oscillaties zullen downstream een aantal processen op gang brengen (corticale granule reactie, uitstoot 2e poollichaam, vorming van de pronuclei) om uiteindelijk tot succesvolle bevruchting te leiden.
Dit calcium patroon kan in het labo gevisualiseerd worden mits kleuringen van de eicel en gebruik van fluorescentiemicroscopie. Studies bij dieren, maar ook bij de mens hebben aangetoond dat een specifiek calcium patroon niet alleen nodig is om de eicelactivatie op gang te brengen, maar dat het patroon ook invloed heeft op latere gebeurtenissen, zoals embryonale ontwikkeling, en zelfs post-implantatie ontwikkelingspotentieel. De rol van de zaadcel en eicel wordt verder verduidelijkt op de slides 37-38.
EMBRYONALE ONTWIKKELING
Na eicelactivatie worden dus pronuclei gevormd in de bevruchte eicel (= zygote), 1 mannelijk pronucleus of voorkern, en 1 vrouwelijke. De aanwezigheid van 2 pronuclei en twee poollichamen zijn dus representatief voor normale bevruchting en worden 16-20h na start van in vitro bevruchting geëvalueerd.
Diezelfde dag, dag 1 na de bevruchting, zal een eerste mitotische deling plaatsvinden tot 2-cellig stadium, waarna de cellen van het embryo (= blastomeren) zullen blijven verder splitsen. Op dag 2 wordt idealiter een 4-cellig embryo waargenomen, maar dit kan variëren van 2-cel tot zelfs 6 cellen. Op dag 3 wordt een ‘topembryo’ gekenmerkt door de aanwezigheid van 8 blastomeren, die zullen compacteren (in elkaar lopen) op dag 4 en dus een morula vormen.
Op dag 5 wordt dan de zogenaamde blastocyst gevormd, die gekenmerkt wordt door een grote holte met vloeistof (= blastocoele) en reeds 2 types cellen;
trofectoderm cellen → extra-embryonale cellen/weefsels (zoals de placenta)
inner cell mass = binnenste celmassa → eigenlijke individu

EMBRYONALE GENOOM ACTIVATIE
Tijdens de pre-implantatie embryonale ontwikkeling gebeurt er op een bepaald moment nieuwe transcriptie vanaf het embryonale genoom (DNA). Vanaf dan worden aldus nieuwe proteinen aangemaakt die de verdere embryonale ontwikkeling zullen ondersteunen en sturen.
Het moment waarop dit gebeurt is species-specifiek. Bij de muis is dit vanaf het 2-cellig stadium, bij de mens gebeurt dit tussen het 4- en 8-cellig stadium. Dit betekent dus dat de eerste deling bij de muis en de eerste 2 delingen bij de mens gestuurd worden door mRNAs of proteinen reeds aanwezig in de eicel. Dit maakt de eicel vooral/uitsluitend verantwoordelijk voor de kwaliteit van de eerste deling(en).
EICEL vs ZAADCEL
Dus wanneer een slechte embryokwaliteit gezien wordt bij de mens op dag 3 wordt dit meestal aan de eicel toegeschreven om dat tot dan er nog geen transcriptie was van het embryo, en dus geen bijdrage was van het paternale genoom. Anderzijds, wanneer de embryo ontwikkeling verslecht vanaf dag 3, wordt er eerder in de richting van de zaadcel gekeken. Met de vooruitgang van meer gevoeliger geworden moleculaire technieken toont recente literatuur echter aan dat er toch een kleine graad van transcriptie reeds begint bij de bevruchting bij alle species. Waarvoor deze nieuwe transcripten dienen is echter nog niet duidelijk.
PDG vs PGS
Vroeger werd bvb de biopsie gedaan van poollichamen van de eicel. Het grote nadeel hierbij is dat enkel iets over de chromosomale normaliteit van de eicel iets gezegd kan worden, maar niet over de chromosomale normaliteit van het paternale DNA, noch van eventuele nieuwe chromosomale abnormaliteiten die zouden kunnen optreden tijdens de embryonale mitotische delingen.
DAG 3
Bij dag 3 biopsie van 1 of 2 blastomeren zijn de grootste nadelen dat;
(i) dit te invasief is en de verdere embryonale ontwikkeling belemmert en
(ii) dat 1 of 2 blastomeren soms niet representatief zijn voor de chromosomale normaliteit van het ganse embryo.
Dit laatste wordt aangeduid met de term ‘mozaïcisme’, dus dat tegelijkertijd cellen binnen het zelfde embryo chromosomaal normaal kunnen zijn, terwijl andere abnormaal zijn.
DAG 5
Een beter stadium om cellen weg te nemen en te analyseren is het dag 5 stadium, de blastocyst, waarbij verschillende trofectoderm (5 tot 10) cellen, die geen aanleiding geven tot het individu, kunnen weggenomen worden en genetisch geanalyseerd kunnen worden. Voordeel is dat dit veel minder invasief is voor het embryo, maw de verdere embryonale ontwikkeling niet belemmert, en dat er meer cellen kunnen geanalyseerd worden en de techniek dus efficiënter is. Verdere uitleg zie slides.
DIAGNOSTIEK EN BEHANDELING VAN GEFAALDE FERTILISATIE NA ICSI
Met intracytoplasmatische sperma-injectie (ICSI) wordt een gemiddeld bevruchtings-percentage van 70% behaald, echter in 1 tot 5% van de ondernomen ICSI cycli wordt er een compleet bevruchtingsfalen waargenomen. Dit is hoofdzakelijk te wijten aan een ontoereikende eicelactivatie die zowel zaadcel als eicel-gerelateerd kan zijn.
Normaliter induceert de zaadcel een specifiek patroon van calcium (Ca2+)- oscillaties in een rijpe eicel, kenmerkend voor de start van het eicelactivatieproces en de daaruit volgende bevruchting. Fosfolipase C zeta (PLCζ) wordt hiervoor verantwoordelijk geacht.
MOAT
Wanneer gefaalde bevruchting optreedt na ICSI, kan de eicelactiverende capaciteit van zaadcellen bepaald worden door injectie van humane zaadcellen in eicellen van muizen. De muizentest of MOAT, een heteroloog ICSI model, evalueert de capaciteit van humane spermatozoa om muizeneicellen te activeren. Deze diagnostische test wordt meestal aangeboden aan patiënten met een totaal falen van bevruchting of een lage bevruchtingsgraad (<33%) na ICSI. Bij MOAT wordt het percentage van geactiveerde muizeneicellen na ICSI vergeleken tussen zaadcellen van de patiënt en controle zaadcellen met bewezen activeringscapaciteit (positieve controle).
Zo werd tot op heden een classificatie van drie groepen gemaakt op basis van het MOAT resultaat: MOAT groep 1: 20% of minder eicellen geactiveerd (zaadcel-gerelateerde deficiëntie), MOAT groep 2: 21-84% geactiveerde eicellen (vermoedelijk zaadcel-gerelateerde deficiëntie) en MOAT groep 3: 85% of meer eicellen geactiveerd (vermoedelijk eicel-gerelateerde deficiëntie).
Deze MOAT (Muis Oocyt Activatie Test) heeft echter enkele nadelen. Enerzijds zijn er de ethische en juridische kwesties met name de heterologe ICSI, en anderzijds vertoont de test een relatief lage gevoeligheid doordat humaan PLCζ een grotere potentie heeft dan muis PLCζ om Ca2+-oscillaties te induceren in muizeneicellen. Verschillende onderzoeksgroepen werken aan het ontwikkelen van moleculaire methoden (qRT-PCR, immunocytochemie) om een verminderd activatievermogen van deze eicelactiverende factor(en) aan te tonen, tot nu toe met weinig diagnostisch potentieel.
MOCA
Ook werden reeds twee mutaties in het PLCζ gen geïdentificeerd in een patiënt. Onze Gentse onderzoeksgroep heeft recent de toegevoegde waarde van het uitvoeren van een Ca2+-patroonanalyse na heterologe ICSI met muizeneicellen (Muis Oocyt Calcium Analyse, MOCA) aangetoond; echter bij een beperkt aantal patiënten. We hebben recent ontdekt dat ook stalen van een patiënt wiens zaadcellen in staat waren om muizeneicellen in een normale mate te activeren na MOAT (MOAT groep 3), abnormale Ca2+-patronen vertoonden na injectie in muizeneicellen, met lagere frequentie- en amplitudepieken of vroegtijdig eindigende Ca2+- oscillaties. Dus is de MOCA (muis oocyt calcium analyse) een gevoeligere test dan de MOAT om het normaal activerend vermogen van zaadcellen te bepalen.
AOA
Een mogelijke oplossing voor gefaalde bevruchting na ICSI is geassisteerde eicelactivatie (assisted oocyte activation, AOA) tijdens ICSI, waarbij de Ca2+-stijgingen artificieel worden opgewekt. Toch zijn de bevruchtingsresultaten na AOA, welke verschillende onderzoeksgroepen rapporteren, inconsistent. Dit kan te wijten zijn aan de inductie van een niet-fysiologisch Ca2+-patroon door AOA met meestal slechts een of enkele Ca2+-stijgingen. Meestal wordt enkel een calcium ionofoor zoals ionomycine gebruikt die leidt tot een enkele calcium piek. Een meer fysiologische wijze van AOA, zoals het gebruik van het recombinante PLCζ eiwit zou voordelig kunnen zijn, aangezien dierproeven hebben aangetoond dat een correct patroon van Ca2+-oscillaties een grote invloed heeft op latere embryonale ontwikkeling.