Biochimie
Biochimie
Des traceurs radioactifs peuvent être injectés à un patient afin de déterminer l’emplacement d’une tumeur cancéreuse une fois observé à l'aide d’une typographie. (Cancer = Croissance de nutriments dans une cellule)
Les Isotopes et le Radio-Isotopes
- Il y a 92 éléments naturels dans le tableau périodique
- 6 Sont à la base de la vie sur terre
- Le Carbone, L’hydrogène, l’azote, L'oxygène, le phosphore et le soufre
- Les isotopes d’un élément de distingue par un nombre de neutrons différents
- Certains isotopes sont radioactifs et se désintègrent à cause de leur instabilité. Ils émettent des ondes électromagnétiques.
Les Tissus Cancéreux et le radio-isotopes
- Les cellules cancéreuses se divisent rapidement donc consomment une grande quantité de glucose pour effectuer la respiration cellulaire
- Le glucose contenant des radioisotopes de carbones sont injectés à un patient
- L’image produite par la tomographie par émission de position ou la tépographie (TEP) permet de découvrir l’emplacement du glucose injecté. L’endroit de grande concentration de la molécule nous indique le tissu cancéreux.
Qu’est-ce que la biochimie
- L’étude des propriétés et de l’activité des molécules biologiquement importantes
- Qu’est-ce qu’une molecule
- C’est l’assemblage chimique électriquement neutre d’au moin deux atomes
- Qu'est Ce qu'une molécule biologiquement importantes
- Une molécule organique, c'est-à- dire une molécule contenant du carbone presque toujours liés entre eux et l' hydrogène.
Est ce qu'il y a d'autres molécules importantes?
Les forces intramoléculaire
Les interactions qui se produisent entre les atomes à l'intérieur d’une même molécule
ex :
- Les liaisons covalentes entre deux atomes non-métallique dont les électrons de valence sont partagés
- Électronégativité des atomes de termes les liaisons possibles et la structure de la molécule en 3D
Les forces intermoléculaire
- Les liaisons hydrogènes
- Les molécules polaires ont des pôles négatifs et positifs qui attirent les autres molécules de pôles opposées
- Se forment à l'intérieur et entre les molécules
- Liaison faibles
- Les interactions hydrophobes (phobie = Peur)
- Aucune interaction avec l’eau
- Les interactions hydrophiles (phile = Aime)
- Attraction à l'eau
L’importance des ions dans les systèmes biologiques
- Ion = Atome ou group d’atomes avec une charge
- Anion = Ion négatif (-)
- Cation = Ion positif (+)
- ex : Respiration cellulaire et Calcium dans contraction musculaire
Les groupement fonctionnels
La structure et la forme des molécules
- Une formule moléculaire indique le nombre de chaque atome (ex : H2O)
- Une formule développée indique les liaisons simples, doubles, ou triples par un trait simple et done la forme bidimensionnelles (2D)
- Les modèles tridimensionnelles permettent de voir comment la forme influence sur leur fonction
Isomères
Lorsque deux molécules possèdent la même formule moléculaire brute, mais ont des formules développées et stéréochimiques différentes. (ex : C4H10, 2 Methylpropane)
La vie sur terre est basée sur le Carbone
4 Catégories de macromolécules organiques
- Les Glucides
- Monosaccharides
- Disaccharides
- Polysaccharides
- Les lipides
- Glycérol + Acides gras = Triglycérides
- Phospholipides
- Cholestérol
- Les protéines
- Acides aminés
- Les acides nucléiques
- ADN
- ARN
Les Glucides
- À base de C:H:O souvent en proportion 1:2:1 (ex. C6H12O6)
- Souvent représentés par la formule (CH2O)
- Fournissent l’énergie à court terme
- Souvent polaires et solubles dans l’eau
- Monosaccharides (1), disaccharides (2), polysaccharides (plusieurs)
- Monosaccharides
- Isomère Deux types
- Structuraux : Deux composés ou plus ayant le même atomes liés différents ex: Galactose et fructose
- Stéréoisomère : deux composés ou plus dont les atomes sont liés de la même manière, mais disposés différemment dans l’espace ex : Glucose et Galactose
- Glucose, Galactose, Fructose
- Deux Monosaccharides forment 1 disaccharide
- Plusieurs monosaccharides forment des liaisons glycosidiques
- Isomère Deux types
Sources de polysaccharides
- Animaux : Emmagasinent de glucose sous forme de glycogène dans le fois
- Plantes : Emmagasinent le glucose sous forme de cellulose dans la paroi cellulaire et dans l’amidon de la vacuole
Lipides
- Plusieurs C-H insolubles dans l’eau (hydrophobes)
- Constitue une réserve d'énergie que les glucides
- 2,25 fois plus d'énergie que les glucides
- Energie contenue dans les liaisons covalentes C-H
- Energie moins accessible aux cellules donc à long terme
- Recouvrir et isoler les organes internes
- Empêcher la perte de chaleur
- Fournir les éléments nécessaire à la fabrication des membranes cellulaires (phospholipides)
- Formes communes : Graisses, huiles, cires
Les triglycérides
Liaison ester : formé entre -COOH et -OH pour former une molécule d’eau et une nouveau g.f ester
Groupes fonctionnels: acides gras = carboxyle (COOH) et glycérol = hydroxyle
Les acides gras saturés et insaturés
- L’acide palmitique est un exemple d’acide gras saturé
- La chaîne de carbone contient le nombre maximal d’hydrogène donc aucune liaisons double
- Structure droite (linéaire 180º)
- L’acide linolénique est un exemple d’a.g. insaturé
- La chaîne de carbone contient des liaisons double cis entre les carbones
- Structure n’est pas droite car les C=C change la forme de la molécule
Conséquences:
- Gras saturé généralement solide à la température du corps humain
(ex: beurre) 🡪 associé maladies du cœur
- Gras insaturé normalement liquide à la température du corps humain (ex: huile d’olive) 🡪 acides gras polyinsaturé comme les oméga sont associé à la réduction du risque de cardiopathie
L’hydrogénation des gras insaturés
- Processus de conservation des aliments.
- Ajout des atomes d’hydrogène aux gras insaturé pour éliminer les doubles liaisons.
- Parfois les doubles liaisons se reforment à nouveau mais en –trans au lieu de l’orientation naturel –cis.
- Le corps ne possède pas les enzymes capables de décomposer ses liaisons en forment –trans donc les gras solides peuvent s’accumuler dans le corps.
Les Stéroïdes
Structure:
4 anneaux liés à base de carbone
Fonction:
- Le cholestérol compose les membranes cellulaires
- Le cholestérol est un précurseur de plusieurs autres stéroïdes comme les hormones sexuelles
- Ex: testostérone - régule les fonctions sexuelles, fabrication des os et de la masse musculaire
- Ex: œstrogène régule les fonctions sexuelles et stocke la graisse
Les Protéines
Groupe de macromolécules très variées.
Fonctions:
- Catalyser les réactions chimiques (enzyme)
- Soutenir la structure (protéines fibreuses)
- Mouvement de l’organisme (contractions musculaires)
- Réguler les processus cellulaires (l’expression génétique)
- Assurer l’immunité contre les maladies
- Transporter des substances (ions à travers les membranes cellulaires, gaz respiratoire dans le sang)
Role :
- L’insuline une hormone qui règle la glycémie
- L’hémoglobine est la protéine contenu dans les érythrocytes qui transport les gaz essentiels à la respiration cellulaire
- L’ATPase permet de produire des molécules d’ATP à l’aide d’un gradient de concentration d’ion H+
- L’amylase permet l’hydrolyse (décomposition) de l’amidon dans la bouche.
Les Protéines jouent un rôle essentiel
- L’insuline une hormone qui règle la glycémie
- L’hémoglobine est la protéine contenu dans les érythrocytes qui transport les gaz essentiels à la respiration cellulaire
- L’ATPase permet de produire des molécules d’ATP à l’aide d’un gradient de concentration d’ion H+
- L’amylase permet l’hydrolyse (décomposition) de l’amidon dans la bouche.
Acides nucléiques (ADN et ARN)
- Contenir le bagage génétique de l’organisme
- Structurer la croissance de l’organisme
- Permet la production des protéines
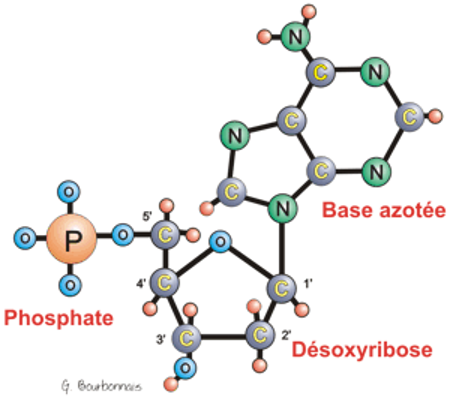
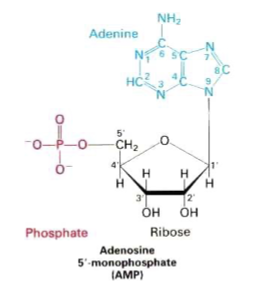
Adenine de ADN Adenine de ARN
ADN (acide désoxyribonucléique): A, T, G, C, ARN (acide ribonucléique): A, U, G, C
Les ARN
ARNt
ARNr
ARNm
Types de réaction chimique associés aux réactions biologiques
- Neutralisations
- Oxydoréductions
- COndensations et Hydrolyses
Un Enzyme
- Une protéine globulaire qui augmente le taux de réaction biochimique en réduisant le seuil d’énergie d’activation (ex. un catalyseur biologique)
L'enzyme abaisse le niveau d'activation de la réaction
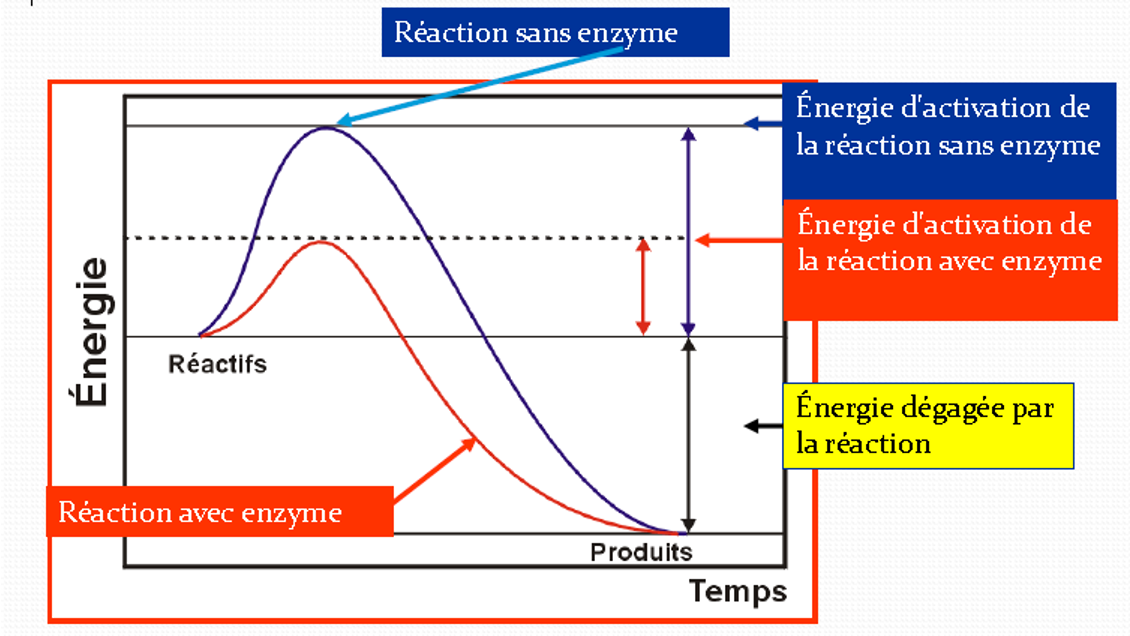
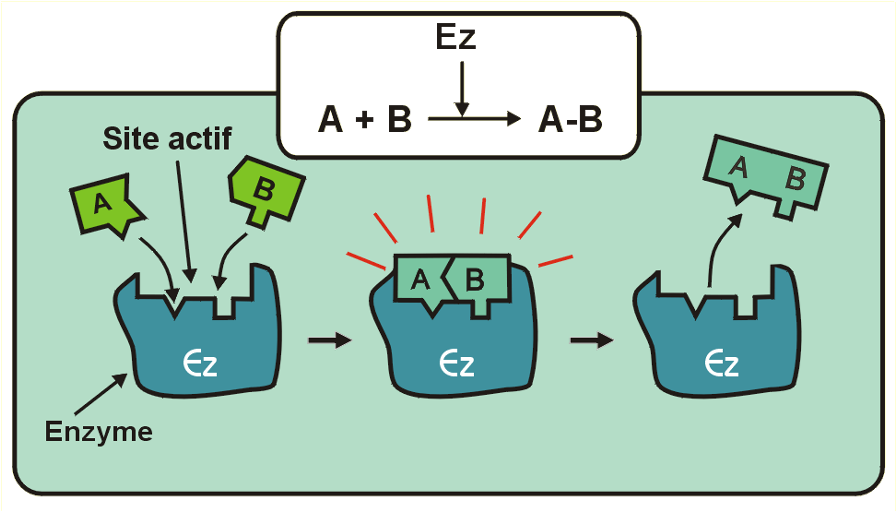
Mode D’action des enzymes
- Les enzymes peuvent catalyser de une à mille réaction à la seconde
- L’enzyme peut resservir à faire à nouveau la réaction
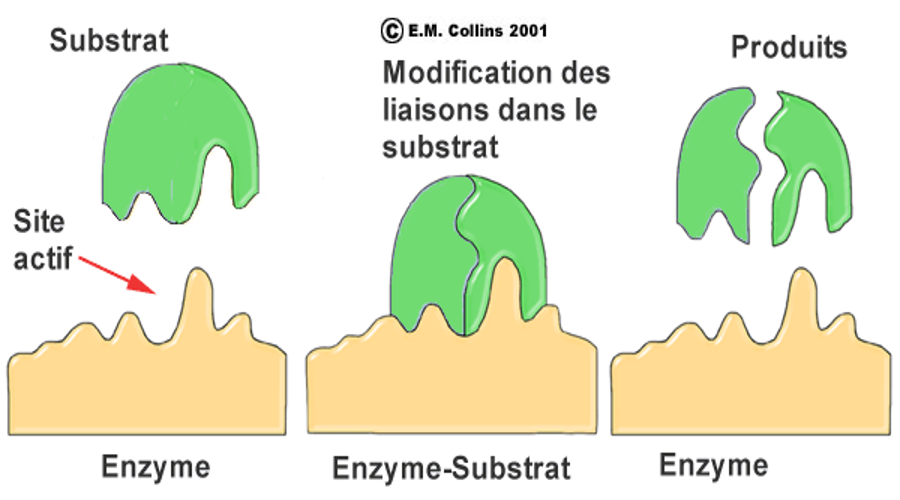
- Enzyme qui lie à son substrat seule
Action enzymatique
Une enzyme fonctionne seulement avec un substrat spécifique et catalyse seulement des réactions spécifiques.
Facteurs Affectant l’activité enzymatique
- PH
- Température
- Concentration de l’enzyme
- Concentration du substrat
- Présence d’activateurs ou d’inhibiteurs
Effet de la temp et le PH de la concentration du substrat
- La température, le pH et la concentration du substrat peuvent tous avoir un impact sur l’activité enzymatique.
- Ci-dessus trois graphiques qui démontrent comment un facteur peut affecter l’activité enzymatique.
Métabolisme
- Le produit d’une première réaction chimique est souvent le substrat d’une autre réaction chimique. Les réactions chimiques qui se déroulent successivement forment une voie métabolique.
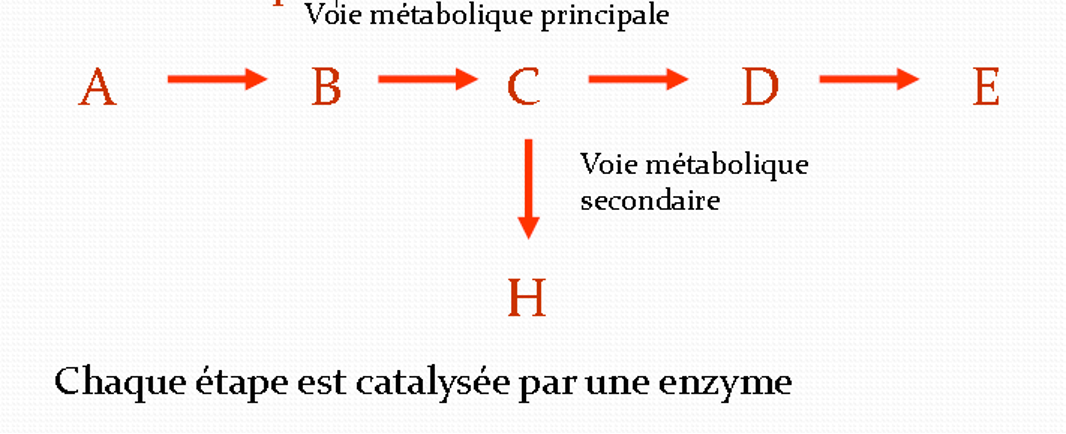
EX : Au cours de la glycolyse, une molécule de glucose est transformée en deux molécules de pyruvate. Chacune des 9 étapes est catalysée par une enzyme spécifique.
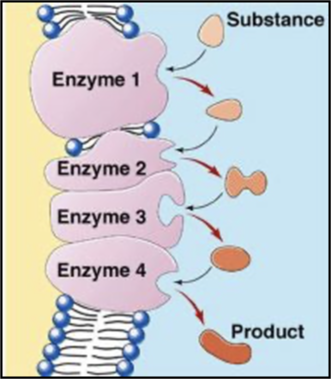
Les enzymes d’une chaîne métabolique peuvent être intégrées dans la membrane de la cellule ou d’un organite de la cellule. Le produit d'une enzyme est immédiatement disponible à l'enzyme suivante qui doit le transformer. (Produit d’enzyme 1 devient substrat de enzyme 2)
Cofacteurs et co-enzymes
Cofacteur = petite molécule se fixant sur le site actif. Sans le cofacteur, le site actif est inactif.
Beaucoup de cofacteurs sont des ions métalliques (Cu, Zn, Mn, etc.)
Certains sont de petites molécules organiques (par rapport à la taille de l’enzyme); on les appelle alors coenzymes.
Beaucoup de vitamines sont des coenzymes (ou sont des précurseurs de coenzymes)
Inhibiteurs
- Substances chimiques qui peuvent inhiber le fonctionnement d’une enzyme
- L’inhibiteur agit en se liant chimiquement à l’enzyme. La liaison de l’inhibiteur avec l’enzyme empêche l’enzyme de fonctionner. L’inhibiteur peut se fixer dans le site actif ou ailleurs sur l’enzyme.
- Un inhibiteur enzymatique peut être :
- Irréversible : la liaison de l’inhibiteur avec l’enzyme est irréversible; l’enzyme ne peut plus fonctionner.
- Réversible : la liaison de l’inhibiteur avec l’enzyme est réversible; si la concentration en inhibiteur diminue, l’inhibiteur peut se séparer de l’enzyme à laquelle il s’était lié.
Un inhibiteur réversible peut être compétitif ou non compétitif :
- Un inhibiteur compétitif ressemble chimiquement au substrat et entre en compétition avec lui pour se fixer au site actif. L’inhibiteur compétitif diminue donc le rendement de l’enzyme.
- Un inhibiteur non compétitif se lie à l’enzyme (site allostérique) et altère la conformation de l’enzyme de sorte que le substrat ne peut plus se lier ou se lie moins bien au site actif. La réaction catalysée est arrêtée ou ralentie.
Statines
Les statines comme l'atorvastatine (Lipitor® ) ou la lovastatine (Mevacor®) sont des médicaments utilisés pour abaisser le taux de cholestérol sanguin chez les patients qui ont un taux élevé de cholestérol. Ce sont des inhibiteurs compétitifs de la HMG-CoA réductase, une enzyme qui joue un rôle capital dans la synthèse du cholestérol dans le foie.
Retro-Inhibition
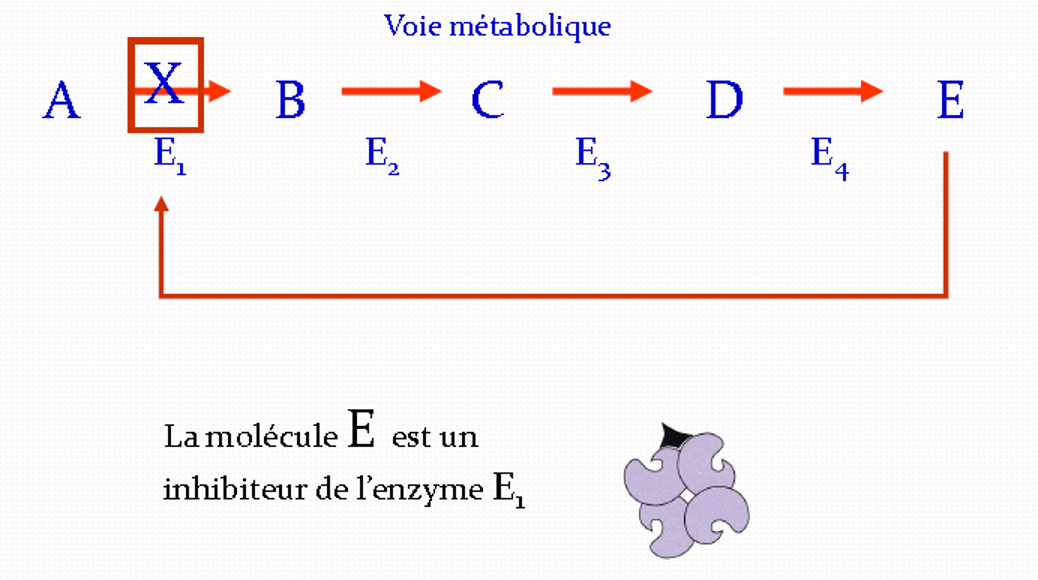
CHAPITRE 2
Les eucaryotes ont une structure cellulaire beaucoup plus complexe que les procaryotes
Cellules eucaryotes
Contiennent un noyau et des organites, Paroi cellulaire (cellulose chez les plantes), Membrane cellulaire, Cytoplasme, Noyau, Ribosomes 80s (Milliers), Réticulum endoplasmique (RE), Appareil de Golgi, Mitochondries, COMPARTIMENTÉES
- 10 à 1000 µm (micromètre) en général
- Nombreux organites internes faits de membranes.
- Matériel génétique délimité par une membrane = noyau
Structure générale
- Dans une région isolée
- Contient les gènes (ADN)
- Chromatine ou chromosome
- La membrane nucléaire est double.
- Nucléoles : lieu de l’assemblage des ribosomes.
- Contient des pores pour les échanges.
- Permet la production de l’ADN à l’abris des fonctions de la cellule.
- Contient l’information génétique
- Sous forme de chromosomes lors de la mitose. Le reste du temps, l’ADN est sous forme de chromatine.
- Le nombre de chromosomes varie par espèce
- Les chromosomes contiennent des brins d’ADN et des protéines (histones)
Cytoplasme :
- Zone entre la membrane cellulaire et le noyau.
- Comprend :
- Le cytosol (la solution)
- Les organites
- Des inclusions: dépend du type de cellules (ex: pigments, lipides, mucus etc.)
Réticulum endoplasmique :
- Réseau de tubes ou canaux entre le noyau et la membrane.
- Rôle de transport interne des matériaux
- Divisé en 2 types: Lisse et Rugueux
- 2 types sont présents dans les cellules.
- Le RE rugueux est normalement plus près du noyau.
RER et Ribosomes
- Fonction : synthèse des protéines
- Donnent l’aspect rugueux du RER
Ribosomes (80s)
- Structures sans membrane externe.
- Responsable de synthèse des protéines.
- Libres dans le cytoplasme ou attachés au RE.
- Toujours composé d’ARNr et de protéines.
- Formés de 2 sous-unités
REL (lisse)
- Pas dans toutes les cellules
- Pas de ribosome (donc pas de synthèse de protéines).
- Dégrade le cholestérol.
- Détoxication (beaucoup dans le foie).
Appareil de Golgi
- Apparence de sacs aplatis empilés l’un sur l’autre.
- Gère la distribution des protéines dans la cellule
- Emballe et modifie les protéines arrivant du RER.
- Fabrique de la membrane.
Mitochondrie
- Ordre de grandeur : similaire à une bactérie
- Contiennent leur propre ADN (Chromosome circulaire)
- Produit ses propres ribosomes. (70s)
- Membrane double
- La membrane interne est repliée avec des crêtes.
- Les crêtes offrent une plus grande surface pour les échanges.
- Espace interne – Matrice
- Zone entre les membranes – Espace inter-membranaire.
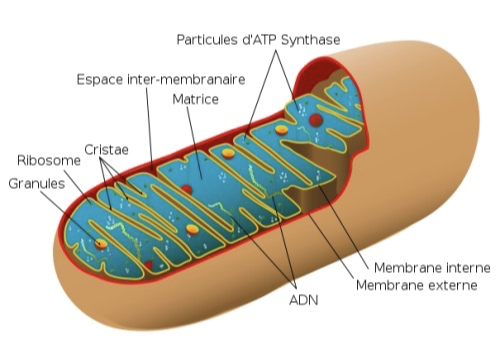
- Fonctions:
- Transformation énergétique.
- Fabrication d’une molécule énergétique appelée ATP grâce à la respiration cellulaire.
- Quantité
- Proportionnelle au travail cellulaire (métabolisme cellulaire).
Production d’énergie par respiration cellulaire
Matière organique (nutriment) + O2 -> Matière inorganique + H2O + Énergie
Tous les glucides peuvent se transformer en glucose.
Glucose = "carburant" dans la respiration cellulaire
1 glucose + 6 O2 -> 6 CO2 + 6 H2O + Énergie
L’énergie est récupérée pour former de l’ATP
Chloroplastes
- Chez les algues et les plantes.
- Contient membranes doubles
- Ordre de grandeur – similaire à une bactérie
- Contient son propre ADN et des ribosomes (70s)
- Lieu de la photosynthèse
Lysosomes :
Centre de digestion intracellulaire.
Sac (vésicule) contenant des enzymes hydrolytiques.
Catalyse les protéines, les acides nucléiques, les lipides et les glucides.
Se fusionnent aux organites endommagés ou vieux pour les détruire.
Bon recycleur.
Intérieur acide
Peroxysomes :
Sacs membranaires
Contiennent des enzymes oxydatives (oxydases)
Dégrade le peroxyde d’hydrogène grâce à une enzyme appelée catalase
Dégrade d’autres molécules toxiques comme l’alcool
Peuvent fabriquer certaines molécules (ex. acides biliaires)
Vacuoles
La vacuole est un organite uniquement présent dans la cellule végétale, les pollens, les cellules fongiques.
Les vacuoles sont des compartiments délimités par une membrane remplis d'eau et contenant diverses molécules inorganiques et organiques telles que des enzymes.
La vacuole n'a pas de forme ou de taille particulière, sa structure variant en fonction des besoins de la cellule.
Cytosquelette
- Formé de protéines fibreuses
Cellules végétales et animales (Les deux végétale et animale ont des mitochondrie)
La membrane cellulaire
- Elle sépare les organismes unicellulaires de leur environnement externe aqueux et les cellules des organismes multicellulaires du liquide extracellulaire
- Sélective et dynamique pour faciliter ou empêcher l’entrée et la sortie des substances
Historique des découvertes
1900: les molécules liposolubles pénètrent dans les cellules plus rapidement que les molécules hydrosolubles.
Conclusion: la membrane doit être constitué de lipides
1925: Analyse chimique démontre que la membrane est composé d’une bicouche de phospholipides
1940: des substances non lipidiques traversent la membrane donc il doit avoir autres composantes comme des protéines
1950: première image d’une membrane cellulaire
Confirme la structure en sandwich (bicouche)
1970 : Frye & Edidin : les protéines diffusent librement de manière latérale dans la membrane cellulaire
1972: Singer et Nicolson propose le modèle de la mosaïque fluide
Singer et Nicolson 1972 proposent la théorie de la mosaïque fluide
La membrane plasmique est constituée d'une bicouche lipidique, de protéines et de glucides associés de diverses manières à la bicouche.
Le modèle de la mosaïque fluide
- Des protéines insérées dans une bicouche de phospholipides avec la partie polaire sortant de la membrane
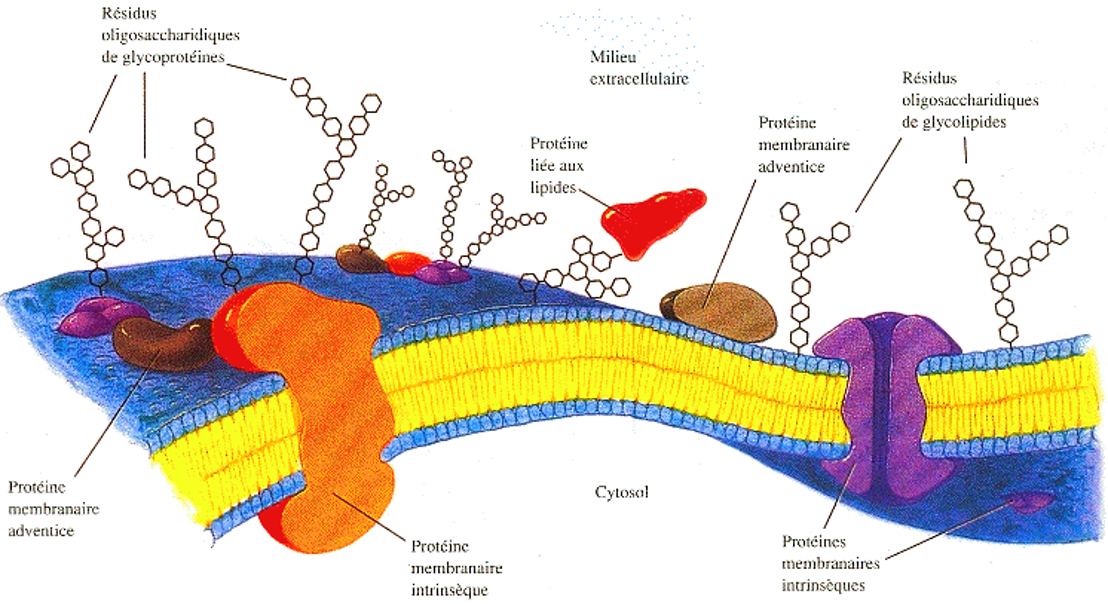
La Fluidité de la membrane (Cholesterol aide à la fluidité membranaire)
Le rôle des phospholipides insaturés:
Plus la membrane est composée de phospholipides insaturés, plus la membrane est fluide
Le rôle de la température:
Une augmentation de température augmente la fluidité de la membrane.
Une diminution de température à un point critique peut solidifier une membrane (plus la membrane est composée de phospholipides saturés, moins elle peut maintenir une fluidité aux températures faibles)
*Certaines plantes peuvent modifier la composition de leurs membranes selon les saisons.
Le rôle du cholestérol
- Contrôle la fluidité en fonction de la température
- Le groupement fonctionnel: -OH donne à la molécule une caractéristique hydrophile
- Presque absent chez les procaryotes
- Absent chez les plantes
- Présent chez les animaux
Transport Membranaire
- Perméabilité sélective
- Transport passif (pas d'énergie requis)
- Diffusion simple
- Diffusion facilitée
- Par Canal
- Par transporteur
- Osmose (H2O et son mouvement)
Perméabilité sélective
- La bicouche lipidique est perméable :
- aux molécules très petites (H2O, CO2, O2)
- aux molécules liposolubles (se dissolvent dans la partie lipidique)
- La bicouche lipidique est imperméable :
- aux grosses molécules et à la plupart des molécules chargées
- aux ions (K+, Na+, Cl-, ...)
Transport passif d’O2 et de CO2
- Ex. Alvéoles d’un poumon
Transport passif
- Transport qui ne nécessite pas de dépense d’énergie:
- Diffusion simple
- Diffusion facilitée
- Osmose
Diffusion simple
- Une substance diffuse suivant son gradient de concentration, c.-à-d. de la zone la plus concentrée vers la zone la moins concentrée jusqu’à l’atteinte d’un équilibre entre les concentrations.
- L’énergie cinétique des molécules explique la diffusion.
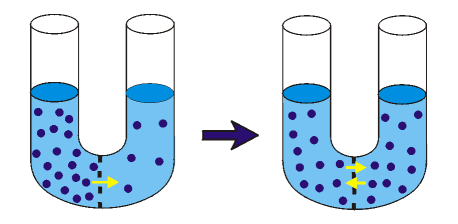
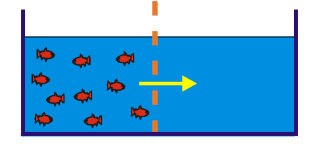
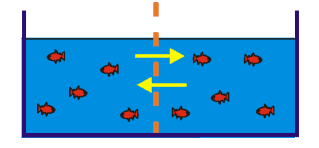
Osmose (diffusion passive) d’H2O
- L’eau passe du côté moins concentré en soluté (hypotonique) vers le côté plus concentré en soluté (hypertonique) dans le but de rendre les deux côtés isotonique (de même concentration)
Application
Les tissus ou les organes devant être utilisés dans des procédures médicales doivent être plongés dans une solution de même osmolarité que le cytoplasme pour éviter l’osmose. (Elle aiment isotonique)
Diffusion facilitée par canal
- La diffusion se fait par l’intermédiaire d’une protéine membranaire.
- Ce processus ne requiert pas de dépense d’énergie et se fait toujours selon le gradient de concentration.
- Change pas de forme
Diffusion facilitée par transporteur
- La diffusion se fait par l’intermédiaire d’une protéine membranaire. Ces transporteurs sont très sélectifs.
- Ce processus ne requiert pas de dépense d’énergie et se fait toujours selon le gradient de concentration.
- change de forme
Application
Les canaux potassiques pour la diffusion facilitée dans les axones
Transport actif primaire
- Nécessite une dépense d’énergie :
- Pompage de solutés assuré par un transporteur protéique qui utilise l’ATP comme source d’énergie.
- Le déplacement des substances se fait contre le gradient de concentration
Transport actif secondaire
- Nécessite une dépense d’énergie :
- Pompage de solutés assuré par un gradient électrochimique.
- Le déplacement d’une substance se fait dans le sens du gradient de concentration et une autre molecule se déplace contre son gradient.
Application
La structure et la fonction des pompes à sodium–potassium dans les axones (parties d’un neurone)
Transport vésiculaire (actif)
- Nécessite une dépense d’énergie (ATP)
- Deux principaux modes :
- Exocytose
- Endocytose (phagocytose et pinocytose)
Exocytose
Permet l’excrétion de substances (hormones, déchets, mucus, etc) via des vésicules.
Ces vésicules se fusionnent à la membrane plasmique.
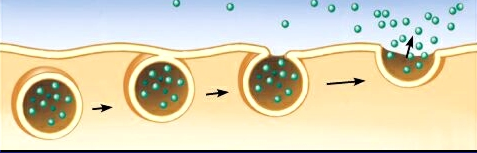
Endocytose
Permet à de grosses particules ou des macromolécules d’entrer dans la cellule.
Phagocytose (absorption d’une grosse particule) et pinocytose (absorption de liquide contenant des solutés)
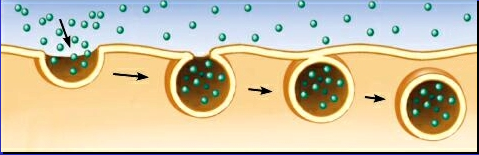
Phagocytose
Globule blanc qui digère une bactérie