Tema 2: Metabolismo glucídico
Glucólisis. Reacciones de la Glucólisis.
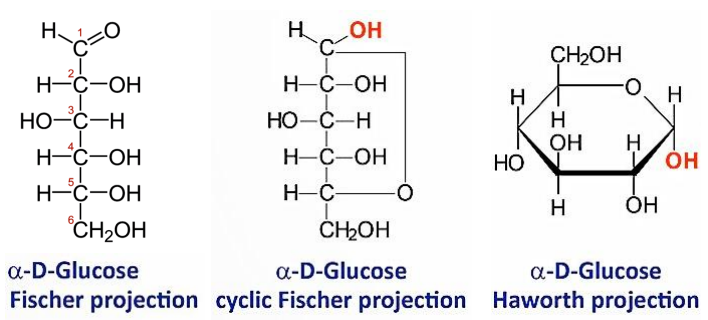
Glucosa
El único azúcar circulante en sangre y que será utilizado por todos los tejidos periféricos es la glucosa. Su principal función es la producción de energía (ATP).
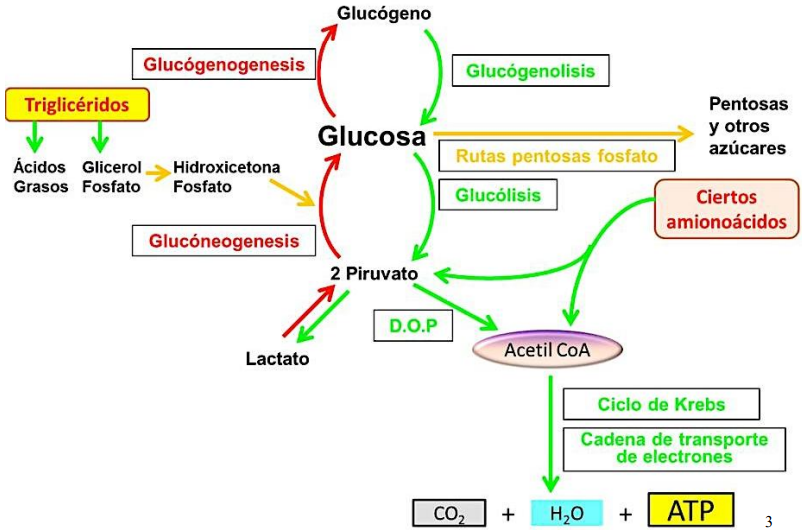
Metabolismo intermediario de la glucosa
Glucólisis
Proceso oxidativo por el que la glucosa (6C) se rompe en 2 moléculas de piruvato (3C).
La ruta más importante del catabolismo de la glucosa.
Ruta universal presente en todas las células de nuestro organismo y en la mayoría de los seres vivos.
Ocurre en el citosol.
NO requiere oxígeno.
Se utiliza con dos finalidades: obtener energía (ATP) e intermediarios metabólicos como fuente de carbono para diversas rutas anabólicas.
Consta de 10 reacciones divididas en 2 fases: preparatoria y de beneficios (Pay-off).
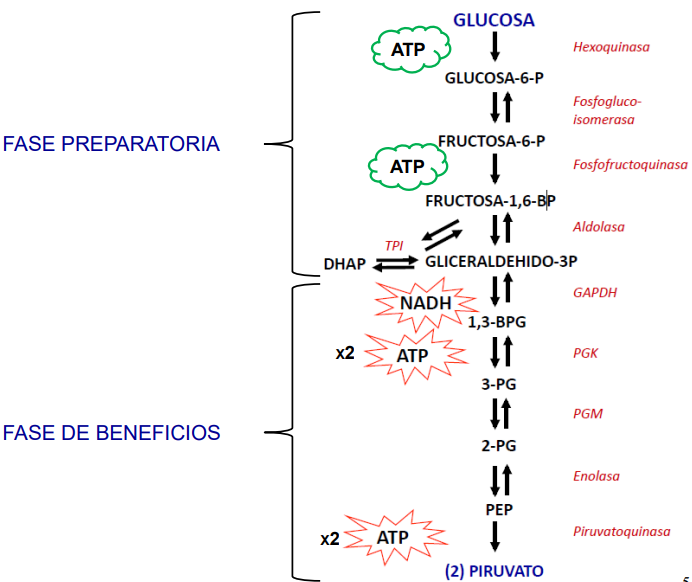
Fase respiratoria
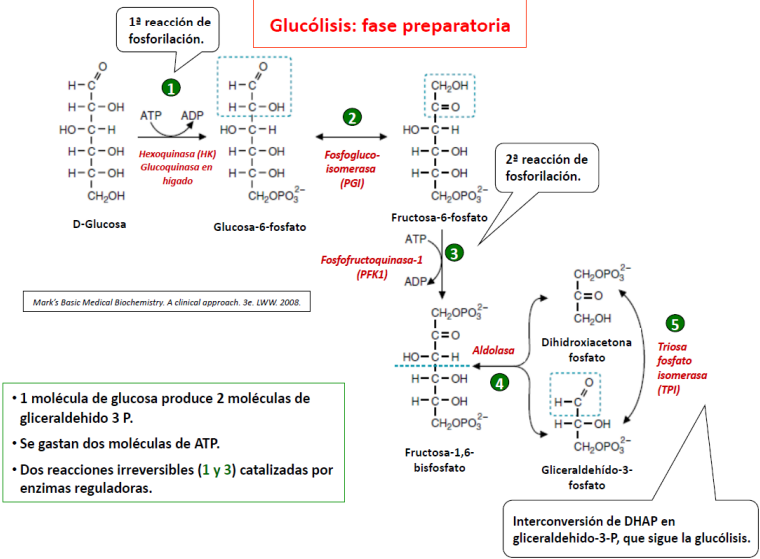
1º Reacción: fosforilación de la glucosa
La glucosa que entra en las células es fosforilada por transferencia de un fosfato desde ATP.
Catalizada por la hexoquinasas (hay diferentes isoenzimas). Requiere Mg2+ que neutraliza la carga negativa del ATP y facilita la transferencia del fosfato. Glucosa-6-fosfato ya no puede salir de la célula.
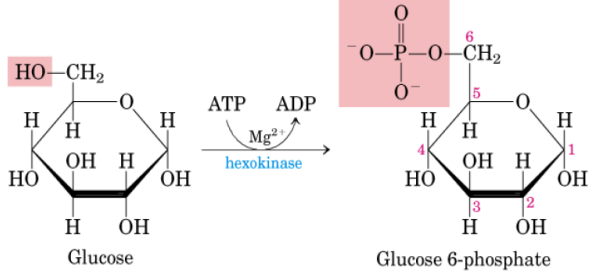
2º Reacción: isomerización de glucosa a fructosa
La Glucosa-6-fosfato se isomeriza a Fructosa-6-fosfato (piranosa → furanosa).
Es una reacción reversible y próxima al equilibrio.
Catalizada por la fosfohexosa isomerasa, que promueve la apertura del anillo de la piranosa, la isomerización de aldosa a cetosa y su ciclación en forma de furanosa.
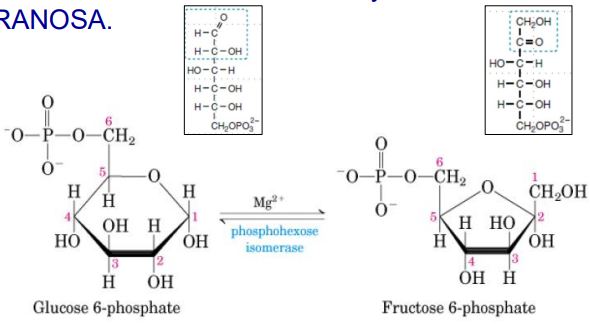
3º Reacción: fosforilación de la fructosa-6-fosfato
La Fructosa-6-fosfato recibe un grupo fosfato en posición 1 generando Fructosa-1,6-bifosfato.
Es una reacción IRREVERSIBLE y requiere ATP y Mg2+ .
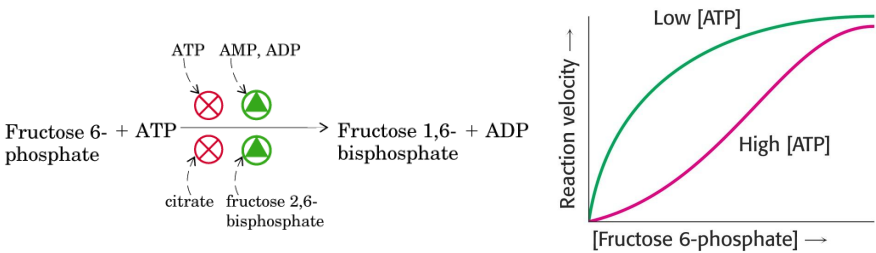
Catalizada por la Fosfofructoquinasa 1 (PFK-1).
Es una enzima fuertemente regulada, respondiendo de forma alostérica a diferentes metabolitos celulares.
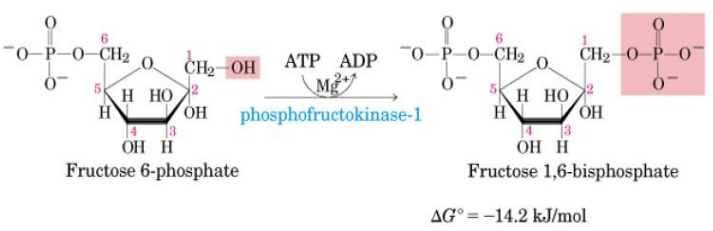
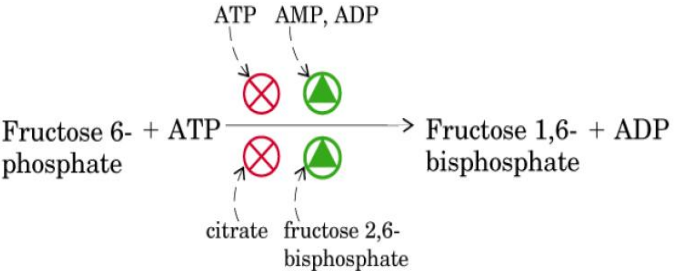
Este es el paso más importante desde el punto de vista de la regulación.
En reprimida por:
ATP (indica que ya hay suficiente energía)
Citrato (inhibición del ciclo del Krebs).
Es activada por:
AMP o ADP (falta energía)
Fructosa 2,6-Bifosfato (aumenta afinidad por el sustrato).
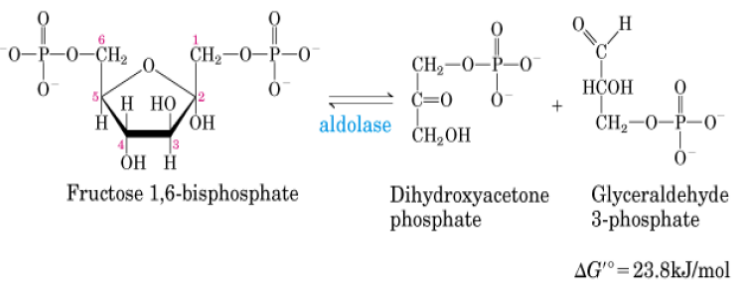
4º Reacción: rotura en triosas
La Fructosa-1,6-bisfosfato se rompe en 2 triosas fosfato (Dihidroxiacetona fosfato y gliceraldehido-3-fosfato ) por un proceso de condensación aldólica reversible.
Catalizada por la Fructosa-1,6-bifosfato aldosa, aunque se suele abreviar por aldosa.
Se han descrito varias isoformas de la aldosa.
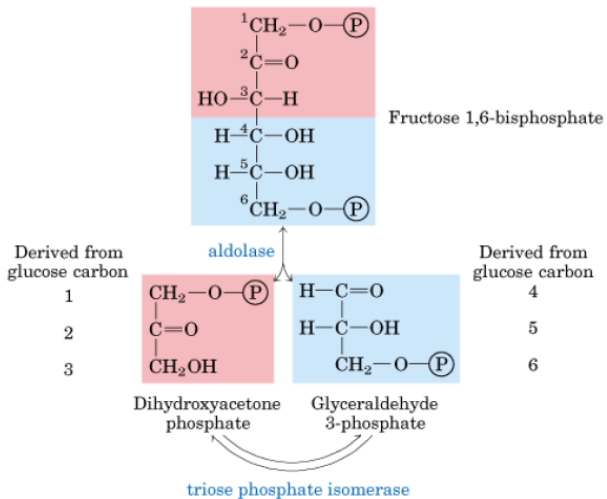
5º Reacción: productos se interconvierten entre sí
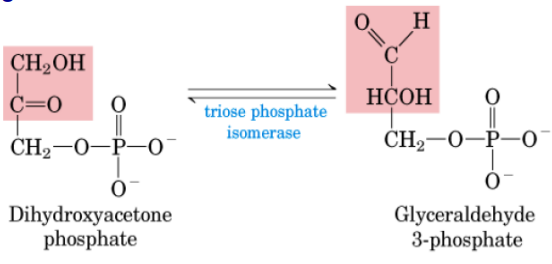
Los productos de la reacción anterior: dihidroxiacetona fosfato (DHAP) y gliceraldehido-3-fosfato (3-PGA) se interconvierten entre sí.
Catalizada por la Triosa-fosfato isomerasa.
Es un punto de encrucijada metabólica: La DHAP puede servir para la síntesis de triacilgliceroles. El 3-PGA prosigue la glucólisis.
Fase de beneficios
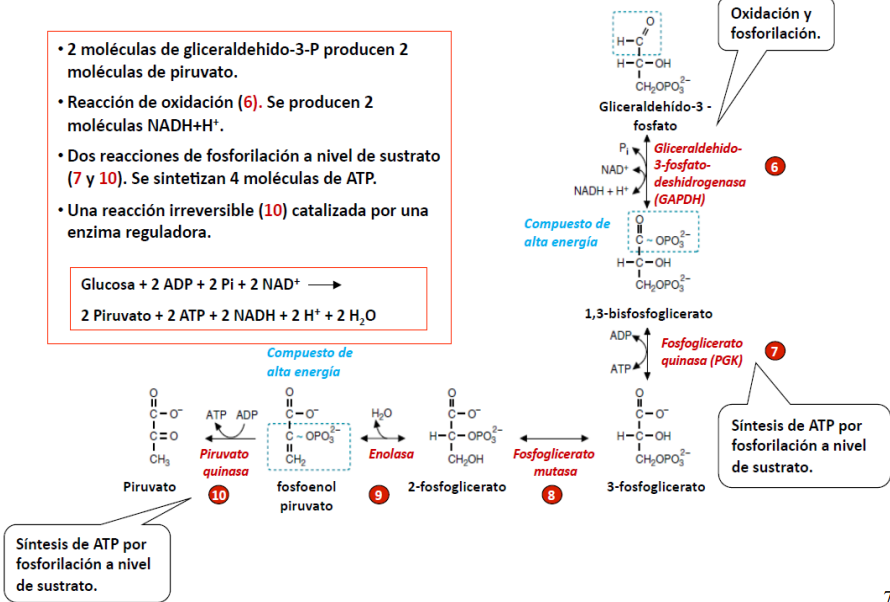
6º Reacción: adición del primer P inorgánico
La primera en la que se incorpora un P inorgánico.
Necesitará un cofactor para obtener poder reductor (por la actuación de la deshidrogenadsa → H+ )
Se produce la oxidación del 3-PGA acoplada a la reducción del NAD+ y su fosforilación con fosfato inorgánico (Pi) para dar 1,3-bisfosfoglicerato (1,3-BPG).
Catalizada por la gliceraldehído-3-fosfato deshidrogenasa.
Esta reacción es reversible.
La energía se almacena en un enlace acil-fosfato rico en energía.
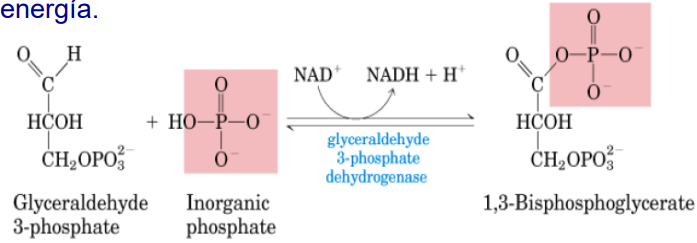
7º Reacción: fosforilación a nivel de sustrato
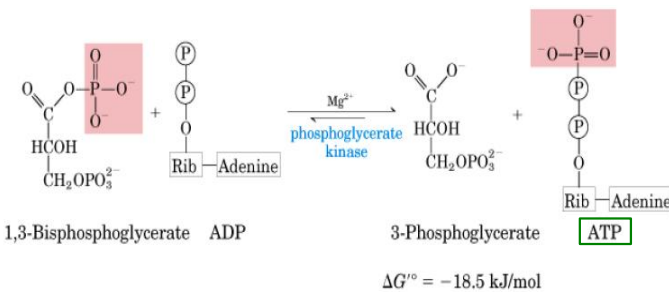
Es una fosforilación a nivel de sustrato, se pasa un grupo fosfato de una molécula a otra, obteniendo ATP de manera directa.
El potencial de transferencia del 1,3-BPG es superior al ATP, por lo que se puede transferir un grupo fosfato desde el 1,3-BPG hasta el ADP.
Catalizada por la fosfoglicerato quinasa.
El conjunto de las dos reacciones 6 y 7 constituye la primera fosforilación a nivel de sustrato en la glucólisis generando 3-PG.
Como estamos trabajando con 2 moléculas simultáneamente, obtendremos 2 ATPs.
8º Reacción: transforación de 3-PG a 2-PG
EL 3-PG se transforma en 2-fosfoglicerato (2-PG).
Catalizada por la fosfoglicerato mutasa.
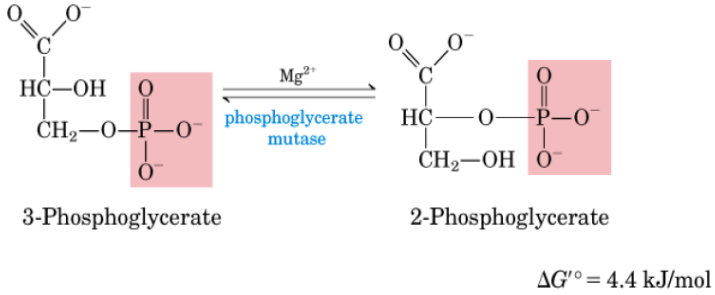
Hay un periodo transitorio de 2,3-Bifosfoglicerato
9º Reacción: pérdida de agua
La posición 2 del grupo fosfato en el 2-PG es crítica para la siguiente reacción, que consiste en la reacción de hidrólisis del 2-PG y la pérdida de una molécula de agua a partir de los átomos asociados a los C 2 y 3.
Catalizada por la enolasa.
Es una reacción reversible que conlleva la producción de fosfoenolpiruvato (PEP), un compuesto rico en energía.
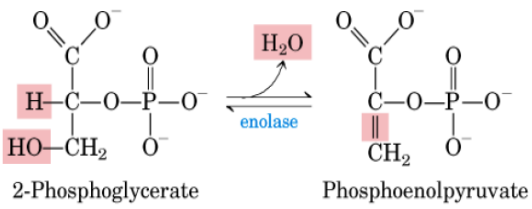
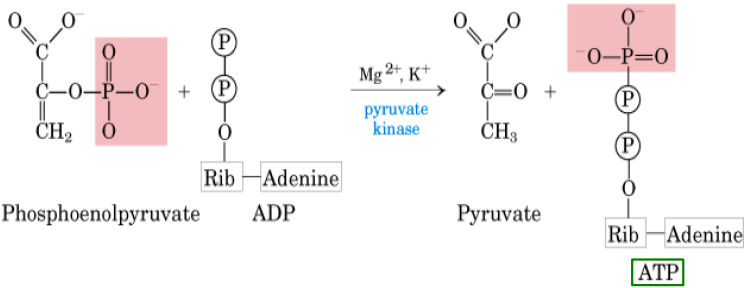
10º Reacción: segunda fosforilación a nivel de sustrato
La transferencia del grupo fosfato desde el PEP hasta el ADP es la segunda fosforilación a nivel de sustrato y la última reacción de la glucólisis.
Catalizada por la piruvato quinasa.
Es una reacción exergónica e irreversible
Se obtienen otros 2 ATPs.
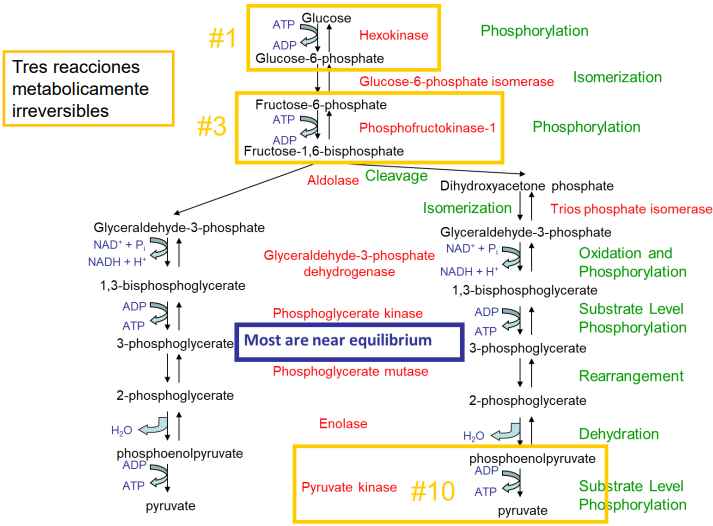
Resumen

Regulación de la glucólisis
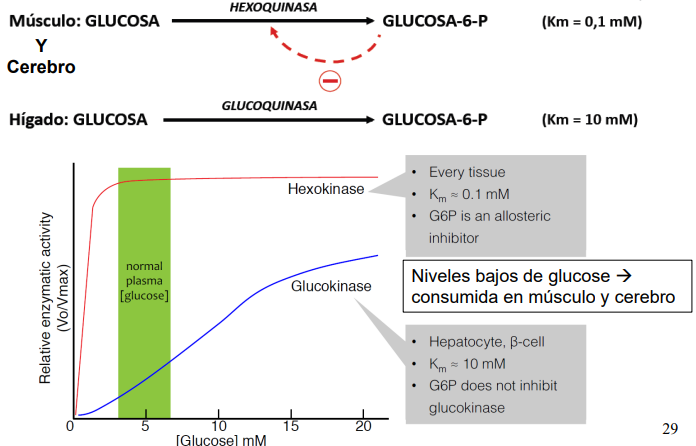
Hexoquinasa
Cataliza la fosforilación de glucosa a glucosa 6-fosfato (G6P).
Se inhibe por su propio producto (G6P)
Existen 2 tipos:
Hexoquinasa, que actúan en músculo y cerebro y tiene una Km inferior (+ afinidad → satura a menor concentración).
Glucoquinasa, Km mucho más superior y no se inhibe por G6P.
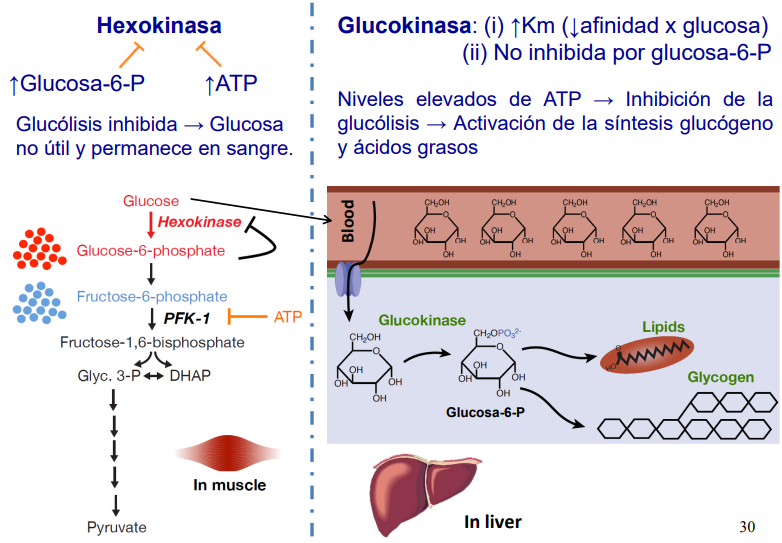
Si se está en reposo, se acumula ATP, que inhibe la glucólisis, haciendo que se quede en fruct6p, la cual es reversible y vuelve a glucosa 6P, que inhibe a la hexokinasa al acumularse. como el musculo y cerebro no usa la glucosa, la mandan a la sangre. Esto hace que la glucokinasa haga glucosa 6P, almacenándola como glucógeno o lípidos.
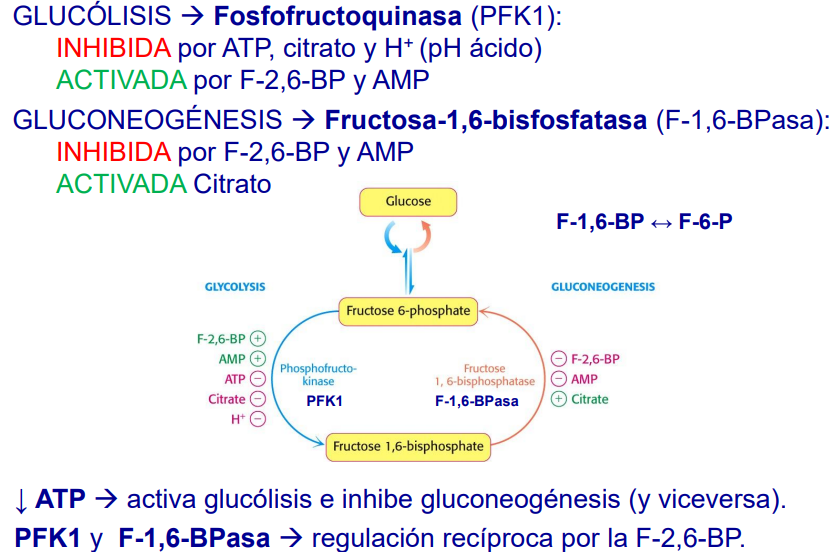
Fosfofructoquinasa-1
PFK-1 cataliza la fosforilación de F6P a F1,6-BP.
ATP → modulador alostérico negativo (indica que ya hay energía)
AMP → modulador alostérico positivo (indica falta de energía)
Citrato → modulador alostérico negativo (inhibición del ciclo del Krebs)
F-2,6-BP → modulador alostérico positivo (aumenta la afinidad por el sustrato, favoreciendo estado R)
Bajo pH disminuye la actividad enzimática.
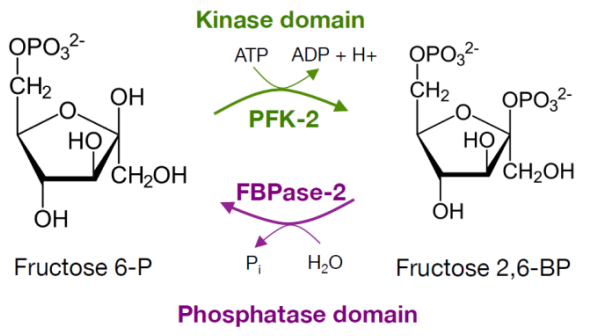
F-2,6-BP es el activador más importante, ya que es sintetizado por PFK2. Esta es una enzima bifuncional, teniendo tanto un dominio quinasa que fosforila, como un dominio fosfatasa que desfosforila. Esto permitirá que regule los niveles de F-2,6-BP, inhibiendo la glucólisis.
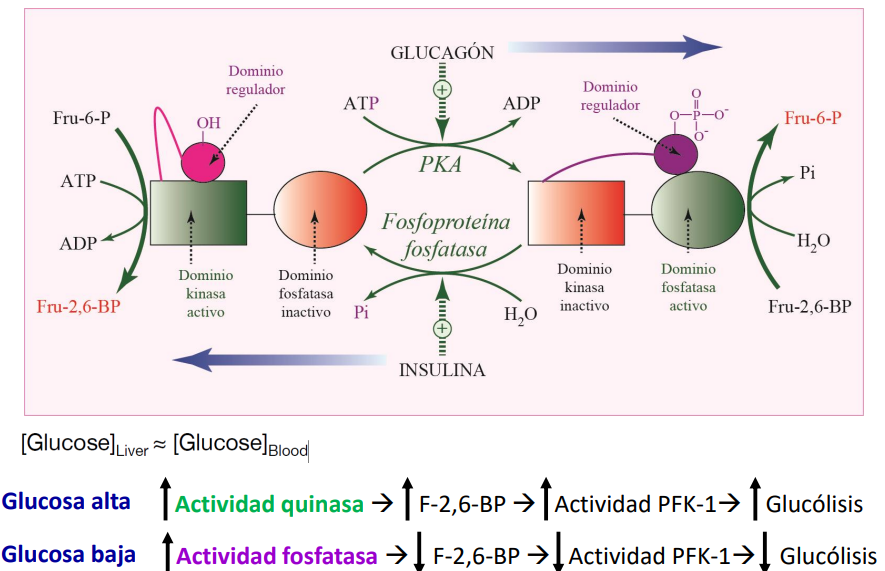
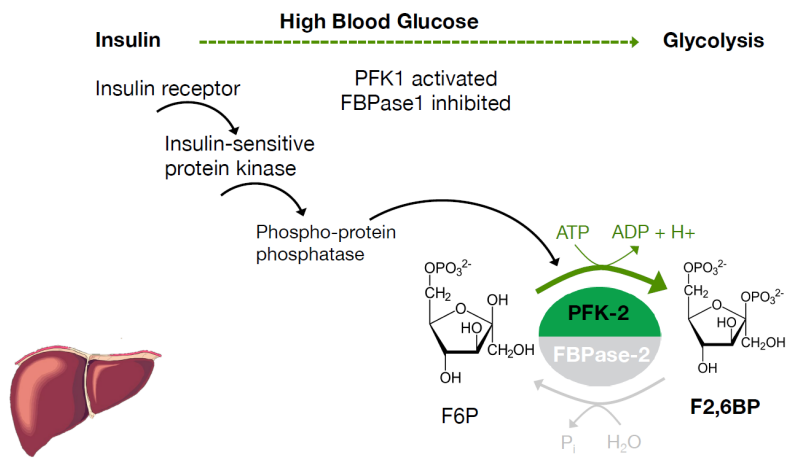
Si la glucosa en sangre es alta, la insulina indica a la proteína fosfatasa que desfosforile el dominio fosfatasa y se activa en su lugar el dominio quinasa, que hace que se genere más F2,6BP, la cual es una activadora de PFK-1, y lo induce a que la glucólisis continúe y se consuma más glucosa.
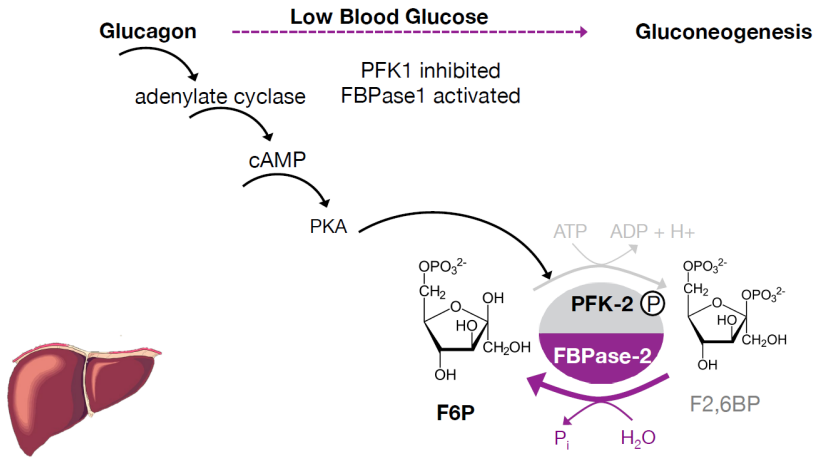
Si es baja, PKA fosforilará el dominio fosfatasa, el cual desfosforila F2,6BP a F6P. Esto hace que se reduzca la actividad de PFK-1, con ello deteniendo el proceso de la glucólisis.
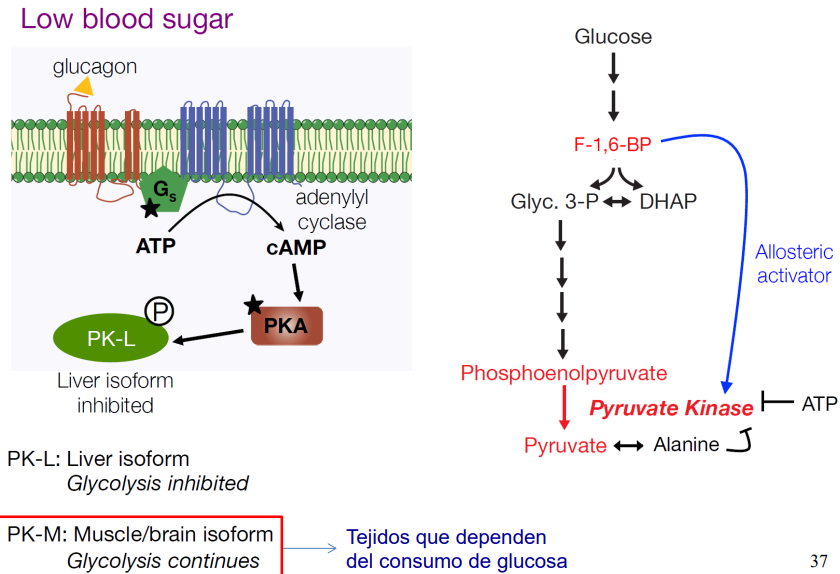
Piruvato quinasa
Existen 2 isoformas de la enzima:
Isoforma hepática L (PK-L): que se regula por la fosforilación → glucagón (inactiva PKL) y desfosforilación → insulina (activa PKL).
Isoforma muscular y cerebral M (PK-M): no se ve afectada por modificaciones covalentes.
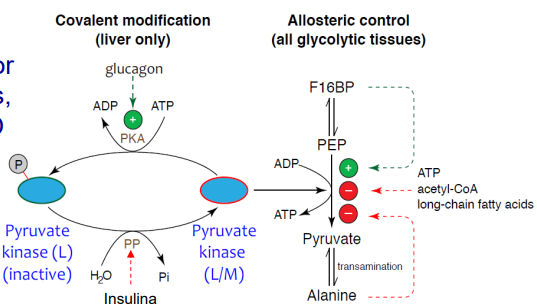
Ambas isoformas tienen regulación alostérica:
ATP → modulador alostérico negativo.
Alanina → modulador alostérico negativo.
F-1,6-BP → modulador alostérico positivo (sintetizada a partir de piruvato).
Destinos fermentativos del Piruvato
Cuando se da la degradación del piruvato en tejidos carentes de mitocondrias, o en hipoxia, en ven de oxidarse en CO2 y H2O, el piruvato servirá para generar NAD para la glucólisis.
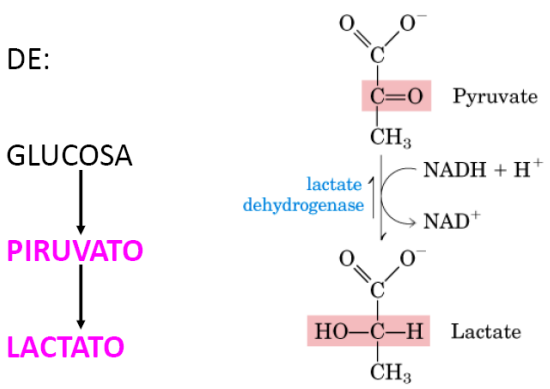
Fermentación láctica
El piruvato se reduce en lactato por la lactato deshidrogenasa (LDH), recuperando NAD+.
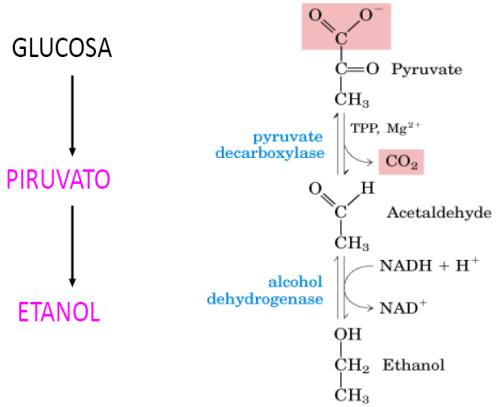
Fermentación alcohólica
El piruvato se puede transformar en alcohol por:
Descarboxilación: la piruvato descarboxilasa utiliza TPP y Mg2+ como cofactores.
Reducción: pasa de acetaldehído a etanol por la alcohol deshidrogenasa.
Entrada de otros azúcares en la ruta glucolítica
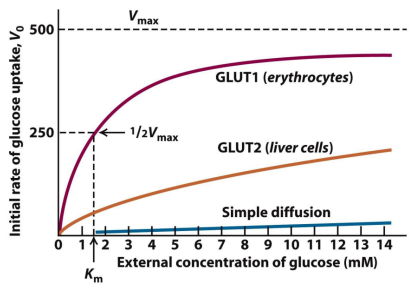
Entrada de glucosa en las células
Se da por transportadores, que permiten la entrada de mns de manera pasiva (a favor de gradiente). Destacan:
GLUT1 (eritrocitos): transporta glucosa y galactosa(Km = 1-2 mM). Su elevada afinidad se debe a que como no tienen mitocondrias, necesitan hacer glucólisis para obtener energía.
GLUT2 (hígado, páncreas): transporta glucosa, galactosa y fructosa (Km = 15-20 mM).
GLUT4 (músculo y T. adiposo): presenta una alta afinidad por glucosa (Km = 5 mM). Dependiente de insulina. Gasta energía pero no necesita tanta como los eritrocitos.
Entrada de disacáridos en la glucólisis
Los 3 disacáridos más importantes en los alimentos son:
Sacarosa: D-fructosa + D-glucosa es uno de los productos naturales más abundantes.
Lactosa: principal componente de la leche, D-galactosa + D-glucosa.
Maltosa: edulcorante artificial y se obtiene de la digestión del almidón. 2 moléculas de D-glucosa.
Estas se suelen hidrolizar en las microvellosidades intestinales, generando:
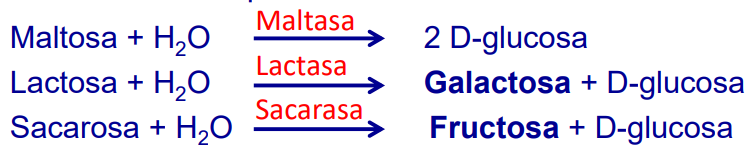
Entrada de la galactosa en la glucólisis
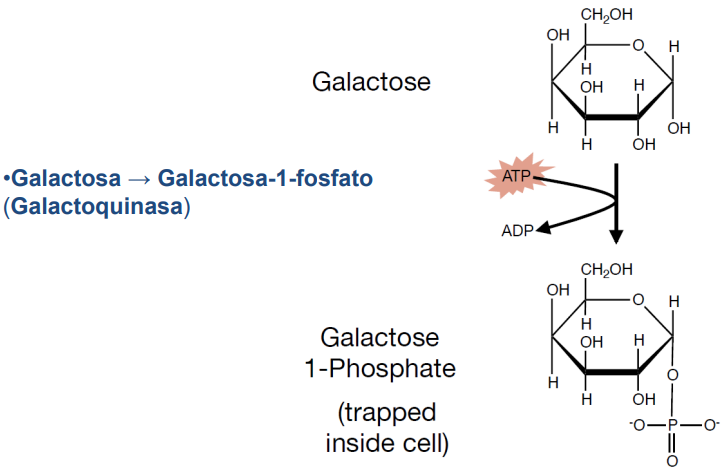
Hay que transformarla en Glu6P para metabolizarla.
Galactoquinasa fosforila Gal a Gal1P.
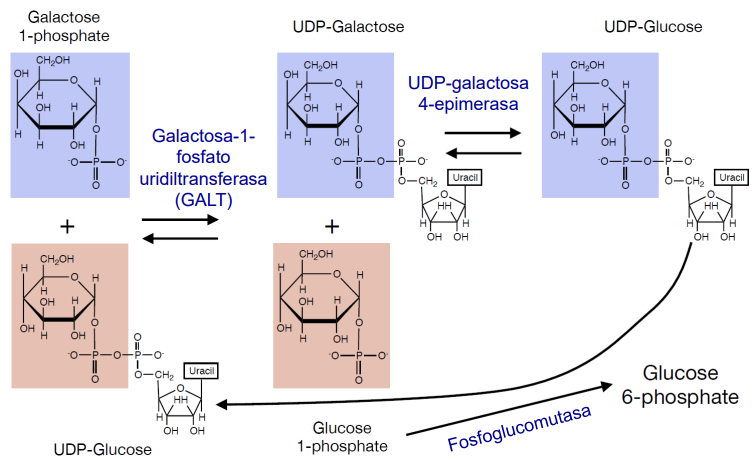
Gal1P reacciona con UDP-Glucosa:
UDP se incorpora en 1 y epimeriza Gal1UPD a Glu1UDP.
G1P se isomeriza en G6P.
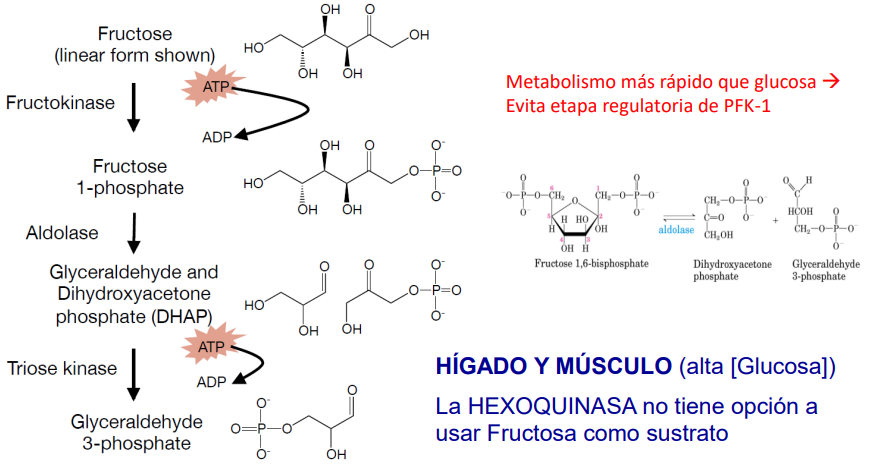
Entrada de la fructosa en la glucólisis
La hexoquinasa cataliza su fosforilación, generando Fru6P. Pero la hexoquinasa tiene mucha más afinidad por la glucosa, por lo que sólo catalizará la reacción donde la glucosa escasee (adipocitos).
En el hígado y músculo de vertebrados:
La fructoquinasa fosforila a F1P.
La aldosa B la disocia en DHAP y Gliceraldehído → G3P.
G3P entra en la glucólisis o en la síntesis de triglicéridos.
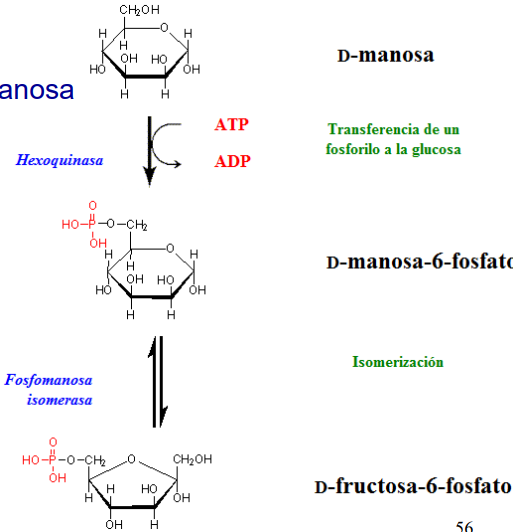
Entrada de manosa en las células
Se produce en 2 etapas:
Se fosforila a M6P por una hexoquinasa.
Se isomeriza a F6P por la fosfomanosa isomerasa.
#ff00f6
Gluconeogénesis
Ruta anabólica que permite la biosíntesis de glucosa a partir de precursores no glucídicos.
Principales sustratos en humanos (precursores de 3-4 átomos de C):
Lactato: procedente de la fermentación anaerobia de la glucosa en músculo y eritrocitos.
Aminoácidos (especialmente alanina): procedentes de la dieta o proteólisis muscular.
Propionato: procendente de la degradación de ác. grasos y AAs.
Glicerol: procedente del catabolismo de TAG en adipocitos.
La gluconeogénesis en hígado y riñón ayuda a mantener el nivel de glucosa necesario en sangre para que cerebro y músculos puedan extraer la suficiente glucosa para atender a sus demandas energéticas.
Etapas enzimáticas de la gluconeogénesis
La mayoría de las reacciones se comparten con la glucólisis (pero en sentido opuesto), utilizándose las mismas enzimas. Pero hay 3 reacciones que están muy alejadas del equilibrio (exergónicas), siendo por lo tanto irreversibles.
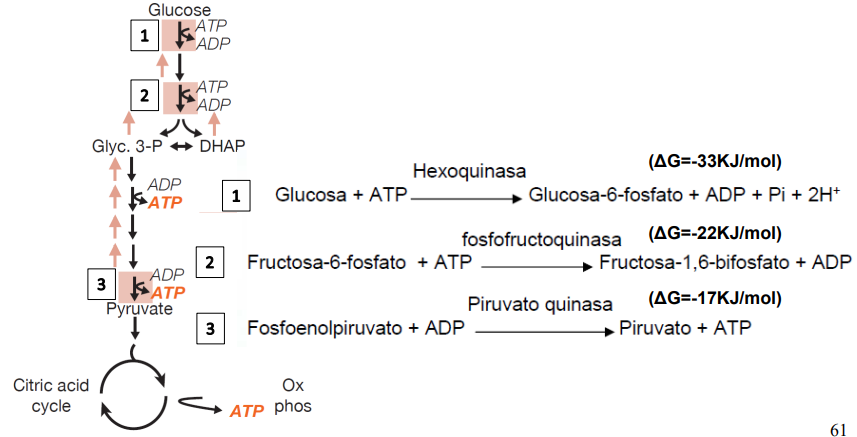
Cual es el único metabolito que sale de la gluconeogénesis y no de la glucólisis → oxalacetato.
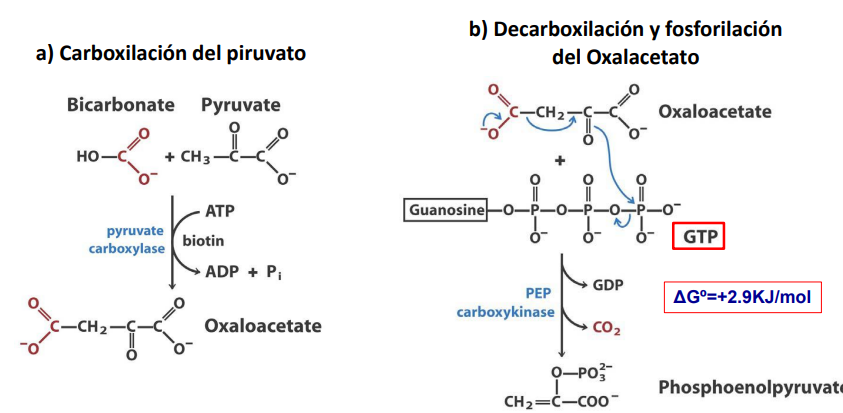
Transformación de piruvato en fosfoenolpiruvato
Tiene 2 etapas:
El piruvato se carboxila en oxalacetato con gasto de ATP, catalizado por la Piruvato carboxilasa, que necesita acetil-CoA como activador alostérico.
El oxalacetato se descarboxila y fosforila para dar fosfoenolpiruvato, con una hidrólisis de GTP, catalizado por la PEPCK (Fosfoenolpiruvato carboxiquinasa).
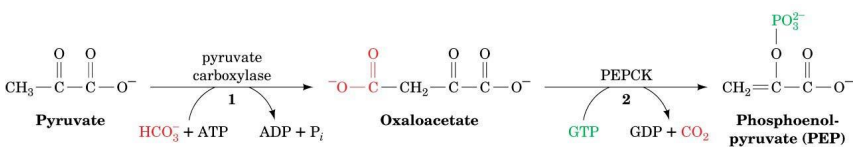
Este proceso ocurre en la matriz mitocondrial. Es una de las reacciones anapleróticas que se utilizan para reponer intermediarios del ciclo del ácido cítrico.
Para continuar la gluconeogénesis el oxalacetato debe salir de la mitocondria al citosol donde se produce el resto de las reacciones. Esto se debe a que el piruvato no tiene un transportador específico pero el malato sí.
Para poder ser transportado, se transforma en Malato por la malato deshidrogenasa.
Una vez se ha salido de la mitocondria, el malato vuelve a oxidarse a oxalacetato.
La Fosfoenolpiruvato carboxiquinasa (PEPCK), necesita acoplar la hidrólisis GTP.
Se libera la molécula de CO2 que se había unido en el paso anterior, por lo que no hay fijación neta de carbono. La PEPCK requiere Mg2+ o Mn2+ y es fácilmente reversible.
Transformación de F-1,6-Bifosfato en F-6-Fosfato
El PEP es metabolizado por los enzimas de la glucólisis pero en sentido inverso hasta llegar a fructosa 1,6-bifosfato. En la gluconeogénesis, este paso se evita mediante la hidrólisis del P1 y está catalizada por la Fructosa-1,6-Bisfosfatasa (F-1,6-Bpasa):
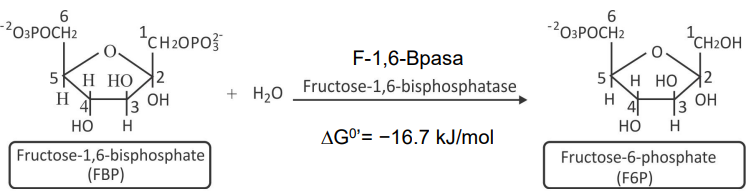
Este enzima requiere Mg2+ y es el principal punto de control de la gluconeogénesis. Moduladores alostéricos:
Negativos: AMP y Fructosa 2,6-bisfosfato.
Positivos: ATP y Citrato.
Transformación de glucosa 6-Fosfato en glucosa
La glucosa-6-fosfato no puede convertirse en glucosa por la acción de la hexoquinasa. Por lo que la Glucosa-6- Fosfatasa, es la que cataliza la hidrólisis del grupo fosfato de la posición 6.
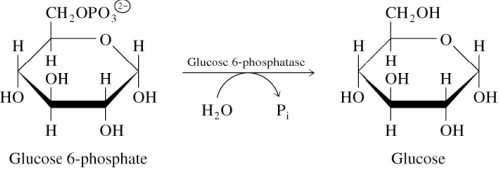
Esta enzima se expresa en órganos de regulación de la glucemia, como los el hígado y en menor grado en los riñones.
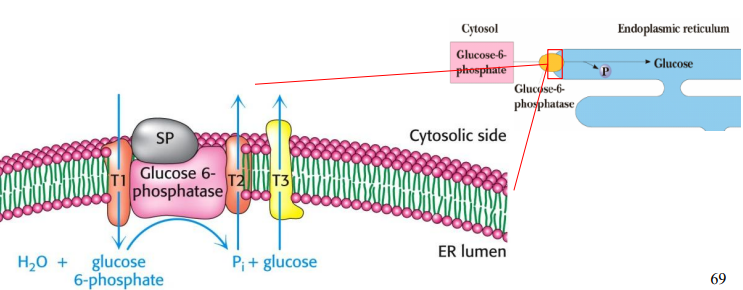
Este proceso ocurre en el lumen del RE, ya que a su membrana está unida esta enzima. Las Glucosa-6-fosfatasa precisa de la presencia de una proteínas estabilizadora de Ca2+ y la utilización de transportadores específicos de glucosa-6-fosfato (T1) que introducen este metabolito en el retículo, así como de transportadores de Pi (T2) y glucosa (T3) que transportan los productos de la reacción de vuelta al citosol.
Regulación de la gluconeogénesis
La gluconeogénesis y glucólisis están coordinadas para que no se den ambas a la vez.
A nivel de sustrato:
La velocidad de la glucólisis esta controlada por concentración de glucosa.
La velocidad de la gluconeogénesis está controlada por concentración de lactato y otros precursores gluconeogénicos (Alanina, glicerol y propionato)
Glucólisis: la Piruvato Quinasa se induce por moduladores alostéricos (F1,6BP) y por fosforilación y se inhibe por altos niveles de ATP y alanina.
Gluconeogénesis: la Piruvato carboxilasa se activa por acetil-CoA y se inhibe por ADP. Análogamente la Fosfoenolpiruvato carboxiquinasa se inhibe por ADP.
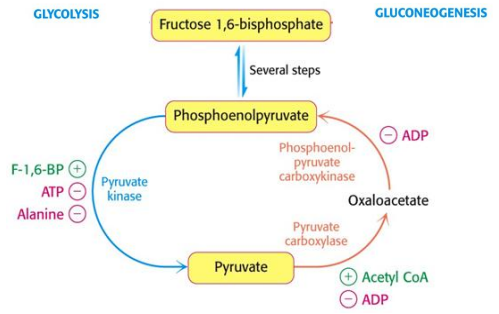
Acetilcoa → indica un estado en el que las necesidades energéticas están cubiertas, por el funcionamiento del ciclo de krebs, indicando que se pueden dar procesos de síntesis de glucosa.
Regulación hormonal en humanos
Es un proceso coordinado a nivel sistémico con otros procesos metabólicos antagónicos como la glucólisis, síntesis de Ac. grasos, síntesis de glucógeno…
Esto se estimula por la siguientes hormonas:
Glucocorticoides (estrés).
Glucagón (baja glucemia).
Adrenalina (emergencia).
Y se inhibe por:
Insulina (alta glucemia).
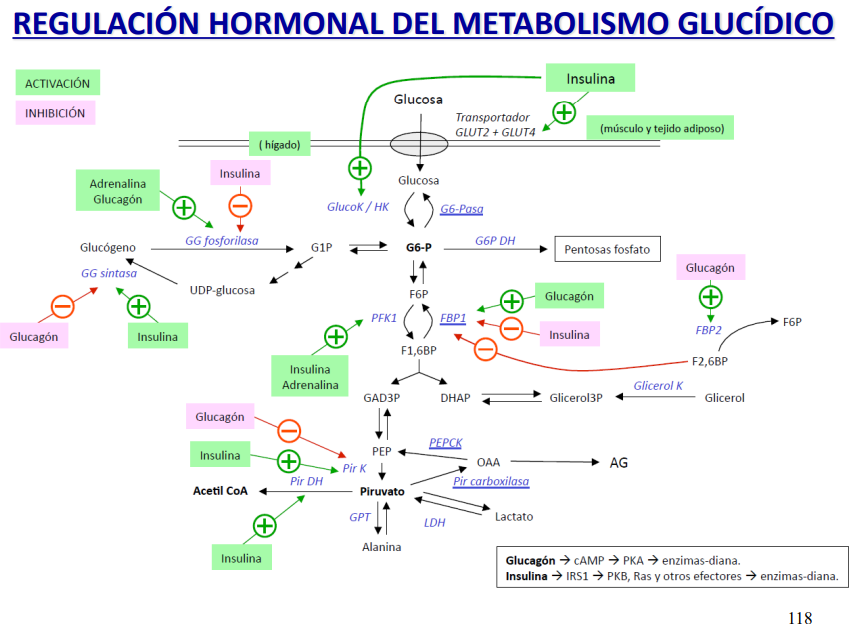
La cantidad de los enzimas clave en la regulación de la glucolisis y gluconeogénesis están sujetos a control hormonal:
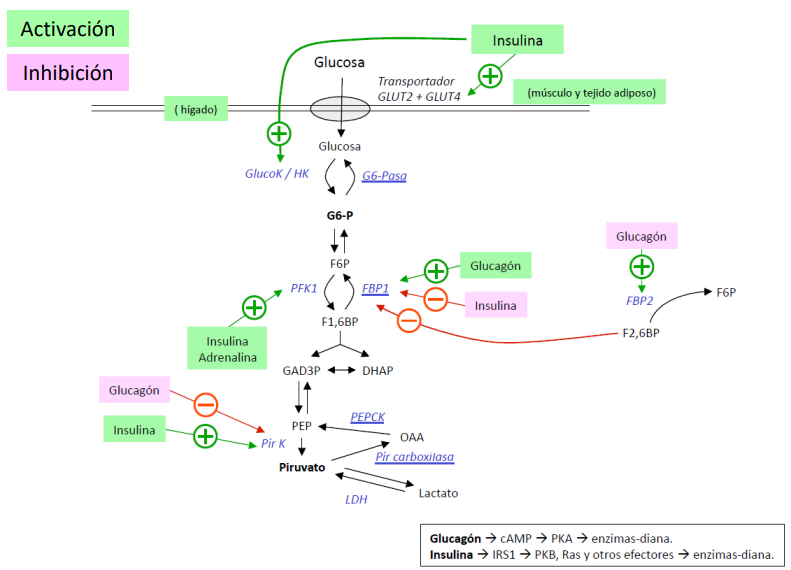
Insulina: induce la expresión de PFK-1, PK y la PFK-2, activando de este modo la glucólisis. Además, reprime piruvato carboxilasa, PEPCK y glucosa-6-fosfatasa, reprimiendo la gluconeogénesis.
Glucagón: inhibe la expresión de PFK-1, PK y la PFK-2 reprimiendo la glucólisis y estimula la síntesis de PEPCK y F-1,6- bifosfatasa, favoreciéndose de este modo la gluconeogénesis.
Corticoides: inducen piruvato carboxilasa, PEPCK y glucosa-6-fosfatasa favoreciendo la gluconeogénesis.
Cortisol: favorece la proteólisis muscular, la liberación de sustratos gluconeogénicos y la gluconeogénesis
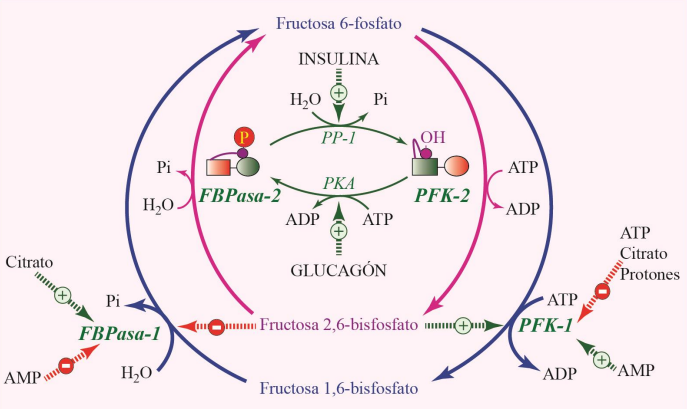
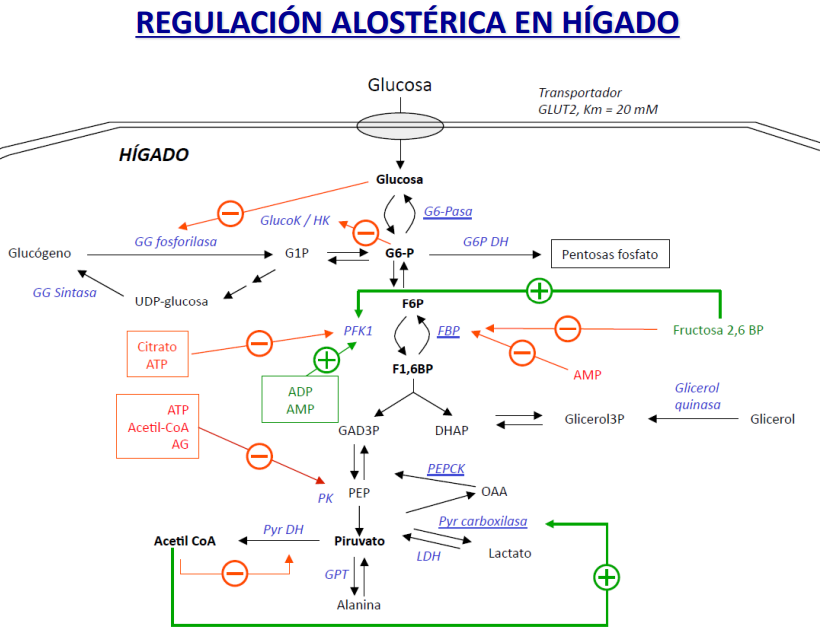
Regulación enzimática
Si hay elevada F2,6 esto activará a la PFK1 (gluconeogénesis) e inhibirán a las fosfatasas (glucólisis).
Metabolismo del Glucógeno y su regulación
Estructura y almacenaje
El glucógeno es un polímero grande y ramificado, compuesto por glucosas unidas en α-1,4 y α-1,6 (ramificación cada 10 residuos).
Se va degradando por enzimas en los extremos reductores.
Se almacena en hígado y músculo:
Hígado → mantiene lvls de glucosa sanguíneos.
Músculo → almacena para autoconsumo.
Metabolismo
Degradación → lleva a la obtención de Glucosa-6-fosfato (G6P) que tiene tres destinos:
glucólisis
ruta de las pentosas fosfato
o transformarse en glucosa libre en el hígado y liberarse en el torrente sanguíneo.
Síntesis → necesita la formación de UDP-glucosa, a partir de Glucosa-1-fosfato (G1P), que se añade a los extremos no reductores del glucógeno.
Glucogenólisis (degradación)
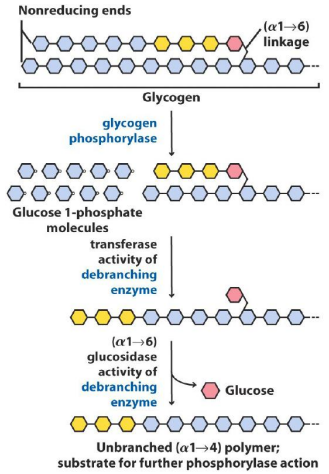
La ruptura del glucógeno requiere de la acción de varias enzimas que se unen simultáneamente a los gránulos de glucógeno para su rotura por fosforolisis:
Glucógeno fosforilasa: libera la última glucosa de la cadena lineal en forma de G1P.
Enzima desramificante: tiene 2 actividades enz., puede transferir 3 residuos de los 4 restantes a una cadena lineal; puede romper enlaces alfa1→6 de la glucosa restante, dejándola libre en el medio sin fosforilar.
Fosfoglucomutasa: transforma las G1P en G6P para su posterior metabolismo.
Glucógeno fosforilasa:
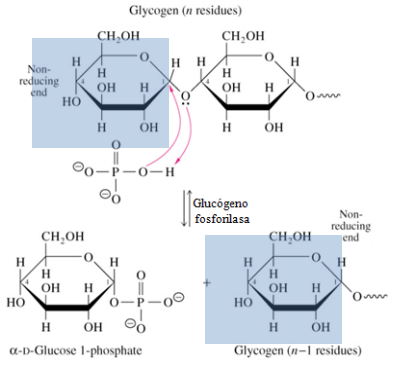
Cataliza la reacción de fosforólisis, rompiendo enlaces α-1,4 entre dos moléculas de glucosa, en el extremo NO reductor del glucógeno, gracias a la adición de ortofosfato (Pi), para producir G1P.
Ventajas:
Proceso energéticamente ventajoso ya que se libera el azúcar fosforilado sin gastar ATP (1 de cada 10 no).
G1P no podrá difundir fuera de la célula ya que está cargada negativamente en condiciones fisiológicas.
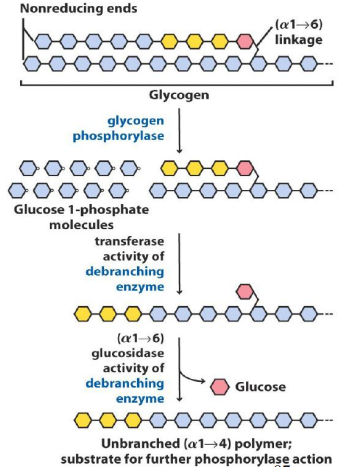
Enzima desramificante:
La glucogeno fosforilasa cesa su actividad al alcanzar la glucosa a 4 residuos de la ramificación. La desramificante continúa, dando lugar a 2 actividades:
Transferasa: transfiere el bloque de 3 residuos de glucosa desde la rama externa a otra, dejando sola la glucosa con enlace α-1→6.
Glucosidasa: hidroliza el enlace α-1→6 y libera la molécula de glucosa no unida a fosfato. Posteriormente, por la hexoquinasa, entrará en la ruta glucolítica o será exportada a la sangre.
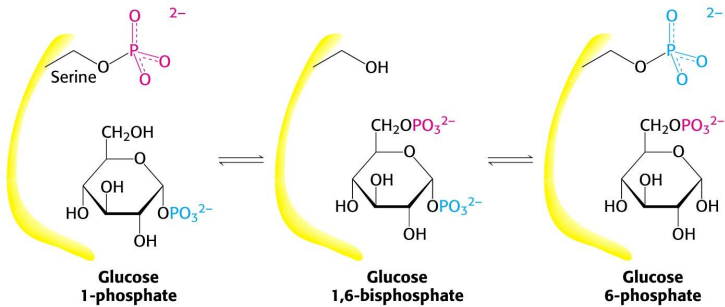
Fosfoglucomutasa:
Cataliza el desplazamiento del grupo fosfato G1P → G6P. Interviene un residuo fosforilado de serina de su centro activo.
El grupo P se transfiere al C6 de la G1P para formar glucosa-1,6-bisfosfato.
El grupo P del C1 de este intermediario pasa al residuo de serina del enzima regenerándola y produciendo G6P.
Biosíntesis de glucógeno
3 actividades enzimáticas
UDP-Glucosa Pirofosforilasa: activa la molécula de glucosa.
Glucógeno Sintasa: añade la molécula de glucosa activada al extremo de la molécula de glucógeno.
Enzima ramificante: genera las ramificaciones del glucógeno.
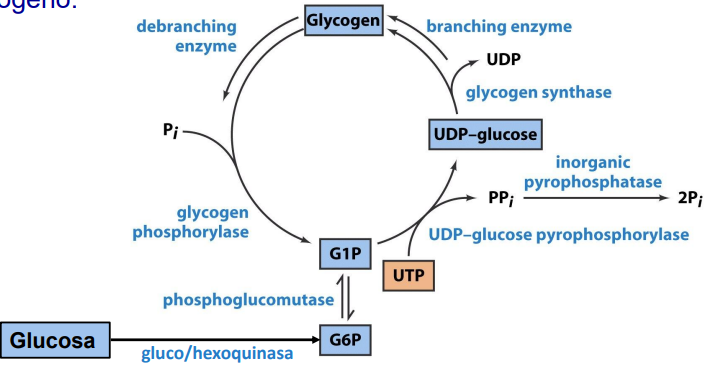
UDP-Glucosa Pirofosforilasa:
Se produce una activación de la molécula de glucosa.
La UDP-glucosa se sintetiza a partir de glucosa-1-fosfato (G1P) y UTP mediante una reacción catalizada por la UDP-Glucosa Pirofosforilasa.
Esta reacción tiene gasto energético.
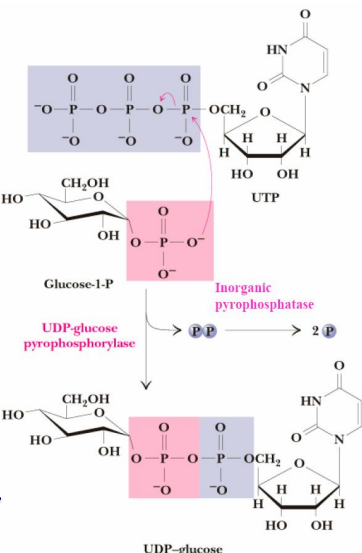
Glucógeno sintasa:
La UDP-glucosa es transferida a los extremos NO reductores del glucógeno, formándose un enlace α-1,4-glicosídico. Esta reacción está catalizada por la Glucógeno sintasa, enzima regulador clave en la biosíntesis del glucógeno.
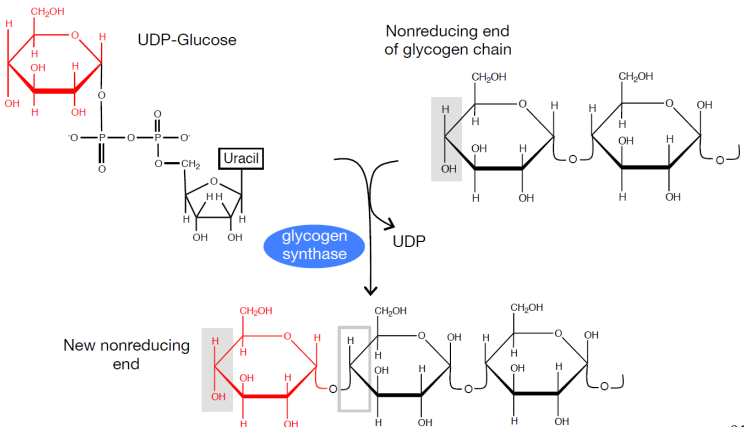
Enzima ramificante:
Después de que un cierto número de unidades de glucosa se hayan unido mediante enlaces α-1,4 por la glucógeno sintasa, las ramas se forman por ruptura de un enlace α-1,4 y formación de un nuevo enlace α-1,6.
Esta enzima transfiere bloques de 6 ó 7 residuos de glucosa hacia un lugar más interior de la molécula de glucógeno.
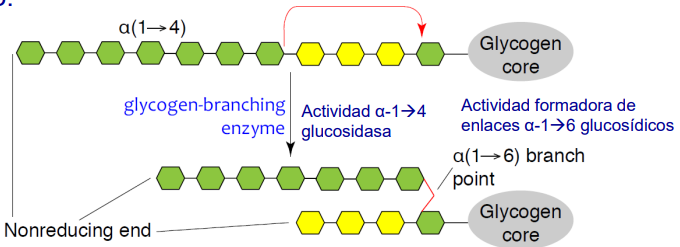
La ramificación suele ocurrir cada 10 residuos de glucosa. La ramificación incrementa la solubilidad, genera un gran número de residuos terminales no reductores e incrementa la velocidad de síntesis y degradación del glucógeno.
#ff00f6
Biosíntesis de novo del glucógeno
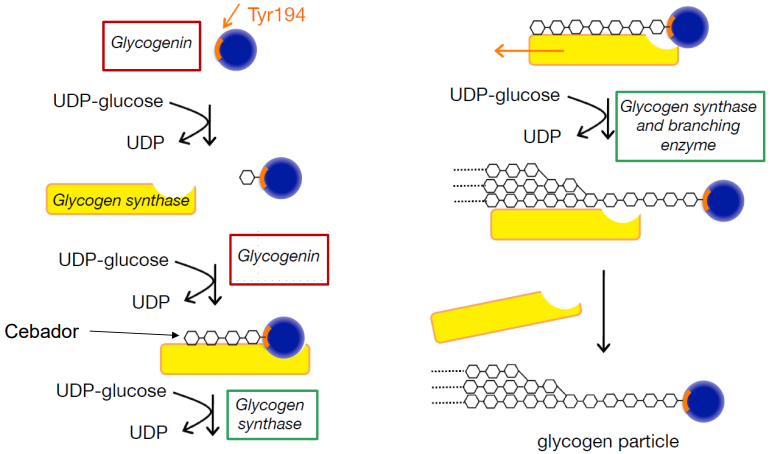
Glucógeno sintasa: añade moléculas de glucosa activada al extremo de una cadena de glucógeno existente. SÓLO cataliza elongación sobre un cebador de, al menos, 4 moléculas de Glucosa.
Glucogenina: proteína responsable de la síntesis de este cebador. Fases del proceso:
Tiene un residuo de Tyr al que se puede unir una molécula de Glucosa desde una UDP-glucosa (enlace entre -OH de la Tyr y C1 de Glucosa)
Una vez la primera Glucosa es unida covalentemente a la Glucogenina, se forma un complejo estable con la Glucógeno sintasa. Sin embargo, las siguientes tres moléculas de glucosa son transferidas por acción de la Glucogenina.
Cuando el cebador se ha ensamblado, Glucógeno sintasa y Enzima ramificante se encargarán de la elongación y biosíntesis de Glucógeno.
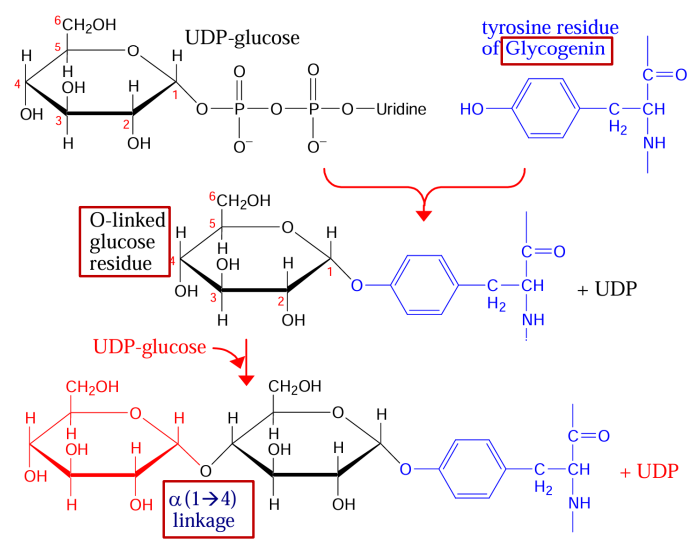
La Glucogenina es una proteína homodimérica (37.2 KDa/subunidad) con actividad glucosil-transferasa que va a generar un pequeño polisacárido (4 residuos de glucosa con enlace α-1,4) que servirá de cebador para la glucógeno sintasa.
Regulación del metabolismo del glucógeno
La Biosíntesis de glucógeno se produce en el hígado y el músculo cuando la concentración de glucosa en sangre es elevada y haya energía suficiente para la activación de glucosa (UTP).
Hígado: reserva de glucosa del organismo y control de la glucemia.
Músculo: almacén autónomo.
Por el contrario, la degradación de glucógeno se producirá en hipoglucemia o cuando se necesite energía.
Las enzimas claves de esta regulación son la Glucógeno fosforilasa y la Glucógenos sintasa.
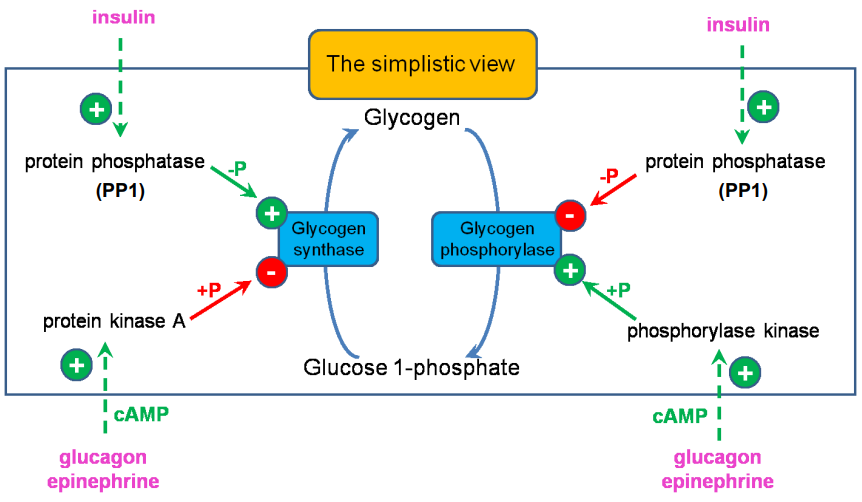
Insulina indica que hay mucha glucosa y que hay que producir glucógeno.
La epinefrina y el glucagón indican que falta glucosa y que hay que degradar el glucagón.
(Para activar la fosforilasa kinasa tiene que ser fosforilada por la proteína kinasa A)
Glucógeno fosforilasa
Posee dos niveles de regulación:
Regulación alostérica: tiene 2 estados
Estado R → relajada
Estado T → inactiva
Regulación hormonal: regulada mediando fosforilación y desfosforilación en los residuos de ser, gracias
Fosforilasa quinasa (fosforila) → a (adrenalina/glucagón)
Proteínas fosfatasa (desfosforila) → b (inducida por insulina)
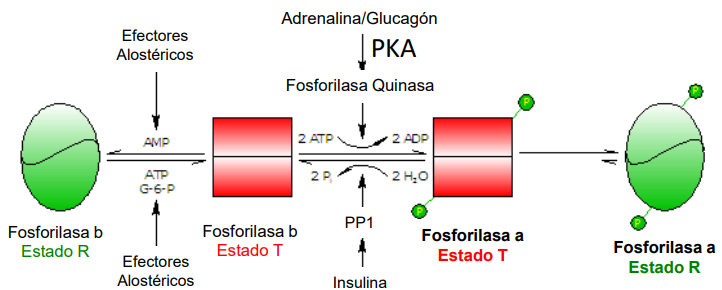
Es más importante la fosforilación que la activación alostérica.
En el hígado:
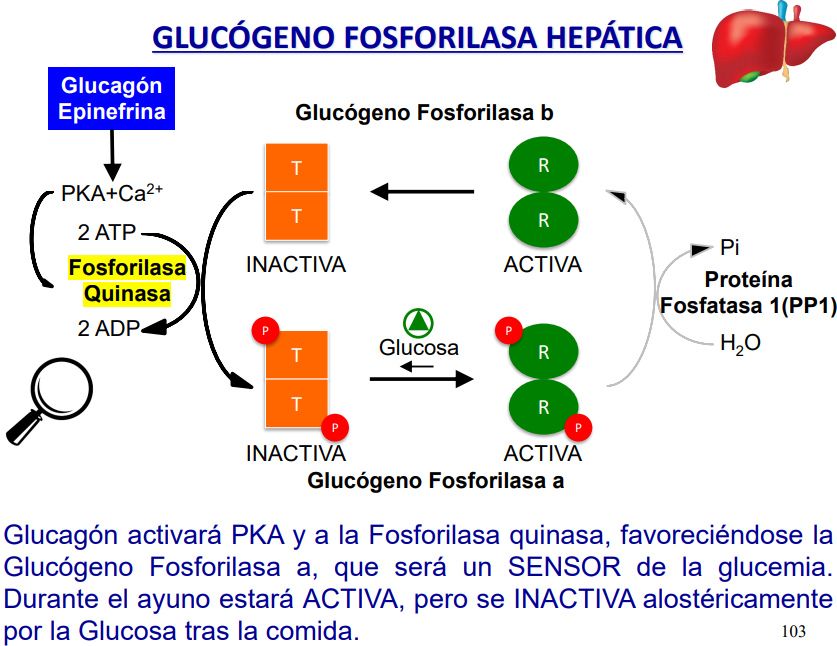
El funcionamiento del calcio y la fosforilación funciona de manera que:
si beta está fosforilado, estará parcialmente activa.
Si gamma está con Ca2+, estará parcialmente activa.
Si se da ambos sucesos, estará completamente activa.
La unión de Ca se da por el impulso nervioso, mientras que la fosforilación vienen dada por acción hormonal
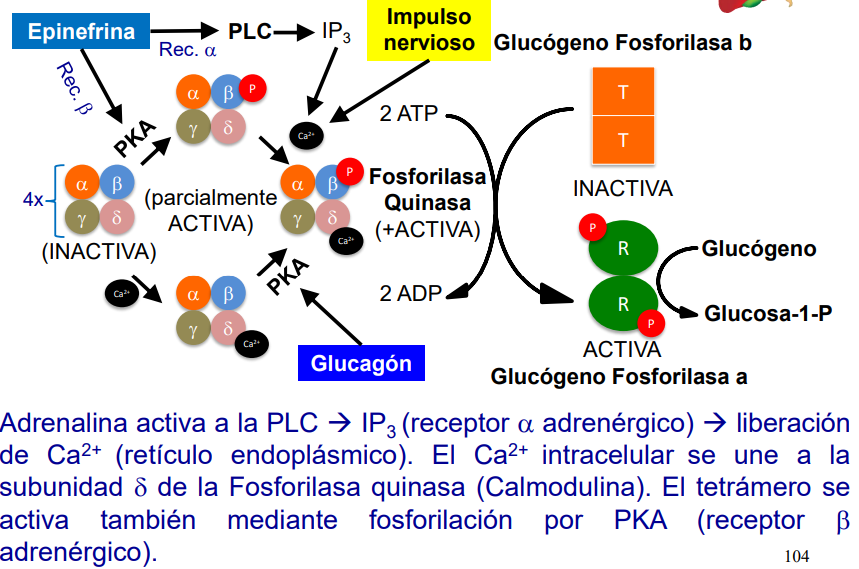
En el músculo:
NO ACTÚA EL GLUCAGÓN.
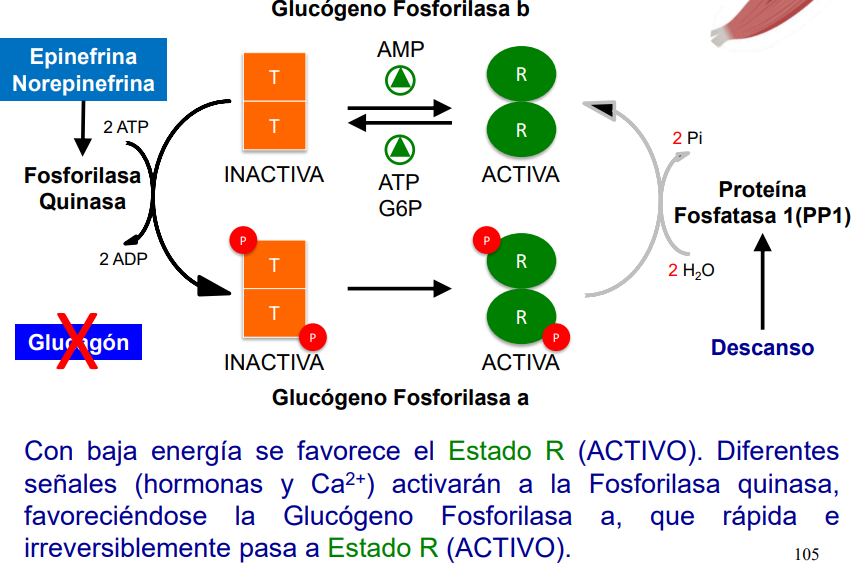
Ahora la movilización de Ca se va a deber a la contracción muscular.
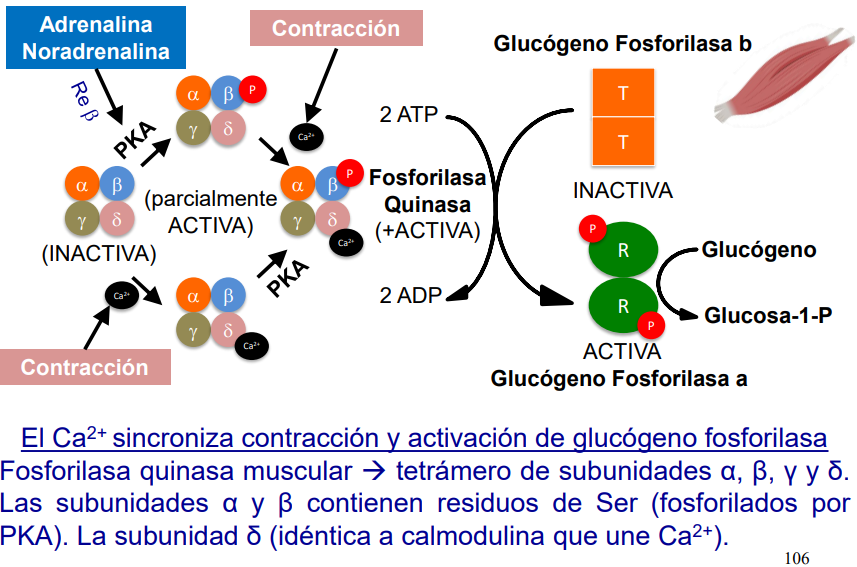
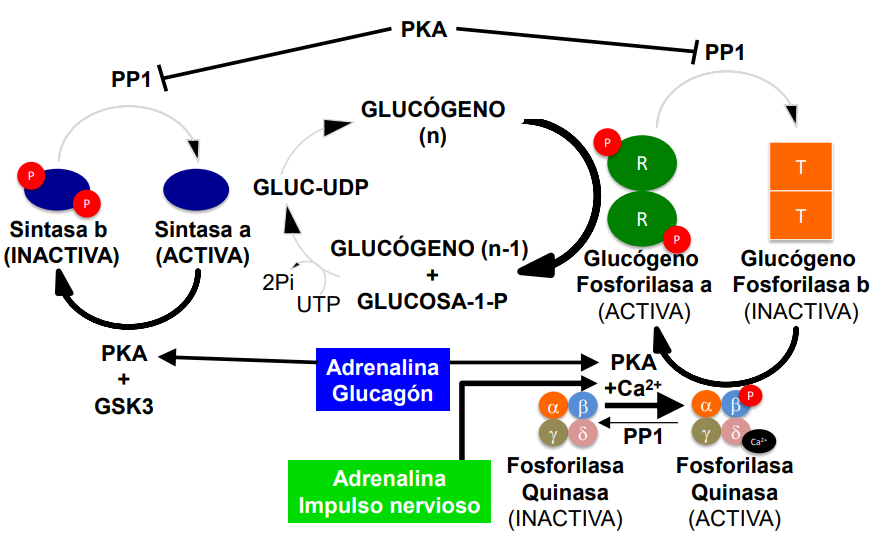
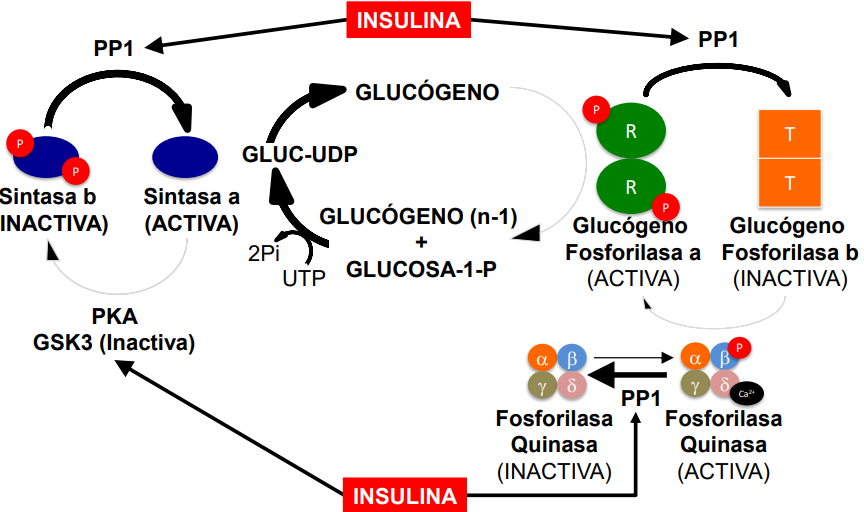
En conjunto
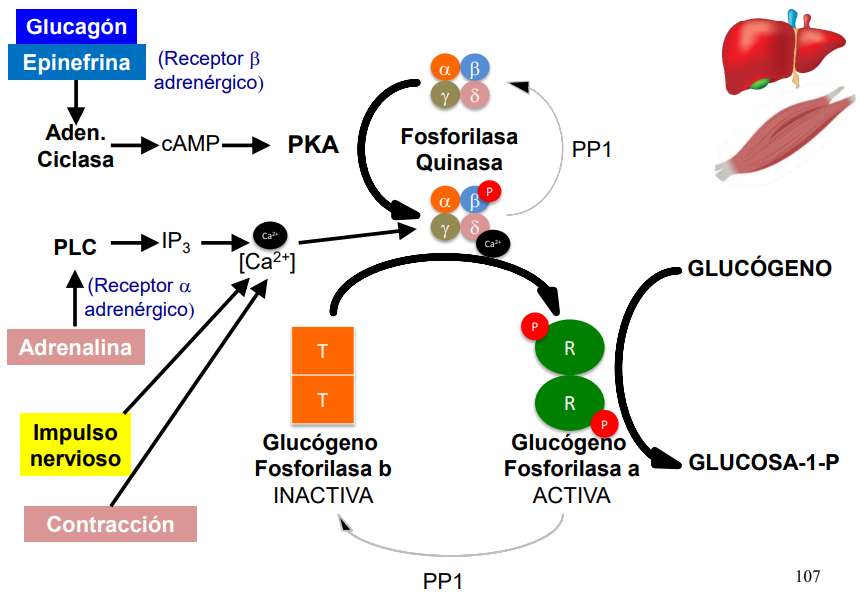
Proteínas fosfatasa (PP1)
Puede desfosforilar:
Glucógeno fosforilsa → inactiva
Fosforilasa kinasa → inactiva
Glucógeno sintasa → activa
Insulina → activará las fosfatasa produciendo una detención de la glucólisis.
Glucógeno → inactivará la fosfatasa permitiendo los procesos
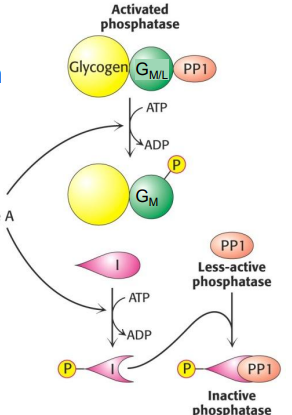
La proteína PP1 esta constituida por tres componentes:
una subunidad catalítica PP1
una subunidad GM(músculo)/GL (hígado) con alta afinidad por glucógeno
una subunidad inhibidora (I-1), que cuando está fosforilada inhibe a PP1.
La adrenalina y glucagón promueven la degradación de glucógeno. Activan PKA que fosforila Gm/l, lo que impide la unión de PP1 y con ello la desfosforilación. Por otro lado, PKA fosforila a la subunidad I-1, que se une a la subunidad PP1 y bloque del todo su actividad.
Cuando hay mucha glucosa en sangre, se libera la insulina que activa la síntesis de glucógeno. La insulina se una a RTK y promueve la cascada de fosforilaciones donde participa PI3K, que fosforila sub Gm/l, en u lugar diferente a la PKA, permitiendo la asociación de Gm/l y PP1, que desfosforilarán la glucógeno sintasa, activándola y la fosforilasa quinasa, que se inactiva.
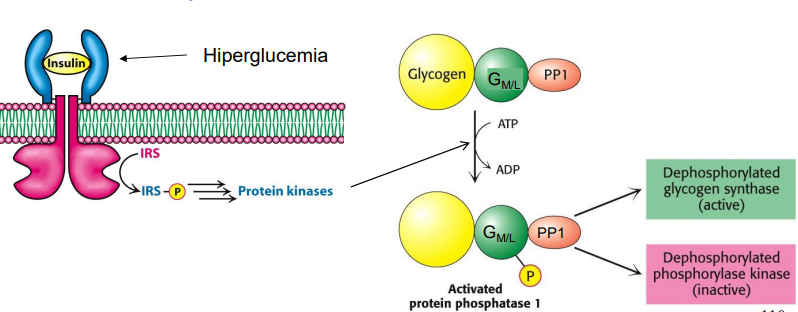
Glucógeno Sintasa Kinasa 3 (GSK3) es la principal kinasa que se encarga de fosforilar la glucógeno sintasa. Cuando actúa la insulina, esta es inactivada por fosforilación gracias a las PKB, activada por la glucosa.
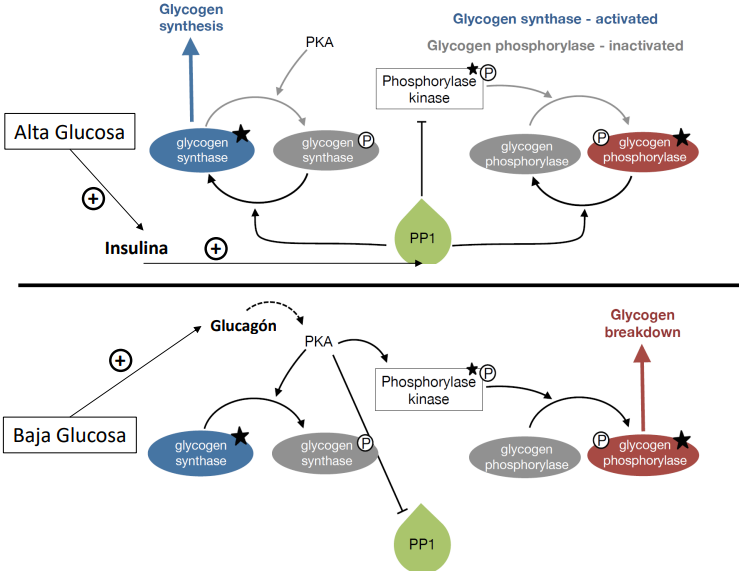
Glucógeno sintasa en condiciones de hipoglucemia o estrés
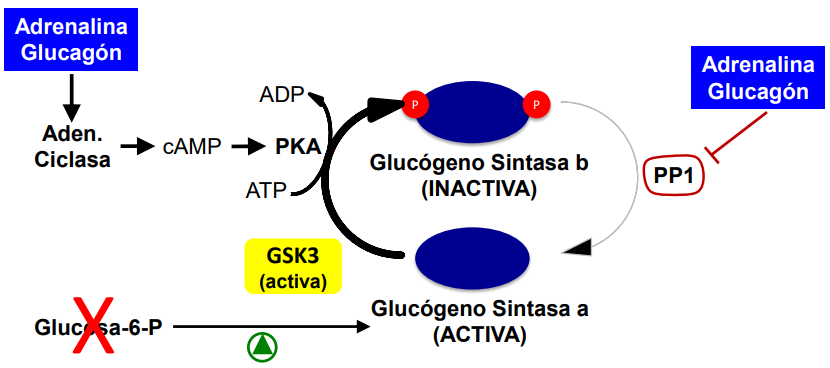
Se fosforila en inactiva la glucógeno sintasa (x la PKA).
GSK3 está activa para tenerla inhibida.
Se fosforila y se inhibe PP1
Se volverá a activar cuando haya G6P, insulina…
Activa la glucógeno fosfatasa
Lo hace todo PKA
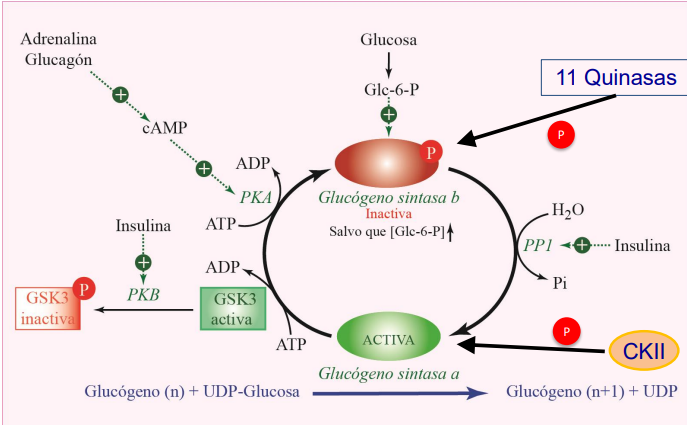
Glucógeno sintasa en hiperglucemia
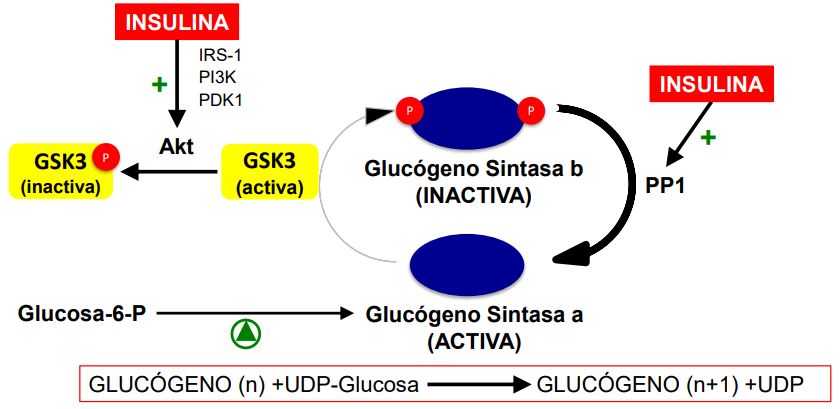
Se fosforila y desactiva GSK3.
Se activa la PP1.
La G6P actúa como regulador alostérico positivo.
PKA también se inactiva
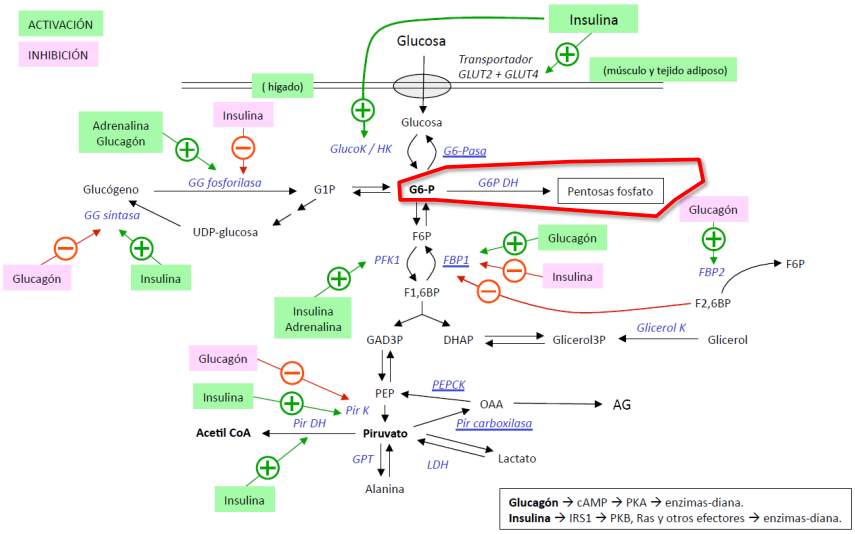
Ruta de las pentosas fosfato: fase oxidativa con generación de poder reductor en forma de NADPH
DIAPOSITIVA NO SUBIDA DE ESQUEMA
Conecta la vía glucolítica con la síntesis de nucleótidos. La G-6-P, el primer intermediario en la glucólisis, puede ser desviado a una serie de reacciones que conducen a la producción de NADPH y Ribosa 5-fosfato.
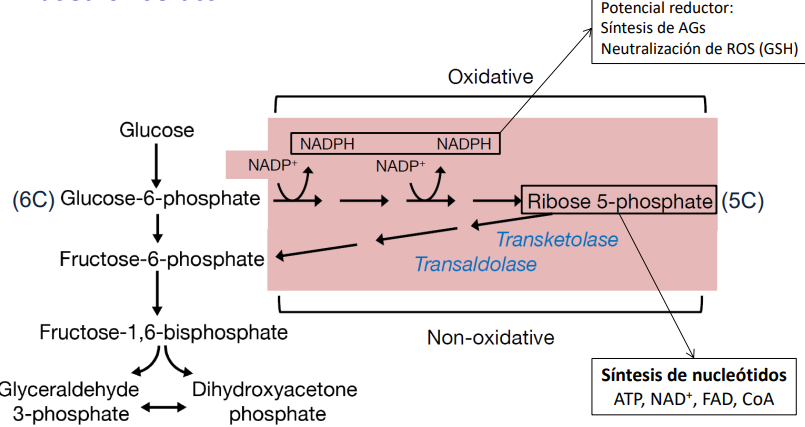
Fase oxidativa
La glucosa 6-fosfato (G6C) se convierte en ribosa 5-fosfato (R5P) y se producen dos NADPH. Fase irreversible. Lo realiza la glucosa-6-P deshidrogenasa
También puede venir una epimerasa, que puede pasar la cetona a aldehído.
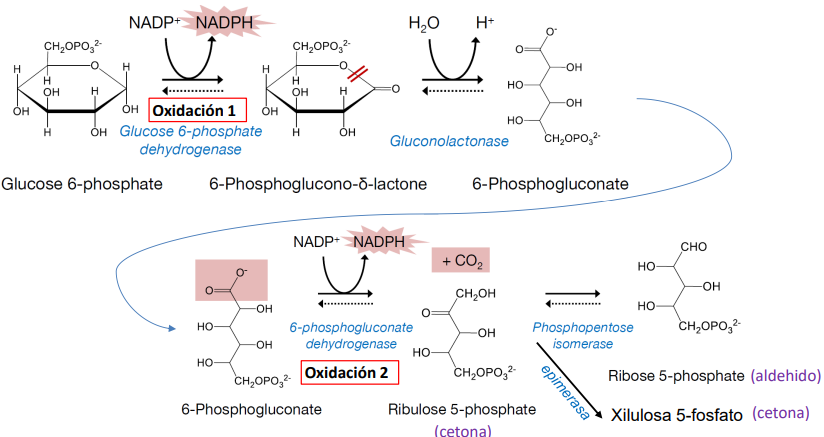
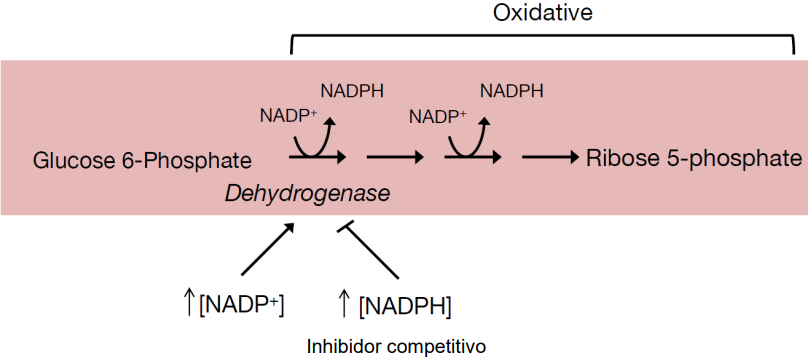
Regulación
La enzima Glu6P deshidrogenasa tiene regulación por retroalimentación, cuando hay mucho NADP+ se activará, mientras que si hay mucho NADPH se detendrá.
Fase no oxidativa
Conversión de ribosa 5-fosfato en fructosa 6-fosfato → requiere dos enzimas; la transcetolasa y la transaldolasa. Fase reversible.
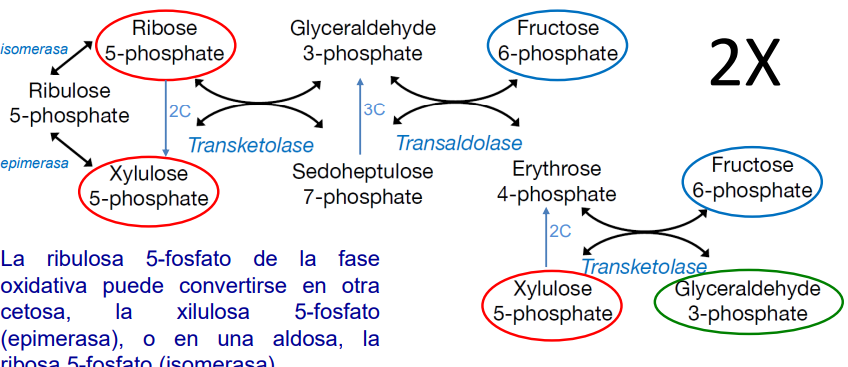
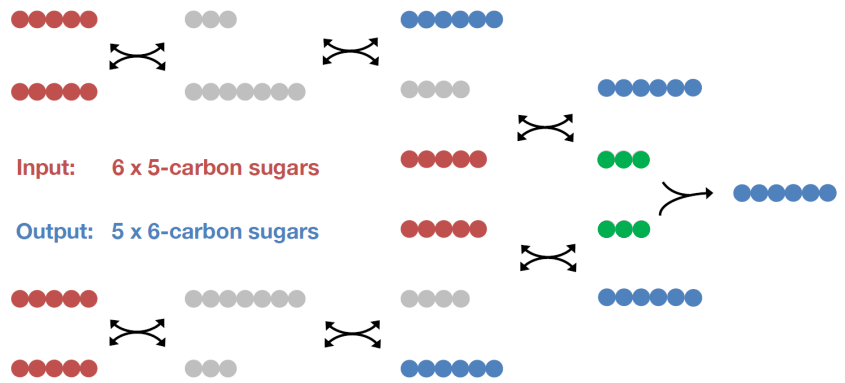
Transferencia de unidades de 2C y 3C entre diferentes monosacáridos para reconstruir moléculas de 6C.
La F-6-P puede entrar en la vía glucolítica o convertirse en G-6-P, alimentando un nuevo ciclo de la vía de la pentosa fosfato.
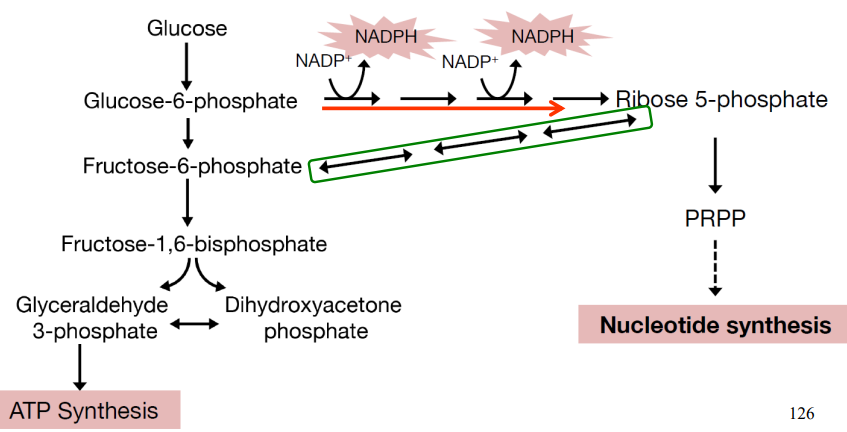
Regulación y usos
Las transaldolasas y transcetolasas catalizan la reacción reversible. La dirección la dictará la disponibilidad de sustrato.
Las necesidades metabólicas de las diferentes células regularán el uso de la vía de las pentosas fosfato.
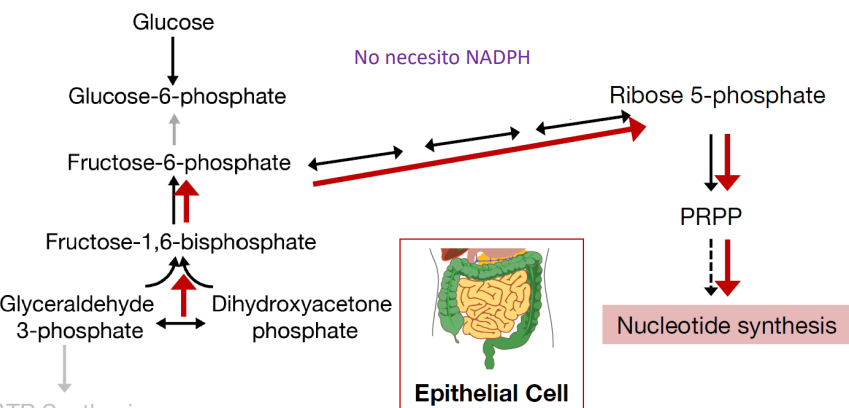
Células del epitelio intestinal: Células muy proliferativas → Necesitan una gran reserva de nucleótidos para fabricar ADN y ARN → fase oxidativa hacia adelante y fase no oxidativa a la inversa.
Adipocitos: Necesitan ↑ NADPH para la síntesis de AGs → Reciclaje de la G-6-P → prevalece la síntesis de NADPH sobre la síntesis de ATP a través de la glucólisis.
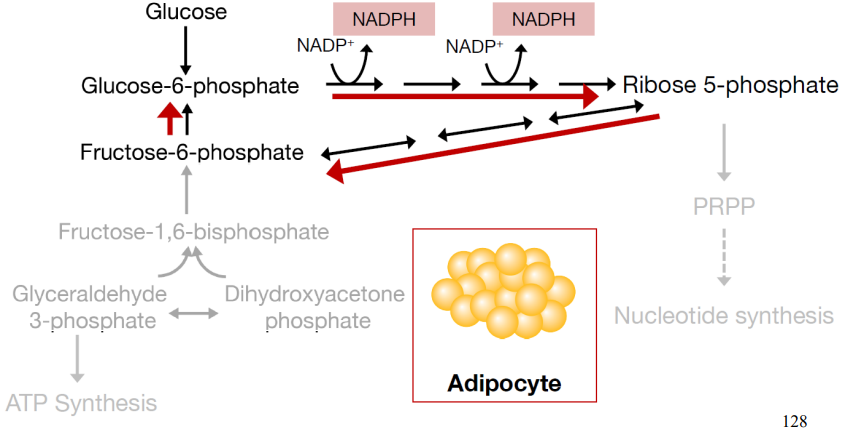
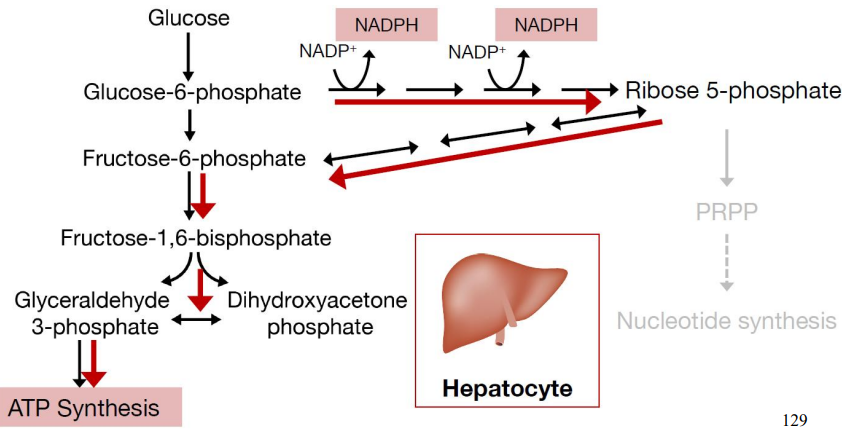
Hepatocitos: Células que necesitan NAPDH y ATP → Fase oxidativa para producir NADPH y fase no oxidativa para devolver la F-6-P a la vía glucolítica para la síntesis de ATP.
El glutatión tiene funciones muy importantes como
evitar que el O2 super oxidado rompa membranas, ya que se pasa a H2O2, y el glutation lo acaba convirtiendo en 2 H2O.
En un eritrocito, el ambiente es muy oxidante. Cuando no hay mucho NADPH+H+, no se puede producir mucho glutatión para combartir las especies reactivas. Como no se pueden combatir, se crean los cuerpos de Heinz, agreagados de hemoglobina, hemólisis y anemia. Esto se debe a la deficiencia de esta enzima.