Tema 8: Regulación de la actividad enzimática
Control de la actividad enzimática
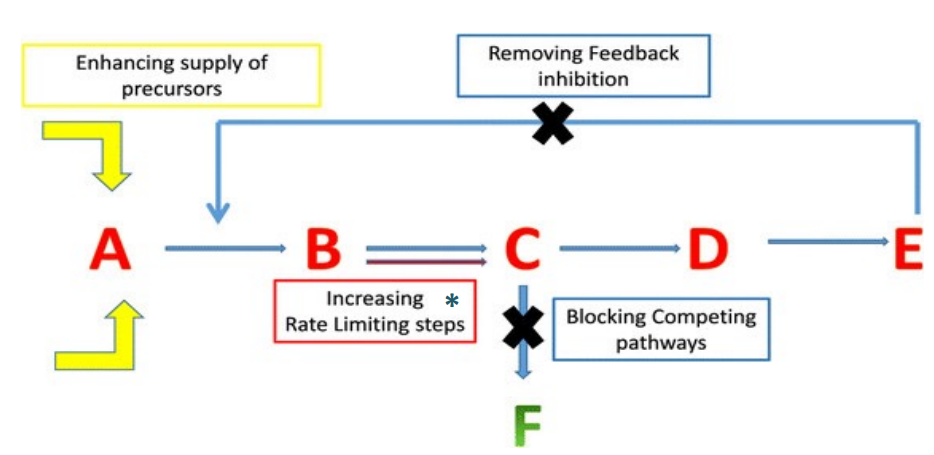
Las reacciones enzimáticas se organizan en rutas metabólicas. Dentro de cada ruta, las enzimas reguladoras controlan el paso más lento (paso limitante), estableciendo así la velocidad global de la ruta metabólica. Esto permite que la célula se adapte rápidamente a cambios en sus condiciones.
La regulación puede producirse en distintos niveles:
Inicio de la ruta metabólica.
Regulación de pasos intermedios.
Regulación por el producto final.
Mecanismos que bloquean o modulan la ruta.
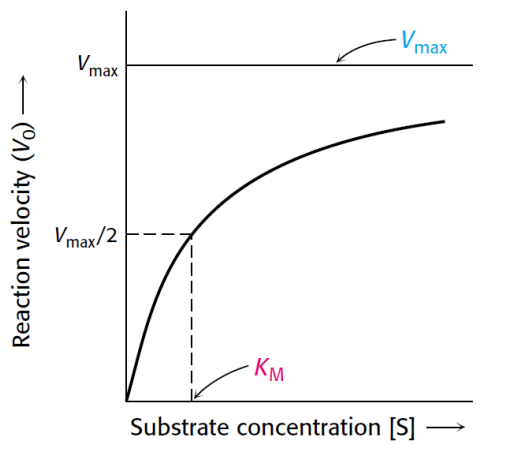
La actividad enzimática se puede regular con la concentración de sustrato, ya que si la aumentamos, aumentará la velocidad de la reacción siempre que la enzima no sea limitante.
Enzimas alostéricas
Cooperatividad
La unión de una molécula a una subunidad provoca un cambio conformacional que se transmite a las subunidades adyacentes. Esto altera su afinidad y con ello su actividad.
La cooperatividad en una forma de alosterismo, pero ocurre cuando las proteínas se dividen en subunidades.
Alosterismo
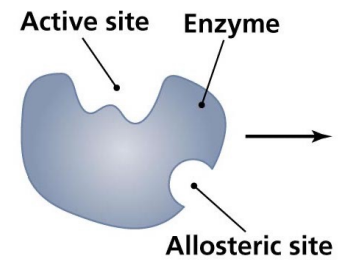
Los moduladores o efectores alostéricos se unen a la enzima y provocan cambios conformacionales que afectan a la afinidad de la enzima por el sustrato.
Además del centro activo, suelen presentar otros centros reguladores.
Estos ligando se unirán de manera no covalente y reversible.
Tipos de moduladores alostéricos
Moduladores homotrópicos
Moléculas idénticas al sustrato, o el propio sustrato puede actuar como modulador alostérico.
Ocurre cuando la enzima tiene varias subunidades y la unión del sustrato a una de ellas provoca un cambio conformacional que afecta la afinidad de las otras subunidades. Es equivalente a efecto cooperativo.
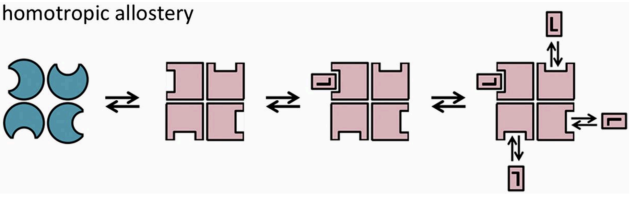
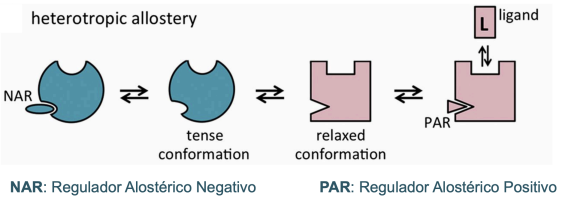
Moduladores heterotrópicos
Moléculas distintas al sustrato que se unen en los sitios alostéricos. Pueden tener efecto:
Positivo: aumenta la afinidad de la enzima por el sustrato.
Negativo: disminuye la afinidad.
Los cambios conformacionales pueden llevar a que obtengan distintas formas:
Formar T (tensas): - afinidad, moduladores negativo
Formas R (relajadas): + afinidad, moduladores positivos.
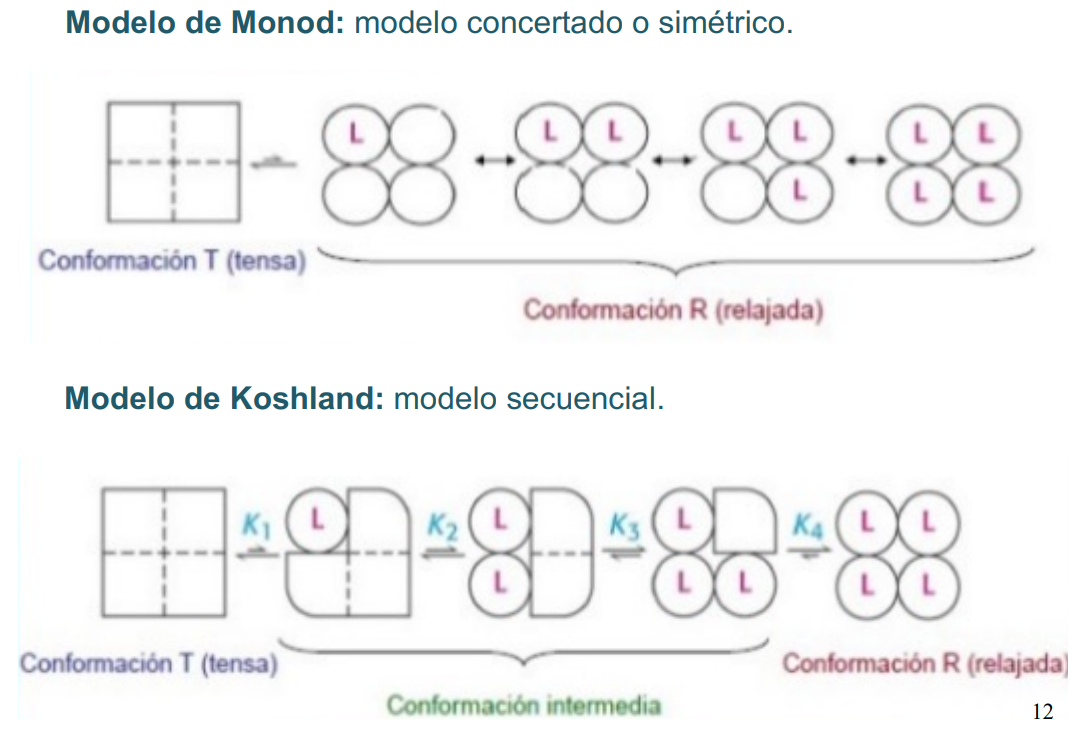
Modelos de alosterismo
Intentan explicar como la unión de un ligando produce cambios conformacionales en las enzimas con varias subunidades. Son hipotéticos y simplificados, en la realidad se suelen dar una mezcla ambos comportamientos.
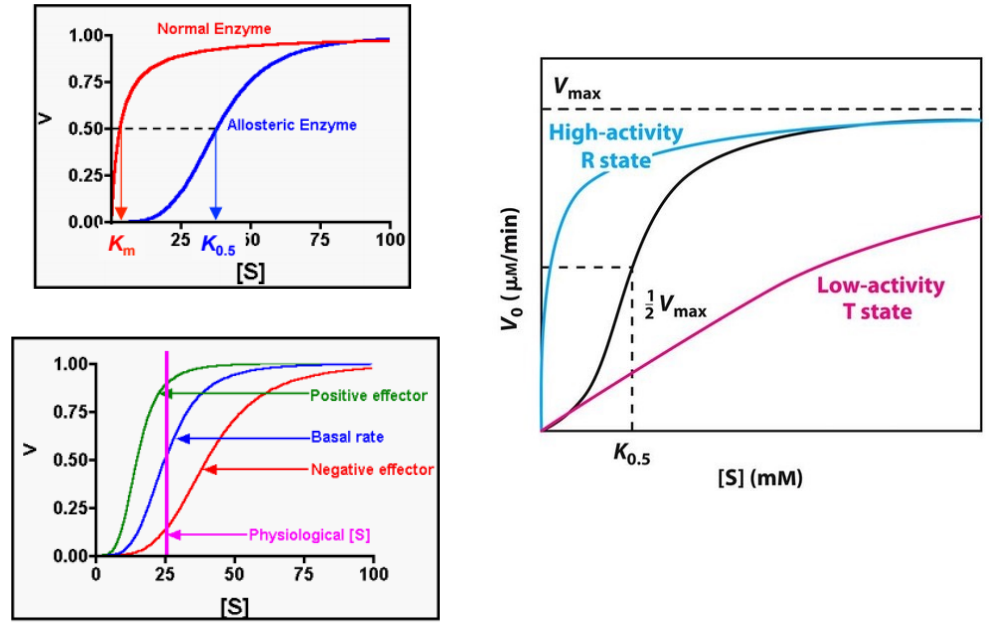
Representación gráfica
Las enzimas alostéricas suelen tener forma sigmoidal debido a sus cambios conformacionales. Por lo tanto, no siguen MM, y su equivalente e la Km será K0,5.
Además, su actividad dependerá de los efectores que estén actuando sobre ella. Los positivos llevarán el equilibrio hacia la forma R, con más afinidad, mientras que los negativos estabilizarán la forma T, que requiere + [S] para llegar a Vmax.
Cinética de enzimas alostéricas
Moduladores homotrópicos: sustrato se une al sitio activo, provocando cambios conformacionales hacia T o R.
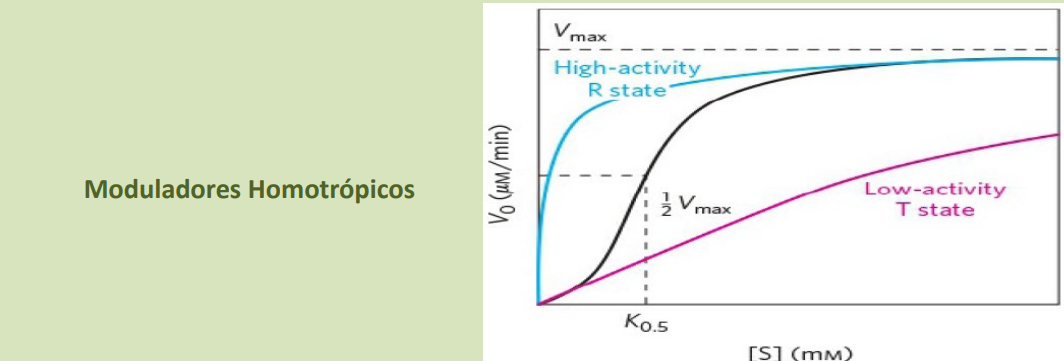
Moduladores heterotrópicos: la regulación depende de la cantidad de efector y del número de sitios alostéricos disponibles.
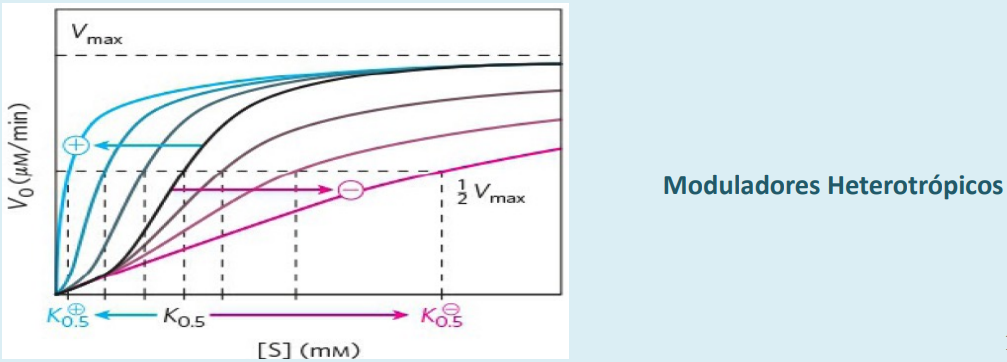
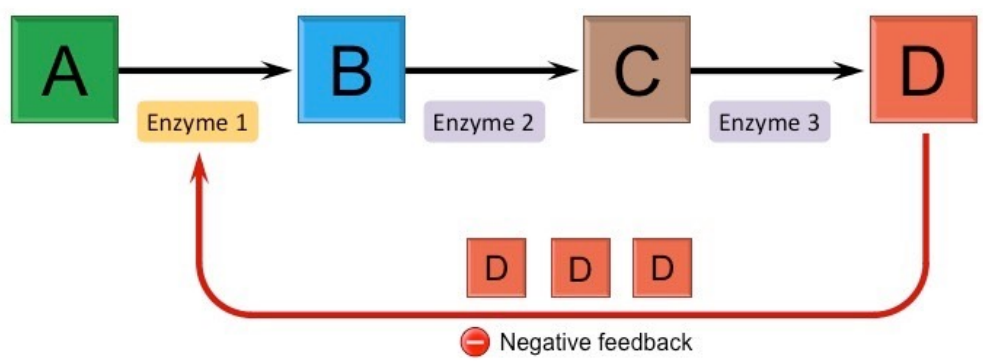
Un ejemplo importante de esta última es la inhibición por retroalimentación o feedback: cuando el producto final se acumula, actúa como modulador negativo, uniéndose a las primeras enzimas de la ruta. Esto evita una sobreproducción del propio producto.
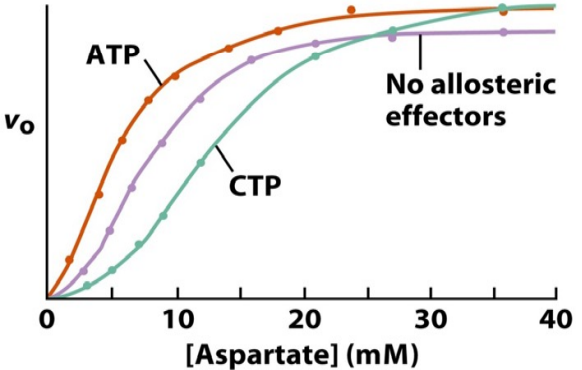
Aspartato transcarbamilasa
ATCasa es una enzima que cataliza la reacción entre asparto y carbamoil fosfato, siendo la primera etapa en la síntesis de nucleótidos pirimidínicios. Está formada por 12 subunidades → 6 catalíticas y 6 reguladoras.
El producto final de la ruta, CTP, actúa como efector negativo, uniéndose a las subunidades reguladoras y estabilizando la forma T. Esto evita que haya exceso de pirimidinas.
Por otro lado, el ATP actúa como efector heterotrópico postivo, favoreciendo la forma R. Así se coordina la producción equilibrada de purinas y pirimidinas en la célula.
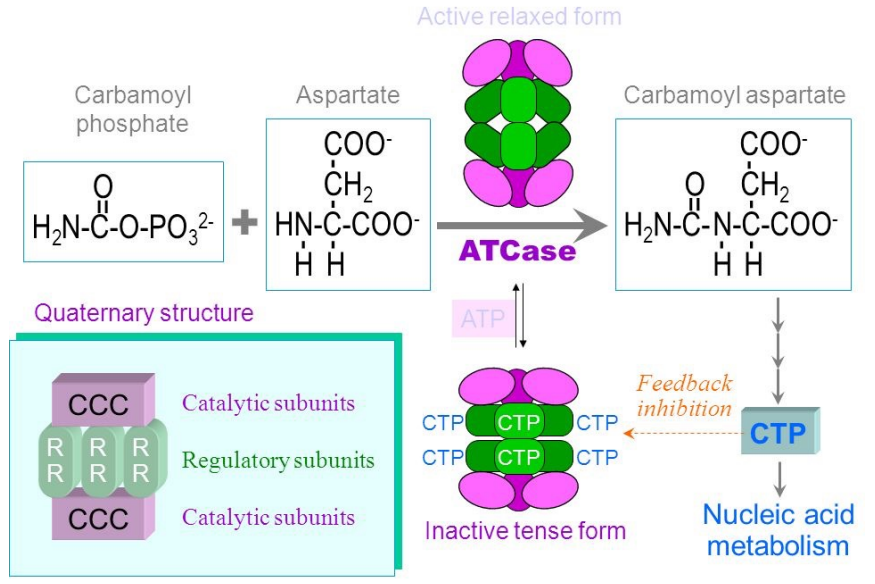
ATCasa también tiene regulación homotrópica, ya que el aspartato actúa como efector homotrópico positivo.
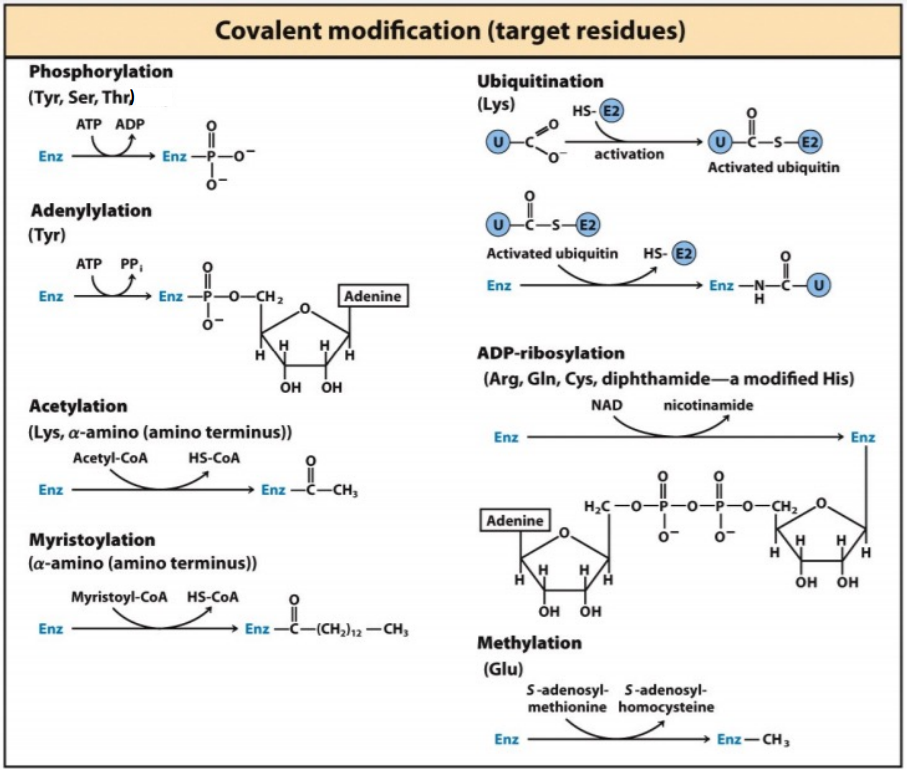
Modulación alostérica covalente
Una variedad de grupos químicos de las enzimas pueden ser modificados de forma covalente y reversible.
Esta modificación implica cambios de conformación que pueden conducir a cambios en la actividad enzimática.
Modificaciones más comunes:
Regulación por fosforilación
La quitinasa añade un grupo P a ciertos aa, mientras que una fosfatasa lo elimina, desfosforilando la enzima.
La glucógeno fosforilasa descompone el glucógeno en G1P que es más activo que su forma desfosforilada.
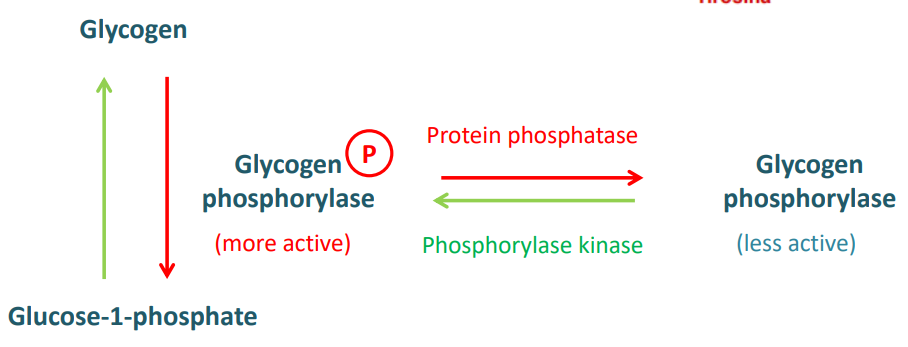
Cuando el organismo necesita glucosa, las quitinasas fosforilan la glucógeno fosforilasa, aumentando su actividad y liberando glucosa del glucógeno. Si la demanda disminuye, las fosfatasas desfosforilan la glucógeno fosforilasa.
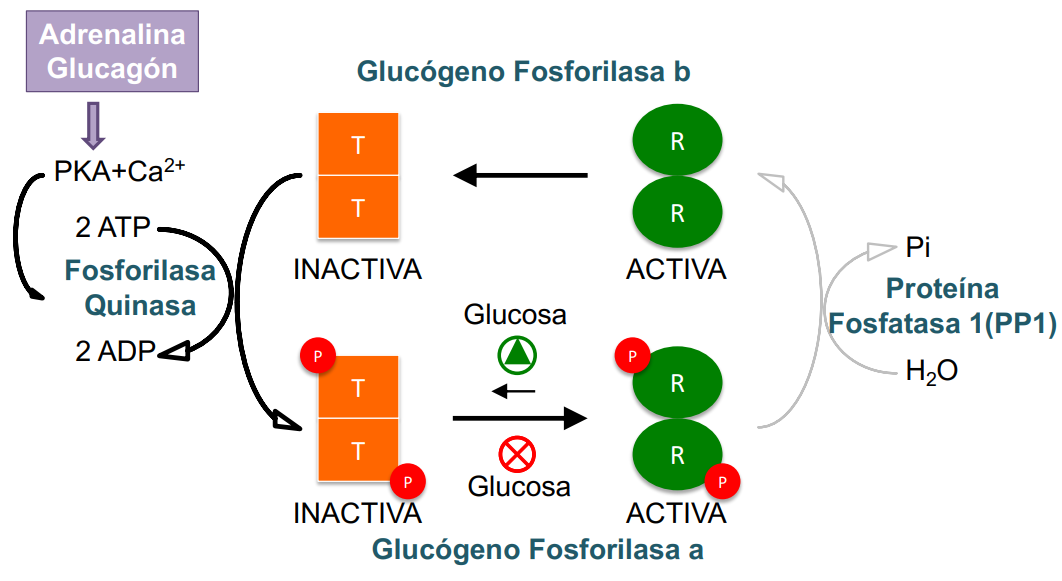
Glucógeno fosforilasa
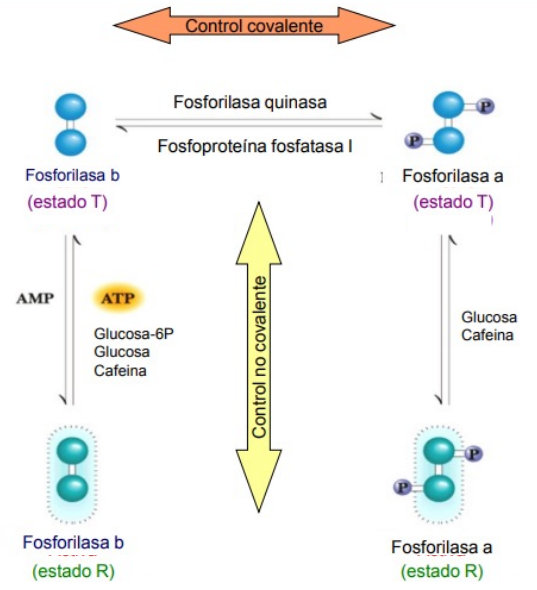
Hepática
La glucógeno fosforilasa se regula mediante señales hormonales → glucagón y adrenalina. Indican la necesidad de glucosa y activan la fosforilasa quinasa (fosforila glucógeno fosforilasa → degrada glucógeno).
La glucosa actúa como modulador alostérico negativo → detienen cuando hay suficiente.
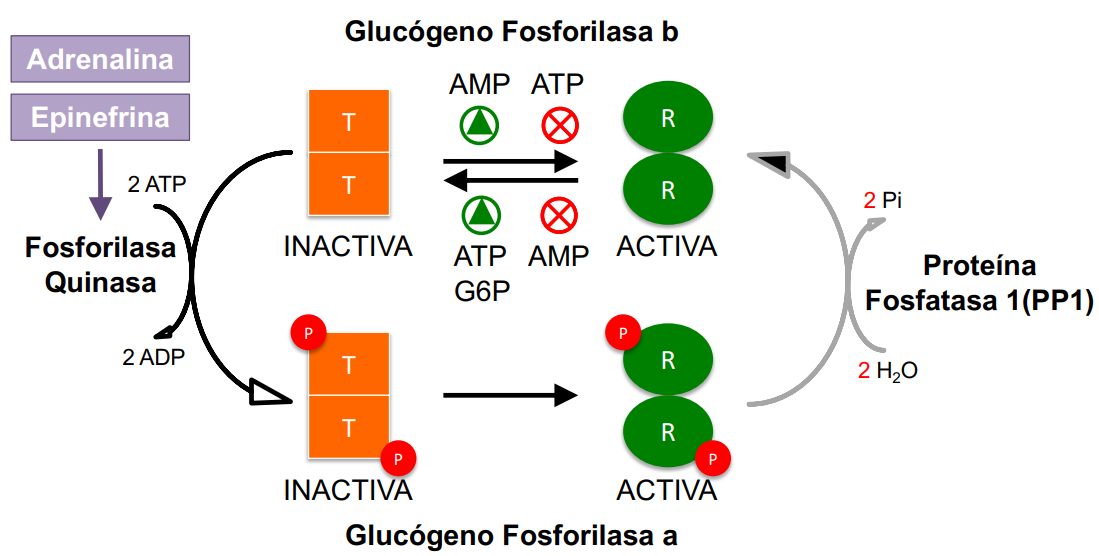
Muscular
La glucógeno fosforilasa se activa cuando necesita ATP. Hormonas como la adrenalina o epinefrina activan la fosforilasa quinasa, que fosforila la enzima anterior y la activa.
También posee regulación alostérica, con moduladores como AMP (activador → indica baja energía) y el ATP o G6P (inhibidores → suficiente energía).
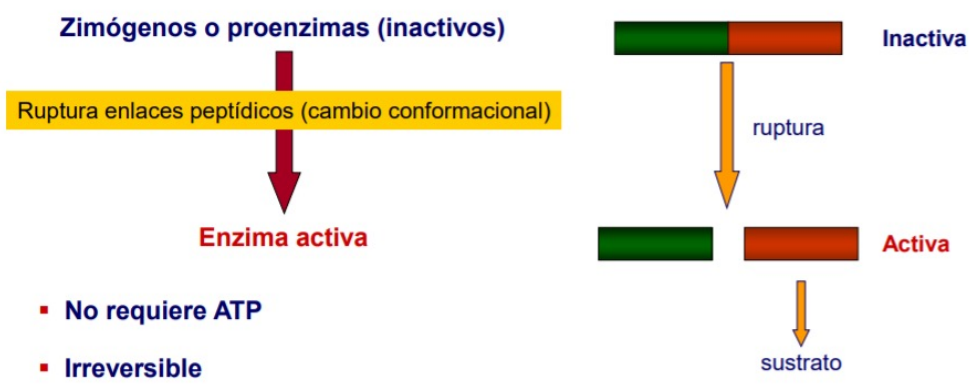
Activación por proteolisis
Muchas enzimas se producen como proenzimas, formas inactivas que requieren una rotura proteolítica específica para activarse. Este tipo de activación es irreversible, no requiere ATP, y tras ella no se puede volver a inactivar, sólo se puede degradar.
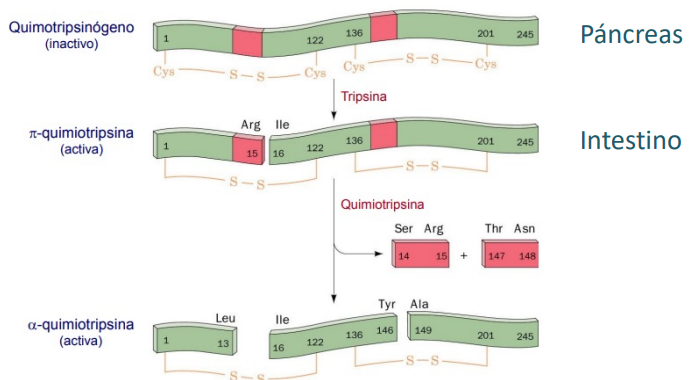
En enzimas digestivas
Tripsina
Se sintetizan en el páncreas como tripsinógeno, se envían al intestino donde se activan, pudiendo activar a otras como la quimiotripsina → efecto cascada. Esto evita daños en el páncreas.
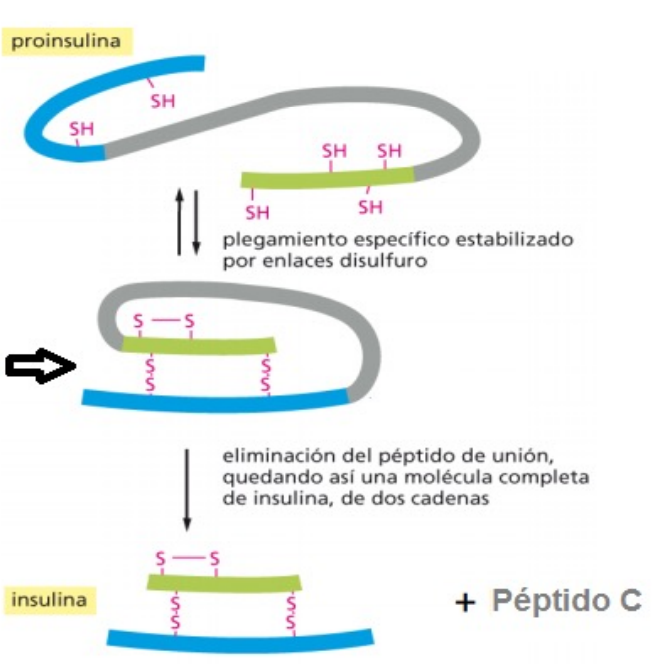
Insulina
Se produce proinsulina en el RE, con 3 segmentos (A, B y C). En el AG se vuelve activa tras eliminar el péptido C, que se libera junto a la insulina funcional, por lo que se suele usar para medir los niveles de insulina.
Isoenzimas
Variantes de una enzima que catalizan la misma reacción, con el mismo sustrato, pero con diferente estructura, regulación y localización (valores dintintos Km y Vmax). Esto les permite adaptarse a las necesidades específicas de distintos tejidos, compartimentos celulares o etapas de desarrollo.
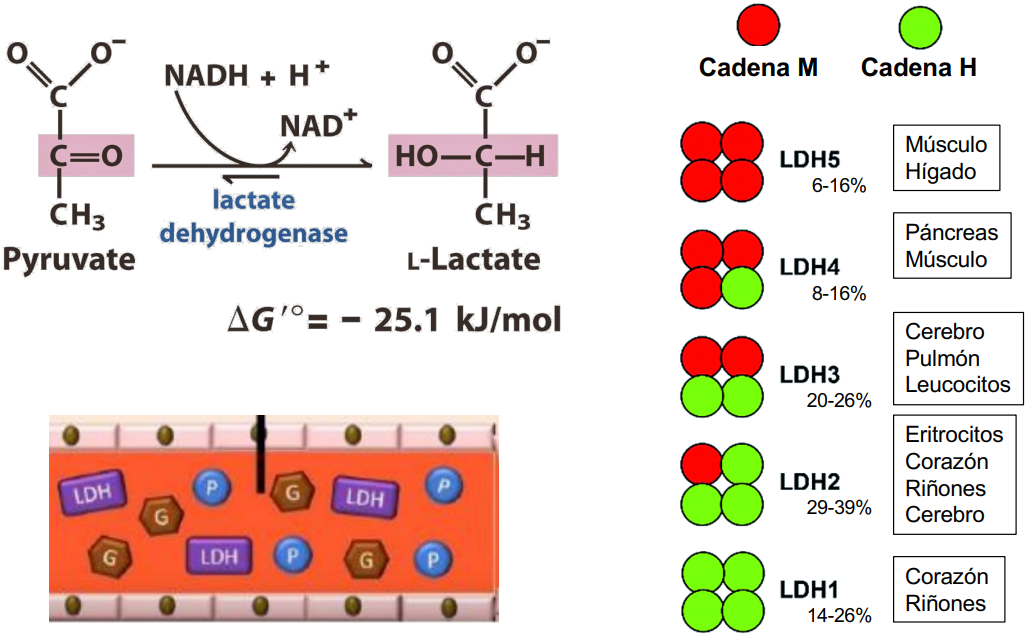
Lactato deshidrogenasa (LDH)
Convierte el piruvato en lactato. Hay 2 tipos de subunidades, M (musculares) y H (cardiacas), que forman 5 isoenzimas.
Cada isoenzima tiene afinidad diferente por el piruvato, lo que permite que el metabolismo energético se adapte a las características específicas de cada tejido. Además, el piruvato puede actuar como modulador alostérico, inhibiendo o regulando ciertas isoenzimas.
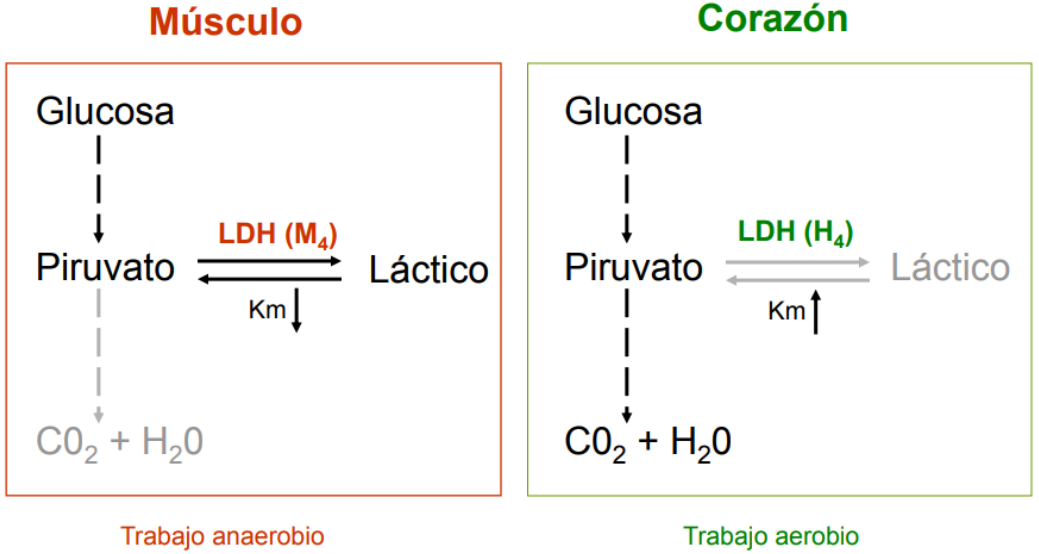
En el músculo esquelético, durante el ejercicio intenso o en condiciones de baja oxigenación, la glucosa se degrada a piruvato, que se convierte a lactato. Esto permite que la célula continúe generando ATP mediante glucólisis anaeróbica, y la LDH está activa para facilitar la formación de lactato.
En el corazón, que requiere energía de manera aeróbica de manera constante, predominan isoenzimas con mayor afinidad por lactato (como LDH1, formada por subunidades H). Estas isoenzimas favorecen la conversión de lactato a piruvato manteniendo la producción de ATP de forma aeróbica.
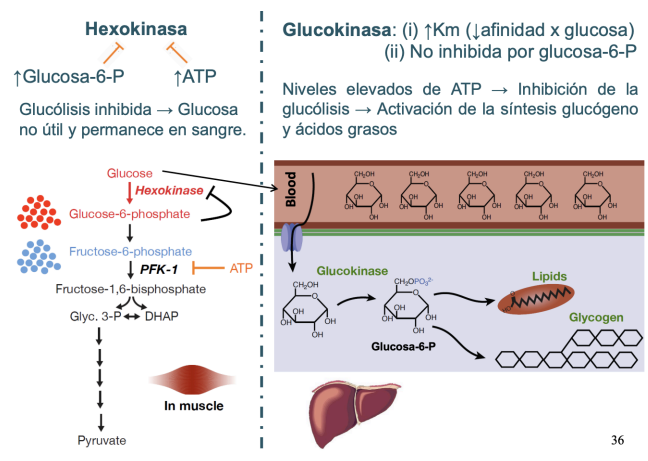
Glucoquinasa y hexoquinasa
En tejidos, la hexoquinasa tiene mayor afinidad por la glucosa (baja Km), por lo que se satura fácilmente y es inhibida por G6P (retroalimentación negativa).
La glucoquinasa se encuentra en el hígado y páncreas, y tiene menos afinidad por la glucosa para que sólo actúe cuando es abundante. Como no es inhibida por G6P, permite almacenar glucosa.