TRASPORTO TRANSMEMBRANA
La permeabilità delle piccole molecole e degli ioni è data dal coefficiente di permeabilità ed è correlata alla loro solubilità.
le molecole polari sono scarsamente permeabili poiché devono attraversare un doppio strato fortemente apolare. Necessitano pertanto di sistemi di transito e di trasporto;
un’eccezione è costituita dall’acqua a causa del mantenimento dell’equilibrio e della presenza delle acquaporine;
i gas e le sostanze lipofile sono altamente permeabili e passano per diffusione semplice da regioni a maggiore a minore concentrazione;
Trasporto passivo
Diffusione semplice
La diffusione semplice è un tipo di trasporto che non necessita di nessun sistema proteico. E’ caratteristico delle sostanze lipofile e dei gas e avviene secondo gradiente di concentrazione fino a quando si raggiunge una situazione di equilibrio.
Diffusione facilitata
La diffusione facilitata ha, come integrali della membrana, delle proteine canale o delle proteine carrier che facilitano e velocizzano il passaggio di una specifica molecola o di uno specifico ione, selezionato grazie alla presenza di precisi filtri molecolari, attraverso la formazione di legami deboli, necessari per facilitare il rilascio della molecola dall'altra parte della membrana. Appartengono a questa tipologia di proteine di trasporto i GLUT, una famiglia di trasportatori formati da 12 eliche TM che mediano il trasporto di zucchero secondo gradiente chimico.
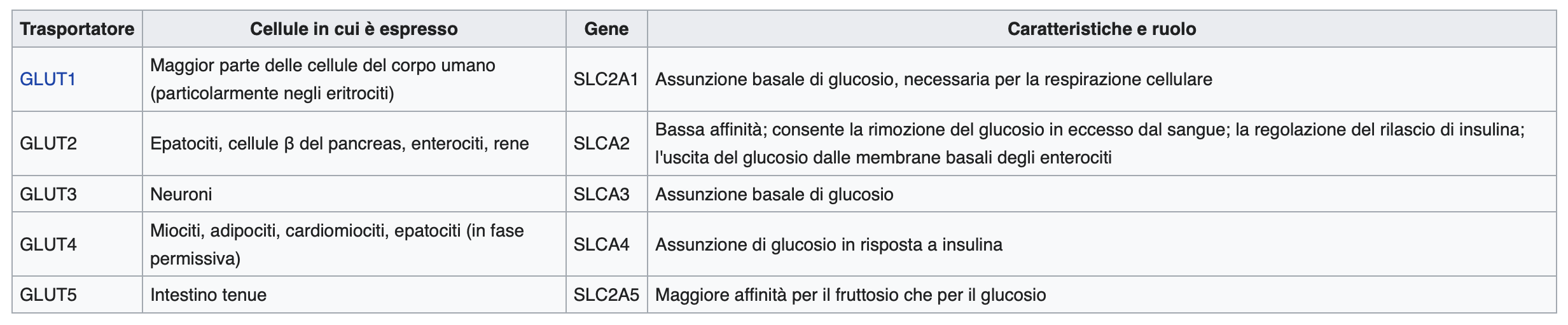
Il modello di trasporto è a uniporto, dipende dalle concentrazioni di glucosio e segue il gradiente. Ci sono due conformazioni che si alternano mediante il meccanismo di inversione/eversione. Per mantenere bassa la concentrazione di glucosio all’interno delle cellule questo viene fosforilato per impedirgli di transitare attraverso i GLUT. L’unico trasportatore che funziona davvero in entrambe le direzioni è il GLUT2, poiché negli eritrociti il glucosio non viene fosforilato ed è pertanto libero di muoversi da una parte all’altra.
Canali per ioni
Si tratta di proteine integrali di membrana che permettono il flusso selettivo di ioni secondo il loro gradiente chimico (sodio da ambiente extracellulare a intracellulare, potassio da intracellulare a extracellulare, calcio da extracellulare a intracellulare). Ne esistono di tre tipologie:
canale attivato da ligando (ligand-gated channel): canale la cui apertura è dipendente da una molecola che si lega ad un sito recettoriale. Un esempio è costituito dai canali che partecipano alla propagazione dell’impulso nervoso, in particolare il canale ligand-gated per l’acetilcolina, il canale nicotinico. E’ formato da cinque subunità che si raggruppano a formare una ciambella. Dalla parte più stretta del poro sono presenti 5 alfa eliche che coprono il foro. La selettività del foro dipende dalla grandezza del canale e dalla presenza di residui anionici (acido glutammico e aspartato), che selezionano solo cationi. Quando si legano due molecole di acetilcolina, le eliche si torcono e vengono introdotti i piccoli residui laterali di serina che liberano il poro. Per fare in modo che la durata dell’impulso sia precisa e breve l’acetilcolinesterasi idrolizza l’acetilcolina in colina e acetile con un meccanismo simile alle serina proteasi. Questo tipo di strategia utilizzata per modulare lo stimolo iniziale è detta via degradativa.
Altre strategie utilizzate per disattivare sono la ricaptazione, la quale prevede l’utilizzo di trasportatori di membrana (vescicole) che allontanano i neurotrasmettitori dallo spazio extracellulare inglobandoli al proprio interno e il sequestro da parte di una proteina con sito di legame simile a quello del sito recettoriale che lega e sequestra le molecole segnale nello spazio.
Meccanismi di disattivazione canale controllato meccanicamente (mechanosensitive channel): canale attivato da stress meccanico che ne altera la conformazione;
canale attivato dal potenziale (voltage-gated channel): canale attivato dalla variazione del potenziale elettrico. Per quanto riguarda la struttura sono costituiti da subunità identiche associate o domini omologhi. In particolare, quelli per sodio e potassio sono formati da 4 subunità formate da 6 alfa eliche. Di queste, 5 sono formate da grandi residui idrofobici, mentre la 4 contiene un residuo cationico (carica positiva, come lisina e arginina). I filtri di selettività sono costituiti dalla grandezza del canale, che opera selezione stereochimica, e dalle zone cariche. Quando si apre il canale possono passare anche ioni più piccoli e con la stessa carica. Nel canale del potassio, però, lo ione sodio non può passare poiché non forma efficientemente quanto il potassio un guscio di pseudoidratazione con le catene laterali dei residui del poro. Pertanto in tale tipo di canale la dimensione da considerare è quella della forma idratata.
In generale i canali per ioni presentano subunità multiple o domini omologhi. In genere sono formati da 4 (voltage-gated), 5 (ligand-gated) o 6 (ligand e voltage gated) subunità/domini. Un esempio di canale costituito da 6 subunità sono le giunzioni comunicanti. La selettività del canale è determinata dalla dimensione del poro e da anelli di residui carichi attorno all’accesso. I canali sono quasi sempre proteine allosteriche che in base a segnali variano la loro conformazione.
Trasporto attivo
Uniporto (trasporto passivo), simporto e antiporto
Il trasporto attivo è mediato da proteine di membrana e si occupa di trasferire molecole contro un gradiente di concentrazione. Si tratta di un processo energeticamente sfavorevole, pertanto questi trasportatori possono agire solo accoppiando una fonte di energia, ottenuta tramite l’idrolisi di ATP, il potenziale chimico ed elettrico e l’accoppiamento del trasporto di una sostanza contro gradiente con uno secondo gradiente. Esistono diversi tipi di trasportatori attivi:
uniporto, che trasporta una sola sostanza secondo gradiente di concentrazione. Appartengono a questa classe i trasportatori per gli amminoacidi neutri come prolina e glicina.
simporto, che trasporta due sostanze nella stessa direzione, una in direzione del proprio gradiente e una contro gradiente. Un esempio di tale tipo di trasportatore è costituito dal simporto Na+-glucosio, noto anche come SGLUT, che concentra il glucosio all’interno degli epiteli intestinali.
antiporto, che trasporta due sostanze in direzioni opposte, una in direzione del proprio gradiente e una contro gradiente. Tra di essi si annoverano i trasportatori per amminoacidi neutri/cationici come la cisteina e il trasportatore Cl-/HCO3-, il quale trasporta il bicarbonato all’interno o all’esterno degli eritrociti secondo un meccanismo dipendente dalla pressione parziale della CO2.
Pompe ioniche principali
Tra questi sono presenti le cosiddette pompe ioniche, proteine che necessitano di energia per pompare ioni contro gradiente di concentrazione. Si tratta di proteine integrali di membrana che derivano l’energia generalmente idrolizzando ATP. Sono transitoriamente fosforilate. Un esempio è costituito dalla pompa sodio-potassio ATPasica, la quale trasporta tre ioni sodio verso l’esterno e due ioni potassio verso l’interno entrambi contro gradiente. All'inizio del processo di trasporto tre ioni di Na+ vanno a legarsi ai siti specifici ad alta affinità della proteina veicolo rivolti verso l'interno della cellula. Questo legame stimola la fosforilazione dipendente dall'ATP della pompa determinando un cambio conformazionale della proteina veicolo, la quale esporrà i siti di legame per gli ioni Na+ verso l'ambiente extracellulare, abbassando così la propria affinità per questi ioni cosicché essi vengano rilasciati al di fuori della cellula. Contemporaneamente alla fuoriuscita degli ioni Na+, due ioni K+ vanno a legarsi ai siti specifici esposti verso l'ambiente extracellulare stimolando la defosforilazione della proteina, la quale tornerà al suo stato conformazionale di partenza e rilascerà questi ioni all'interno della cellula. Una volta completata l'operazione, la proteina sarà pronta a ripetere il ciclo. Questo meccanismo viene definito di eversione/inversione. Un’altra pompa ionica è la pompa calcio ATPasica. A livello del reticolo sarcoplasmatico prende il nome di SERCA e ha il compito di trasferire due ioni calcio dal citoplasma al reticolo sarcoplasmatico trasportandolo contro gradiente al fine di promuovere il rilassamento muscolare. E’ un omodimero con quattro domini funzionali: TM, dove si lega il calcio, A, che funge da adattatore, P, dove avviene la fosforilazione e N, dove si lega il nucleotide. Presenta inoltre due diverse conformazioni: E1 ed E2. Quando la proteina si trova in E1 il calcio entra nel dominio TM contemporaneamente all’ATP nel dominio N. Si attiva il dominio P che porta alla fosforilazione (trasferimento di un gruppo fosfato su un residuo di aspartato mediato da magnesio). SI forma la struttura fosforilata E1-P, cui segue l’eversione in E2-P. La pompa perde affinità per il calcio, che esce. La perdita di calcio promuove la perdita di ADP, la defosforilazione (passaggio alla forma E2) e il ritorno alla forma E1.
Altri tipi di trasportatori attivi
Ci sono diversi trasportatori ATPasici:
ATPasi V (vacuoli): trasportano ioni H+ e sono responsabili dell’acidificazione dei compartimenti;
ATPasi F o ATPsintasi: il flusso di protoni H+ contro gradiente promuove la sintesi di ATP, tramite la condensazione di ADP e Pi.
trasportatori ABC o ATP Binding Cassette: intervengono nel trasporto di una grande quantità di sostanze attraverso le membrane endo ed extra cellulari, inclusi farmaci, prodotti metabolici, lipidi e steroli.