Chemie examen
Inleiding
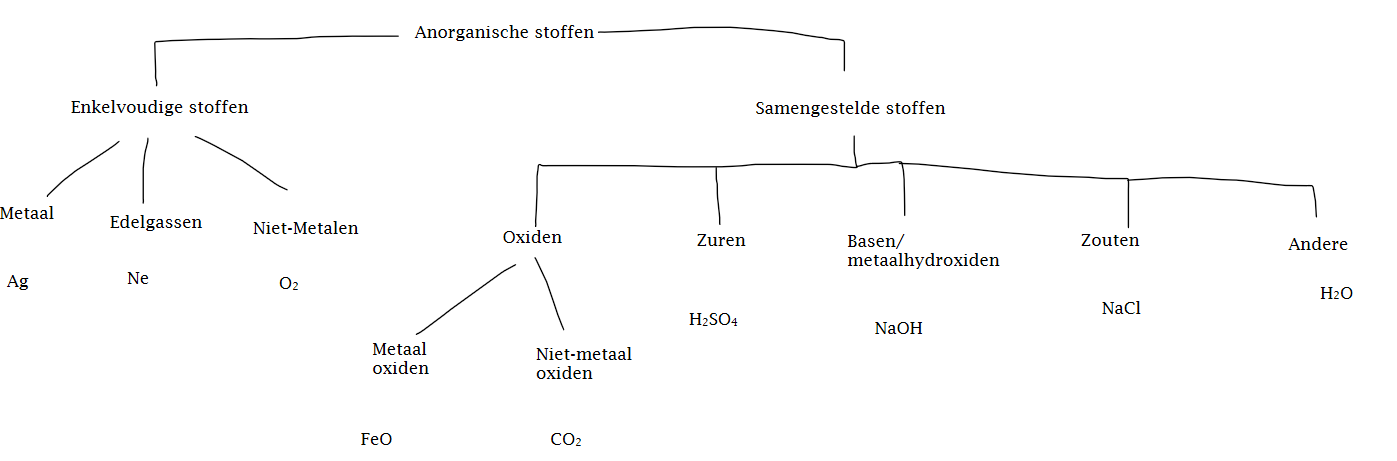
Enkelvoudige stof = een stof die bestaat uit slechts één soort chemisch element, wat betekent dat alle atomen in de stof van dezelfde soort zijn.
Samengestelde stof = een chemische verbinding die bestaat uit twee of meer verschillende chemische elementen die chemisch aan elkaar gebonden zijn in een vaste verhouding
Verschil: Het verschil is dat een enkelvoudige stof bestaat uit slechts één soort atomen van hetzelfde element, terwijl een samengestelde stof bestaat uit twee of meer verschillende soorten atomen van verschillende elementen die chemisch aan elkaar gebonden zijn.

Protonen, elektronen en neutronen te weten:
Protonen = atoomnummer dus, 12
Elektronen = ZONDER LADING!! is hetzelfde aan aantal protonen, dus ook 12
Neutronen = massagetal - atoomnummer/protonen, 24 - 12 = 12
Chemische bindingen
Covalente binding = Nm + Nm
Metaalbinding = M + M
ionaire binding = M + Nm
Hoofdstuk 1
Oxiden
Metaaloxiden
Bouw metaaloxide:
ionaire stoffen = m + Nm
Positieve metaalionen: M+
Negatieve oxide-ionen: O2-
Formules en naamgeving
Metaal uit Ia, IIa, IIIa met gekende lading
→ kruisregel toepassen
Vb: Oxide van Na
Na+ en O2- → Na2O
Metaal niet uit Ia, IIa, IIIa, ongekende lading
mevr Soens regel
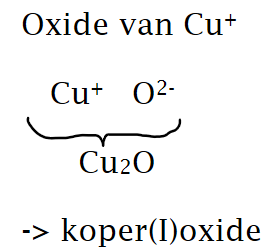
Soorten notaties
→ stocknotatie: FeO → ijzer(II)oxide
→ naam met indexen: Fe2O3 → di-ijzertrioxiden
Vorming van metaaloxiden
metaaloxiden kunnen gemaakt worden door een metaal te verbranden
om de correcte reactievergelijking te schrijven volg je best deze stappen:
aan linkerkant van de reactiepijl schrijf je de formule van het metaal en die van O2, van elkaar gescheiden door een plusteken
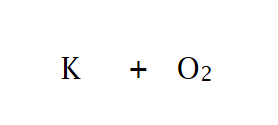
aan de rechterkant noteer je de correcte formule van het metaaloxide
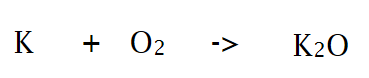
tenslotte pas je de voorgetallen aan zodanig dat alle elementen evenveel keer voorkomen aan beide kanten van de reactiepijl
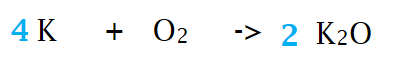
Niet-metaaloxiden
Bouw
Covalente bindingen ( Nm+ Nm)
Formules en naamgeving
Griekse voorvoegsels
1 | mono |
2 | di |
3 | tri |
4 | tetra |
5 | penta |
6 | hexa |
7 | hepta |
8 | octa |
9 | nona |
10 | deca |
bekendste niet-metaaloxiden zijn: koolstofmonoxide ( CO ) en koolstofdioxide ( CO2 )
Vorming van niet-metaaloxiden
gemaakt door een niet-metaal te verbranden
Zuren
Bouw van een zuur
covalente stoffen ( Nm + Nm ) → geen ionen!
bevatten altijd 1 of meerdere waterstofatomen met een zuurrest
zuurrest is ofwel een:
niet-metaal: binair zuur
niet-metaal en 1 of meer O: ternair zuur en oxozuur
Formules en naamgeving
alle zuren bevatten 1 of meer waterstofatomen in hun formule.
Vorming van zuren
binaire zuren worden gevormd door reactie tussen een niet-metaal en waterstofgas. Ternaire zuren kunnen gemaakt worden door een niet-metaaloxide te laten reageren met water ( H2O )
→ binair : H2 + nM
→ ternair : nMO + H2O
Vb:
De reactie voor de vorming van fosforzuur uit disfosforpentaoxide
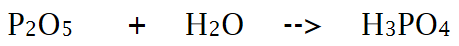
voorvoegsels
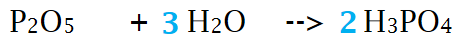
Eigenschappen
wanneer zuren worden opgelost in water → moleculen breken in stukken.
brokstukken zijn ionen = splitsing in ionen: H+ -ion en zuurrest-ion
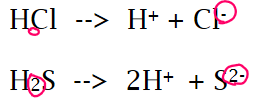
zuren zijn corrosief = ze tasten andere stoffen aan:
onedele metalen( edele metalen = goud, zilver, platina ): hierbij wordt waterstofgas gevormd en metaal lost op. denk aan proef met trouwring in zuur
kalksteen: hierbij wordt CO2 gevormd, kalksteen lost op. Heeft gevolgen voor gebouwen uit kalksteen of marmer ( zure regen, buitenste laag wordt aangetast )
organisch materiaal: zuren veroorzaken vaak brandwonden, zuren met een hoog concentratieniveau kan ernstige gevolgen hebben.
Binaire zuren
Binaire zuren bevatten naast waterstof nog 1 ander niet-metaal!
→ de naam eindigt op de uitgang -ide
Formule | Syst. naam | Triviaalnaam |
HF | waterstoffluoride | |
HCl | waterstofchloride | zoutzuur |
HBr | waterstofbromide | |
HI | waterstofjodide | |
H2S | waterstofsulfide | |
HCN | waterstofcyanide | blauwzuur |
Ternaire zuren
zijn zuren die naast waterstof ook nog een tweede niet-metaal en 1 of meer zuurstofatomen bevatten. vaak meerdere combinaties → onderscheid tussen stamzuren en afgeleide zuren
Stamzuren eindigt op uitgang -aat
stamzuren hebben een verschillend aantal waterstof en zuurstofatomen
Stamzuren:
Formule | syst. naam | triviaalnaam |
HClO3 | waterstofcloraat | chloorzuur |
HNO3 | waterstofnitraat | salpeterzuur |
H2CO3 | waterstofcarbonaat | koolzuur |
H2SO4 | waterstofsulfaat | zwavelzuur |
H3PO4 | waterstoffosfaat | fosforzuur |
afgeleide ternaire zuren bevatten minder of meer zuurstofatomen dan hun stamzuur!
het aantal waterstofatomen blijft gelijk!
Als er 1 zuurstofatoom minder is dan het stamzuur dan eindigt de naam op de uitgang -iet !!!!!
Afgeleide ternaire stamzuren:
Stamzuur | afgeleid zuur | syst. naam |
HClO3 | HClO2 | waterstofchloriet |
HNO3 | HNO2 | waterstofnitriet |
H2SO4 | H2SO3 | waterstofsulfiet |
H3PO4 | H3PO3 | waterstoffosfiet |
bij de zuren die chloor bevatten zijn er nog 2 extra mogelijkheden: men gebruikt voorvoegsels
: waterstofhypochloriet ( nog 1 zuurstof minder dan waterstofchloriet )
HClO4 : waterstofperchloraat ( 1 zuurstof meer dan waterstofchloraat )
Metaalhydroxiden / basen
Bouw van een metaalhydroxide
ionaire stoffen ( M + nM )
positieve metaal ionen: Mx+
negatieve hydroxide-ionen: OH-
Formules en naamgeving
metalen waarvan de lading van het ion gekend is:
kruisregel!!!!
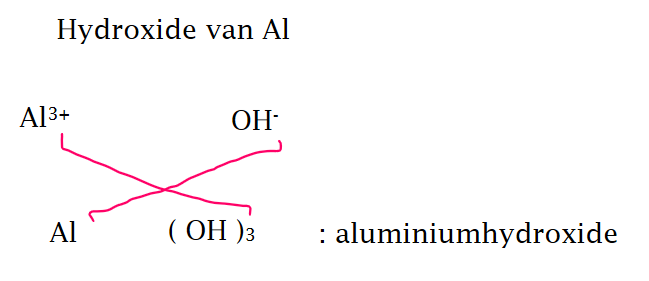
metalen waarvan de lading van het ion ongekend is:
lading moet gegeven worden,
ook zelfde kruisregel
net als bij de metaaloxiden worden 2 namen gebruikt:
de Stocknotatie: hierin schrijven we de lading van het metaal tussen haakjes na de naam van het metaal in Romeinse cijfers vb: chroom(III)hydroxide
de naam met indexen: vb: chroomtrihydroxide
voorkeur aan stocknotatie
UITZONDERING!
Ammoniak, Dit is een base die geen metaalhydroxide is maar een covalente stof met als formule NH3
want: bevat geen metaal, bevat geen hydroxide is wel covalent maar heeft wel dezelfde eigenschappen als metaalhydroxiden
Vorming van metaalhydroxiden
metaalhydroxiden ontstaan door metaaloxide te laten reageren met water
metaaloxiden worden daarom ook wel basevormende oxiden genoemd
Belangrijk ! Vorming van vb: natriumhydroxide ( reactie tussen natriumoxide en water )
vorm juiste formules
natriumoxide: Na+ O2- → Na2O
water: H2O
natriumhydroxide: Na+ OH- → NaOH
Na2O + H2O → 2 NaOH
Voorgetallen : 2
Eigenschappen van basen
Basen lossen in eiwitten op!
geconcentreerde oplossingen van base zijn dus heel belangrijk!
wanneer een base wordt opgelost in water, valt het ionenrooster uit elkaar
hierbij worden hydroxide-ionen gevormd.
Waarom is ammoniak een base? Wanneer ammoniak met water reageert bekomt het ammoniumhydroxide dat erna uiteenvalt in ionen , zoals andere basen.
Zuurtegraad van een oplossing
Zuur-base indicatoren
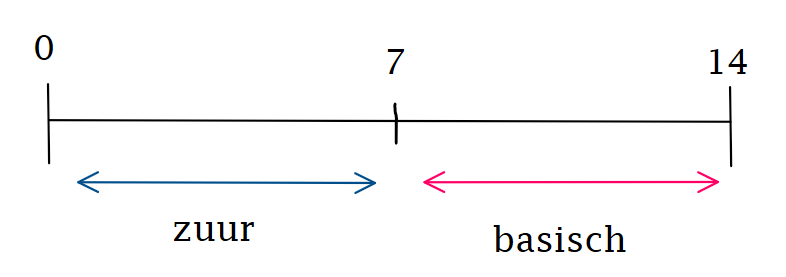
7 = neutraal ( H2O )
Hoe lager de pH-schaal, hoe zuurder
Hoe hoger de pH-schaal, hoe basischer
Een zuur-base-indicator is een kleurstof waarmee je kan aantonen of een oplossing een zuur of base bevat.
Natuurlijke en synthetische indicatoren
natuurlijk: rode kool
indicator | zure kleur | basische kleur |
fenolftaleïne fft | kleurloos | paars |
broomthymolblauw btb | geel | blauw |
methyloranje mo | rood | geel |