1. RECOMBINANT-DNA TECHNOLOGIE
In de moderne biotechnologie vormt recombinante DNA-technologie de basis voor het op grote schaal bestuderen van genen en het produceren van eiwitten. Hoewel PCR een onmisbare tool is voor de initiële amplificatie, fungeert de bacterie als de uiteindelijke, kosteneffectieve fabriek. In vivo replicatie biedt namelijk niet alleen een superieure foutcorrectie en enorme schaalbaarheid, maar stelt de cel ook in staat om het ingebrachte genetische recept daadwerkelijk te vertalen naar functionele eiwitten.
Kloneren is het gecontroleerd inbrengen van een individuele DNA molecule in een autonoom replicerende vector → recombinant DNA = combinatie van DNA moleculen met verschillende oorsprong
opm; wij bespreken in wat volgt enkel het gebruik van plasmiden als vectoren
PLASMIDE
PROKARYOTE KLONERINGSVECTOR
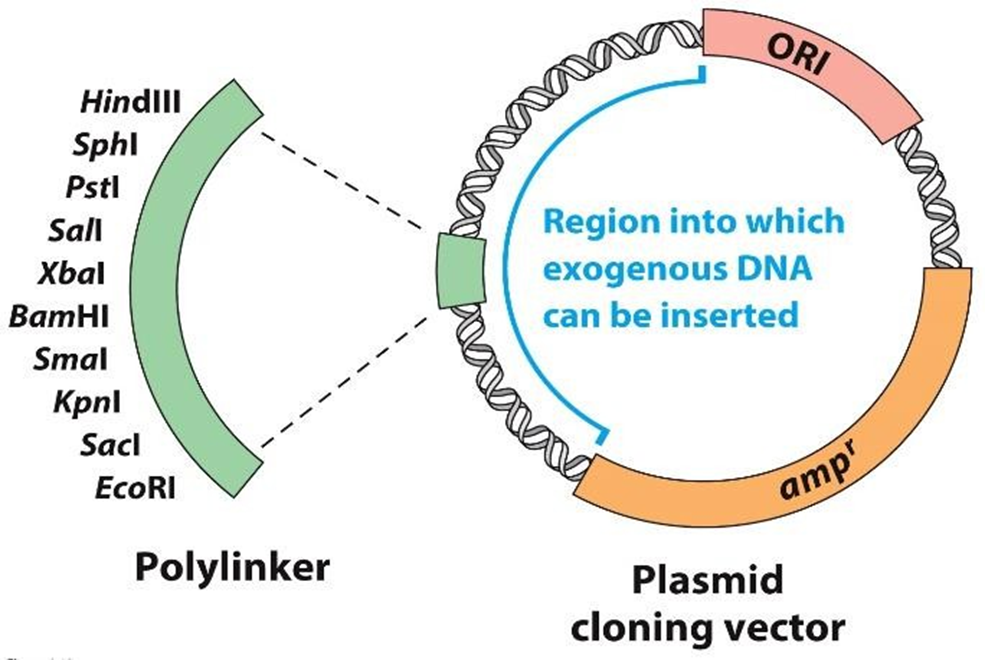
beperkt in grootte
insertieplaats voor vreemd DNA
polylinker = multiple cloning site = MCS
bevat herkenningsplaatsen voor restrictie-enzymen
ORI = origin of replication
resistentiegenen
natuurlijk aanwezig
resistentie tegen ampicilline = ampr
geen promotor aanwezig → geen expressie
EUKARYOTE / PROKARYOTE EXPRESSIEVECTOR
= “SHUTTLE VECTOR”
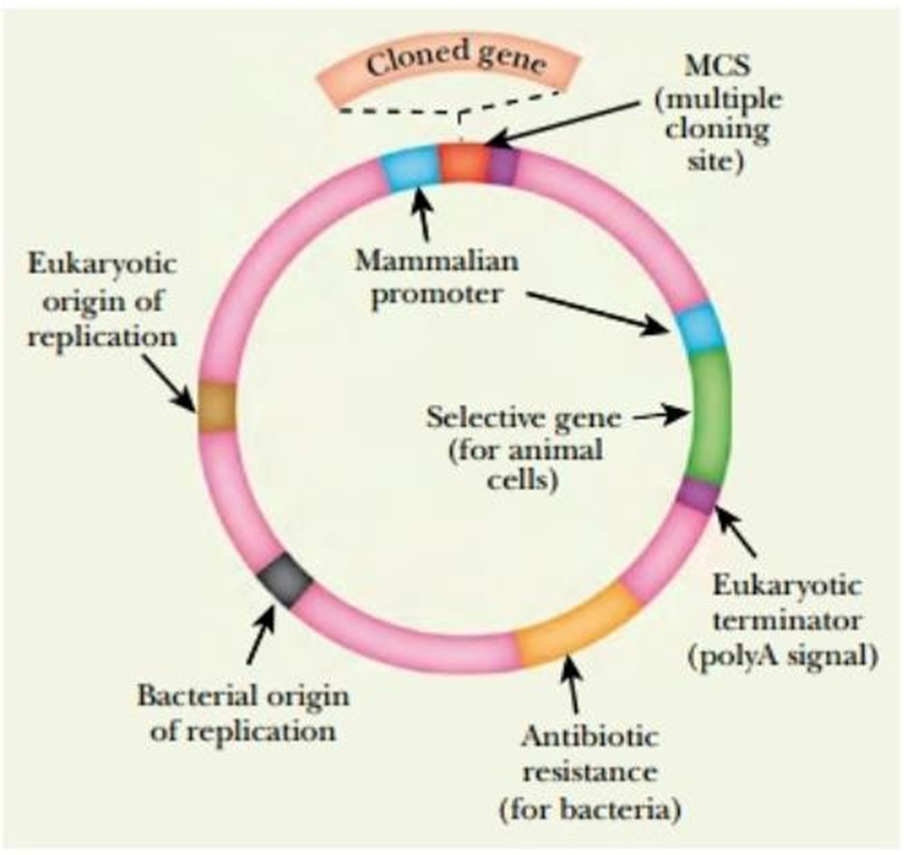
beperkt in grootte, complexer dan plasmide voor enkel prokaryoten
replicatie
2× ORI = origin of replication
verschillend voor pro- en eukaryoot
transcriptie
promotor nodig; RNA moet kunnen binden vóór MCS
terminatiesignaal voor loskomen transcript
selectiegen (eukaryoot) ~ antibiotica-resistentiegen (prokaryoot)
“KNIP-EN-PLAK”
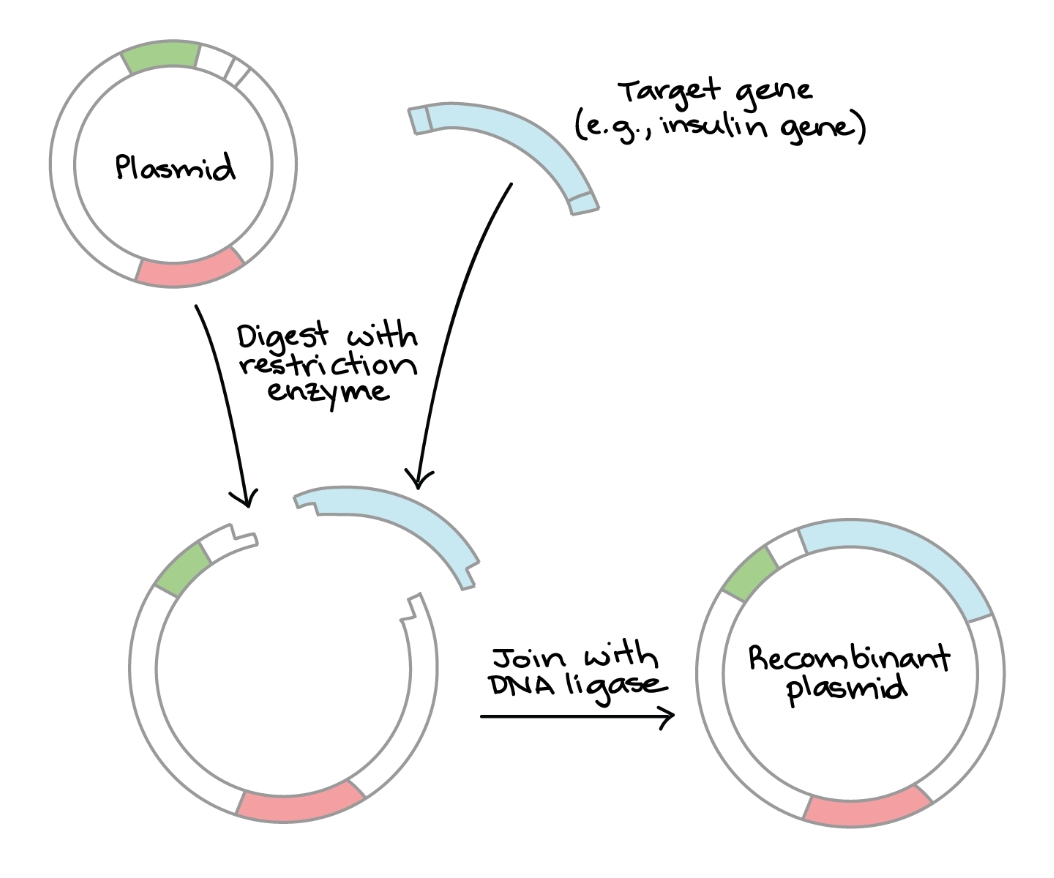
restrictie-enzymen
natuur; afweer tegen bacteriofaag infectie
labo; “moleculaire scharen”
bescherming tegen knipping in bacterieel genoom;
knippen enkel in bepaalde bacteriestam(men)
niet werkzaam bij gemethyleerd DNA
werkwijze
knip met zelfde restrictie-enzym;
in MCS v/h vector-DNA = plasmide-DNA → openen vector
insert-DNA = vreemd-DNA*
geknipte DNA-stukken samenvoegen + DNA ligase
resultaat; recombinant plasmide
opm*; het gebruikte DNA is niet rechtstreeks, in die vorm, terug te vinden in de cellen, het DNA wordt op een specifieke manier bekomen; DNA → mRNA → cDNA door reverse transcriptase opdat het klein genoeg zou zijn, én bovendien ook minder complex (bacteriën “begrijpen” intronen niet) (zie ook verder)
opm; over het algmeen worden DAM+ bacteriestammen gebruikt bij kloneren vanwege de goede mismatch repair, maar in één specifiek situatie moet je DAM- bacteriestammen gebruiken;
DAM = DNA adenine methylase
enzym methyleert adenines in het DNA op specifiek herkenningsmotief, namelijk 5’ — GATC — 3’
methylatie beïnvloedt negatief werking restrictie-enzymen; indien de herkenningsplaats van restrictie-enzym dus ligt op, of direct naast de herkenningssequentie voor DAM, dan zouden we problemen ondervinden
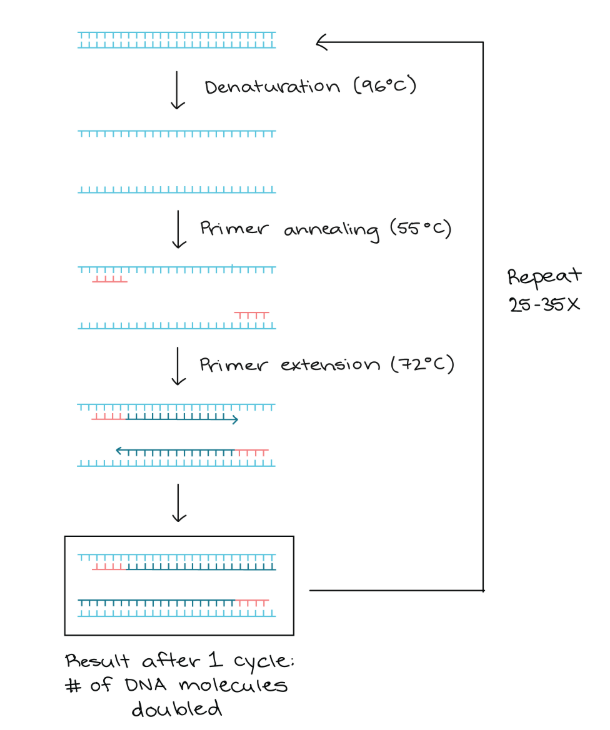
TOEPASSING PCR
PCR is een vaak gebruikte tool binnen het grotere proces van recombinant DNA-technologie, vooral handig om een specifiek gen van cDNA voor te bereiden op cloning;
cDNA amplificeren
we voegen op het cDNA restrictieplaatsen toe via de primers; zo past het gen later als een puzzelstukje perfect in de plasmide
PROBLEEMSTELLING
bij eukaryoten bevat een gen intronen en exonen;
exonen: stukjes DNA die coderen voor eiwitten
intronen: stukjes DNA die niet coderen en verwijderd moeten worden voor een werkend eiwit
plasmiden (kleine circulaire DNA-moleculen gebruikt voor cloning) kunnen meestal max. 10 kb aan DNA bevatten; grote intronen maken het moeilijk om het gen in een plasmide te zetten — bovendien kunnen de meeste bacteriën niet omgaan met intronen, deze zijn te complex
we kunnen dus niet zomaar in DNA gaan knippen, want deze bevat de grote sequenties aan intronen waar geen plaats voor is
OPLOSSING
mRNA is al ‘gespliced’; alle intronen verwijderd, alleen exonen over
isoleren mRNA uit cel;
Poly-A staart mRNA bindt aan oligo(dT)-strengen
vormen complementair DNA (cDNA);
door reverse transcriptase (enzym)
resultaat; DNA-versie van het gen, zonder intronen, dat in plasmide past
PCR cDNA
gebruik van PCR heeft 2 belangrijke functies;
amplificeren van één bepaalde sequentie
specifieke primers ontwerpen om alleen het gen van interesse te amplificeren
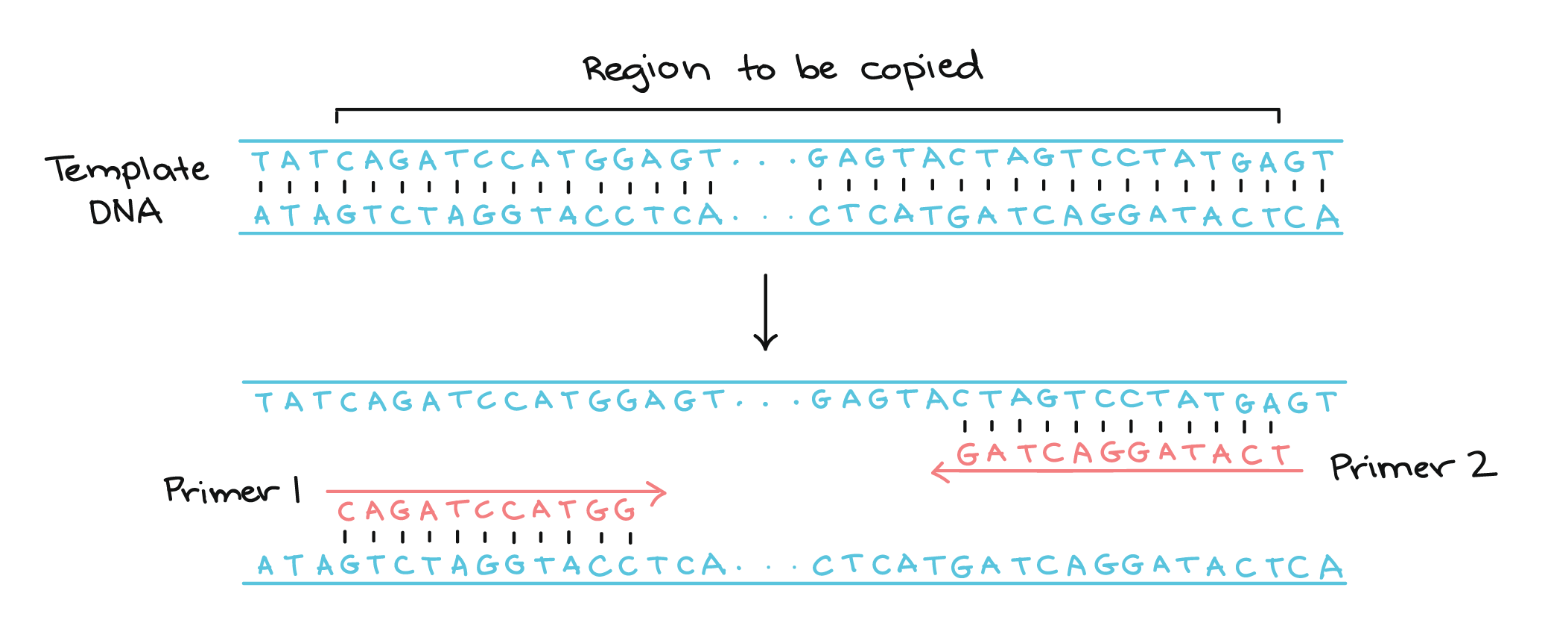
Primers worden steeds aan 3’ v/d DNA-streng gebonden, bij de start v/h gen van interesse;
3’ kant primer = bindend deel; complementair aan je gen, zorgt dat PCR kan starten
5’ kant primer = overhangend deel; "hangt" in het begin los, het bevat de code voor de knipplaats van het RE — na de eerste paar cycli v/d PCR is deze volledig geïncorporeerd in alle nieuwe DNA-strengen
Stel dat de onderste streng de template strand is, dan stelt primer 1 de “forward” primer voor en primer 2 de “reverse” primer. Het overhangend eindje van de “forward” primer bevat steeds de knipplaats voor het RE dat het dichtst bij de promotor zit.
Hieronder voorgesteld is ons gen van interesse, gelegen tussen beide primers. Merk op dat de eigenlijke DNA strengen veel langer zijn en doorlopen langs beide kanten (3’ en 5’). Het “overhangend” eindje is daarbij niet complementair met die strengen en hangt dus los.
5’ ___________________________ 3’
3’ ————— 5’
5’ __________ 3’
3’ ——————————————— 5’
Door twee verschillende restrictieplaatsen te kiezen, dwing je het gen om in de juiste richting in de plasmide te gaan zitten; dit noemen we directionele klonering. Dit is cruciaal, want als het gen er ondersteboven in zou komen, leest de bacterie de foute streng af en wordt bijgevolg een foute keten aminozuren gemaakt, waardoor we niet het juiste, functionele eiwit verkrijgen. De "forward" primer (zit steeds op de template strand) moet altijd de knipplaats bevatten voor het restrictie-enzym dat het dichtst bij de promotor van de plasmide zit.
RECOMBINANT DNA TECHNOLOGIE
geamplificeerde gen → plasmide → gastheercel (vb. bacterie)
in gastheercel; amplificatie gen / productie eiwit
SAMENGEVAT
probleem; eukaryotisch gen bevat intronen
mRNA + reverse transcriptase (RT) → cDNA zonder intronen
toepassing PCR
amplificatie cDNA
knipplaatsen RE toevoegen
toepassing recombinant DNA-technologie
kloneringsvector; amplificatie gen van interesse
expressievector; gastheercellen produceren eiwitten
INBRENGEN PLASMIDE IN GASTHEER
We bespreken transformatie, transfectie en transductie;
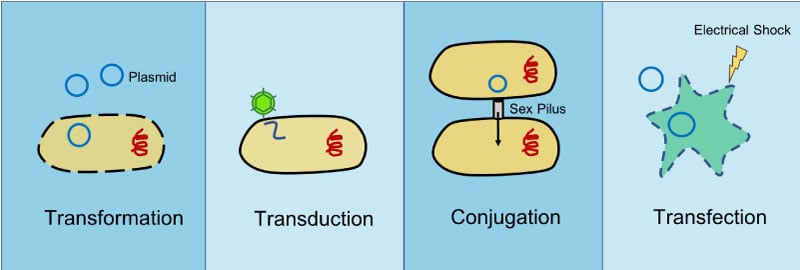
TRANSFORMATIE — PROKARYOTEN
doel; DNA (meestal plasmide) in bacteriën krijgen
mechanisme;
bacteriën worden “competent” gemaakt
nemen plasmide-DNA op uit de omgeving
COMPETENT MAKEN BACTERIËN
chemisch — CaCl₂ + hitteshock
DNA is negatief geladen (door fosfaatgroepen) en de celwand van de bacterie is ook negatief, ze stoten elkaar af
positieve calcium-ionen fungeren als een bruggetje dat de lading neutraliseert, waardoor het DNA tegen de celwand aan kan gaan liggen
temperatuurverschil zorgt voor een plotselinge drukverandering en creëert tijdelijke poriën in het membraan waardoor het DNA naar binnen glipt
fysisch — elektroporatie
meer efficiënt, maar ook invasiever
bacteriën krijgen een korte, krachtige elektrische stroomstoot
elektriciteit blaast tijdelijk gaatjes (poriën) in het celmembraan, waardoor het DNA direct naar binnen kan stromen
WELKE KOLONIES HEBBEN PLASMIDE MÉT INSERT OPGENOMEN?
RESTRICTIEDIGEST
je haalt plasmide uit de bacterie;
U = undigested; negatieve controle
D = digested = verknipping met zelfde RE als waarmee je oorspronkelijk hebt gewerkt; band bij verwachte grootte van insert?
opm; mogelijke stukken die je op gel kan terugvinden: lege plasmide, los insert of plasmide mét insert (indien knipping niet volledig gelukt/mislukt)
KOLONIE PCR
je test rechtstreeks een stukje bacterie uit een kolonie als template met dezelfde primers die je eerder gebruikte
band op verwachte grootte insert?
opm; als je ook juiste oriëntatie wil controleren; gebruik één primer die op de plasmide bindt (vlak voor het gen) en één primer die op gen zelf bindt — alleen als het gen in de juiste oriëntatie zit, wijzen de primers naar elkaar toe en krijg je een bandje op je gel. Zit het gen er omgekeerd in? Dan wijzen ze van elkaar af en zie je niets!
BLUE-WHITE SCREENING
bacteriën zijn niet resistent tegen ampicilline, plasmide bevat een resistentiegen
plasmide bevat daarnaast ook lacZα-fragment dat β-galactosidase (enzym) produceert, dit enzym is een "schaartje" dat de stof X-gal (die op voedingsbodem aanwezig is) doorknipt → diepblauwe kleur
binnen lacZα-fragment zit een MCS; indien het insert aanwezig is, is die op de MCS ingebracht waardoor productie β-galactosidase wordt stopgezet
geen plasmide → geen groei op ampicilline
plasmide zonder insert → groei kolonie met β-galactosidase (blauw)
plasmide mét insert → groei kolonie zonder β-galactosidase (wit)
opm; soms zie je witte kolonies die tóch geen insert hebben; dit gebeurt als er een mutatie in het lacZ-gen is opgetreden
Kenmerk | 1. Restrictiedigest | 2. Kolonie PCR | 3. Blue-white screening |
Focus: Wat test je? | De fysieke aanwezigheid en grootte van de insert. | De aanwezigheid van de DNA-code (sequentie). | De verstoring van het lacZ-gen (indirecte indicatie). |
Grootste Voordeel | Hard bewijs: Je ziet het losse "puzzelstukje" echt op de gel liggen. | Snelheid: Je kunt tientallen kolonies tegelijk testen zonder DNA te zuiveren. | Eerste filter: Je hoeft alleen kolonies te onderzoeken die potentieel goed zijn. |
Grootste Nadeel | Arbeidsintensief: Je moet de plasmiden eerst uit de bacterie isoleren (miniprep). | Kans op vals-positieven door achtergebleven DNA op de plaat. | Onzekerheid: Een witte kolonie zegt niets over de lengte of richting van je gen. |
Resultaat op Gel/Plaat | Twee bandjes: één voor de vector en één voor je insert. | Eén bandje op de verwachte grootte van je gen. | Witte kolonies (met insert) vs. Blauwe kolonies (zonder insert). |
TRANSFECTIE — EUKARYOTEN
doel; DNA (plasmide, siRNA, vectoren…) in eukaryote cellen krijgen
mechanisme;
chemisch
DEAE-dextraan
calcium / fosfaat = CaPO₄
liposoom gemedieerd
fysisch
micro-injectie
elektroporatie
TRANSDUCTIE — PRO- EN EUKARYOTEN
doel; DNA in cellen krijgen via infectie virussen
mechanisme;
prokaryoot; bacteriofaag infecteert cellen
eukaryoot; lentivirus infecteert cellen
LENTIVIRALE TRANSDUCTIE
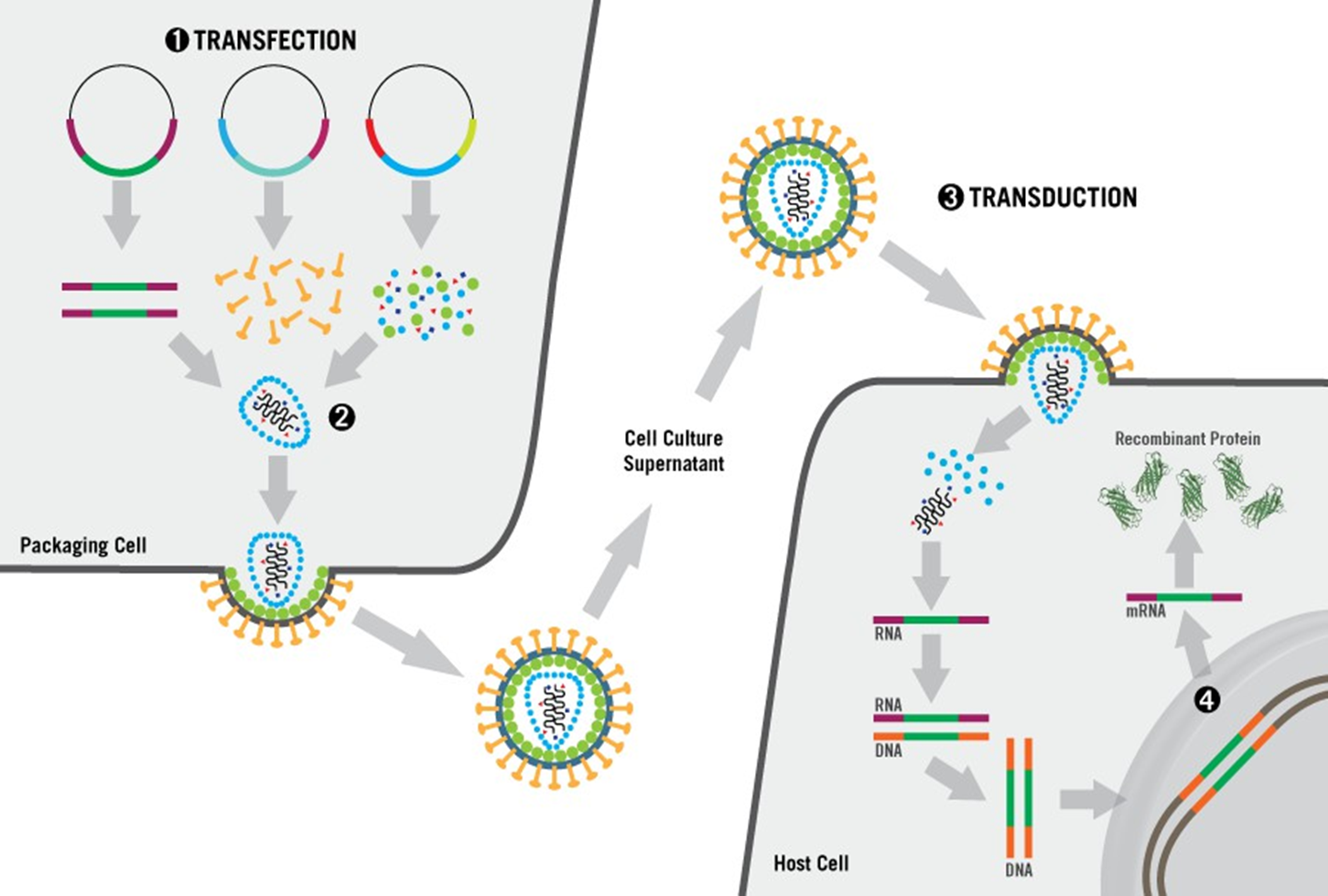
TRANSFECTIE
Plasmide | Functie | Belangrijkste onderdelen |
transfer | "recept" dat vervoerd moet worden | LTR's, -signaal, promotor + transgen |
packaging = helper | "fabrieksmachine", levert structurele en enzymatische eiwitten die nodig zijn om virusdeeltjes te bouwen | gag (structuur: capside + matrix) en pol (enzymen: RT, integrase, protease) |
envelope = viral-coat | vormt "buitenkant" (bepaalt het adres) | vaak VSV-G (voor een breed tropisme) |
opm; de genetische code (het RNA) voor Gag, Pol en Env. wordt niet mee verpakt; doelcel krijgt wel het transgen, maar niet de instructies om nieuwe Gag/Pol-eiwitten te maken → virus kan zich in de doelcel niet meer vermenigvuldigen
opm; tropisme = “welke cellen kunnen geïnfecteerd worden?”
VIRUSSTRUCTUUR
geel → envelope spikes voor binding aan doelcel
groen → lipide membraan; dit steelt het virus van de producer-cel wanneer het naar buiten "budt"
blauw stippenpatroon → matrix/capside-eiwitten; beschermende huls rondom het genetisch materiaal
zwart kronkelend binnenin → ingepakte virale RNA v/h vectorplasmide; dit is het enige deel dat het -signaal bevat, waardoor de cel weet: "dít moet ik inpakken"
TRANSDUCTIE
fusie: virus landt op de cel en versmelt ermee
uncoating: capside valt uit elkaar
reverse transcriptie: enzym RT maakt van het virale RNA een dubbelstrengig DNA
integratie: enzym integrase opent DNA v/d gastheer en plakt transgen er middenin
expressie: doelcel ziet het nieuwe stukje DNA nu als zijn eigen code en begint het eiwit te produceren
opm; In de meeste gevallen blijft het plasmide "los" in het cytoplasma, bij prokaryoten, of los in de kern, bij eukaryoten, zweven. Het wordt niet vastgeplakt aan de menselijke chromosomen. Na verloop van tijd, als de cel deelt, gaat de plasmide vaak verloren. Dit noemen we transiënte (tijdelijke) expressie. MAAR uitzonderlijk bij lentivirussen wordt het gen wél in het chromosoom geplakt. Elke keer als die cel deelt, wordt dat nieuwe stukje netjes mee gekopieerd als onderdeel van het eigen genoom.