Bio 2.2.-2.3. p267-271
2.2. Structuur en functie van een ribosoom
Na de transcriptie verlaat het rijpe mRNA de kern en komt het in het cytoplasma terecht.
Daar wacht het ribosoom.
Een ribosoom bestaat uit 2 ongelijke delen:
De kleine subeenheid
bindt het mRNA
zorg ervoor dat de codons op het mRNA correct worden gelezen
controleerd of het anticodon (tRNA) complementair is aan het codon op het mRNA
De grote subeenheid
bevat ‘peptidyl trans ferase centrum’ PT
plek waar de peptidebindingen tussen aminozuren worden gevormd
Deze subeenheden vormen samen een volledig werkend ribosoom.
Beide subeenheden bestaan uit:
Ribosomaal RNA (rRNA)
Ribosomale proteïnen
Het rRNA speelt een structurele rol en een katalytische functie:
Het helpt bij het vormen van de bindingen tussen aminozuren.
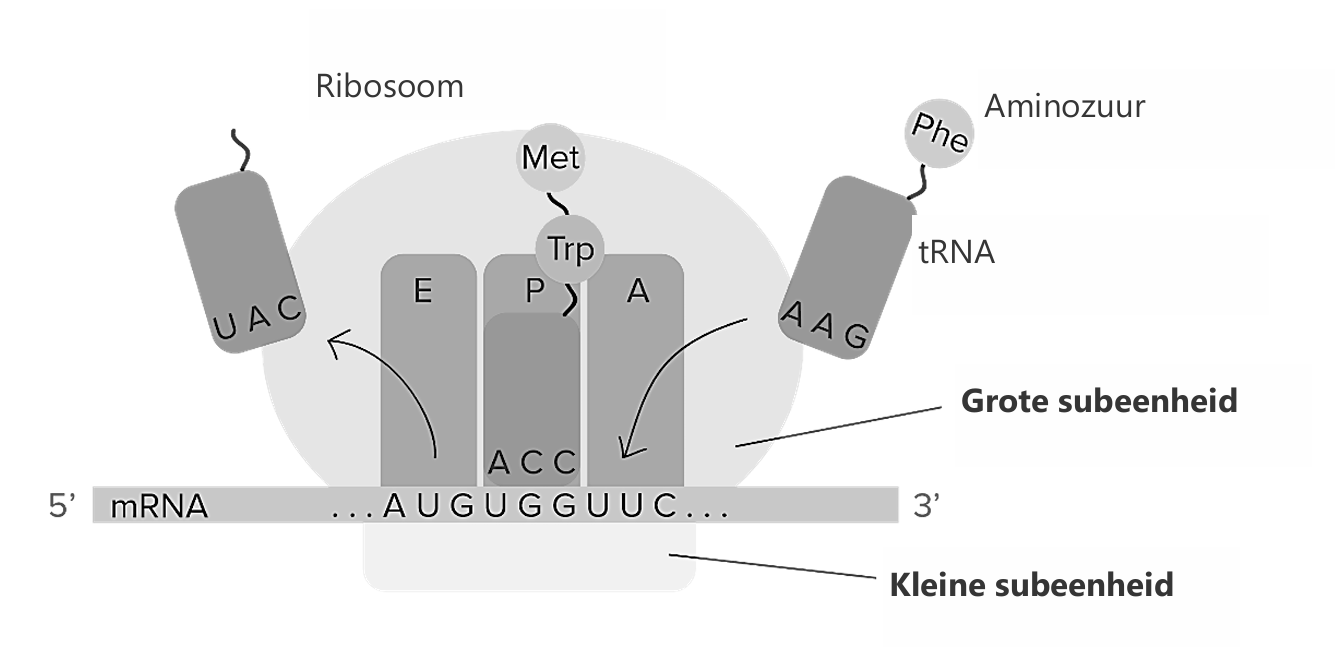
Bindingsplaatsen in het ribosoom
Samen zorgen onderstaande onderdelen ervoor dat codon per codon de juiste aminozuren in de juiste volgorde aan elkaar worden gezet.
A-plaats (Aminoacyl-plaats)
Hier komt een tRNA binnen met zijn gekoppelde aminozuur.
Het anticodon van dit tRNA moet complementair zijn aan het codon dat op het mRNA boven de A-plaats ligt.
P-plaats (Peptidyl-plaats)
Bevat het tRNA waaraan de groeiende polypeptideketen vastzit.
polypeptideketen: reeds gevormde aminozuurvolgorde
Hier vindt de ‘peptidyl transferase activiteit’ plaats:
Het aminozuur of de aminozuurketen wordt overgedragen naar het aminozuur op het tRNA in de A-plaats, waardoor de keten 1 aminozuur langer wordt.
E-plaats (Exit-plaats)
Nadat het aminozuur is overgedragen, verschuift het inmiddels “lege” tRNA naar de E-plaats en verlaat dan het ribosoom.
2.3. Translatie: mRNA naar eiwit
Translatie is de tweede grote stap van genexpressie:
Tijdens de translatie wordt de informatie in het rijpe mRNA omgezet in een polypeptideketen, die zich daarna kan vouwen tot een werkend eiwit.
Translatie gebeurt in het cytoplasma, op de ribosomen.
Translatie verloopt, net als transcriptie, in een aantal fasen.
Meestal onderscheiden we:
Activatie van aminozuren
Initiatie
Elongatie
Terminatie
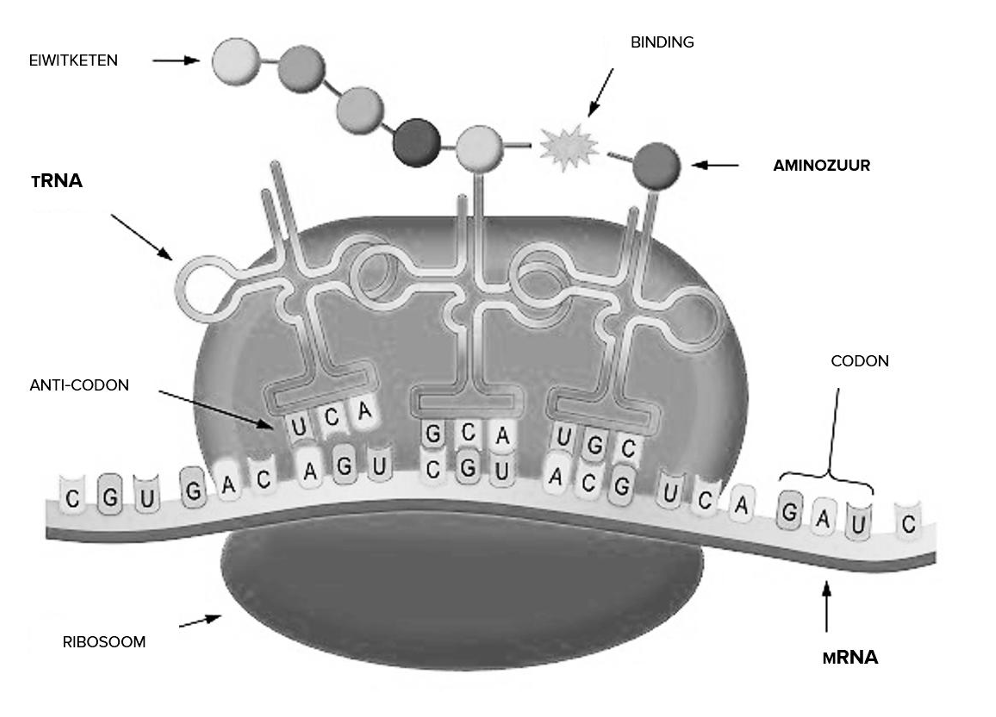
Activatie van aminozuren
Voordat een aminozuur kan worden ingebouwd in een eiwit, moet het gekoppeld worden aan het juiste transfer-RNA (tRNA).
Elk tRNA heeft een anticodon, een triplet dat complementair is aan een codon op het mRNA.
Een speciaal enzym, een aminoacyl-tRNA-synthetase, herkent zowel een bepaald aminozuur als het bijpassende tRNA.
Het enzym koppelt onder verbruik van energie (ATP) het aminozuur vast aan het tRNA:
Het resultaat is een “geladen” tRNA, klaar om zijn aminozuur naar het ribosoom te brengen.
Initiatie
Tijdens de initiatie bindt de kleine ribosomale subeenheid aan het mRNA, meestal ter hoogte van het 5’-uiteinde.
Het ribosoom “zoekt” het eerste startcodon (meestal AUG) in het juiste leesraam.
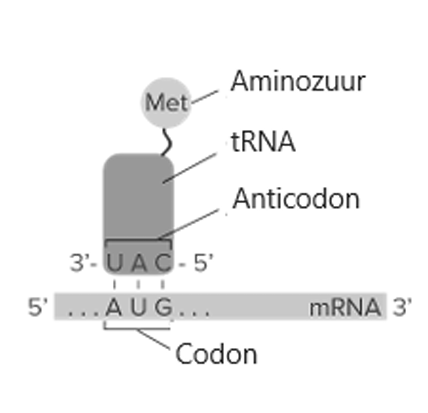
Een speciaal initiator-tRNA, dat het aminozuur methionine draagt en een anticodon heeft dat complementair is aan AUG, bindt op dit startcodon.
Wanneer het initiator-tRNA correct gepositioneerd is, bindt ook de grote subeenheid.
Zo ontstaat een volledig functioneel ribosoom, met het initiator-tRNA in de P-plaats.
Vanaf dat moment is het systeem klaar om de rest van het eiwit op te bouwen.
Elongatie
Tijdens de elongatie wordt de polypeptideketen stap voor stap verlengd:
Een nieuw geladen tRNA met een specifiek aminozuur bindt met zijn anticodon aan het volgende codon op het mRNA in de A-plaats.
Het peptidyltransferase (PT) in de grote subeenheid katalyseert de vorming van een peptidebinding tussen het aminozuur in de P-plaats en het nieuwe aminozuur in de A-plaats:
De hele keten komt zo te liggen op het tRNA in de A-plaats.
Vervolgens schuift het ribosoom 1 codon verder over het mRNA (van 5’ naar 3’), een proces dat translocatie wordt genoemd.
Het tRNA met de keten komt nu in de P-plaats terecht, en het “lege” tRNA verschuift naar de E-plaats en verlaat het ribosoom.
Na iedere toevoeging schuift het ribosoom één codon verder over het mRNA (van 5’ naar 3’).
Terminatie
Vroeg of laat bereikt het ribosoom een stopcodon op het mRNA: UAA, UAG of UGA.
Deze codons hebben geen bijbehorend tRNA met aminozuur.
In plaats daarvan bindt er een release factor (RF) aan het ribosoom wanneer een stopcodon in de A-plaats verschijnt.
De release factor geeft het signaal dat de polypeptideketen moet worden vrijgelaten.
Het ribosoom knipt de keten los van het laatste tRNA waarna de 2 ribosomale subeenheden en het mRNA uit elkaar gaan.
De vertaling van dit mRNA is nu voltooid.
Na de translatie: verschillende eiwitten uit één gen
Wanneer de polypeptideketen is vrijgekomen, is het werk nog niet altijd af.
De keten moet zich vaak eerst vouwen tot zijn uiteindelijke driedimensionale structuur.
Daarnaast ondergaat het eiwit soms nog posttranslationele modificaties:
Er kunnen suikergroepen worden toegevoegd.
Fosfaatgroepen worden aangehecht.
Bepaalde stukjes van de keten worden afgeknipt.
Ook kan je door alternatieve splicing van het pre-mRNA verschillende varianten van mRNA uit 1 en hetzelfde gen krijgen.
Elk van die mRNA-varianten kan leiden tot een eiwit met een iets andere aminozuurvolgorde.
Samen zorgen alternatieve splicing én posttranslationele modificaties ervoor dat 1 gen kan resulteren in meerdere verschillende proteïnen, met soms uiteenlopende functies in de cel.
Dit verklaart hoe een mens met relatief “weinig” genen toch een enorme rijkdom aan eiwitten kan hebben.