SINDROME NEFRÍTICO/GLOMERULOPATIAS
1/81
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
82 Terms
Qué es el sindorme nefrítico?
Es el daño al endotelio y a la membrana basal glomerular por inflamación
Qué caracteriza al síndrome nefrítico
Hematuria (eritrocitos dismórficos, cilindros hemáticos)
Proteinuria <3.5 g/día
Azotemia: elevación de creatinina
BUN > 18 mg
Cr > 1.2 mg/dL
Hipertensión (por retención de agua y sodio)
Edema
Distención venosa yugular
Mecanismo de lesión del síndrome nefrítico: formación de inmunocomplejos y activación del complemento en el espacio subendotelial o en el mesangio. Patología que lo causa?
Glomerulonefritis postestreptocócica
Nefropatía por IgA
nefritits lúpica
Mecanismo de lesión del síndrome nefrítico: anticuerpos circulantes contra la MBG. Patología que lo causa?
Enfermedad por anticuerpos anti MBG
Síndrome de goodpasture (síndrome pulmonar renal de hemoptisis y hematuria, mutación de colágeno IV)
Mecanismo de lesión del síndrome nefrítico: anticuerpos circulantes dirigidos contra antígenos citoplasmáticos de neutrófilos (ANCAs). Patologia que lo causa?
Poliangeitis sistémicas
Cuáles son las tres clasificaciones de la glomerulonefritis rapidamente progresiva
Tipo 1: Enfermedad mediafa por anticuerpos anti-MBG (good pasture syndrome)
Tipo 2: Enfermedad mediada por depósitos de inmunocomplejos
Tipo 3: Glomerulonefritis con semilunas pauciinmunitaria, NO ANTI-GBM, NO DEPÓSITOS DE COMPLEJOS INMUNES, PERO ANTICUERPOS CITOPLÁSMICOS ANTINEUTRÓFILOS (ANCA) EN SANGRE
c-ANCA: granulomatosis de wegener
p-ANCA: poliangitis microscópica, sindrome de churg-strauss
De que otra manera es conocida la enfermedad Anti-MBG?
Good Pasture syndrome
Qué causa el good pasture syndrome?
Anticuerpos IgG dirigidos contra la membrana basal glomerular (especificamente al colágeno tipo IV)
Manifestaciones clínicas de enfermedad anti-GBM (good pasture syndrome)
Hemoptisis (por afectación pulmonar)
Descenso repentino de hemoglonina
Fiebre
Disnea
Hematuria
Oliguria (casi siempre mal pronóstico)
Cómo se presenta el good pasture syndrome?
Causa necrosis glomerular y semilunas → una glomerulonefritis rapidamente progresiva
También ataca pulmón casuando hemoptisis y hemorragia alveolar
Dx de good pasture syndrome
Hematuria severa, cilindros hemáticos
Serología: anti-MBG positivos en suero
Usar dominio a3 NC1 de la colágena IV como objetivo o sitio de acción
Inmunofluorescencia lineal de IgG y C3
Creatinina elevada, TFG reducida
Tx de good pasture syndrome
Plasmaféresis para remover anticuerpos
Corticosteroides (prednisona oral) + ciclofosfamida para suprimir producción de anticuerpos
Dosis bajas de inmunosupresores hasta que la concentración de anticuerpos sea negativa (rituximab, azatioprina, micofenolato de mofetilo)
Para transplante renal se debe esperar 6 meses hasta que no haya anticuerpos en suero
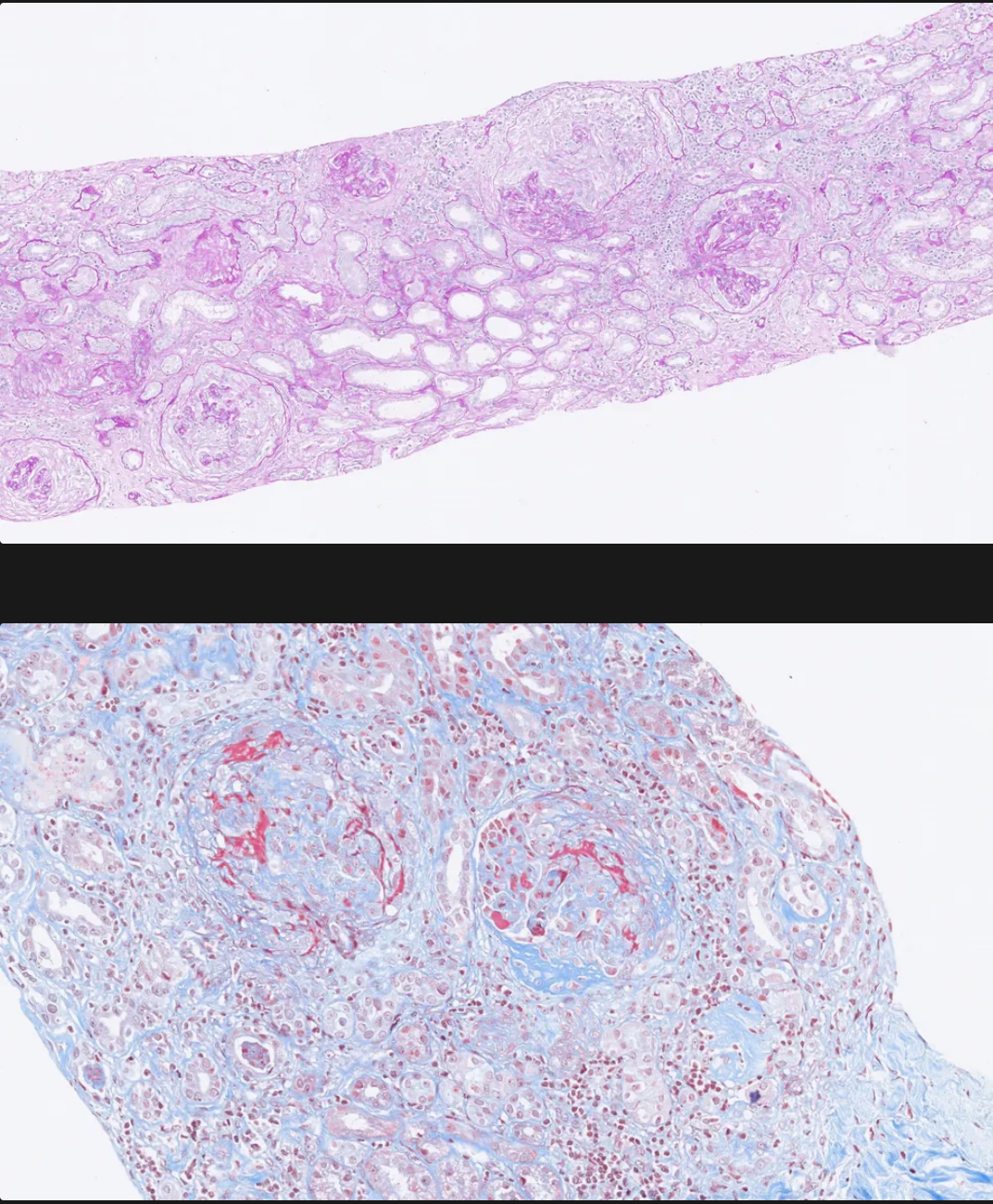
Qué se aprecia en la imágen y a que patologia está asociada?
Necrosis focal y segmentaria y formación de semilunas en el espacio de Bowman.
Enfermedad anti-GBM Good pasture syndrome

Qué se puede ver en la inmunofluorescencia? que patrón sigue? a que enfermedad está asociada?
Se ven: anticuerpos anti-GBM y complemento (IgG, a veces IgA)
Patrón: lineal
Enfermedad anti-GBM (Enfermedad de good pasture)
Qué son los ANCAs?
ANCA = Anti-Neutrophil Cytoplasmic Antibodies
→ anticuerpos dirigidos contra proteínas dentro de los neutrófilos.
Los ANCA activan los neutrófilos de forma exagerada → los neutrófilos atacan las paredes de los vasos sanguíneos → se produce vasculitis necrotizante (inflamación severa + daño + muerte de tejido)
Los ANCA son anticuerpos dirigidos contra enzimas de los neutrófilos:
PR3 (Proteinasa 3) → produce un patrón c-ANCA
MPO (Mieloperoxidasa) → produce un patrón p-ANCA
Estos anticuerpos no deberían existir, pero el sistema inmune los fabrica por error.
Vasculitis mediada por ANCA
La vasculitis mediada por ANCA es un grupo de enfermedades en las que el sistema inmune ataca vasos sanguíneos pequeños (capilares, vénulas y arteriolas) porque produce anticuerpos anormales llamados ANCA.
Enfermedades vasculitis mediadas por ANCA
Granulomatosis con Poliangeítis (GPA / Wegener)
Usualmente ANCA tipo PR3/c-ANCA
Forma granulomas (senos, pulmones)
Poliangeítis Microscópica (PAM)
Usualmente ANCA tipo MPO/p-ANCA
Daño renal y pulmonar severo, sin granulomas
Granulomatosis Eosinofílica con Poliangeítis (GEPA / Churg-Strauss)
ANCA tipo MPO/p-ANCA en 30–40%
Eosinofilia + asma + vasculitis
Qué causa la Granulomatosis con Poliangeitis (de Wegener)?
ANCAs anti PR3 activan neutrófilos causando necrosis fibrinoide de vasos pequeños.
Pacientes expuestos a polvo de silicio
Deficiencia de antitripsisna a1
Como se forman los granulomas en la granulomatosis con poliangeitis de Wegener?
Activación inmune también recluta macrófagos y linfocitos T
Estos forman masas inflamatorias destructivas
Se localizan especialmente en vías respiratorias superiores y pulmones
AGREGAR IMÁGEN
Manifestaciones clínicas de la granulomatosis con poliangeitis de Wegener?
Fiebre
Rinorrea purulenta
Úlceras nasales
Dolor sinusal
Hemoptisis
Púrpura cutánea
Sinusitis inflamatoria con granulomas mucosos o lesiones ulcerativas de nariz, paladar o faringe
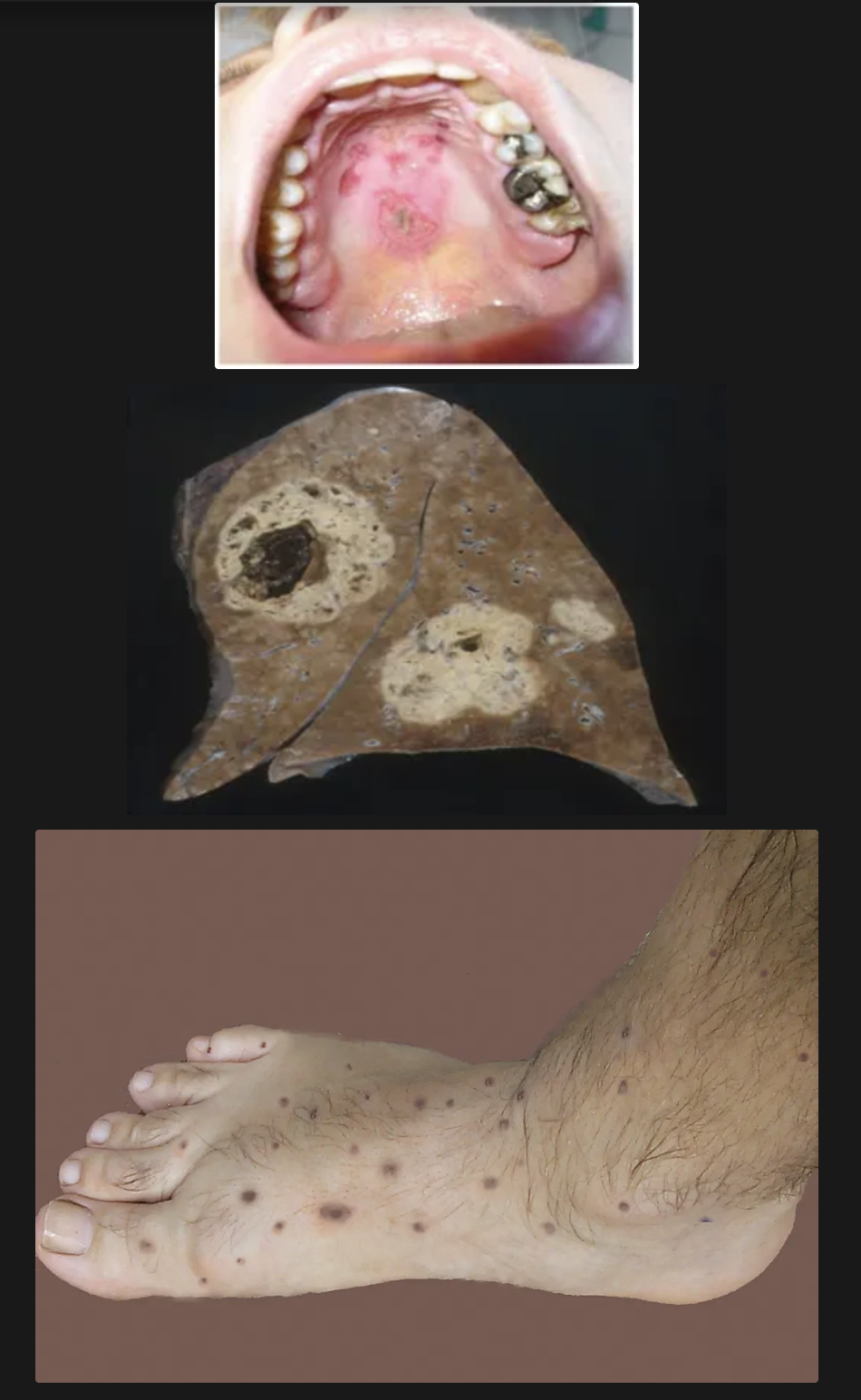
Dx de la granulomatosis con poliangitis de wegener?
Rx de torax:
nódulos e infiltrado pesistentes, a veces cavidades
Biopsia de tejido afectado:
Inflamación de vasos pequeños (vasculitis), granulomas caseosos
Biopsia renal:
Glomerulonefritis segmentaria necrotizante sin depósitos inmunitarios .
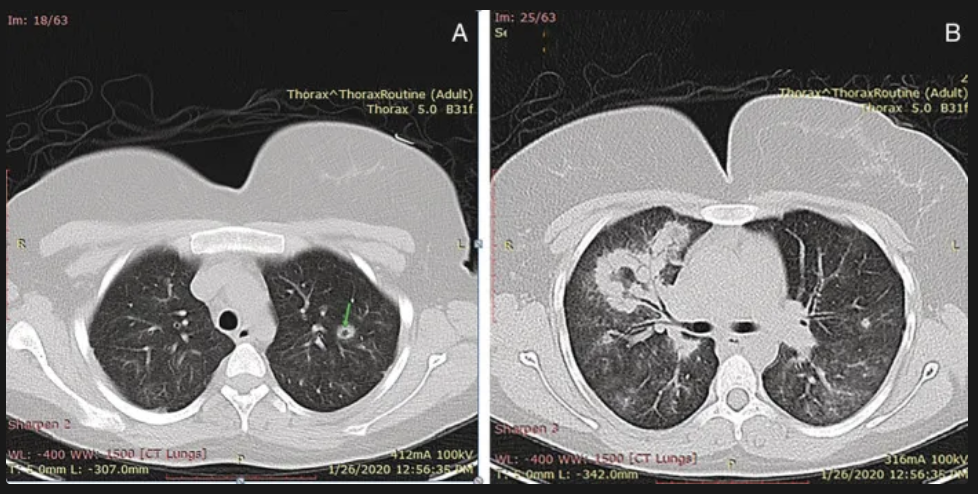
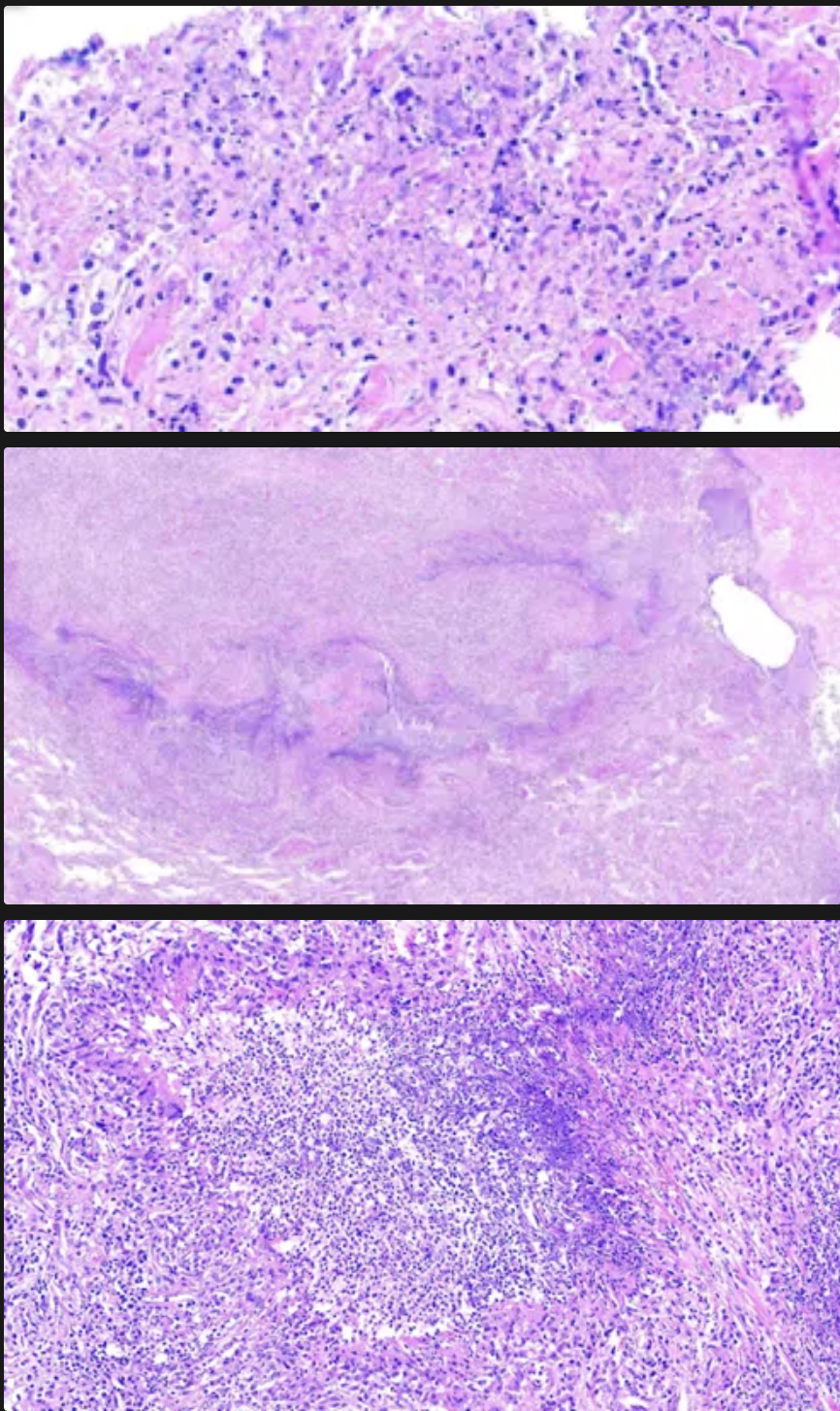
La granulomatosis con poliangitis (de Wegener), tiene granulomas con patrones _____ de necrosis central caseosa y estos granulos mas están rodeados por una zona de _______ con células gigantes e infiltrado leucocitario
Geográficos (contornos irregulares de la necrosis); Fibroblastos porliferativos
Qué causa la poliangeitis microscópica (PAM)?
Daño directo por neutrófilos activados por ANCA-MPO
que afecta la poliangeitis microscópica?
Riñones
Pulmones (hemorragia alveolar)
Piel (púrpura palpable)
Cuál es el otro nombre conocido para la granulomatosis eosinofílica con poliangeitis?
Churg-Strauss
Anticuerpo predominante en la granulomatosis eosinofílica con poliangeitis o Churg-Strauss
ANCA-p (MPO)
Manifestaciones clínicas de la granulomatosis eosinófilica con Poliangeítis (Síndrome de Churg-Strauss)
Eosinofilia periférica (en sangre >500/L)
Púrpura cutánea
Mononeuritis (entumecimiento, dolor, homigueo)
Rinitis alérgica
Derrames pleurales exudativos con eosinofilia
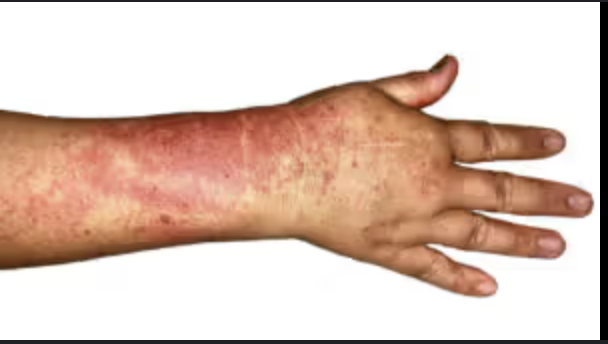
Dx de granulomatosis eosinófilica con poliangeitis (Síndrome de Churg-Strauss)
Hipergammaglobulinemia
Alta concentración de IgE en suero
Presencia de factor reumatoide
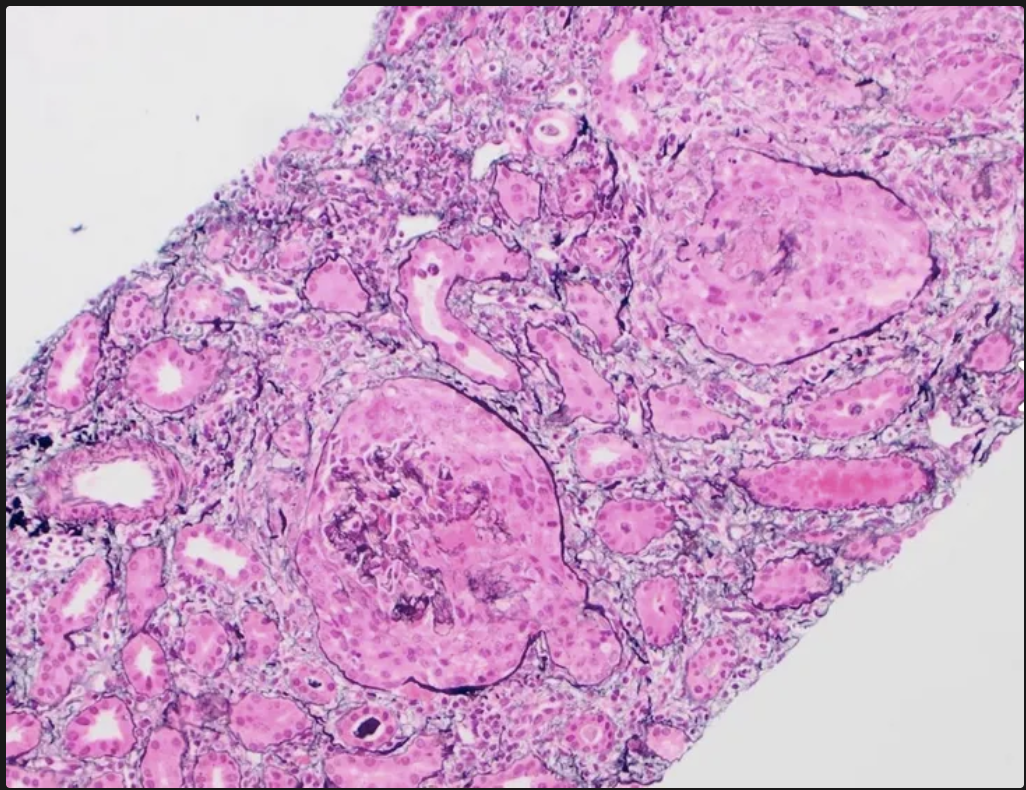
La granulomatosis eosinófilica con poliangeitis (Churg-Strauss) está conformada por vasculitis de _________ y _________, pero no hay eosinófilos ni _______
Vasos pequeños; Glomerulonefritis necrosante focal; granulomas
Tx para todas las glomerulonefritis asociadas a ANCA
Glucocorticoides
Ciclofosfamida o rituximab
Plasmaféresis
Tx de mantenimiento: Dosis reducidad de esteroides y ciclofosfamida hasta por 1 año
A que tipo de glomerulonefritis pertenece la nefropatía asociada al lupus eritematoso generalizado o nefritis lúpica?
Al tipo 2, por complejos inmunes
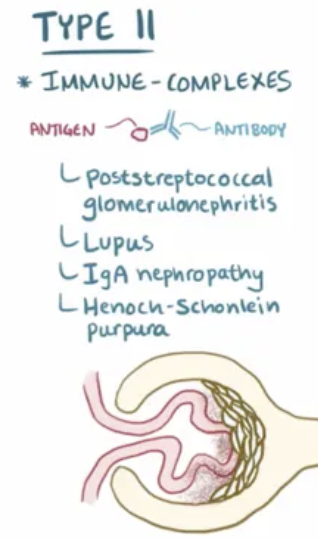
Clasificación patologica de la nefropatia asociada a lupus:
Clase 1
Nefritis mesangial mínima lúpica de clase 1
Estrucutra histológica normal fel glomérulo
En microscopía electrónica e inmunofluorescencia hay depósitos mínimos de inmunocomplejos en el mesangio
Presentación clínica:
Función renal normal
Rara vez hay síndrome nefrótico
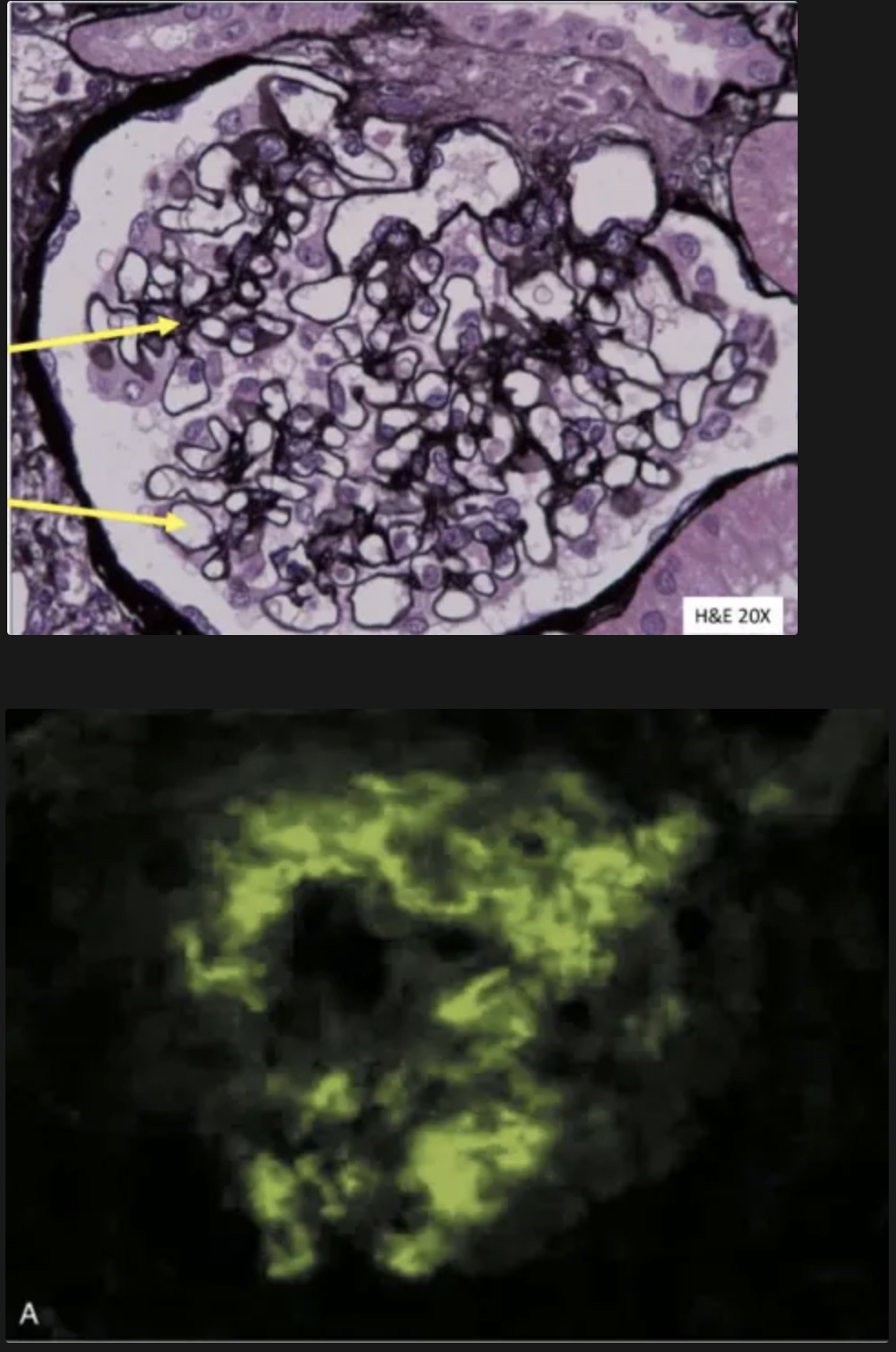
Clasificación patológica de la nefropatía asociada a lupus:
clase 2
Nefritis Proliferativa Mesangial de clase 2
Proliferación de células mesangiales
Acumulación de matriz mesangial y depósitos mesangiales granulares de inmunoglobulinas y complemento sin afectación a capilares glomerulares
Presentación clínica:
Función renal normal
Rara vez hay síndrome nefrótico
Clasificación patológica de la nefropatia asociada a lupus:
clase 3
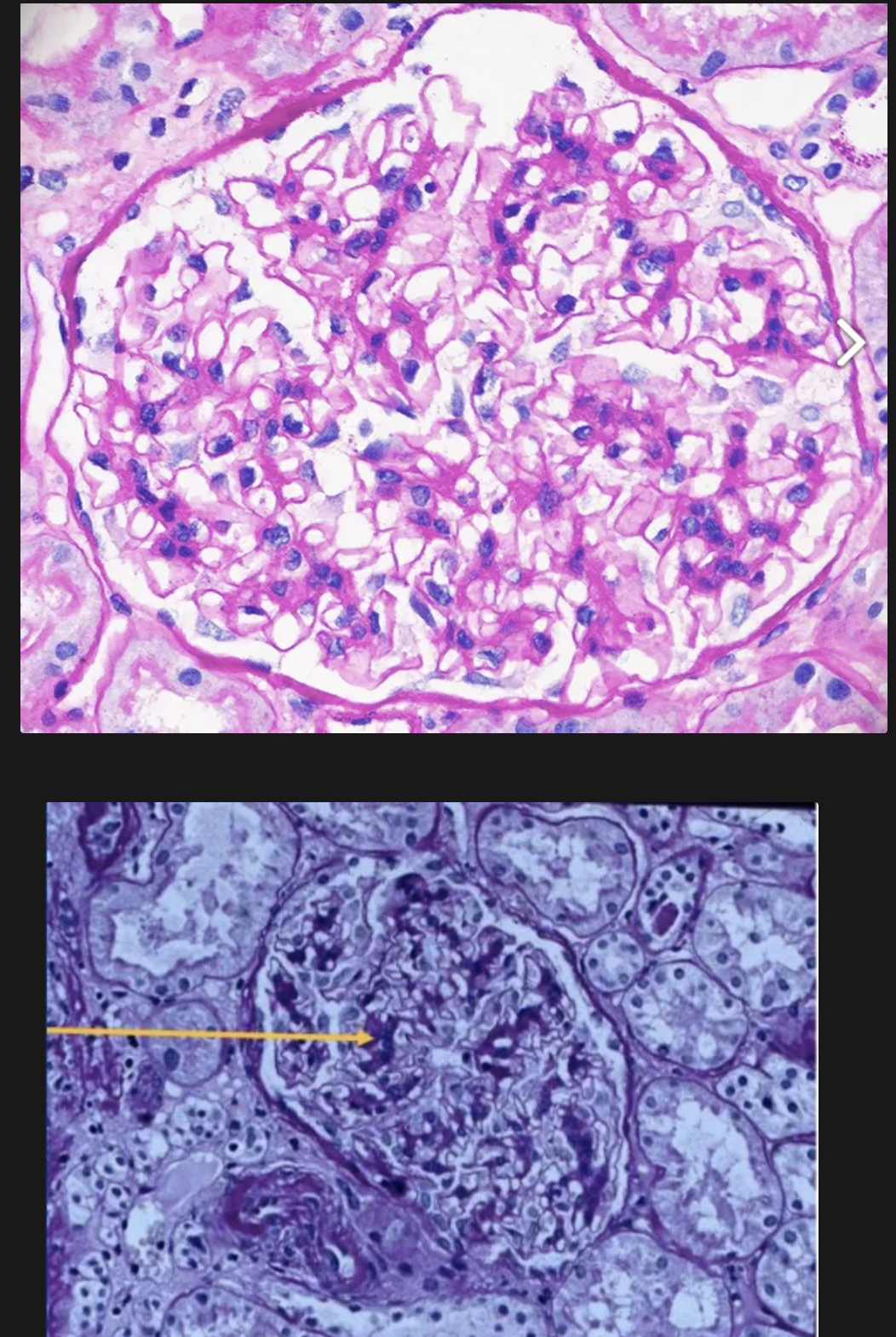
Nefritis lúpica focal de clase 3
Afectación con proliferación o cicatrización de menos del 50% de los glomérulos focal y segmentaria
Puede haber lesiones segmentarias o globales
Glomérulos con proliferación endotelial y mesangial, con acumulación de leucocitos
Necrosis capilar y trombos hialinos
Proliferación extracapilar asociada a necrosis focal y formación de semilunas
Presentación clínica:
Hematuria y proteinuria leve
Sedimento urinario activo
Síndrome nefrótico
Hipertensión y GFR reducido
Clasificación patológica de la nefropatia asociada a lupus:
clase 4
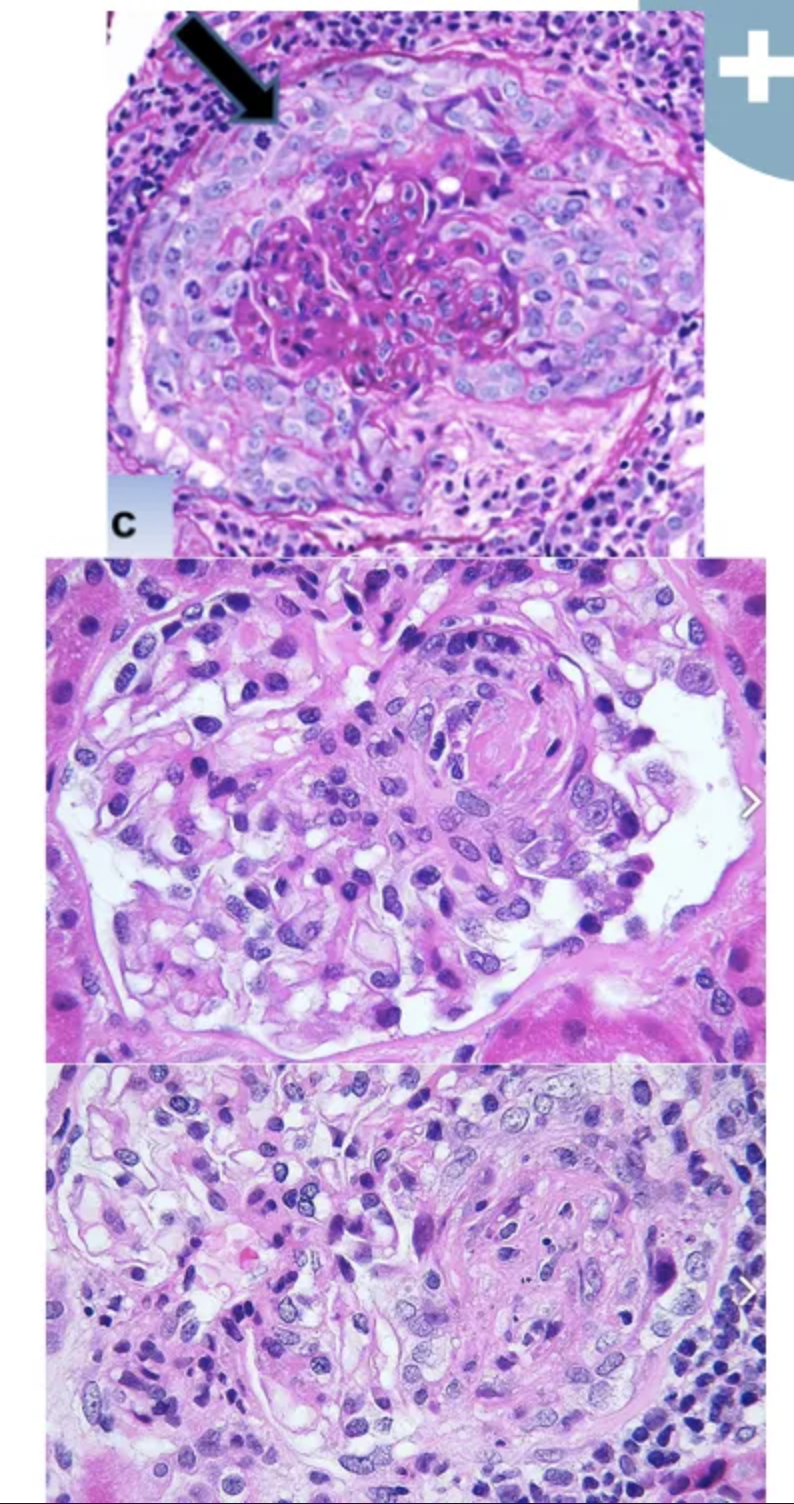
Nefritis Lúpica de clase IV
Forma más frecuente y grave
Lesiones similares a las de clase 3, pero la afectación es difusa osea >50% de los glomérulos afectados
Lesiones pueden ser segmentarias (IV-S) o globales (IV-G)
Proliferación de células endoteliales, mesangiales y epitelilales
se pueden formar semilunas es espacio de Bowman
Engrosamiento de la pared capilar a forma de “asa de alambre“ en microscopía óptica
Hay inmunocomplejos por inmunofluorescencia
Presentación clínica
Hematuria y proteinuria
Cilindros eritrocitarios
Concentración elevada de anticuerpos anti-ADN
Complemento sérico reducido
Hipertensión
Clasificación patológica de la nefropatia asociada a lupus:
clase 5
Nefritis membranosa lúpica de clase V
Engrosamiento difuso de las paredes capilares debido al depósito subepitelial de inmunocomplejos
Mayor producción de material “similar“ a la membrana basal glomerular
Similar a la nefropatía membranosa, también puede haber spikes
Puede haber nefritis lúpica focal o difusa
Presentación clínica
Proteinuria intensa o síndrome nefrótico
Trombosis de vena renal u otras complicaciones
Hipertensión e insuficiencia renal

Clasificación patológica de la nefropatia asociada a lupus:
clase 6
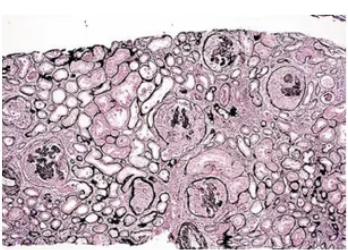
Nefritis esclerosante avanzada lúpica
Esclerosis de más del 90% de los glomerulos
Nefropatía terminal
¿Cuál anticuerpo es el responsable de la formación de los complejos inmunitarios en la nefritis lúpica?
anti-DNA (mecanismo de hipersensibilidad tipo 3)
anti-dsDNA
Una vez que se formaron los inmunocomplejos y se depositaron en los espacios mesangiales, subendoteliales o subepiteliales, surgue la activación de la cascada del ______, que causan la entrada de células inflamatorias causando expansión y engrosamiento del mesangio, paredes capilares y membrana basal glomerular
complemento clásica
Manifestaciones clínicas
Proteínuria
Hematuria
Hipertensión
Edema
Sedimento urinario activo con cilindros eritrocítarios
Dx de nefritis lúpica:
Creatinina elevada
Proteinuria
Hematuria
Cilindros eritrocitarios, de hemoglobina, granulares, tubulares o mezclados
TFG disminuida
Hipocomplementemia
anti-dsDNA elevado
Biópsia de riñón (gold standard)
radio proteina:creatinina >0.5 g/g
Tx de nefritis lúpica
Para nefritis lúpica clase IV y clase V
esteroides y ciclofosfamida o micofenolato
porv2-6 meses
metilprednisona vía intravenosa o prednisona vía oral
ciclofosfamida IV mensual u oral diaria
segunda fase de mantenimiento
dosis menores de corticoesteroides
diálisis o transplante renal si progresa
Nombre de glomerulonefritis rapidamente progresiva
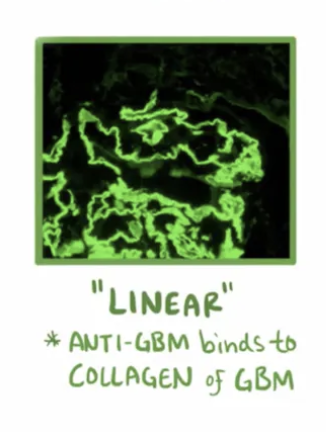
Tipo 1: Enfermedad mediada por anticuerpos anti-MBG
Good pasture syndrome
ES LINEAR
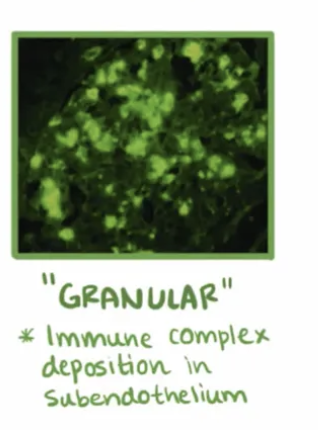
Nombre de glomerulonefritis rapidamente progresiva
Tipo 2: Enfermedad mediada por complejos inmunes
Glomerulonefritis posestreptocócica
lupus
Nefropatia por IgA
Henoch-Schonlein purpura

Nombre de glomerulonefritis rapidamente progresiva
Tipo 3: Pauci-inmune
No hay nada pintado por que no hay anticuerpos anti-gmb y no hay complejos inmunes, solamente ANCAS
Granulomatosis de wegener
Poliangitis microscópica
Síndrome de churg-strauss
¿Qué es la nefropatía por inmunoglobulina A (enfermedad de berger)?
Presencia de depósitos prominentes de IgA en la región mesangial, con hematuria de repetición
cómo se encontrarán las concenctraciones de IgA plasmáticas en la enfremdad de berger?
aumentadas
por qué la fijación de cadenas de azúcares que contienen galactosa, especificamente de IgA1 está mal?
Puede ser por un defecto hereditario o adquirido , el cuerpo va agenerarl antiguerpos IgG contra la IgA defectuosa y froman inmunocomplejos que se depositarán en el mesangio
Una vez ñlos inmunocomplejos depositados en el mesangio in situ, qué ocurre?
activación de células mesangiales
proliferación de células mesangiales que producen mas mátriz y esto causa la liberación de citocinas y factores inflamatorios.
qué vía se altera en el sindrome de berger?
la viá alternativa
C3 positivo
C1q y C4 negativos
Porqué el cuerpo ataca la IgA en la enfermedad de berger?
La IgA1 tiene una parte llamada región bisagra, esta región debe de estar cubierta por azúcares como:
galactosa
N-acetilgalactosamina (GalNac)
Tienen función protectora que veita que la IgA sea reconocida como extraña.
En la enfermedad de berger la IgA1 está mal galactosilada o deficiente de galactosa, casuando que la GalNac que se encuentra debajo de la galactosa quede expuesto. El cuerpo no reconoce la GalNac por que no está acostumbrado a ver ese azúcar y produce anticuerpos IgG o IgA especificamente dirigidos contra esa GalNac.
Una vez los anticuerpos se pegan a la IgA anormal, se forman los _____
Inmunocomplejos, los cuales se forman en el mismo mesangio
Por qué los inmunocomplejos dañan el glomérulo?
Activan el complemento (vía alternativa)
Proliferación mesangial
Producción de matriz
Inflamación
Hematuria, proteinuria, daño progresivo
Por que esta enfermedad se agrava después de infecciones?
Cuando el cuerpo entra en contacto con un virus o bacteria se incrementa la producción de IgA.
Aumenta la producción de IgA anormal
Se generan mas inmunocomplejos
Aparece cuadro clásico: hematuria después de una infección respiratoria o digestiva
Enfermedades donde puede haber depósitos de IgA:
Hepatopatía crónica
Enfermedad de crohn
Enfermedad celiaca
Bronquiectasias crónicas
Neumonia intersticial idiopática
VIH
Enfermedad de sjörgen
Dx de enfermedad de Berger o nefropatia por depósitos de IgA
Biopsia renal
Medición de concentraciones séricas de IgA
Microscopía óptica de la enfermedad de Berger
Glomérulos normales o con ensanchamiento mesangial
Presencia de leucocitos en capilares glomerulares
Lesiones visibles: la curación lleva a esclerosis focal y segmentaria, necrosis con formación de estructuras semilunares
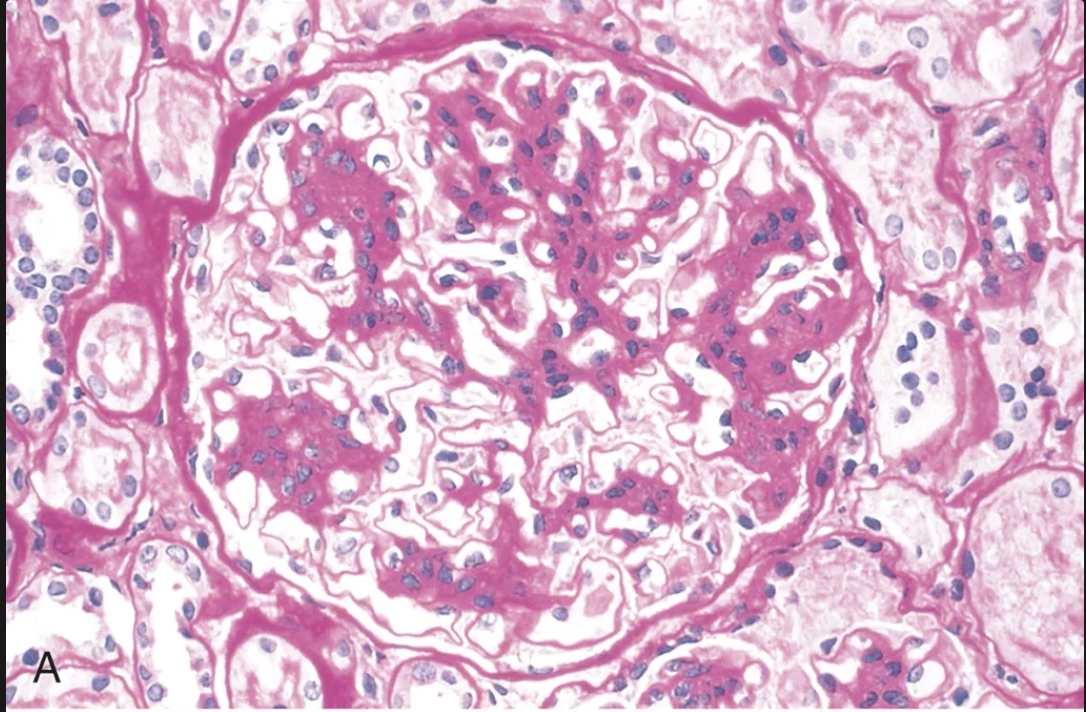
En la inmunofluorescencia de la enfermedad de berger se pueden ver depósitos de ______, puede haber ___ y ____ y cantidades menores de IgG o IgM
IgA; C3; properdina
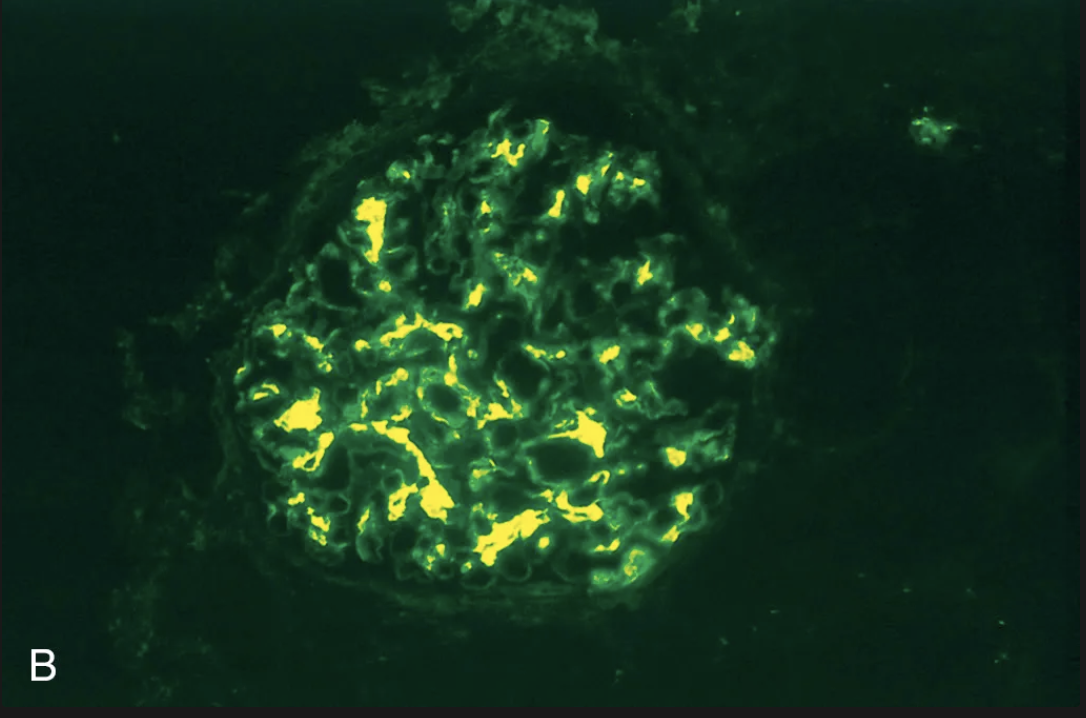
Tx de la nefropatía por IgA
Inhibidores del SRAA : IECAS:
A personas con proteinuria
deterioro de la función renal
Hipertensión
por que funcionan? reducen presión traglomerular (disminuye fuga de proteínas), disminuyen inflamación y fibrosis, protección renal
SI HAY PROTEINURIA IECAS O ARA-II SIEMPRE
Amigdalectomía y aceite de pescado
A personas asiáticas
pacientes que presentan brotes de hematuria post-infección de vías aéreas superiores.
por que funciona? las amigdalas son fuente de producción de IgA
Corticoesteroides:
A personas con proteinuria >1 g/día después de etsar 3-6 meses con IECA/ARAII
Personas con TFG moderadamente reducida
Por que funcionan? por inflamación mesangial. SOLO CASOS MODERADOS-GRAVES
Tx agresivo para la forma rápidamente progresiva de nefropatia por depósitos de IgA
Corticoesteroides intravenosos en pulsos
Ciclofosfamida
Plasmaféresis (sobretodo si hay hemorragia alveolar o púrpura)
Lesión glomerular sin etiología específica en la cual hay perdida relativamente rápida y progresiva de la función renal asociada a la oliguria intersa y sugnos de síndrome nefrítico
Glomerulonefritis rápidamente progresiva
¿Cuál es la otra forma en la que es conocida la glomerulonefritis asociada a infecciones o post-estreptocócica?
Glomerulonefritis proliferativa endocapilar aguda
¿Qué es la glomerulonefritis asociada a infecciones?
Proliferación difusa de las células del glomérulo, asociada a la entrada de exudado leucocitario, que se deben normalmente a inmunocomplejos
Qué tipo de glomerulopatía rápidamente progresiva es la glomerulonefritis asociada a infecciones?
Tipo 2
Cuál es la razón de que el antígeno desencadenante sea exógeno?
Una glomerulitis post infecciosa, mas común asociada a estreptococos
¿Cuánto tiempo después de ina infección por estreptococos inicia el daño renal?
1 a 4 semanas después de una infección de la faringe o la piel
Cuál es la razón de que el antígeno desencadenante sea endógeno en una glomerulonefritis asociada a infecciónes?
Patrón endógeno por LES
Inmunocomplejos que contienen antígenos estreptococícos
Cepas de estreptococus B-hemolíticos del grupo A
Tipos 12, 4 y 1 tipificados por la proteína M
Exotina piógena estreptocócica B (SpeB): activan el complemento.
NAP1r: Receptor de plasmina asociado a nefritis
Estos antígenos se implantan en las paredes subendoteliales de los capilares glomerulares, induciendo la formación in situ de inmunocomplejos y desencadenando respuesta inflamatoria
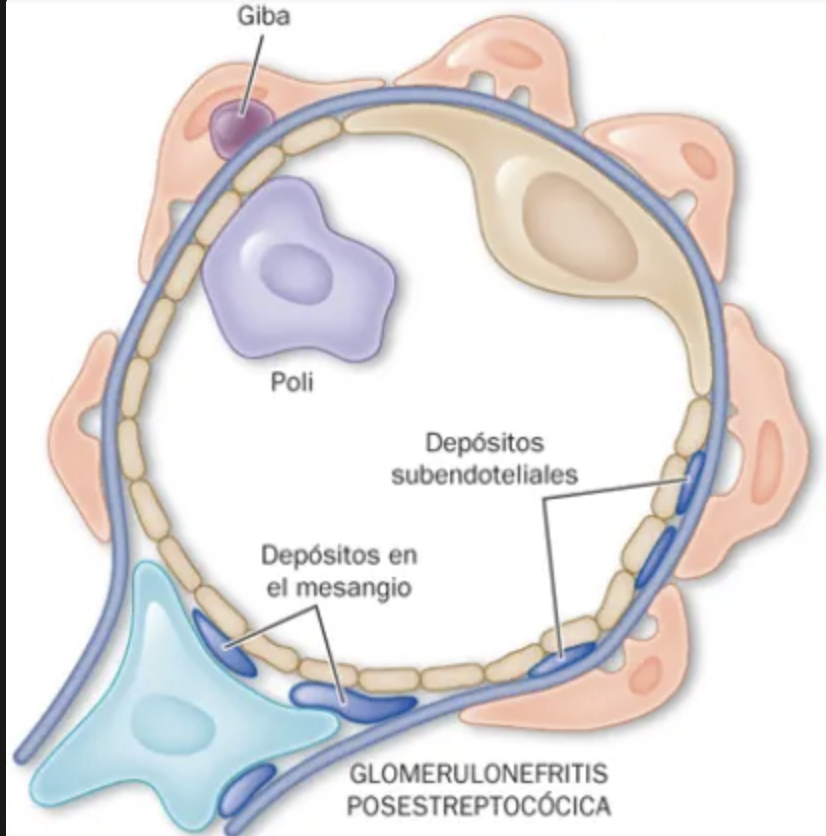
Por qué se forman los inmunocomplejos en la glomerulonefritis infecciosa?
El estreptococo B-hemolítico produce un antígeno catiónico (cargado positivamente) y como la membrana basal glomerular está cargada negativamente, este antígeno puede pasar facilmentey se pega en el espacio subepitelial (entre mbg y podocitos). Los podocitos son muy selectivos por lo que al llegar al espacio subepitelila el antpigeno no podrá pasar quedando atrapado.
Por que se tarda de 2-4 semanas en mostrar manifestaciones clínicas el paciente?
Después de la infección faríngea o cutanea el cuerpo producirá anticuerpos IgG contra el antígeno bacteriano, pero estos anticuerpos tardan entre 10-14 días en formarse (por eso hay retraso en manifestaciones clínicas). Una vez que los anticuerpos IgG pasan por el glomérulo, estos se unen al antígeno catiónico producido por la bacteria en la aprte subepitelial y se forma un inmunocomplejo in situ.
Cuál es la reacción de hipersensibilidad formada por la formación de inmunocomplejos en la glomerulonefritis infecciosa?
Reacción de hipersensibilidad de tipo 3 (igual que en LES). Los inmunocomplejos IgG + antígeno activan el complemento, sobre todo C3 de la vía alternativa
Una vez que sucede la reacción de hipersensibilidad y hay inflamación glomerular, daño a la pared capilar que causa aumento de la permeabilidad y hay retención de sodio y agua, ¿a qué progresa le glomerulonefritis infecciosa?
A un síndrome nefrítico, el cual puede progresar a un síndrome nefrótico después de haber disminuido la inflamación, los depósitos subendoteliales s reducen y los podocitos ya quedaron dañados.
¿Cuál sería un caso típico de glomerulonefritis infecciosa?
Un niño pequeño con desarrollo abrupto de malestar, fiebre y náuseas, oligura y hematura, orina color coca cola, 1-2 semanas después de haber tenido un catarro.
¿Qué se encontrará en la orina del niño?
Eritrocitos dismórficos
Cilindros hemáticos
Proteinuria leve <1gr/día
Edema periorbitario
Hipertensión leve-moderadaede
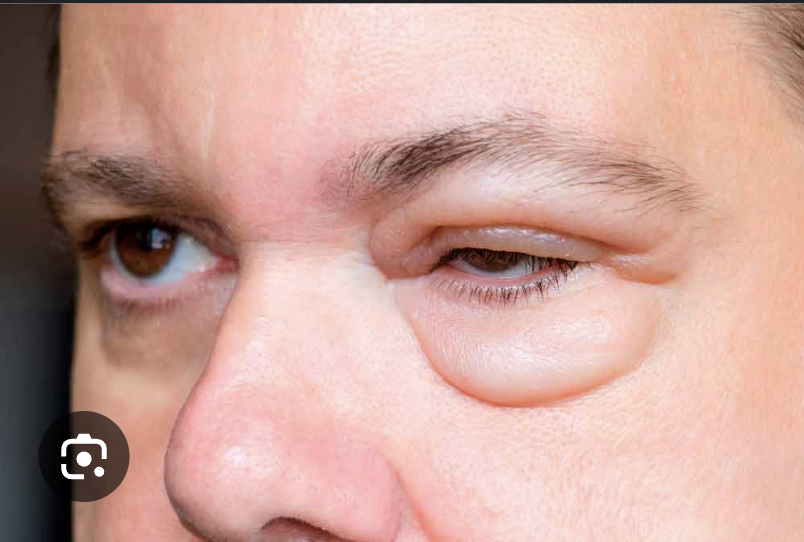
Diagnóstico de la glomerulonefritis infecciosa?
Gold standard:
Mayor concentración de ASO
anti-DNAsa
Anticuerpos contra hialuronidasa
Hipocomplementemia:
Disminución de C3 y niveles normales de C4
Cultivos en busca de infección estreptocócica positivos
Urianálisis con microscopia
Hematuria y cilindros eritrocitarios
Proteinuria
Piuria (pus en orina)
BMP:
Aumento de BUN y creatinina
Hiperkalemia e hiponatremia
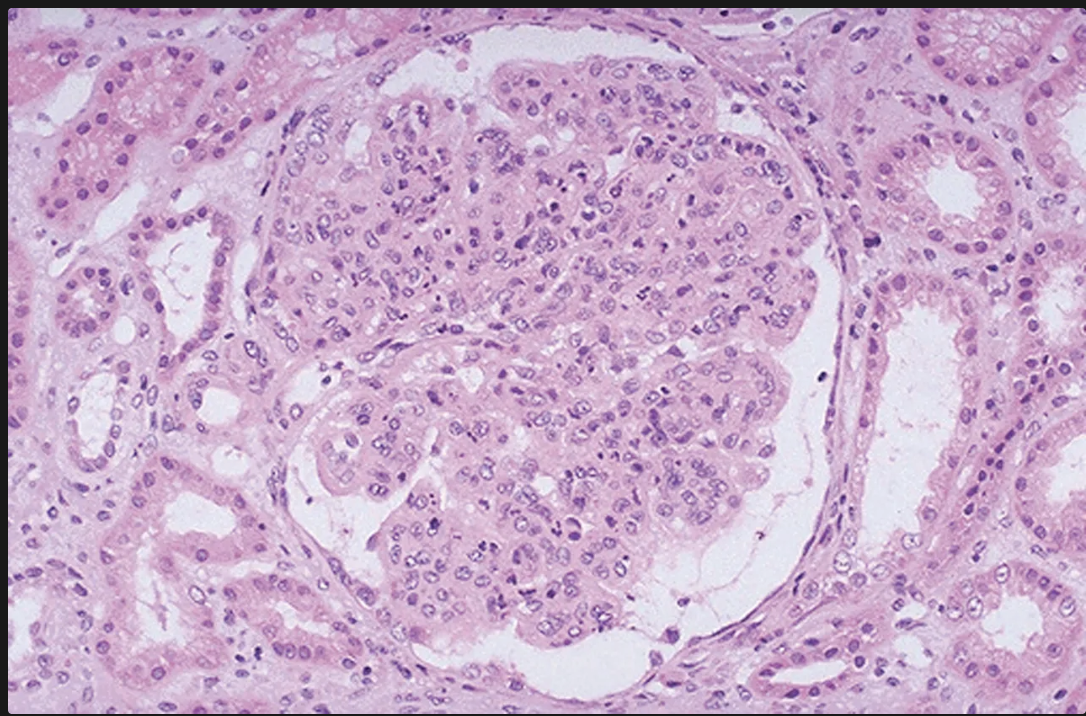
Cómo se ven los glomérulos en la glomerulonefritis infecciosa?
Glomérulos hipercelulares de gran tamaño
Infiltración de leucocitos (es global y difuso osea en tdoso los lóbulos de todos los glomérulos)
Proliferación de células endoteliales y mesangiales
Formación de semilunas
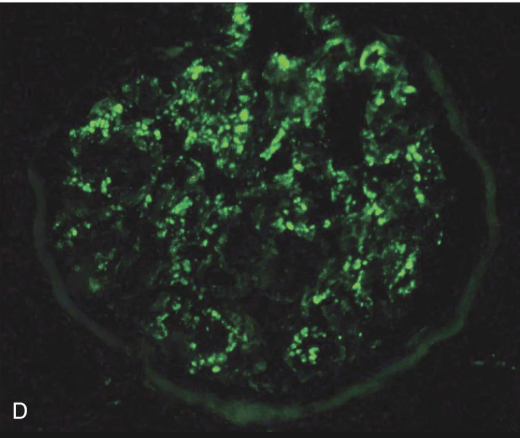
En la inmunofluorescencia de la glomerulopatia infecciosa, que depósitos célulares se pueden ver?
IgG
C3
C4
C5 - C9
Si la glomerulonefritis rápidamente progresiva es la tipo 2, cómo se verá en inmunofluorescencia?
Granular
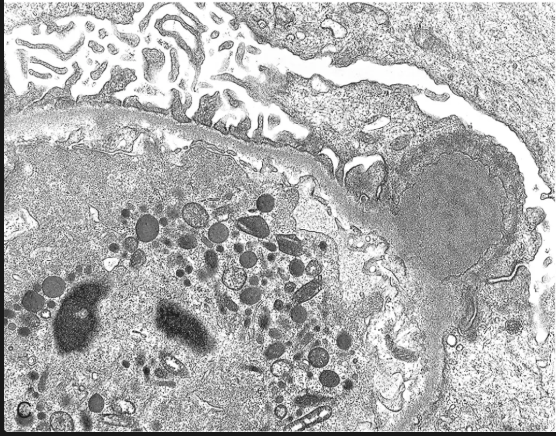
En la microscopía electrónica que es lo que más hace que se distinga de la glomerulopatia infecciosa?
Depósitos definidos, amorfos y electrodensos en la vertiente epitelial de la membrana a modo de JOROBAS
En en caso del tratamiento de la glomerulonefritis infecciosa es necesario dar una dieta baja en ____ y restricción de ______ además de dar ______ como la furosemida, todo esto para regular la hipertensión y edema
sodio <2 g/día; líquidos <2L/día; diuréticos de asa